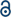 オープンアクセスの記事
オープンアクセスの記事 このオープンアクセスの記事は、クリエイティブ*コモンズ表示-非商業3.0Unportedライセンス
このオープンアクセスの記事は、クリエイティブ*コモンズ表示-非商業3.0Unportedライセンス
Intek Song a,Jinyoung Koo
a,Jinyoung Koo b,Shok Min Yoon
b,Shok Min Yoon *c
*c
安東国立大学応用化学科,1375慶東路,慶北36729,韓国
浦項大学化学学科科学技術の,77cheongam-RO,pohang,keongbuk37673,大韓民国
cdepartment of bio-nano chemistry,wonkwang University,460iksandae-RO,iksan,jeonbuk54538,大韓民国. 電子メール:[email protected]…..kr
2019年8月6日初版
dブロック原子またはfブロック原子の間に形成される四重結合は、超短結合距離やδとδ*の間の狭いエネルギーギャップなどのユニークな性質のため、興味深い研究テーマです。 種々の多重結合錯体の中で,四重結合c r(I I)酢酸塩は付加配位子のLewis塩基度によってδ–δ*エネルギーギャップを制御するのに有用であると考えられた。 しかし、軸配位子(Cr2(OAc)4L2)と配位したCr(II)酢酸塩の高品質、大型結晶の合成と調製は、好気性条件下での代表的な酸化剤であるO2に対する脆弱性のた 安定に連結されたCr2(OAc)4L2を得るために、無水Cr(II)酢酸塩(Cr2(OAc)4)溶解したO2の脱気された配位子溶媒Lに溶解しました。 また、Cr2(OAc)4L2のサブミリスケール単結晶は、滴下乾燥プロセスによって時間未満のために急速に生成されました。 合成したCr(I I)錯体の単結晶相をX線回折法により測定し,cr-C r四重結合距離に対する付加軸配位子のLewis塩基度の依存性を確認した。 さらに、Cr2(OAc)4L2の四重結合のラマンピークは、軸配位子の塩基度の増加とともに赤シフトすることが観察された。
はじめに
コットングループが四重結合の酢酸Cr(II)(Cr2(OAc)4)を合成して以来、遷移金属間の多重結合の研究分野ではかなり進歩している1,2最近では、パワーグループが四重結合に加えてCr2五重結合を報告している3、金属-金属間(M-M)結合の詳細な研究を刺激している。4–6多重M-M結合、特に四重結合が存在するのは、金属のd軌道またはf軌道がδ結合(δ)だけでなく、σ結合および二つのπ結合(π)結合を生じるためである(図4-6)。 およびb)。1,2四重結合の形成にはd軌道が必要であるため、超短(≤2Å)の金属-金属結合1,2と狭いエネルギーギャップを提供する。また、図7に示すように、種々の配位子は、M−M多重結合錯体の軸方向の位置に配位することができる。 このように,m–M結合に対する軸方向配位は,配位子の種類に応じてM–M結合長とその反応性を制御するための重要な研究課題であった。したがって、遷移金属原子の一次元鎖を構築し、O2の選択的かつ可逆的吸着を可能にし、有望な効率的な触媒を可能にするために四重結合が使用され8,980円(税込)図7は、反磁性一重項状態(σ2σ2δ2)と常磁性三重項状態(σ2σ2δ δ*)との間のδ-to-δ*遷移によって室温で磁気が変化することができることを報告した。
δ結合を有する様々な有機金属錯体があり、例えば、Re2Cl82−、10Mo2(mhp)4,11Cr2(OAc)4,12などがある。その中でも、重要な例としては、軸配位子を欠くパドルホイール構造無水酢酸Cr(II)(Cr2(OAc)4)、および軸配位子(Cr2(OAc)4L2、L=配位子)を有するそれらの誘導体(図1-6)が挙げられる(図1-6)。 1a)。1,13Cr(II)はd4電子配置を持っているので、酢酸塩中の二つのCr(II)イオンは四重結合(結合次数=4)の四つの結合軌道を完全に埋める(図。 1b)。 Cr(II)の酢酸塩はこうしてCrcl2のような他のCr(II)の混合物とは違って適度に空気安定しています; Pourbaixダイアグラムによって決定されるように、14ほとんどのCr(II)化合物は非常に吸湿性があり、Cr(III)に非常に容易に酸化されます。 さらに、酢酸Cr(II)は、それらの軸方向の位置で電子対を受け入れる良好なルイス酸である。 これらの電子供与体は空のδ*反結合軌道(LUMO)に寄与するので、配位子のルイス塩基度はδとδ*軌道の間の狭いエネルギーギャップを調節することによって物理化学的性質に影響を与える。1,12,13,15したがって、様々な軸配位子L(Cr2(OAc)4L2)とCr(II)酢酸塩の合成は、ユニークなデルタ結合の性質に関する基礎的な研究を容易にするだろう。
従来、Cr2(OAc)4L2は水和物の配位子交換によって調製されてきましたが、例えば、水和物(L=H2O)の水溶液の上にピリジン(py)を層化すると、Cr2(OAc)4(py)2.16の小さな結晶が析出しますが、このような界面拡散により、Cr2(OAc)4(H2O)2の結晶が副生成物として生成する可能性があります(図)。 S1†)。 所望の配位子を配位するためのかなり簡単な方法は、Cottonらによって指摘されているように、Cr2(OAc)4を標的配位子溶媒に溶解することである。しかし、この方法はCH3OHのような少数の種類の配位子に制限されています。7
cr(II)酢酸塩は、cr(II)からCr(III)への酸化を防ぐために注意して取り扱う必要があります17それらは、酸化を完全に回避するのに十分な強さではな これは、空気中のO2が非常に良好な酸化剤であり、四重結合を効果的に破壊するためである。 従って、溶媒の分解された酸素はCr(II)のアセテートを分解する前に取除かれるか、または脱気されるべきです。 それにもかかわらず、脱ガスプロセスは、我々の知る限り、明示的に言及または報告されていない。1,7,12,16
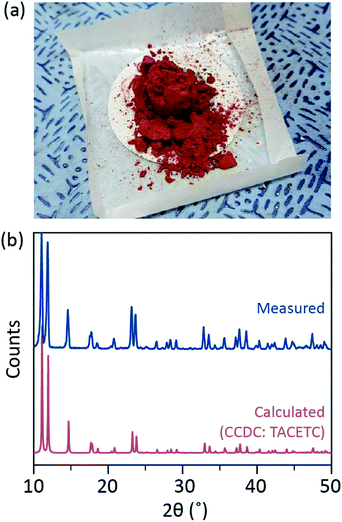
ここでは、無水酢酸Cr(II)の軸方向の位置での様々なライゲーションのための簡単な溶媒脱気プロセスを発表し、結晶Cr2(OAC)4L2(L=H2O、CH3OH(MeOH)、およびピリジン(py))を調製する(図。 1c)。 そして、溶液の温度を低下させるか、または滴下乾燥することにより、ターゲット結晶が得られる(図2)。 3a)。 従来の合成方法は、以前の文献によると、数日かかったが、全体のプロセスは、サブミリメートルスケールの結晶を得るために一日未満かかります。15,18私たちの発見は、金属原子間の四重結合の探査、金属から金属(M-M)多重結合ベースのネットワークの拡張、配位ポリマー19、20または金属-有機フレームワーク8、21を形成するために、ならびに四重結合のユニークな物理的および化学的性質の研究を促進することに貢献するであろう。
結果と考察
無水Cr2(OAc)4の合成
無水Cr2(OAc)4、Cr2(OAc)4L2の前駆体は、水和物またはエタノラート(L=EtOH)を真空中でアニールすることによって調製されている。 しかし、このプロセスは、容易に酸化される非晶質粉末を生成する。12,17酢酸とクロモセン(Cr(C2H5)2)との間の直接化学反応によってCr2(OAc)4を調製するための変更されたアプローチが、クロモセンは空気に敏感で可燃性の複合体である。したがって、両方の方法は、空気中で安定なCr2(Oac)4を調製するのには適していない。
最近、Levy et al.Cr(O)粉末、酢酸、無水酢酸、およびHbrのような空気安定な前駆体を使用して、結晶性Cr2(Oac)4を調製する別の合成方法を報告した。 さらに、この製品は、前任者のものとは異なり、数時間まで空気中で安定しています。 したがって、我々はLevyらを適応させた。わずかな改変を伴うCr2(OAc)4の高純度結晶の調製のための方法(ESI βの詳細については実験のセクションを参照)。
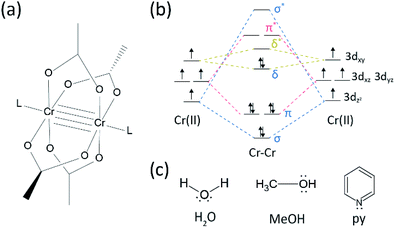
当社の合成プロセスでは、HBrまたはKBrの代わりに濃縮(37%)HCl(aq)を使用し、Cr粉末を基準の量で半分にしました。 全反応時間は、Cr(III)への酸化を防止するために1時間未満であった。 このような改変は、最終生成物中の副生成物または未反応の反応物(例えば、それぞれ酢酸Cr(III)およびcr(0)粉末)の排除を保証するためである。 したがって、生成物を単純に濾過し、過剰なアセトンで洗浄して酢酸Cr(III)を除去した後に赤色結晶性粉末を調製した(図10B)。 2a)。
次いで、粉末を室温で真空中で数時間乾燥させた。 図に示すように。 図2bに示すように、粉末X線回折(pxrd)により、赤色粉末は、三斜晶単位格子を有するCr2(Oac)4であることが明らかになった(P−1、a=7.4(ccdc#:tacetc)。<3 2 0 1><3 7 6 1>なお、得られた粉末は精製することが非常に困難であったため、これ以上精製せずに使用した。 Cr2(OAc)4の気相再結晶精製のために試みられたとき、何もArの流れの下で270°Cの下で蒸発しませんでした。 赤色粉末のわずかな部分のみが270℃以上300℃以下の温度で蒸発し、残りは黒色粉末に分解された(図。 2012年12月2日に発売。 蒸発した粉末を再結晶して赤みを帯びた薄膜にしたが,Cr(III)への緑色を意味する酸化に非常に迅速に分解したため,さらなる反応のために取り出すことができなかった。 300°Cの上の温度で粉は蒸発なしで十分に分解しました。 このような気相再結晶の困難さは以前の報告と一致していた。1,13,15
Cr2(OAc)4L2の合成
軸配位子(Cr2(OAc)4L2)と配位したCr(II)酢酸塩を合成するために、まず、MeOH、H2O、pyのような標的配位子溶媒を選択した(図。 1c)。 これらの配位子は電子の孤立電子対を持ち、Cr2(OAc)4と安定な配位結合を形成する。 それらは異なるルイス塩基度(MeOH<H2O<py)を有し、したがって連結錯体中の四重結合の核間距離は2.288Å(無水)、2に及ぶことが知られている。329Å(MeOH)、2.362Å(H2O)、および2.369Å(py)に、軸配位子のルイス塩基度によると。7,12,16,23
配位子溶媒は、Arガスを注入して沸点のすぐ下に加熱することによって脱気した(図。 3a)。 この脱気プロセスは、溶解したO2による激しい酸化を妨げるように、四重結合の劣化を防止するためのターゲット溶媒中のCr2(OAc)4の溶解のための 脱気した溶媒にCr2(Oac)4を溶解すると、溶液の色は即座にCr2(Oac)4のように赤色に変化した(図3)。 3b)。 脱気されたH2Oへの溶解は瞬間的ではなく、脱気されたH2Oに少量のCr2(OAc)4を入れたとき、最初は青色であり、次に余分な量の溶質を加えると最終的に赤褐色になったことに注意してください。 このような2段階の溶解は、以下の通り、Cr2(oa c)4(a q)とCr2+(a q)との間の平衡に起因し得る:1,2 4(i)Cr2(Oa C)4≦2CR(Oa C)2、(i i)Cr(Oa C)2≦Cr(Oa C)++Oac−、(iii)Cr(Oa C)+≦Cr2++OAc−。
対照的に、Cr2(Oac)4を非脱気溶媒に溶解した場合、溶液はh2Oに対して青色であり、Meohおよびピリジンに対して橙色であり、これはCr2(Oac)4の分解に帰 S3†)。なお、脱気処理後もCr2(OAc)4を溶解しない溶媒も存在する。 Cr2(OAc)4を供与する電子孤立電子対を持たないヘキサンまたはトルエンに入れたとき、溶解も配位も観察されなかった; 全ての粉末は反応容器の底部に沈んだ(図1)。 (2010年4月現在)。 このような選択的溶解性は、配位子の配位がCr2(OAc)4の溶解を伴い、その逆もまた同様であることを示している。1
Cr2(OAc)4L2の結晶化
無酸素状態でのライゲーションが終了したら、cr粉末または未溶解Cr2(OAc)4粉末のような残りの反応物の沈殿のためにstirring拌を停止した。 温度は、脱気および溶解プロセス(すなわち、配位子溶媒の沸点のすぐ下)と同一に保たれた。 結紮複合体(Cr2(OAc)4L2)の結晶を得るために、溶液は非常に空気に敏感であるため、明確な上清は、室温で無酸素条件下で冷却するためのAr充填バイアル A rで満たされたバイアル中の小さな赤色結晶は、2 4時間未満でバイアルの底部で成長させていた(図1の結晶化プロセス(i))。 3a)。 また、上清を基材上に滴下乾燥させることによっても非常に迅速に結晶を得ることができ、周囲条件下では一時間未満である(図中の結晶化プロセス(ii))。 3a)。 両方法による結晶生成物は同一であり、それらはサブミリメートルスケールの赤みを帯びた結晶であり、そのうちの配位子によって微妙に色が異なる(Fig. 3b-d)。
Cr2(OAC)4L2の特性評価
さらに、単結晶X線回折(SCXRD)研究により、得られたCr2(OAc)4L2結晶の結晶構造が以前に報告された結晶と一致することが確認された(表1)。7,12,16結晶の収率が高くないため、PXRDの代わりに大型単結晶の構造確認のためにSCXRDが試みられたことに注意してください(L=H2Oでは7.94%、L=MeOHでは11.26%、L=pyでは3.70%)。 このような低収率は、配位子溶媒中のCr2(OAc)4の溶解度が悪く、1、また、連結された複合分子のほとんどが結晶化後も溶質として残ることに起因する。 さらに、SCXRD研究を通じて、M–M間の核間距離は、追加の軸配位子のルイス塩基度(ルイス塩基度:MeOH<H2O<py)に依存して伸長することが確認されている。 したがって、Cr2(Oac)4L2のM−M距離の順序は、SCXRDによって以下のように開示される:Cr2(OAc)4<6 0 2 0>Cr2(Oac)4(Meoh)2<6 0 2 0>Cr2(Oac)4(H2O)2<6 0 2 0>Cr2(Oac)4(py)2。 さらに、迅速に合成された連結された結晶は、元のCr2(OAc)4結晶と同じように、12時間空気中でも安定であったが、それによって限定されなかった。 可能性のある理由は、O2のような特定の酸化剤による攻撃を妨げる可能性のある結晶中の分子のパッキングであろう。 これらの証拠のズタズタは、我々の簡単な結晶化法は、多様な配位子が容易に増加した安定性とCr–Cr四重結合の軸方向の位置に付着することを教えて
| L | a(Å) | b(Å) | c(Å) | Α(°) | β(°) | γ(°) | 体積(Å3) | スペースグループ | 注 |
|---|---|---|---|---|---|---|---|---|---|
| H2O | 13.105 | 8.568 | 13.838 | 90.00 | 116.71 | 90.00 | 1388 | C2/c | 31 |
| MeOH | 8.065 | 7.406 | 13.296 | 90.00 | 92.84 | 90.00 | 793.2 | P21/n | 32 |
| py | 12.875 | 8.589 | 19.524 | 90.00 | 90.00 | 90.00 | 2159 | Pbca | 33 |
Raman分光法は,Cr,Mo,W,Reを含む多重結合二核錯体の振動モードと,種々の配位子によるM-M結合強度と距離との相関を研究するための強力なツールとして用いられている。図1,25-27に示すように。 図4に示すように、共焦点ラマン分光法(Alpha300R,WITec)は、Cr(II)酢酸塩の結晶の振動モードを明らかにした。 Cr(II)酢酸塩のラマンスペクトルデータは、結晶がレーザー励起源(532nm、0.5mW、Ndによって照射された間、複合体の劣化を防ぐために、数分未満に収集された:YAG)
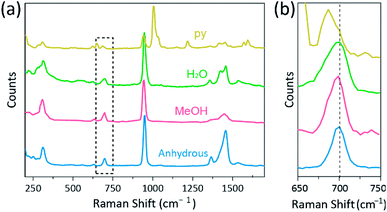
我々の実験では、Cr2(OAc)4(H2O)2の測定されたラマンスペクトルは、以前の報告と同一である25が、無水Cr2(OAc)4を含む他の合成複合体のラマンスペクトルは、我々の知る限りでは報告されていない。 Cr−Cr四重結合錯体を図1に示す。 図4は、おそらく分子構造の類似性のために、Cr2(OAc)4(H2O)2のラマンスペクトルの同様のパターンを有する。 ラマンスペクトルでは、550cm−1と350cm−1の周りのバンドは、それぞれ、Cr(II)酢酸塩のCr–Crストレッチとねじれ/曲げモードに割り当てられています。25,28,29それにもかかわらず、正確なバンド位置は、その低強度18または広い幅のために、すべてのCr(II)酢酸塩の測定されたラマンスペクトルとはほとんど区別されない(Fig. S5†). 別の方法として、Cr–Cr四重結合の振動の倍音包絡線は、明らかに700cm−1(2×√350cm−1)の周りに表示されます(図2)。 4b)。実際に、軸方向配位子の塩基度が増加するにつれて、倍音バンドはそれに応じて赤シフトする。30この手がかりは、軸配位子のルイス塩基度を増加させるように、四重結合の結合強度が弱くなっていることを反映している。29また、ラマンスペクトルにおけるCr(II)酢酸塩の赤シフトの程度は、そのCr-Cr距離に相関している。 したがって、Cr2(OAc)4の倍音バンドは最高のumberを示しますが、Cr2(OAc)4(py)2はCr–Cr四重結合錯体の中で最も低いumberを持っています。
結論
我々は、L=H2O、MeOH、pyのCr2(OAc)4L2のサブミリスケール単結晶を合成するための実現可能かつ迅速な方法を開発しました。 成功への鍵は、Cr2(OAc)4の結晶性粉末を溶解する前に、配位子溶媒に溶解した酸化剤の除去である。 また、特定の配位子溶媒中のCr2(OAc)4の溶解は、無水酢酸Cr(II)(ルイス酸)と配位子分子(ルイス塩基)との間に配位結合が形成される場合にのみ起こる。 その結果,種々の分子が軸配位子として配位して結合した有機金属錯体を容易なプロセスによって増殖させることができることを示した。 このような汎用性とシンプルさは、パドルホイール配位子と金属原子を置き換えるためにさらに拡張することができ、M-M連鎖配位ポリマーや金属–有機骨格などのM–Mベースのネットワークシステムの大部分を開発するためにさらに多様な組み合わせを達成することができる。 このような新しい錯体の設計と調製は、デルタ軌道と多重結合の基本的な理解と物理学、化学、および関連工学の様々な分野への応用に貢献するであろう。
利益相反
宣言すべき矛盾はありません。
謝辞
忠南大学のミンジョン-ユン教授と浦項科学技術大学のチェ-ヒチョル教授に貴重なコメントを感謝している。 この作品は2018年にウォンクワン大学によって支援されました。
メモと参考文献
- F. A.Cotton,C.A.Murillo and R.A.Walton,Multiple Bonds Between Metal Atoms,Springer-Verlag,New York,2005Search PubMed.
- F.A.Cotton,B.G.DeBoer,M.D.LaPrade,J.R.Pipal and D.A.Ucko,J.Am. ケム Soc.、1970、92、2926-2927CrossRef CAS。
- T.Nguyen,A.D.Sutton,M.Brynda,J.C.Fettinger,G.J.Long and P.P.Power,Science,2005,310,844-847CrossRef CAS PubMed.
- F.R.Wagner,A.Noor and R.Kempe,Nat. ケム,2009,1,529-536CrossRef CAS PubMed.
- K.A.Kreisel,G.P.A.Yap,O.Dmitrenko,C.R.Landis and K.H.Theopold,J. アム… ケム Soc.,2007,129,14162-14163CrossRef CAS PubMed.
- A.Falceto,K.H.Theopold and S.Alvarez,Inorg. ケム,2015,54,10966-10977CrossRef CAS PubMed.
- F.A.Cotton,H.Chen,L.M.Daniels and X.Feng,J.Am. ケム Soc.,1992,114,8980-8983CrossRef CAS.
- E.D.Bloch,W.L.Queen,M.R.Hudson,J.A.Mason,D.J.Xiao,L.J.Murray,R.Flacau,C.M.Brown and J.R.Long,Angew. ケム,Int. エド,2016,55,8605-8609CrossRef CAS PubMed.
- L.J.Murray,M.Dinca,J.Yano,S.Chavan,S.Bordiga,C.M.Brown,J.R.Long,J.Am. ケム Soc.,2010,132,7856-7857CrossRef CAS PubMed.
- F.A.Cotton and C.B.Harris,Inorg. ケム,1965,4,330-333CrossRef CAS.
- W.Clegg,C.D.Garner,L.Akhter and M.H.Al-Samman,Inorg. ケム,1983,22,2466-2468CrossRef CAS.
- F.A.Cotton,C.E.Rice and G.W.Rice,J.Am. ケム Soc. 1977,99,4704-4707CrossRef CAS.
- S.N.KetkarおよびM.Fink,J.Am. ケム Soc.、1985、107、338-340CrossRef CAS。
- Pourbaix,atlas of electrochemical equilibria in aqueous solutions,National Association of Corrosion Engineers,1974Search PubMed.
- F.A.Cotton,E.A.Hillard,C.A.Murillo and H.C.Zhou,J.Am. ケム Soc.,2000,122,416-417CrossRef CAS.
- F.A.Cotton and T.R.Felthouse,Inorg. ケム,1980,19,328-331CrossRef CAS.
- J.C.Reeve,J.Chem. エデュック…,1985,62,444CrossRef CAS.
- F.A.Cotton,M.W.Extine and G.W.Rice,Inorg. ケム,1978,17,176-186CrossRef CAS.
- H.-C.Chang,J.-T.Li,C.-C.Wang,T.-W.Lin,H.-C.Lee,G.-H. LeeおよびS.-M.Peng,Eur. J.Inorg. ケム,1999,1999,1243-1251CrossRef.
- M.Yang,T.-W.Lin,C.-C.Chou,H.-C.Lee,H.-C.Chang,G.-H.Lee,M.Leung and S.-M.Peng,Chem. コミュ…、1997年、2279-2280RSC。
- L.J.Murray,M.Dinca,J.Yano,S.Chavan,S.Bordiga,C.M.Brown,J.R.Long,J.Am. ケム Soc.,2010,132,7856-7857CrossRef CAS PubMed.
- O.Levy,B.Bogoslavsky and A.Bino,Inorg. チム Acta,2012,391,179-181CrossRef CAS.
- F.A.Cotton,B.G.DeBoer,M.D.LaPrade,J.R.Pipal and D.A.Ucko,Acta Crystallogr.、セクト。 B:構造体。 クリスタルグルー… クライスト ケム,1971,27,1664-1671CrossRef CAS.
- R.D.CannonとJ.S.Stillman,Inorg. ケム、1975、14、2207-2214CrossRef CAS。
- Y.M.Huang,H.R.Tsai,S.H.Lai,S.J.Lee,I.C.Chen,C.L.Huang,S.M.Peng and W.Z.Wang,J.Phys. ケム C,2011,115,13919-13926CrossRef CAS.
- R.E.Da Re,J.L.Eglin,C.N.Carlson,K.D.John,D.E.Morris,W.H.Woodruff,J.A.Bailey,E.Batista,R.L.Martin,F.A.Cotton,E.A.Hillard,C.A.Murillo,A.P.Sattelberger and R.J.Donohoe,J.Am. ケム Soc.,2010,132,1839-1847CrossRef CAS PubMed.
- W.C.Trogler and H.B.Gray,Acc. ケム Res.,1978,11,232-239CrossRef CAS.
- F.A.Cotton,P.E.Fanwick,R.H.Niswander,J.C.Sekutowski,J.Am. ケム Soc. 1978,100,4725-4732CrossRef CAS.
- R.E.Da Re,J.L.Eglin,C.N.Carlson,K.D.John,D.E.Morris,W.H.Woodruff,J.A.Bailey,E.Batista,R.L.Martin,F.A.Cotton,E.A.Hillard,C.A.Murillo,A.P.Sattelberger and R.J.Donohoe,J.Am. ケム Soc.,2010,132,1839-1847CrossRef CAS PubMed.
- Cr2(OAc)4(py)2の場合、650cm−1付近の強いピークではなく、680cm−1付近の弱いピークが倍音モードとして割り当てられていたことに注意してください。 他の錯体に共通しているCr2(OAc)(py)2のラマンピークは珍しいピークよりも実質的に弱いので、この割り当ては、それにもかかわらず、許容されます。.
- Cr2(OAc)4(H2O)2:C8H12O10Cr2、Mr=372.18、結晶寸法0.10×0.09×0.02mm3、単斜晶系、C2/c、a=13.105(3)Å、b=8.5680(17)Å、c=13.838(3)Å、β=116.71(3)°、v=1388。0(6)Å3,T=-173°C,Z=4,rcal=1.781g cm−3,m=0.15cm−1,2076年のユニークな反射(I>2s(I),94個のパラメータ,2.925°<q<29.848°,R1=0.0425,Wr2=0.1183,GOF=0.927 CCDC預金番号1131602..Cr2(OAc)4(MeOH)2:C10H18O10Cr2、Mr=402.24、結晶寸法0.05×0.04×0.05mm3、単斜晶系、P21/n、a=8.0650(16)Å、b=7.4060(15)Å、c=13.296(3)Å、β=92.84(3)°,v=793.2(3)Å3,T=−173°C,Z=2,Rcal=1.684G Cm−3,m=0.135cm-1,2197i>2s(i)を持つ2277のうちのユニークな反射,105パラメータ,3.102° < q < 29.841°, R1 = 0.0439, wR2 = 0.1198, GOF = 0.862. Refer to ref. 7..
- Cr2(OAc)4(py)2: C18H22O8N2Cr2, Mr = 496.36, crystal dimensions 0.09 × 0.08 × 0.09 mm3, orthorhombic, Pbca, a = 12.875(3) Å, b = 8.5890(17) Å, c = 19.524(4) Å, V = 2159.0(7) Å3, T = −173 °C, Z = 4, rcal= 1.533 g cm−3, m = 0.10 cm−1, 2797 unique reflections out of 3243 with I > 2s(I), 138 parameters, 2.579° < q < 29.860°, R1 = 0.0452, wR2 = 0.1206, GOF = 1.043. CCDC deposit number 1100915..
脚注
† 利用できる電子補足情報(ESI)。 参照DOI:10.1039/c9ra04189c