solusykli on tapahtumasarja, joka säätelee solun elämää. Tämä asetus syntyy useiden eri säätelyteiden signaalien yhdistelmästä, jotka aktivoituvat vastauksena tiettyihin ärsykkeisiin. Solusyklillä on keskeinen rooli solujen kasvun ja proliferaation säätelyssä. Se joutuu usein geneettisen muuntelun kohteeksi, jonka kertyminen voi johtaa näiden järjestettyjen tapahtumien sääntelyn purkamiseen ja saattaa liittyä syövän puhkeamiseen. Lisääntyvän ymmärryksen solusyklin säätelyn tärkeästä roolista kasvainmuodostuksessa ja apoptoosissa solusyklin estäjiä on tutkittu edelleen syövän hoidossa.
Sykliinistä riippuvaiset kinaasit (CDK)
eteneminen solusyklin läpi varmistetaan tietyillä proteiinikomplekseilla, sykliinistä riippuvaisilla kinaasilla (CDKs). CDK: t ovat hyvin säilyneiden seriini – /treoniinikinaasien suku, joilla on korkea homologia tietyllä alueella. CDK voi ohjata solusykliä fosforyloimalla erilaisia kohteita, jotka puolestaan voivat aktivoitua tai inaktivoitua. CDK/sykliiniaktiivisuuden säätely voi tapahtua säätelevien proteiinien, kuten CDK-estäjien (CKIs) kautta. CKIs voi estää CDK: n aktiivisuutta liittymällä in vivo CDK-alayksikköön, sykliiniin tai sykliini/CDK-kompleksiin. Tämä inhibitio voi tapahtua eri tavoin, kuten estämällä CDK-kinaasiaktiivisuutta, häiritsemällä CAK-välitteistä CDK-aktivaatiota tai kilpailemalla sykliinien kanssa sitoutumisessa katalyyttiseen alayksikköön. Inhibitorinen prosessi voidaan suorittaa yhdellä tai näiden mekanismien yhdistelmällä. Näiden CKIs: ien ilmentymistä voivat indusoida ärsykkeet, kuten vanheneminen, kontaktin estäminen, solunulkoiset anti-mitogeeniset tekijät ja solusyklin tarkistuspisteet.
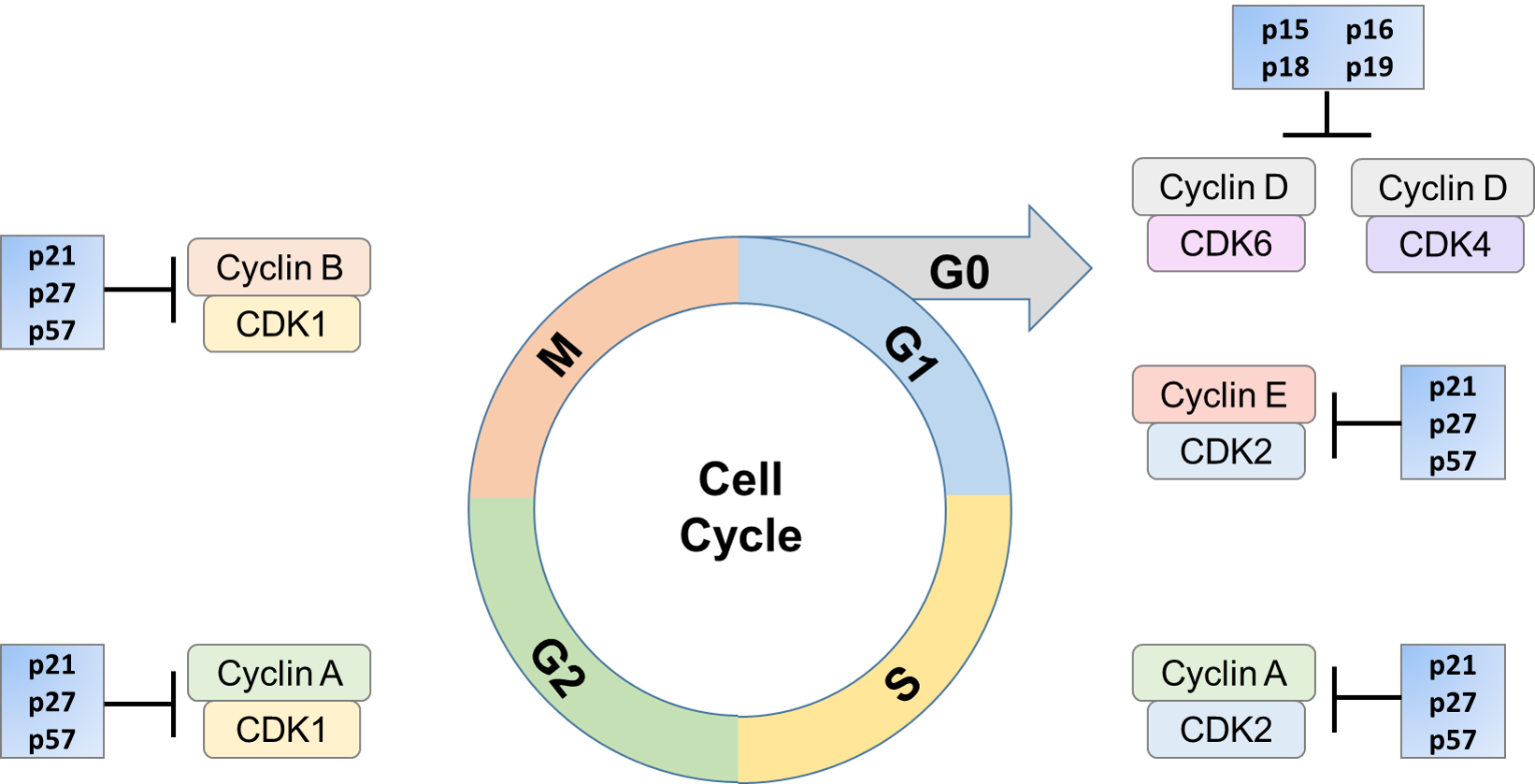
niiden rooli solusyklin säätelyssä on ratkaiseva. Useissa syövän muodoissa CKIs, kuten p16 ja p27, mutatoituvat. Lisäksi niiden on todettu halventavan useita syöpätyyppejä. Pienet p27-tasot korreloivat huonon kliinisen ennusteen kanssa. Näitä estäjiä voidaan tarvittaessa säätää uudelleen, jolloin sykliini estää CDK: n aktivoitumisen. Tämä pidättää solun tietyssä solusyklin osassa, kunnes olosuhteet ovat sellaiset, että se voi jatkaa proliferaatiota tai tarvittaessa ohjata sitä kohti solukuolemaa.
- INK4-suku
Kkisukuja on kaksi. Ensimmäiseen perheeseen kuuluvat INK4-proteiinit (cdk4: n inhibiittorit), jotka ovat saaneet nimensä kyvystään erityisesti inhiboida CDK4: n ja CDK6: n katalyyttisiä alayksiköitä. Tähän perheeseen kuuluu neljä proteiinia, p16INK4a, p15INK4b, p18INK4c ja p19INK4d. nämä proteiinit koostuvat useista aniirin toistoista ja sitoutuvat vain CDK4: ään ja CDK6: een.
| INK4 | kuvaus |
| P15 | Sykliinistä riippuvainen kinaasi 4: n estäjä B, joka tunnetaan myös nimellä multiple tuumorisuppressori 2 (MTS-2) tai p15INK4b, indusoituu TGF-hoidon avulla ja ilmenee kaikkialla. Proteiinia koodaa ihmisillä CDKN2B-geeni, joka poistetaan usein ihmisen syövissä, mikä viittaa siihen, että geenin häviämisellä voi olla merkittävä vaikutus tietyntyyppisten kasvainten kehittymiseen. |
| CDKN2A-geeni koodaa ihmisillä P16 | p16, joka tunnetaan myös nimillä p16ink4a, sykliiniriippuvainen kinaasi-inhibiittori 2A ja multippeli tuumorisuppressori 1. Se tunnistettiin kahden hybridin seulonnassa käyttäen CDK4: ää syöttinä. p16 voi estää CDK4: n ja CDK6: n toiminnan eristämällä katalyyttisen alayksikön tai estämällä valmiiksi koottujen kompleksien kinaasiaktiivisuuden. Johtuen siitä, että useat ihmisen syövät liittyvät P16-toiminnan menetykseen, tätä geeniä ehdotettiin tuumorisuppressoriksi in vivo. |
| p18 | P18, joka tunnetaan myös sykliiniriippuvaisena kinaasi 4: n inhibiittorina C, on entsyymi, jota ihmisellä koodaa CDKN2C-geeni. p18: n on osoitettu olevan vuorovaikutuksessa CDK4: n tai CDK6: n kanssa ja estävän CDK-kinaasien aktivoitumista, jolloin se toimii solukasvun säätelijänä, joka ohjaa solusyklin G1 etenemistä. Sekä p18 että p19 jakautuvat laajasti eri solutyyppeihin ja kudoksiin. |
| p19 | P19, joka tunnetaan myös sykliiniriippuvaisena kinaasi 4: n inhibiittorina D, on entsyymi, jota ihmisellä koodaa CDKN2D-geeni. Eräissä solutyypeissä P19-tasot värähtelevät solusyklin aikana ja käyvät läpi induktion solujen siirtyessä s-vaiheeseen. p19 voi toimia säätelemällä sykliini-D-riippuvaisten kinaasien aktiivisuutta solujen poistuessa G1-faasista. Kaikilla neljällä estäjällä on samanlaiset ominaisuudet ja ne voivat reagoida eri tavoin anti-proliferatiivisiin signaaleihin. |
- CIP/KIP-suku
jälkimmäinen suku koostuu Cip / Kip-suvun jäsenistä, ja siihen kuuluvat p21Cip1, p27Kip1 ja p57Kip2, jotka kaikki sisältävät aminoterminaaliosuuksissaan tyypillisiä motiiveja, joiden avulla ne voivat sitoutua sekä sykliini-että CDK-alayksiköihin. Cip-perheen jäsenet sitoutuvat aktiiviseen sykliini/CDK-kompleksiin ja estävät sitä.
| CIP / KIP | kuvaus |
| CDKN1A-geeni koodaa ihmisillä P21 | p21cip1: tä, joka tunnetaan myös sykliiniriippuvaisena kinaasi-inhibiittorina 1 tai CDK-vuorovaikutteisena proteiinina 1, ja se voi toimia voimakkaana ja yleisenä CDK-aktiivisuuden estäjänä. Se estää CDK2 -, CDK4-ja CDK6-kinaaseja ja kykenee indusoimaan solusyklin pysähtymistä G1: ssä yliekspressoituna. Normaalisti syklisissä soluissa p21 on kompleksissa sykliinin / CDK: n kanssa. |
| P27 | Sykliinistä riippuvainen kinaasi-inhibiittori 1B (p27Kip1) on entsyymin inhibiittori, jota ihmisellä koodaa CDKN1B-geeni. p27 tunnistettiin TGF: n aiheuttamaa kasvua estävää aktiivisuutta koskeneessa tutkimussarjassa, ja toisessa tutkimuksessa se eristettiin kahden hybridin seulonnalla käyttäen CDK4: ää syöttinä. p27 muistuttaa rakenteellisesti p21: tä ja estää CDK2 -, CDK3 -, CDK4-ja CDK6-komplekseja in vitro. |
| p57 | Sykliinistä riippuvainen kinaasi-inhibiittori 1C (p57, Kip2) on proteiini, jota ihmisellä koodaa CDKN1C-geeni. p57 sitoutuu ja estää useita sykliini / CDK-komplekseja ja sen ilmentyminen näyttää olevan kudosrajoitteista. p57, kuten p27, ei näytä tarvitsevan p53: A ja pRb: tä toimiakseen. p57 kartoittaa 11p15-kromosomin lokuksen, jossa tapahtuu usein poistoja tai uudelleenjärjestelyjä monissa ihmisen syövän muodoissa. |
Tuumorisuppressori ja solusyklin ohjaus
Tuumorimuutos on monivaiheinen prosessi, johon liittyy proto-onkogeeneihin tai tuumorisuppressorigeeneihin vaikuttavien geneettisten leesioiden klooninen kertyminen. Näiden geenien tuotteilla on myöhemmin tärkeä rooli signaalin transduktioradoissa säätelemällä solusykliä, solujen erilaistumista ja jopa solukuolemaa. Nyt on yhä enemmän näyttöä siitä, että normaali solusyklin eteneminen on seurausta tasapainoisesta vuorovaikutuksesta useiden säätelytekijöiden, kuten tuumorisuppressorigeenituotteiden ja solusykliin liittyvien proteiinien, välillä. Ei ole yllättävää, että perustason muutokset tuumorisuppressorigeeneissä voivat johtaa sääntelemättömään solusykliin ja lopulta tuumorimuutokseen. Siksi ihmiset saattavat määritellä syövän perinnölliseksi solusyklin sairaudeksi.
tuumorisuppressorin prototyypin geenit ovat p53 ja RB. Osallistuminen näiden tuumorisuppressorigeenien syöpään on yleistä ja usein geenit osoittavat suurta spesifisyyttä tiettyjen kasvaintyyppien. Yleisin näistä geeneistä löydetty muutos on deleetio tai pistemutaatio. Lisäksi tuumorisuppressorigeenien inaktivoituminen voi johtua vuorovaikutuksesta viruksen onkoproteiinien kanssa. Itse asiassa virusaineet pystyvät integroitumaan isännän geneettiseen materiaaliin ja voivat häiritä normaalin solukasvun ja proliferaation säätelyä vuorovaikutuksessa tuumorisuppressorigeenien, kuten p53-ja pRb-perheiden, toiminnan kanssa.
solun säätely ja solusyklin säätely
solusykli ei ole itsenäinen solumekanismi, vaan prosessi, joka liittyy läheisesti muihin solun säätelymekanismeihin. Esimerkiksi kromatiinin remodelaatiota säätelevät proteiinit vaikuttavat myös solusykliin, kuten ADNP-geeni; solujen energia-aineenvaihduntaa estävät proteiinit estävät myös solusykliä, kuten ALDH1L1; syöpäsolujen kasvua ja kromatiinin tiivistymistä estävät proteiinit voivat toimia myös solusyklin inhibiittoriproteiineina, kuten ASB2. Muu soluprosessi, mukaan lukien apoptoosi, solujen kasvu, ubikitinaatio, kalsiumvastaava transkriptio jne., voi vaikuttaa normaaliin solusykliin. Solubiologia on monimutkainen ja vuorovaikutteinen verkko, joten solusyklin estäjien mekanismien ymmärtämiseksi sinun on ymmärrettävä multiplex-solujen säätelyprosessi.
johtopäätös
solusyklin estäjillä on laajat mahdollisuudet ihmisen syöpähoidossa. Erilaisia CDK-estäjiä on kliinisissä ja prekliinisissä tutkimuksissa. Aiemmat tutkimukset ovat osoittaneet, että nämä lääkkeet voivat estää solusyklin ja aiheuttaa apoptoosin kasvainsoluissa. Kliinisissä tutkimuksissa paras vaikutus näillä lääkkeillä voidaan saavuttaa on tilan vakauttaminen. Yleensä solusyklin estäjät ovat yksi syövän hoidon tehokkaista strategioista ja ansaitsevat perusteellisia kokeita ja tutkimusta.