a sejtciklus az események sorozata, amelyek szabályozzák az élet a sejt. Ez a Szabályozás különböző szabályozási útvonalakból származó több jel kombinációjából származik, amelyek specifikus ingerekre reagálva aktiválódnak. A sejtciklus központi szerepet játszik a sejtnövekedés és a proliferáció szabályozásában. Gyakran válik a genetikai változás célpontjává, amelynek felhalmozódása ezen rendezett események deregulációjához vezethet, és összefüggésben lehet a rák kialakulásával. A sejtciklus-szabályozás fontos szerepének megértésével a tumorképződésben és az apoptózisban a sejtciklus-inhibitorokat tovább tanulmányozták a rákkezelés területén.
ciklin-függő kináz (CDK) inhibitorok
a Sejtcikluson keresztüli progressziót bizonyos fehérjekomplexek, a ciklin-függő kinázok (CDK) biztosítják. A CDK-k egy erősen konzervált család szerin / treonin kinázok, amelyek egy adott régióban magas homológiával rendelkeznek. A CDK-k különböző célok foszforilezésével szabályozhatják a sejtciklust, amelyek viszont aktiválhatók vagy inaktiválhatók. A CDK/ciklin aktivitás szabályozása szabályozó fehérjék, például CDK-gátlók (cki-k) révén történhet. A cki-k gátolhatják a CDK aktivitását azáltal, hogy in vivo társulnak a CDK alegységhez, a ciklinhez vagy a ciklin/CDK komplexhez. Ez a gátlás különböző módon fordulhat elő, például a CDK kináz aktivitás gátlása, interferencia a CAK által közvetített CDK aktiválással, vagy verseny a ciklinekkel a katalitikus alegységhez való kötődésben. A gátló folyamat ezen mechanizmusok egyikével vagy kombinációjával hajtható végre. Ezen cki-k expresszióját olyan ingerek indukálhatják, mint az öregedés, a kontakt gátlás, az extracelluláris anti-mitogén faktorok és a sejtciklus ellenőrző pontjai.
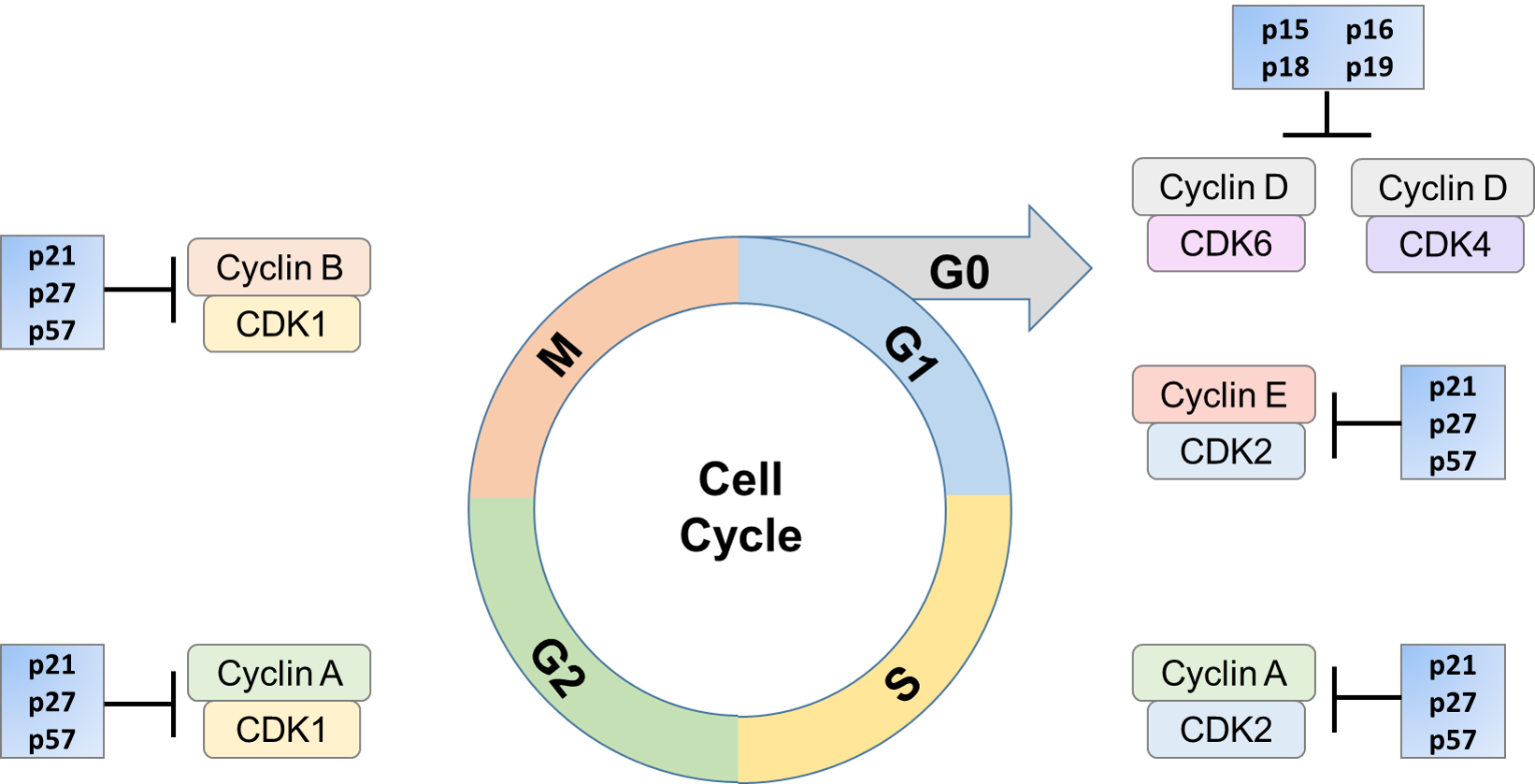
a sejtciklus szabályozásában betöltött szerepük döntő fontosságú. A rák számos formájában a cki-k, például a p16 és a p27 mutálódnak. Azt is megállapították, hogy a rák több típusában lebomlanak. A p27 alacsony szintje korrelál a rossz klinikai prognózissal. Ezek az inhibitorok szükség esetén szabályozhatók, ezáltal blokkolva a CDK ciklin általi aktiválását. Ez megállítja a sejtet a sejtciklus egy bizonyos részében, amíg a körülmények olyanok nem lesznek, Hogy folytatódhasson a proliferáció felé, vagy ha szükséges, a sejthalál felé irányuljon.
- INK4 család
a cki-knek két családja van. Az első családba tartoznak az INK4 fehérjék (a CDK4 inhibitorai), amelyeket azért neveztek el, mert képesek specifikusan gátolni a CDK4 és CDK6 katalitikus alegységeit. Ez a család négy fehérjét tartalmaz, a p16INK4a, a p15INK4b, a p18INK4c és a p19INK4d. ezek a fehérjék több ankirin ismétlődésből állnak, és csak a CDK4 és a CDK6-hoz kötődnek.
| INK4 | leírás |
| p15 | ciklin-függő kináz 4 inhibitor B, más néven többszörös tumorszuppresszor 2 (MTS-2) vagy p15INK4b, a TGF kezelés indukálja és mindenütt expresszálódik. A fehérjét az emberekben a CDKN2B gén kódolja, amelyet az emberi rákokban gyakran törölnek, ami arra utal, hogy a gén elvesztése jelentős lehet bizonyos típusú daganatok kialakulásában. |
| p16 | p16, más néven p16INK4a, ciklin-függő kináz inhibitor 2AÉS többszörös tumor szuppresszor 1, A CDKN2A gén kódolja az emberekben. Egy két hibrid szűrésen azonosították, a CDK4-et csaliként használva. a p16 képes blokkolni a CDK4 és CDK6 funkciókat a katalitikus alegység megkötésével vagy az előszerelt komplexek kináz aktivitásának blokkolásával. Annak a ténynek köszönhetően, hogy számos emberi rák társul a p16 funkció elvesztésével, ezt a gént in vivo tumorszuppresszorként javasolták. |
| p18 | a P18, más néven ciklinfüggő kináz 4 inhibitor C, egy enzim, amelyet emberben a CDKN2C gén kódol. kimutatták, hogy a p18 kölcsönhatásba lép a CDK4-gyel vagy a CDK6-tal, és megakadályozza a CDK kinázok aktiválódását, így sejtnövekedés-szabályozóként működik, amely szabályozza a sejtciklus G1 progresszióját. Mind a p18, mind a p19 széles körben elterjedt a különböző sejttípusokban és szövetekben. |
| p19 | p19, más néven ciklin-függő kináz 4 inhibitor D, egy enzim, amelyet emberben a CDKN2D gén kódol. Egyes sejttípusokban a P19 szint a sejtciklus alatt oszcillál, indukción megy keresztül, amikor a sejtek belépnek s fázis. a p19 a ciklin d-függő kinázok aktivitásának szabályozásával működhet, amikor a sejtek kilépnek a G1 fázisból. Mind a négy inhibitor hasonló tulajdonságokkal rendelkezik, és eltérő módon reagálhatnak az anti-proliferatív jelekre. |
- CIP / KIP család
ez utóbbi család a Cip/Kip család tagjaiból áll, és magában foglalja a p21Cip1-et, a p27Kip1-et és a p57Kip2-t, amelyek mindegyik amino-terminális részükön belül olyan jellegzetes motívumokat tartalmaznak, amelyek lehetővé teszik mind a ciklin, mind a CDK alegységekhez való kötődést. A Cip család tagjai kötődnek és gátolják az aktív ciklin / CDK komplexet.
| CIP / KIP | leírás |
| p21 | p21Cip1, más néven ciklin-függő kináz inhibitor 1 vagy CDK-kölcsönható fehérje 1, kódolja a CDKN1A gén emberben, és működhet, mint egy erős és univerzális inhibitora CDK aktivitás. Gátolja a CDK2, CDK4 és CDK6 kinázokat, és képes sejtciklus-leállást indukálni a G1-ben, ha túlexpresszálják. Normál ciklikus sejtekben a p21 komplexben van ciklin/CDK. |
| p27 | ciklin-függő kináz inhibitor 1B (p27Kip1) egy enzim inhibitor, amelyet emberben a CDKN1B gén kódol. a p27-et a TGF által kiváltott növekedésgátló aktivitással kapcsolatos vizsgálatok sorozatában azonosították, egy másik vizsgálatban pedig két hibrid szűréssel izolálták, csaliként CDK4-et használva. a p27 szerkezetileg rokon a p21-gyel, és in vitro gátolja a CDK2, CDK3, CDK4 és CDK6 komplexeket. |
| p57 | ciklin-függő kináz inhibitor 1C (p57, Kip2) olyan fehérje, amelyet emberben a CDKN1C gén kódol. a p57 számos ciklin/CDK komplexhez kötődik és gátolja, és expressziója szöveti korlátozottnak tűnik. úgy tűnik, hogy a p57, akárcsak a p27, nem igényli a p53-at és a pRb-t a működéséhez. a p57 a 11p15 kromoszómális lókuszra térképez, amely az emberi rák számos formájában gyakori deléciókon vagy átrendeződéseken megy keresztül. |
Tumor szuppresszor és sejtciklus kontroll
a Tumor transzformáció egy többlépcsős folyamat, amely magában foglalja a proto-onkogéneket vagy tumorszuppresszor géneket érintő genetikai elváltozások klonális felhalmozódását. Ezeknek a géneknek a termékei később fontos szerepet játszanak a jelátviteli útvonalakban a sejtciklus, a sejtdifferenciálódás, sőt a sejthalál szabályozásával. Egyre több bizonyíték van arra, hogy a normális sejtciklus progressziója több szabályozó tényező, például a tumorszuppresszor géntermékek és a sejtciklushoz kapcsolódó fehérjék kiegyensúlyozott kölcsönhatásának eredménye. Nem meglepő, hogy a tumor szuppresszor gének alapvető változásai szabályozatlan sejtciklust és esetleges tumor transzformációt eredményezhetnek. Ezért az emberek meghatározhatják a rákot a sejtciklus genetikai betegségeként.
a tumor-szuppresszor gének prototípusa a p53 és az RB. Ezeknek a tumor-szuppresszor géneknek a részvétele a rákban széles körben elterjedt, és gyakran a gének nagy specificitást mutatnak bizonyos tumortípusokra. Ezekben a génekben a leggyakoribb változást deléció vagy pontmutáció képviseli. Ezenkívül a tumor-szuppresszor gének inaktiválása a vírusos onkoproteinekkel való kölcsönhatásból eredhet. Valójában a vírusok képesek integrálni a gazdaszervezet genetikai anyagába, és zavarhatják a normális sejtnövekedés és proliferáció szabályozását azáltal, hogy kölcsönhatásba lépnek a tumor szuppresszor gének, például a p53 és a pRb családok funkciójával.
Sejtszabályozás és sejtciklus-Szabályozás
a sejtciklus nem független sejtmechanizmus, hanem olyan folyamat, amely szorosan kapcsolódik más sejtszabályozó mechanizmusokhoz. Például a kromatin átalakítását szabályozó fehérjék szintén befolyásolják a sejtciklust, például az ADNP gént; a sejtenergia-anyagcserét gátló fehérjék szintén gátolják a sejtciklust, például az ALDH1L1; a rákos sejtek növekedését gátló fehérjék és a kromatin kondenzáció szintén sejtciklus-gátló fehérjékként működhetnek, mint például az ASB2. Egyéb sejtfolyamat, beleértve az apoptózist, a sejtnövekedést, az ubiquitinációt, a kalciumra reagáló transzkripciót, et al., befolyásolhatja a normál sejtciklust. A sejtbiológia összetett és kölcsönhatásban lévő hálózat, ezért a sejtciklus-gátlók mechanizmusainak teljes megértéséhez meg kell értenie a multiplex sejtszabályozási folyamatot.
következtetés
a sejtciklus-gátlók széles kilátásokkal rendelkeznek az emberi rákterápia területén. A klinikai és preklinikai vizsgálatokban számos CDK inhibitor található. Korábbi tanulmányok kimutatták, hogy ezek a gyógyszerek gátolhatják a sejtciklust és apoptózist indukálhatnak a tumorsejtekben. A klinikai vizsgálatok során a legjobb hatás, amelyet ezek a gyógyszerek elérhetnek, az állapot stabilizálása. Általában a sejtciklus-gátlók az egyik hatékony stratégia a rák kezelésében, és érdemesek mélyreható kísérletekre és kutatásokra.