Der Zellzyklus ist die Reihe von Ereignissen, die das Leben der Zelle regulieren. Diese Regulation resultiert aus einer Kombination mehrerer Signale verschiedener Regulationspfade, die als Reaktion auf bestimmte Reize aktiviert werden. Der Zellzyklus spielt eine zentrale Rolle bei der Kontrolle des Zellwachstums und der Zellproliferation. Es wird häufig zum Ziel genetischer Veränderungen, deren Anhäufung zur Deregulierung dieser geordneten Ereignisse führen und mit dem Auftreten von Krebs zusammenhängen kann. Mit dem wachsenden Verständnis der wichtigen Rolle der Zellzyklusregulation bei der Tumorbildung und Apoptose wurden Zellzyklushemmer auf dem Gebiet der Krebsbehandlung weiter untersucht.
Cyclin-abhängige Kinase (CDK)-Inhibitoren
Die Progression durch den Zellzyklus wird durch bestimmte Proteinkomplexe, die Cyclin-abhängigen Kinasen (CDKs), sichergestellt. Die CDKs sind eine Familie hochkonservierter Serin / Threonin-Kinasen, die in einer bestimmten Region eine hohe Homologie aufweisen. CDKs können den Zellzyklus steuern, indem sie verschiedene Ziele phosphorylieren, die wiederum aktiviert oder inaktiviert werden können. Die Regulation der CDK / Cyclin-Aktivität kann durch regulatorische Proteine wie CDK-Inhibitoren (CKIs) erfolgen. Die CKIs können die Aktivität von CDK hemmen, indem sie in vivo mit der CDK-Untereinheit, dem Cyclin oder dem Cyclin / CDK-Komplex assoziieren. Diese Hemmung kann auf verschiedene Arten erfolgen, wie z. B. Hemmung der CDK-Kinaseaktivität, Interferenz mit CAK-vermittelter CDK-Aktivierung oder Konkurrenz mit Cyclinen bei der Bindung an die katalytische Untereinheit. Der inhibitorische Prozess kann durch einen oder eine Kombination dieser Mechanismen durchgeführt werden. Die Expression dieser CKIs kann durch Stimuli wie Seneszenz, Kontaktinhibierung, extrazelluläre antimitogene Faktoren und Zellzyklus-Checkpoints induziert werden.
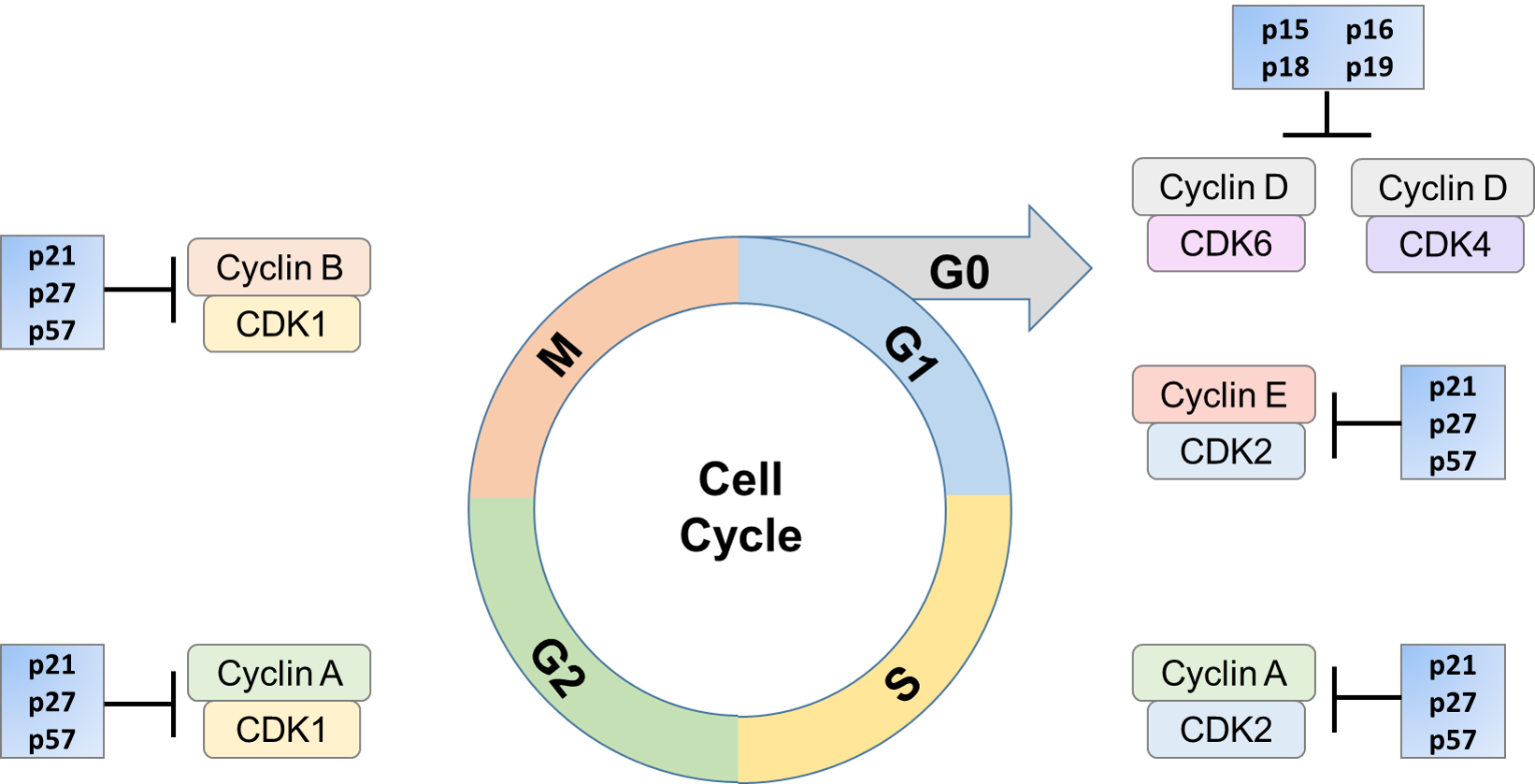
Ihre Rolle bei der Steuerung des Zellzyklus ist entscheidend. Bei verschiedenen Krebsformen sind CKIs wie p16 und p27 mutiert. Es wurde auch festgestellt, dass sie bei verschiedenen Krebsarten abgebaut werden. Niedrige p27-Spiegel korrelieren mit einer schlechten klinischen Prognose. Diese Inhibitoren können bei Bedarf hochreguliert werden, wodurch die Aktivierung des CDK durch ein Cyclin blockiert wird. Dadurch wird die Zelle in einem bestimmten Teil des Zellzyklus angehalten, bis die Bedingungen so sind, dass sie weiter in Richtung Proliferation oder, falls erforderlich, in Richtung Zelltod gesteuert werden kann.
- INK4-Familie
Es gibt zwei Familien von CKIs. Die erste Familie umfasst die INK4-Proteine (Inhibitoren von CDK4), die nach ihrer Fähigkeit benannt sind, die katalytischen Untereinheiten von CDK4 und CDK6 spezifisch zu hemmen. Diese Familie umfasst vier Proteine, p16INK4a, p15INK4b, p18INK4c und p19INK4d. Diese Proteine bestehen aus mehreren Ankirin-Wiederholungen und binden nur an CDK4 und CDK6.
| INK4 | Beschreibung |
| p15 | Cyclin-abhängiger Kinase-4-Inhibitor B, auch bekannt als multipler Tumorsuppressor 2 (MTS-2) oder p15INK4b, wird durch TGF-Behandlung induziert und ubiquitär exprimiert. Das Protein wird vom CDKN2B-Gen beim Menschen kodiert, das häufig bei menschlichen Krebsarten deletiert wird, was darauf hindeutet, dass der Verlust des Gens bei der Entwicklung bestimmter Arten von Tumoren signifikant sein kann. |
| p16 | p16, auch bekannt als p16INK4a, Cyclin-abhängiger Kinase-Inhibitor 2A und multipler Tumorsuppressor 1, wird beim Menschen vom CDKN2A-Gen kodiert. Es wurde in einem Zwei-Hybrid-Screening mit CDK4 als Köder identifiziert. p16 kann die CDK4- und CDK6-Funktion blockieren, indem es die katalytische Untereinheit sequestriert oder die Kinaseaktivität vormontierter Komplexe blockiert. Aufgrund der Tatsache, dass mehrere menschliche Krebsarten mit dem Verlust der p16-Funktion verbunden sind, wurde dieses Gen als Tumorsuppressor in vivo vorgeschlagen. |
| p18 | p18, auch bekannt als Cyclin-abhängiger Kinase-4-Inhibitor C, ist ein Enzym, das beim Menschen vom CDKN2C-Gen kodiert wird. es wurde gezeigt, dass p18 mit CDK4 oder CDK6 interagiert und die Aktivierung der CDK-Kinasen verhindert, wodurch es als Zellwachstumsregulator fungiert, der das Fortschreiten des Zellzyklus G1 steuert. Sowohl p18 als auch p19 sind in verschiedenen Zelltypen und Geweben weit verbreitet. |
| p19 | p19, auch bekannt als Cyclin-abhängiger Kinase-4-Inhibitor D, ist ein Enzym, das beim Menschen vom CDKN2D-Gen kodiert wird. In einigen Zelltypen oszillieren die p19-Spiegel während des Zellzyklus und werden induziert, wenn Zellen in die S-Phase eintreten. p19 kann funktionieren, indem es die Aktivität von Cyclin-D-abhängigen Kinasen reguliert, wenn Zellen die G1-Phase verlassen. Alle vier Inhibitoren haben ähnliche Eigenschaften und können unterschiedlich auf antiproliferative Signale reagieren. |
- CIP / KIP-Familie
Die letztere Familie setzt sich aus den Mitgliedern der Cip / Kip-Familie zusammen und umfasst p21Cip1, p27Kip1 und p57Kip2, die alle charakteristische Motive in ihren aminoterminalen Einheiten enthalten, die es ihnen ermöglichen, sowohl an Cyclin- als auch an CDK-Untereinheiten zu binden. Mitglieder der Cip-Familie binden an den aktiven Cyclin/CDK-Komplex und hemmen ihn.
| CIP/KIP | Beschreibung |
| p21 | p21Cip1, auch bekannt als Cyclin-abhängiger Kinase-Inhibitor 1 oder CDK-interagierendes Protein 1, wird vom CDKN1A-Gen beim Menschen codiert und kann als potenter und universeller Inhibitor der CDK-Aktivität wirken. Es hemmt CDK2-, CDK4- und CDK6-Kinasen und kann bei Überexpression einen Zellzyklusstillstand in G1 induzieren. In normalerweise zyklischen Zellen ist p21 mit Cyclin / CDK komplex. |
| p27 | Cyclin-abhängiger Kinase-Inhibitor 1B (p27Kip1) ist ein Enzyminhibitor, der beim Menschen durch das CDKN1B-Gen kodiert wird. p27 wurde in einer Reihe von Studien zur durch TGF induzierten wachstumshemmenden Aktivität identifiziert und in einer anderen Studie durch ein Zwei-Hybrid-Screening unter Verwendung von CDK4 als Köder isoliert. p27 ist strukturell mit p21 verwandt und hemmt CDK2-, CDK3-, CDK4- und CDK6-Komplexe in vitro. |
| p57 | Cyclin-abhängiger Kinase-Inhibitor 1C (p57, Kip2) ist ein Protein, das beim Menschen durch das CDKN1C-Gen kodiert wird. p57 bindet an und hemmt mehrere Cyclin / CDK-Komplexe und seine Expression scheint gewebsbeschränkt zu sein. p57 scheint wie p27 p53 und pRb für seine Funktion nicht zu benötigen. p57 bildet den Chromosomenlocus 11p15 ab, der bei vielen Formen von menschlichem Krebs häufigen Deletionen oder Umlagerungen unterliegt. |
Tumorsuppressor und Zellzykluskontrolle
Die Tumortransformation ist ein mehrstufiger Prozess, bei dem genetische Läsionen, die Protoonkogene oder Tumorsuppressorgene betreffen, klonal akkumuliert werden. Die Produkte dieser Gene spielen später eine wichtige Rolle in Signaltransduktionswegen, indem sie den Zellzyklus, die Zelldifferenzierung und sogar den Zelltod steuern. Es gibt nun zunehmend Hinweise darauf, dass ein normaler Zellzyklusverlauf das Ergebnis einer ausgewogenen Interaktion zwischen mehreren regulatorischen Faktoren wie Tumorsuppressor-Genprodukten und zellzyklusassoziierten Proteinen ist. Es ist nicht überraschend, dass grundlegende Veränderungen in Tumorsuppressorgenen zu einem ungeregelten Zellzyklus und einer eventuellen Tumortransformation führen können. Daher können Menschen Krebs als eine genetische Erkrankung des Zellzyklus definieren.
Die Prototyp-Tumorsuppressorgene sind p53 und RB. Die Beteiligung dieser Tumorsuppressorgene an Krebs ist weit verbreitet und oft zeigen die Gene eine große Spezifität für bestimmte Tumortypen. Die häufigste Veränderung in diesen Genen wird durch Deletion oder Punktmutation dargestellt. Darüber hinaus kann die Inaktivierung von Tumorsuppressorgenen aus der Interaktion mit viralen Onkoproteinen resultieren. Tatsächlich sind virale Wirkstoffe in der Lage, sich in das genetische Material des Wirts zu integrieren, und können die Regulation des normalen Zellwachstums und der Proliferation stören, indem sie mit der Funktion von Tumorsuppressorgenen wie den Familien p53 und pRb interagieren.
Zellregulation und Zellzykluskontrolle
Der Zellzyklus ist kein unabhängiger zellulärer Mechanismus, sondern ein Prozess, der eng mit anderen zellulären Regulationsmechanismen zusammenhängt. Zum Beispiel beeinflussen Proteine, die den Chromatinumbau regulieren, auch den Zellzyklus, wie das ADNP-Gen; proteine, die den zellulären Energiestoffwechsel hemmen, hemmen auch den Zellzyklus, wie ALDH1L1; Proteine, die das Wachstum von Krebszellen und die Chromatinkondensation hemmen, können auch als Zellzyklusinhibitorproteine wie ASB2 wirken. Andere Zellprozesse, einschließlich Apoptose, Zellwachstum, Ubiquitinierung, Calcium-Responsive-Transkription, et al., kann den normalen Zellzyklus beeinflussen. Um die Mechanismen von Zellzyklusinhibitoren vollständig zu verstehen, müssen Sie den Multiplex-Zellregulationsprozess verstehen.
Schlussfolgerung
Zellzyklusinhibitoren haben breite Perspektiven auf dem Gebiet der Krebstherapie beim Menschen. Eine Vielzahl von CDK-Inhibitoren befindet sich in klinischen und präklinischen Studien. Frühere Studien haben gezeigt, dass diese Medikamente den Zellzyklus hemmen und Apoptose in Tumorzellen induzieren können. In klinischen Studien ist die beste Wirkung, die diese Medikamente erzielen können, die Stabilisierung des Zustands. Im Allgemeinen sind Zellzyklushemmer eine der wirksamen Strategien zur Krebsbehandlung und verdienen eingehende Experimente und Forschungen.