細胞周期は、細胞の寿命を調節する一連のイベントです。 この調節は、特定の刺激に応答して活性化される異なる調節経路からのいくつかの信号の組み合わせに起因する。 細胞周期は、細胞の増殖および増殖を制御する上で中心的な役割を有する。 それは頻繁に蓄積がこれらの順序されたでき事の規制緩和をもたらし、癌の手始めと関連しているかもしれない遺伝の変化のターゲットになります。 腫瘍形成およびアポトーシスにおける細胞周期調節の重要な役割の理解の成長に伴い、細胞周期阻害剤は、癌治療の分野でさらに研究されている。
サイクリン依存性キナーゼ(CDK)阻害剤
細胞周期を通る進行は、特定のタンパク質複合体であるサイクリン依存性キナーゼ(Cdk)によって保証される。 Cdkは、特定の領域で高い相同性を共有する高度に保存されたセリン/スレオニンキナーゼのファミリーです。 CDKは、異なる標的をリン酸化することによって細胞周期を制御してもよく、これは次に活性化または不活性化されてもよい。 CDK/サイクリン活性の調節は、CDK阻害剤(Cki)のような調節タンパク質を介して起こり得る。 Ckiは、CDKサブユニット、サイクリンまたはサイクリン/CDK複合体とin vivoで会合させることによってCDKの活性を阻害することができる。 この阻害は、CDKキナーゼ活性の阻害、CAK媒介CDK活性化への干渉、または触媒サブユニットへの結合におけるサイクリンとの競合など、様々な方法で起こり得る。 阻害プロセスは、これらの機構の1つまたは組み合わせによって実施することができる。 これらのCkiの発現は、老化、接触阻害、細胞外抗有糸分裂促進因子および細胞周期チェックポイントなどの刺激によって誘導され得る。
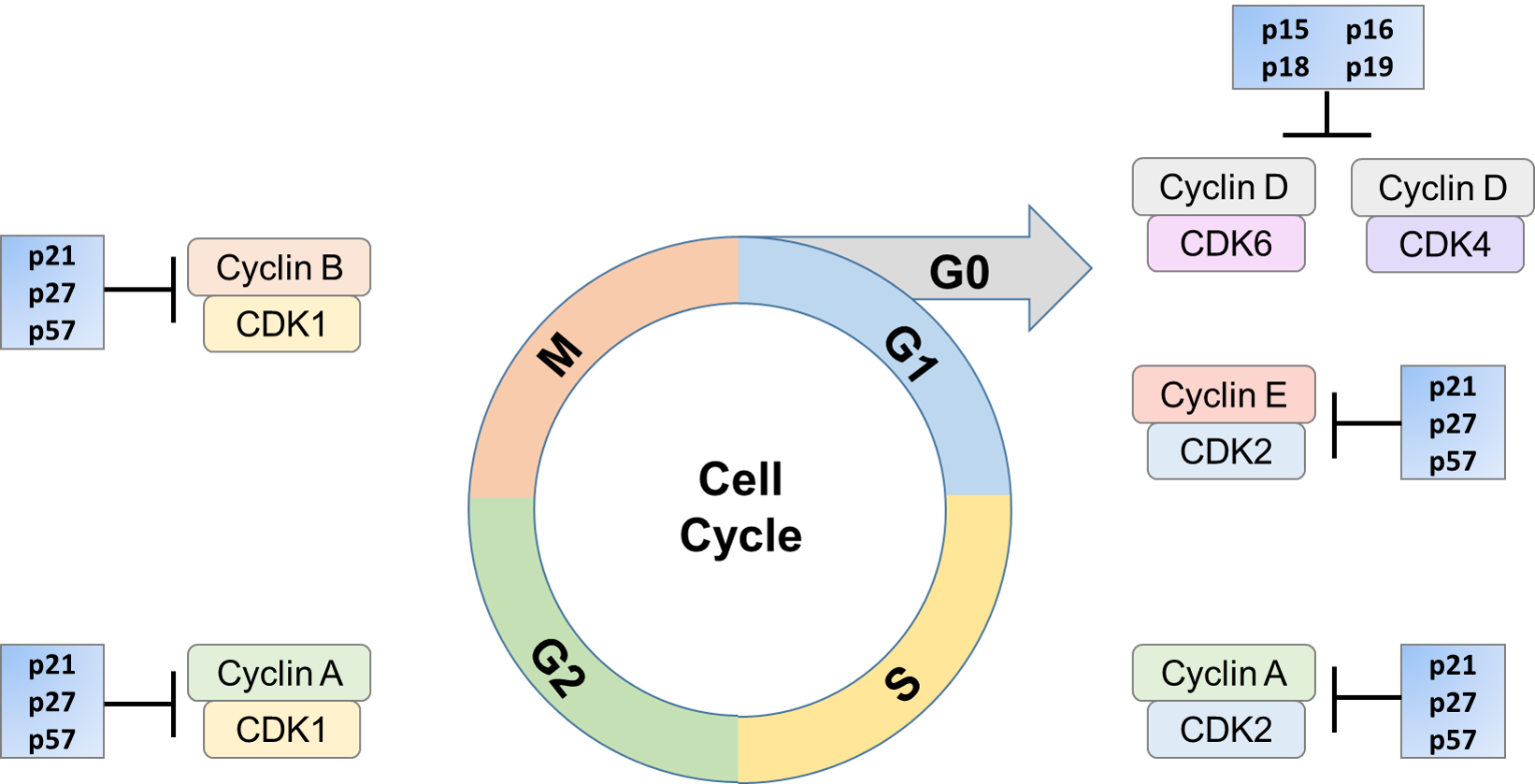
細胞周期の制御におけるそれらの役割は重要である。 いくつかの形態の癌では、p1 6およびp2 7などのCkiが変異している。 また、それらはいくつかのタイプの癌において分解されることが見出されている。 低レベルのp27レベルは、臨床予後不良と相関している。 これらの阻害剤は、必要に応じて上方制御され、したがってサイクリンによるCDKの活性化を遮断することができる。 これは、細胞周期の特定の部分の細胞を、増殖に向かって継続することができるか、または必要であれば、細胞死に向かって操縦されるような条件になるまで停止させる。
- INK4ファミリー
Ckiには二つのファミリーがあります。 最初のファミリーには、INK4タンパク質(CDK4の阻害剤)が含まれており、CDK4およびCDK6の触媒サブユニットを特異的に阻害する能力にちなんで命名された。 このファミリーには、p16ink4a、p15ink4b、p18ink4c、p19ink4dの四つのタンパク質が含まれており、これらのタンパク質は複数のアンキリンリピートから構成され、CDK4およびCDK6にのみ結合する。
| インク4 | 説明 |
| P15 | サイクリン依存性キナーゼ4阻害剤Bは、複数の腫瘍抑制剤2(MTS-2)またはp15ink4bとしても知られており、TGF治療によって誘導され、遍在的に発現 このタンパク質はヒトのCDKN2B遺伝子によってコードされており、ヒトの癌では頻繁に欠失されており、遺伝子の損失が特定のタイプの腫瘍の発症に有意である可能性があることを示唆している。 |
| p16 | p16は、p16ink4a、サイクリン依存性キナーゼ阻害剤2A、および複数の腫瘍抑制剤1としても知られており、ヒトのCDKN2A遺伝子によってコードされている。 これは、餌としてCDK4を使用して二ハイブリッドスクリーニングで同定された。 p16は、触媒サブユニットを隔離することによって、または事前に組み立てられた複合体のキナーゼ活性を遮断することによって、CDK4およびCDK6 いくつかのヒト癌がp16機能の喪失に関連しているという事実のために、この遺伝子はin vivoでの腫瘍抑制剤として提案された。 |
| p18 | p18は、サイクリン依存性キナーゼ4阻害剤Cとしても知られており、ヒトではCDKN2c遺伝子によってコードされる酵素である。 p18は、CDK4またはCDK6と相互作用し、CDKキナーゼの活性化を防止することが示されているため、細胞周期G1進行を制御する細胞増殖調節因子として機 P18およびp19の両方は、異なる細胞型および組織に広く分布している。 |
| p19 | p19は、サイクリン依存性キナーゼ4阻害剤Dとしても知られており、ヒトではCDKN2D遺伝子によってコードされる酵素である。 いくつかの細胞型では、p19レベルは細胞周期の間に振動し、細胞がS期に入ると誘導を受ける。 p19は、細胞がG1期を終了するとサイクリンD依存性キナーゼの活性を調節することによって機能することができる。 すべての4つの阻害剤は、同様の特性を共有し、抗増殖シグナルに異なる応答をすることができます。 |
- CIP/KIPファミリー
後者のファミリーは、Cip/Kipファミリーのメンバーで構成され、p21cip1、p27kip1およびp57kip2を含み、これらはすべて、サイクリンおよびCDKサブユニットの両方に結合することを可能にするアミノ末端部分内に特徴的なモチーフを含む。 Cipファミリーのメンバーは、活性サイクリン/CDK複合体に結合し、阻害する。
| CIP/KIP | 説明 |
| p21 | p21cip1は、サイクリン依存性キナーゼ阻害剤1またはCDK相互作用タンパク質1としても知られており、ヒトのCDKN1A遺伝子によってコードされ、cdk活性の強力かつ普遍的な阻害剤として作用することができる。 これは、CDK2、CDK4、およびCDK6キナーゼを阻害し、過剰発現したときにG1で細胞周期の停止を誘導することができる。 通常の循環細胞では、p21はサイクリン/CDKと複合体である。 |
| P27 | サイクリン依存性キナーゼ阻害剤1B(p27kip1)は、ヒトではCDKN1B遺伝子によってコードされる酵素阻害剤である。 p27は、TGFによって誘導される成長阻害活性に関する一連の研究で同定され、別の研究では、餌としてCDK4を使用して、ツーハイブリッドスクリーニングに p27は、構造的にp21に関連しており、CDK2、CDK3、CDK4、およびcdk6複合体in vitroを阻害します。 |
| P57 | サイクリン依存性キナーゼ阻害剤1C(p57、Kip2)は、ヒトではCDKN1C遺伝子によってコードされるタンパク質である。 p57に結合し、いくつかのサイクリン/CDK複合体を阻害し、その発現は組織制限されているようです。 p57は、p27と同様に、その機能のためにp53とpRbを必要としないように見えます。 p57は、ヒト癌の多くの形態で頻繁に欠失または再配列を受ける11p15染色体遺伝子座にマップします。 |
腫瘍抑制および細胞周期制御
腫瘍形質転換は、原発癌遺伝子または腫瘍抑制遺伝子に影響を及ぼす遺伝的病変のクローン蓄積を含む多段階のプロセ これらの遺伝子の産物は、後に、細胞周期、細胞分化、さらには細胞死を制御することによって、シグナル伝達経路において重要な役割を果たす。 現在、正常な細胞周期の進行は、腫瘍抑制遺伝子産物と細胞周期関連タンパク質などの複数の調節因子間のバランスのとれた相互作用の結果であ 腫瘍抑制遺伝子の基本的な変化が、調節されていない細胞周期および最終的な腫瘍形質転換をもたらす可能性があることは驚くべきことではない。 したがって、人々は癌を細胞周期の遺伝病と定義することができる。
原型の腫瘍抑制遺伝子はp53とRBである。 癌におけるこれらの腫瘍抑制遺伝子の関与は広範であり、多くの場合、遺伝子は特定の腫瘍タイプに対して大きな特異性を示す。 これらの遺伝子に見られる最も一般的な変化は、欠失または点突然変異によって表される。 さらに、腫瘍抑制遺伝子の不活性化は、ウイルスの癌タンパク質との相互作用に起因する可能性がある。 実際、ウイルス剤は宿主の遺伝物質に統合することができ、p53およびpRbファミリーなどの腫瘍抑制遺伝子の機能と相互作用することにより、正常な細胞増殖および増殖の調節を妨げる可能性がある。
細胞調節と細胞周期制御
細胞周期は独立した細胞機構ではなく、他の細胞調節機構と密接に関連するプロセスである。 例えば、クロマチンリモデリングを調節するタンパク質は、ADNP遺伝子などの細胞周期にも影響を与える; 細胞エネルギー代謝を阻害するタンパク質はまた、ALDH1L1などの細胞周期を阻害し、癌細胞の増殖およびクロマチン凝縮を阻害するタンパク質は、ASB2などの細胞周期阻害タンパク質としても作用することができる。 アポトーシス、細胞増殖、ユビキチン化、カルシウム応答性転写などを含む他の細胞プロセス。、正常な細胞周期に影響を与えることができます。 細胞生物学は複雑で相互作用するネットワークであるため、細胞周期阻害剤のメカニズムを完全に理解するには、多重細胞調節プロセスを理解する
結論
細胞周期阻害剤は、ヒト癌治療の分野で幅広い見通しを持っています。 種々のCDK阻害剤が臨床試験および前臨床試験にある。 これまでの研究では、これらの薬物が細胞周期を阻害し、腫瘍細胞におけるアポトーシスを誘導することが示されている。 臨床試験では、これらの薬物が達成できる最良の効果は、状態を安定させることである。 一般に、細胞周期阻害剤は、癌治療のための効果的な戦略の1つであり、詳細な実験および研究に値する。