cellesyklusen er serien av hendelser som regulerer cellens levetid. Denne forskriften kommer fra en kombinasjon av flere signaler fra forskjellige regulatoriske veier som aktiveres som svar på spesifikke stimuli. Cellesyklusen har en sentral rolle i å kontrollere cellevekst og proliferasjon. Det blir ofte målet for genetisk endring, akkumuleringen av disse kan føre til deregulering av disse bestilte hendelsene og kan være relatert til kreftutbrudd. Med den økende forståelsen av den viktige rollen som cellesyklusregulering i tumordannelse og apoptose, har cellesyklushemmere blitt studert videre innen kreftbehandling.
Cyklinavhengige Kinasehemmere (CDK)
Progresjon gjennom cellesyklusen sikres av spesielle proteinkomplekser, de cyklinavhengige kinasene (CDKs). CDKs er en familie av høyt konserverte serin / treoninkinaser, som deler en høy homologi i en bestemt region. Cdk-er kan styre cellesyklusen ved å fosforylere forskjellige mål, som igjen kan aktiveres eller inaktiveres. Regulering AV CDK / cyklinaktivitet kan skje gjennom regulatoriske proteiner, som CDK-Hemmere (CKIs). CKIs kan hemme AKTIVITETEN TIL CDK ved å assosiere in vivo med CDK-underenheten, cyclin eller cyclin/CDK-komplekset. Denne hemmingen kan forekomme på forskjellige måter, som hemming AV CDK-kinaseaktiviteten, interferens MED CAK-mediert CDK-aktivering eller konkurranse med sykliner i binding til den katalytiske underenheten. Den hemmende prosessen kan utføres av en eller en kombinasjon av disse mekanismene. Ekspresjonen av Disse Ckiene kan induseres av stimuli som senescens, kontakthemming, ekstracellulære anti-mitogene faktorer og cellesykluskontrollpunkter.
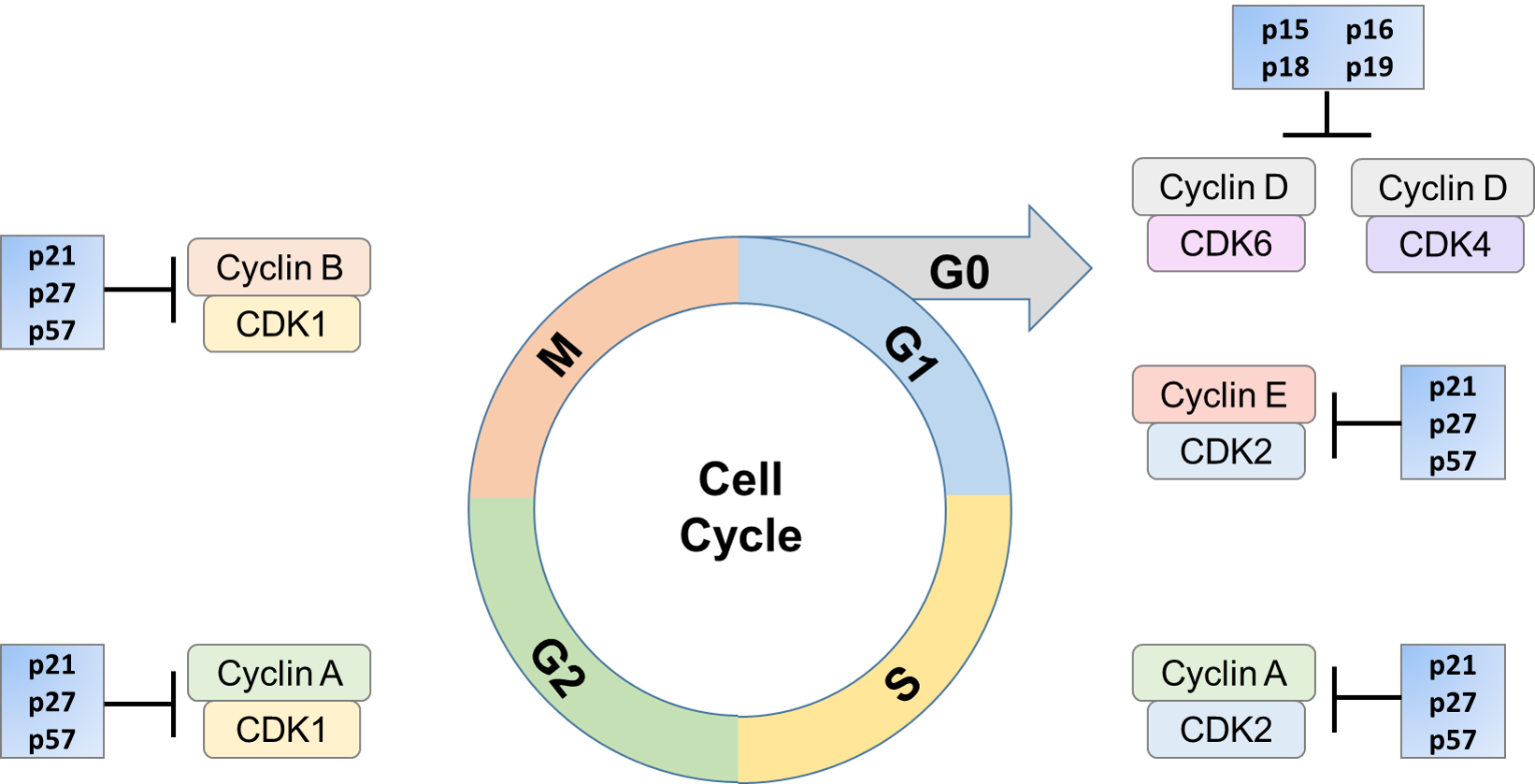
deres rolle i å kontrollere cellesyklusen er avgjørende. I flere former for kreft er CKIs som p16 og p27 mutert. Også, de har blitt funnet å bli degradert i flere typer kreft. Lave nivåer av p27-nivåer er korrelert med dårlig klinisk prognose. Disse inhibitorene kan oppreguleres når det er nødvendig, og blokkerer dermed AKTIVERINGEN AV CDK med et syklin. Dette arresterer cellen i en bestemt del av cellesyklusen til forholdene er slik at den kan fortsette mot spredning eller, om nødvendig, styres mot celledød.
- INK4 Familie
Det er to Familier Av Ckier. DEN første familien inkluderer INK4-proteiner (inhibitorer AV CDK4), så oppkalt etter deres evne til spesifikt å hemme de katalytiske underenhetene CDK4 og CDK6. Denne familien inneholder fire proteiner, p16INK4a, p15INK4b, p18INK4c og p19INK4d. disse proteinene består av flere ankirin-gjentakelser og binder bare TIL CDK4 og CDK6.
| INK4 | Beskrivelse |
| p15 | Cyklinavhengig kinase 4-hemmer B, også kjent som multiple tumor suppressor 2 (MTS-2) eller p15INK4b, induseres VED TGF-behandling og uttrykkes allestedsnærværende. Proteinet er kodet AV CDKN2B-genet hos mennesker, som ofte slettes i humane kreftformer, noe som tyder på at tapet av genet kan være signifikant i utviklingen av visse typer tumorer. |
| p16 | p16, også kjent som p16INK4a, cyklinavhengig kinasehemmer 2A OG multiple tumorsuppressor 1, er kodet AV CDKN2A-genet hos mennesker. Det ble identifisert i en to-hybrid screening ved HJELP AV CDK4 som agn. p16 kan blokkere CDK4-og CDK6-funksjonen ved å sekvestere den katalytiske underenheten, eller ved å blokkere kinaseaktiviteten til forhåndsmonterte komplekser. På grunn av det faktum at flere humane kreftformer er forbundet med tap av p16-funksjon, ble dette genet foreslått som en tumor suppressor in vivo. |
| p18 | p18, også kjent som cyklinavhengig kinase 4-hemmer C, er et enzym som hos mennesker er kodet AV CDKN2C-genet. p18 har vist seg å interagere MED CDK4 eller CDK6, og forhindre aktivering AV CDK-kinaser, og dermed fungere som en cellevekstregulator som styrer cellesyklus G1-progresjon. Både p18 og p19 er utbredt i forskjellige celletyper og vev. |
| p19 | p19, også kjent Som cyklinavhengig kinase 4-hemmer D, er et enzym som hos mennesker er kodet AV CDKN2D-genet. I noen celletyper svinger p19-nivåene under cellesyklusen, som gjennomgår induksjon når cellene går Inn I s-fasen. p19 kan fungere ved å regulere aktiviteten til cyklin d-avhengige kinaser når cellene går Ut Av G1-fasen. Alle fire inhibitorer har lignende egenskaper og kan reagere forskjellig på antiproliferative signaler. |
- CIP/KIP Familie
sistnevnte familie består av medlemmene Av cip / Kip familien, og inkluderer p21Cip1, p27Kip1 og p57Kip2, som alle inneholder karakteristiske motiver innenfor sine amino-terminale enheter som gjør dem i stand til å binde seg til både cyclin og CDK underenheter. Medlemmer av cip-familien binder seg til og hemmer det aktive cyklin / CDK-komplekset.
| CIP / KIP | Beskrivelse |
| p21 | p21Cip1, også kjent som cyklinavhengig kinasehemmer 1 eller CDK-interagerende protein 1, er kodet AV CDKN1A-genet hos mennesker, og kan fungere som en potent og universell hemmer AV CDK-aktivitet. Det hemmer CDK2, CDK4 og CDK6 kinaser og er i stand til å indusere celle syklus arrest I G1 når overuttrykt. I normalt syklusceller er p21 i kompleks med cyclin / CDK. |
| p27 | Cyklinavhengig kinasehemmer 1B (p27Kip1) er en enzymhemmer som hos mennesker er kodet AV CDKN1B-genet. p27 ble identifisert i en rekke studier på veksthemmende aktivitet indusert AV TGF, og i en annen studie ble isolert ved en to-hybrid screening, VED BRUK AV CDK4 som agn. p27 er strukturelt relatert til p21 og hemmer cdk2 -, CDK3 -, CDK4-og CDK6-kompleksene in vitro. |
| p57 | Cyklinavhengig kinasehemmer 1C (p57, Kip2) er protein som hos mennesker er kodet AV CDKN1C-genet. p57 binder seg til og hemmer flere cyklin / CDK-komplekser, og uttrykket ser ut til å være vevsbegrenset. p57, som p27, ser ikke ut til å kreve p53 og pRb for sin funksjon. p57 kart til 11p15 kromosom locus, som gjennomgår hyppige slettinger eller rearrangements i mange former for kreft hos mennesker. |
Tumorsuppressor Og Cellesykluskontroll
Tumortransformasjon er en flertrinns prosess som involverer klonal akkumulering av genetiske lesjoner som påvirker proto-onkogener eller tumorsuppressorgener. Produktene av disse genene spiller senere en viktig rolle i signaltransduksjonsveier ved å kontrollere cellesyklus, celledifferensiering og til og med celledød. Det er nå økende bevis på at normal cellesyklusprogresjon er resultatet av en balansert interaksjon mellom flere regulatoriske faktorer, som tumor suppressor genprodukter og cellesyklusassosierte proteiner. Det er ikke overraskende at grunnleggende endringer i tumorsuppressorgener kan resultere i uregulert cellesyklus og eventuell tumortransformasjon. Derfor kan folk definere kreft som en genetisk sykdom i cellesyklusen.
prototypen av tumorsuppressorgener er p53 og RB. Involveringen av disse tumorsuppressorgenene i kreft er utbredt, og ofte viser genene stor spesifisitet for bestemte svulsttyper. Den vanligste endringen som finnes i disse genene er representert ved sletting eller punktmutasjon. I tillegg kan inaktivering av tumor-suppressorgener skyldes interaksjon med virale onkoproteiner. Faktisk er virale midler i stand til integrering i vertens genetiske materiale og kan forstyrre reguleringen av normal cellevekst og proliferasjon ved å interagere med funksjonen av tumorsuppressorgener som p53-og pRb-familiene.
Celleregulering Og Cellesykluskontroll
cellesyklusen er ikke en uavhengig cellulær mekanisme, men en prosess som er nært knyttet til andre cellulære reguleringsmekanismer. For eksempel påvirker proteiner som regulerer kromatin remodeling også cellesyklusen, som ADNP-genet; proteiner som hemmer cellulær energi metabolisme hemmer også cellesyklusen, SLIK SOM ALDH1L1; proteiner som hemmer kreftcellevekst og kromatinkondensasjon kan også fungere som cellesyklusinhibitorproteiner, slik SOM ASB2. Andre celleprosesser, inkludert apoptose, cellevekst, ubiquitination, kalsium responsive transkripsjon, et al., kan påvirke den normale cellesyklusen. Cellebiologi er et komplekst og interagerende nettverk, så for å forstå mekanismene til cellesyklushemmere, må du forstå multiplekscellereguleringsprosessen.
Konklusjon
cellesyklushemmere har brede utsikter innen human kreftbehandling. EN rekke CDK-hemmere er i kliniske og prekliniske studier. Tidligere studier har vist at disse stoffene kan hemme cellesyklusen og indusere apoptose i tumorceller. I kliniske studier er den beste effekten disse stoffene kan oppnå, å stabilisere tilstanden. Generelt er cellesyklushemmere en av de effektive strategiene for kreftbehandling og er verdig til grundige eksperimenter og forskning.