Abstrakti
Kirroosiperäinen kardiomyopatia on äskettäin tunnustettu tila, joka koostuu sydänlihaksen toimintahäiriöstä, joka ilmenee kirroosipotilailla ilman aikaisempaa sydänsairautta. Taustalla patogeneettiset mekanismit sisältää ”miokardiotoksinen” ympäristö, joka johtaa blunted sydämen vaste stressiin, olipa fyysinen tai farmakologinen. Tämä ehto on nyt paremmin ymmärretty ja voidaan diagnosoida tuettu kliininen, laboratorio elektrokardiografia ja kaikukardiografia kriteerit. Kliinisesti systolinen epäpätevyys on selvintä, kun kirroosipotilaat ovat stressaantuneita, olivatpa ne fyysisiä tai farmakologisia. Siitä huolimatta, että ne ymmärretään hyvin, ei ole tietoa, joka soveltaisi niitä oikein käytäntöön. Viimeaikaiset tapausraportit ovat ehdottaneet, että CCM on hoidettava aikaisin, koska se voi olla laukaiseva tekijä kirroosi komplikaatioita. Tutkimuksia tarvitaan sellaisten mahdollisten hoitojen tunnistamiseksi, jotka muuttavat kirroosipotilaiden sydänsairauksien luonnollista historiaa, erityisesti niissä vaiheissa, joissa potilaat ovat oireettomia.
avainsanat
maksakirroosi, sydämen vajaatoiminta, kardiomyopatia
Johdanto
Kirroosiinen kardiomyopatia (CCM) on sydämen toimintahäiriö, jolle on ominaista suboptimaalinen supistumiskyky stressille ja heikentynyt diastolinen toiminta ilman aikaisempaa sydänsairautta . Nykyään tutkimus on ehdottanut, että kirroosipotilailla on luontainen sydämen toimintahäiriö, joka voi vaikuttaa munuaisten vajaatoiminnan kehittymiseen pitkälle edenneessä maksasairaudessa .
vuodesta 2002 lähtien maksasairauden verenkiertohäiriöitä koskevat löydökset ovat kehittyneet diagnostisilla menetelmillä, mikä korostaa CCM: n tunnistamisen merkitystä kliinisessä käytännössä . Kuitenkin, siellä on vielä aukko tietoa hallinnasta tämän ehdon . Maksakirroosissa esiintyvä sydänlihaksen toimintahäiriö lisää hepatorrenaalisen oireyhtymän (HR) ja sydäntapahtumien riskiä ja liittyy suurempaan kuolleisuuteen .
kävimme läpi Pubmedissa saatavilla olevaa kirjallisuutta kirroosikomplikaatioiden merkkiaineista sekä sydämen ja maksan yhteisvaikutuksista. Tämän tarkastelun tarkoituksena on keskustella tarpeesta seurata ja hoitaa CCM: ää varhaisessa vaiheessa, koska se voi olla kirroosin komplikaatioiden laukaiseva tekijä, mikä tuo uusia oivalluksia kliiniseen käytäntöön.
määritelmä ja esiintyvyys
CCM kuvaa sydämen kroonista toimintahäiriötä kirroosipotilailla, vaikka heillä ei ollut aiempaa rakenteellista sydänsairautta . Se määritellään yhdellä tai useammalla seuraavista: rakenteelliset poikkeavuudet sydämen kammioissa; diastolinen toimintahäiriö; normaali tai voimistunut systolinen toiminta levossa, mutta heikko supistumiskykyinen vaste stressiin; ja elektrofysiologiset muutokset . Näitä poikkeavuuksia voidaan havaita jopa 50%: lla kirroosipotilaista .
Fysiopatologia
kirroosin fysiopatologia tunnetaan typpioksidin (NO) ylituotannosta splanchnic-aluksissa ja siitä johtuvasta systeemisestä vasodilataatiosta. Tämä mekanismi laukaisee renniini-angiotensiini-aldosteronijärjestelmän (RAAS) ja sympaattisen hermoston aktivaation ja nostaa seerumin vasopressiinitasoa, mikä johtaa hyperdinamiinitilaan, joka voi vaikuttaa soluista kliinisiin asetuksiin.
näillä potilailla seerumin hiilimonoksidi (CO) on lisääntynyt sympaattisen hyperaktiivisuuden ja tulehduksellisten sytokiinien seurauksena. CO-pitoisuus lisääntyy, ja siihen liittyy suuri NO-pitoisuus, endokannabinoidien ja muiden vasodilataattoreiden kertyminen. Nämä aineet lisäävät syklistä guanosiinimonofosfaattia (cGMP), joka estää syklistä adenosiinimonofosfaattia (cAMP) kardiomyosiiteissa, mikä aiheuttaa kalsiumin sisäänvirtausta ja lisää supistumiskykyä (Kuva 1,2). Sydänlihassoluanalyysi osoittaa, että kolesterolikertymän aiheuttama plasmaattisen kalvon juoksevuus vähenee, mikä vaikeuttaa aineiden, kuten beeta-adrenergisten reseptorien ja G-proteiinien, vuorovaikutusta . Kammion myokiitti voi myös vähentää kaliumkanavien toimintaa, mikä johtaa suboptimaaliseen sydämen rentoutumiseen ja siitä johtuvaan diastoliseen toimintahäiriöön .
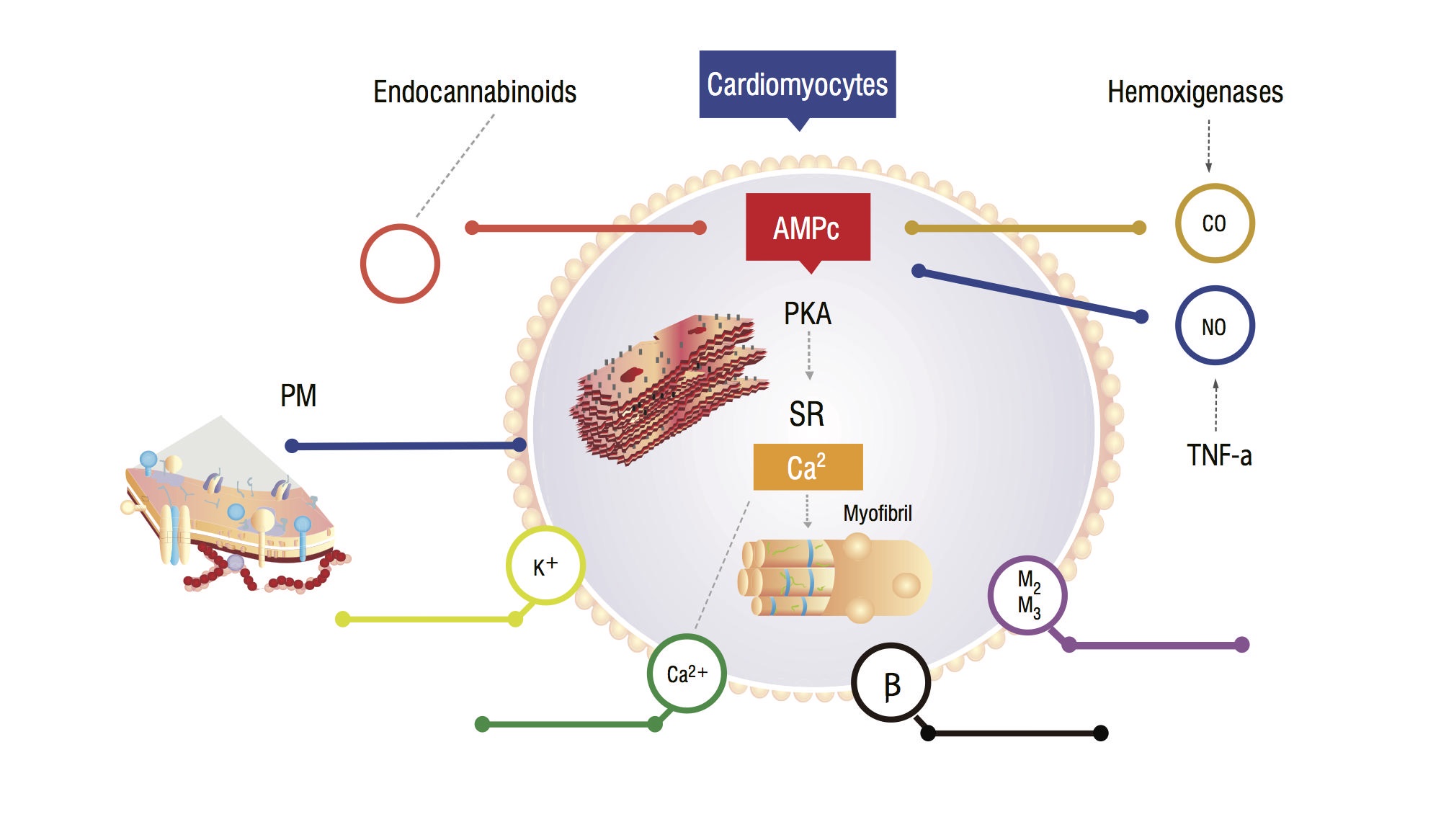
Kuva 1. Kardiomyosyyttien fysiopatologinen malli, jossa näkyvät tärkeimmät signalointireitit, jotka johtavat myokardiaaliseen vasteeseen stressiin. PM: Plasmaattinen kalvo; CO: Hiilioksidi; NO: typpioksidi; TNF-a: tuumorinekroositekijä alfa; SR: Sarkoplasmaattinen reticullum; AMPc: syklinen adenosiinimonofosfaatti; PKA: proteiinikinaasi A.
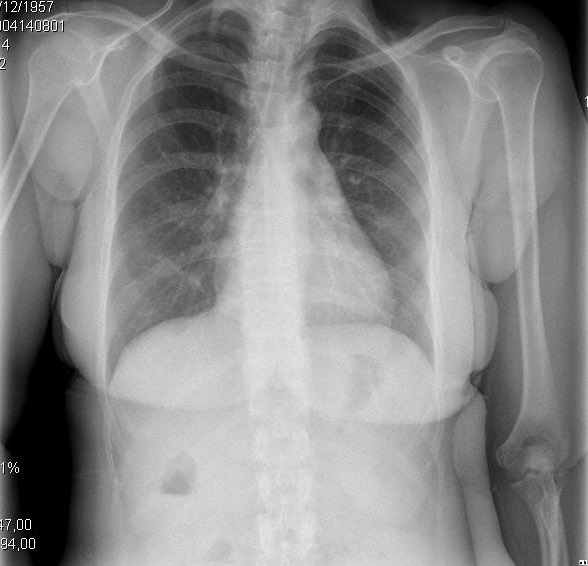
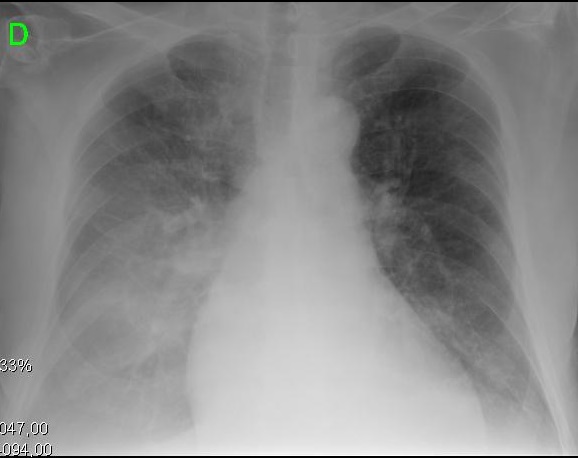
kuva 2. Kirroottisen kardiomyopatian eri kehitysvaiheiden kliiniset ja radiologiset esitykset. A. vasemmassa kuvassa näkyy pieni pleuraeffuusio ja CTI 0,50. B. oikeassa kuvassa on vakava keuhkojen tukkoisuus ja CTI 0,67.
Taulukko 1. Kliiniset ja ilmaiset kriteerit CCM: n diagnoosille. Mukautettu viitteestä 29 luvan kanssa.
pysyvät beetasalpaajaärsykkeet indusoivat säätelyä ja vähentävät sydämen reseptorien tiheyttä muuttaen kalsiumkanavan aktivoitumisesta vastaavia signalointikaskadeja; tuloksena on supistumiskyvyn heikkeneminen . Tämän reitin kliininen jälkiseuraus on myokardiaalinen toiminta ja sydämen biomarkkerien lisääntyminen .
CCM: n tunnistaminen perustuu hienovaraisiin kliinisiin piirteisiin, jotka voivat paljastua taudin edetessä tai tulla selvästi esiin tietyissä kliinisissä kantaskenaarioissa, ja siitä tulee haaste sen suhteen, hoidetaanko ja milloin.
luonnonhistoria ja diagnoosi
diagnostiset kriteerit on koottu taulukkoon 1 ja ne perustuvat kliinisiin, kuvantamiseen ja biomarkkereihin.
kliiniset ominaisuudet
CCM: n kliinisiä piirteitä voi esiintyä potilailla, joiden sydämen toiminta on ilmeisesti normaali, koska kardiomyosyyttien krooninen sopeutuminen kirroosiympäristöön johtaa kaikkiin näihin solumuutoksiin .
kirroosipotilaille kehittyy natriumin ja nesteen kertymistä, perifeeristä vasodilataatiota , sympaattista hyperaktiivisuutta ja ”miokardiotoksisten” aineiden kertymistä, mikä vaatii kardiomyosyyttien adaptiivisen prosessin. Tämä jatkumotasapaino voidaan rikkoa ja paljastaa piilevä sydämen vajaatoiminta stressitilanteissa, kuten maksansiirto, transjugulaarinen intrahepaattinen portosystemic suntti tai infektioita .
vaikka kirroottinen kardiomyopatia on yleensä krooninen sairaus, tutkimukset osoittavat, että sydänlihaksen toimintahäiriön kliiniset oireet voivat palautua jopa 15 kuukaudessa onnistuneen maksansiirron jälkeen, samoin kuin QT-ajan pidentyminen .
Laboratoriolöydökset
koska tulehdukselliset biomarkkerit voivat heijastaa sydämen toimintahäiriöitä, uusia sydän-ja proinflammatorisia markkereita on äskettäin tutkittu ja ne korreloivat lisääntyneeseen kuolleisuuteen johtavien komplikaatioiden kehittymiseen .
viimeaikaiset tutkimukset kuvaavat korrelaatiota ANP: n (proANP) ja B-tyypin natriureettisen peptidin (BNP), kopeptinin ja korkean herkkyyden troponiini T: n (hs-TnT) sekä liukoisen urokinaasin plasminogeeniaktivaattorireseptorin (suPAR) ja erittäin herkän C-reaktiivisen proteiinin (hs-CRP) pitoisuuksien välillä sekä maksakirroosin sydän-ja verisuonikomplikaatioiden välillä. Sen kliinistä käyttöä kuitenkin vielä arvioidaan .
sydänlihassolut erittävät natriureettista peptidiä vasteena tilavuus-tai painekuormitukselle tai sydänlihasiskemialle kompensoidakseen Raas-vaikutusta natrium-ja vesitasapainossa . BNP saattaa olla yksi käytettävissä olevista biomarkkereista, jonka avulla sydänoireet voidaan tunnistaa varhaisessa vaiheessa . Sen seerumipitoisuus on sitä suurempi, mitä vakavammat maksa-ja sydänsairaudet ovat .
lupaavien tutkimusten mukaan korkeita adrenomedulliinipitoisuuksia on havaittu myös kirroosissa, johon liittyy tai ei liity kliinistä sydänoiretta; tämä aine vapautuu verenkierrossa vasodilataattorina ja pyrkii vähentämään jälkikuormitusta . Galektiini-3, viimeisin tutkittu biomarkkeri, joka on kohonnut kirroosipotilailla, on yhdistetty sydänlihaksen fibroosiin ja saattaa korreloida kirroosin vaikeusasteeseen. Tämä merkkiaine on osoittautunut herkemmäksi kuin BNP diastolisen toimintahäiriön arvioinnissa, vaikka se on vähemmän spesifinen .
elektrokardiogrammi
oireettomalla CCM-potilaalla voidaan varhain havaita EKG-poikkeavuuksia, jotka voivat korreloida kammioperäisiin rytmihäiriöihin ja äkkikuolemaan . Yleisin EKG-löydös on QT-ajan piteneminen, jota voidaan havaita noin 30-40%: lla kirroosipotilaista, pääasiassa Child-Pugh B: stä tai C: stä, kirroosin etiologiasta riippumatta .
tämä EKG-kuvio saattaa johtua kardiomyosyyttien repolarisaatiohäiriöistä kaliumkanavissa ja näiden kanavien pitoisuuden vähenemisestä plasmakalvossa, kun portaalipaineen muutokset ovat vähäisiä . Ionikanavien toimintahäiriöt aiheuttavat siten sydänlihassolujen toimintapotentiaalin pidentymistä, mikä johtaa pitempään kammion systoliin ja QT: hen . Pidempi supistumisaika merkitsee heikentynyttä rentoutumista, mikä aiheuttaa diastolisen toimintahäiriön .
sähkömekaanista irtoamista on kuvattu sähköisen ärsykkeen ja systolisen sydämen mekaanisen vasteen välisenä dyssynkroniana, joka johtaa näillä potilailla etenevään sydänlihaksen toiminnan menetykseen ja kongestiiviseen sydämen vajaatoimintaan1 . Kronotrooppiselle epäpätevyydelle on ominaista sinussolmun kyvyttömyys vastata fysiologisiin tai farmakologisiin ärsykkeisiin , mikä on määräävä seikka CCM-fysiopatologiassa. Nämä muutokset ovat sekundaarisia myös portaalihypertensiolle, autonomiselle toimintahäiriölle, hyperdynaamiselle verenkierrolle ja potilaan sydänlihakseen vaikuttavien proinflammatoristen tekijöiden läsnäololle .
sydämen Kaikukuvaus
sydämen Kaikukuvaus antaa olennaista tietoa sydämen toiminnasta ja sitä käytetään kirroottisen kardiomyopatian diagnostisina kriteereinä .
näiden potilaiden tärkeimmät löydökset ovat vasemman kammion loppudiastolinen laajentuminen, huippunopeuden väheneminen ja systolinen epämuodostumanopeus; lisääntynyt loppudiastolinen vasemman kammion paine ilman asianmukaista LVEF-laajenemista. Vasemman eteisen (LA) laajentuminen yli 34 mL/m2 voi viitata krooniseen diastoliseen toimintahäiriöön, ja kun se liittyy LV-massan vähenemiseen, se voi viitata huonompaan ennusteeseen . LA-arviointi voidaan tehdä kahden ulottuvuuden kaikukuvauksen ja täpläseurannan avulla .
yleiset löydökset sydämen doppler-kaikukardiografiassa viittaavat sydänlihaksen relaksaatiohäiriöön kirroosipotilailla: e/a-suhteen pieneneminen (<1) ja pidentynyt e-aallon hidastumisaika (DT) ja isovolumetrinen relaksaatioaika (IVRT) > 80ms .Mitä vakavampi on diastolinen toimintahäiriö, lyhyempi on IVRT ja mitraalinen DT, ja korkeampi on e/a-nopeussuhde, joka luonnehtii edennyttä diastolista toimintahäiriötä, lisääntynyttä LA-painetta ja huonompaa funktionaalista luokkaa.
viimeaikaiset tutkimukset Global longitudinal strain (GLS) evaluation osoittavat, että tämä saattaa olla hyödyllinen menetelmä sydämen toimintahäiriön, lähinnä systolisen lepovaiheen toimintahäiriön, varhaiseen toteamiseen kirroosipotilaalla .
e / a-suhde voi olla luotettava parametri kirroosipotilaiden diastolisen toimintahäiriön diagnosoinnissa, vaikka potilaan nesteytysaste vaikuttaakin arvoihin, vaikkakin se voi vaihdella askitesin ja tilavuuden ylikuormituksen vuoksi . Samaan aikaan isovolumetrinen rentoutumisaika, vaikka se onkin erittäin herkkä, ei edusta LV-täyttöä ja vaihtelee sykkeen muuttuessa .
lievä systolinen toimintahäiriö ja diastolinen toimintahäiriö voidaan esittää maksakirroosin asteesta riippumatta. Diastolista toimintahäiriötä esiintyy kuitenkin yleisimmin kirroosipotilailla ja se edeltää yleensä edellistä .
Keskustelu
tässä katsauksessa käsitellään CCM: n fysiopatologian lisääntyvää tunnistamista ja ymmärtämistä, sen korrelaatiota kirroosipotilaiden huonoon ennusteeseen ja herää huoli terapeuttisesta lähestymistavasta.
tässä artikkelissa tiivistettiin lääketieteellisessä kirjallisuudessa jo vahvistetut diagnostiset kriteerit (Taulukko 1) painottaen uusia biomarkkereita, joita on tutkittu diagnostisen täydentämisen kannalta. Tutkimukset ovat osoittaneet, että sydänlihaksen toimintahäiriöitä esiintyy maksakirroosin eri vaiheissa. On kuvattu, että jos potilaalla on korkea BNP ja kammion toimintahäiriö sydämen ultraäänitutkimuksessa, munuaisten vajaatoiminnan hoito on hyvin vaikeaa; toisaalta varhainen puuttuminen potilailla, joilla ei ole vielä todettu sydänsairaus on alue, jota ei ole vielä tutkittu.
Taulukko 1. Kliiniset ja ilmaiset kriteerit CCM: n diagnoosille. Mukautettu viitteestä 29 luvan kanssa.
kliiniset ominaisuudet
ei kardiopulmonaalisia oireita levossa
heikko toiminnallinen sydänreservi
hiperadrenerginen tila, johon liittyy natriumin ja nesteen kertymistä
biomarkkerit (troponiini I, pro-BNP ja BNP, muut)
Eletrosardiografia
Elektrofysiologiset poikkeavuudet (QT-ajan piteneminen ja muut)
Ekokardiografiset kriteerit
diastolinen arviointi
E / a-suhde <1.0 (Ikä korjattu)
pitkittynyt isovoluminen relaksaatioaika (>80msec)
pitkittynyt hidastumisaika (>200msec)
vasemman kammion hypertrofia
systolinen arviointi
ejektiofraktio levossa < 55%
Supistumiskykyinen vaje stressissä
maksan vajaatoiminnan merkit ja oireet ovat yleensä myöhäisiä, ja siihen liittyy hienovaraisia kliinisiä ja laboratoriooireita, joita on joskus vaikea tulkita. Erikoislääkäri tai jopa yleislääkäri voi kohdata potilaan, jolla on hengenahdistus-valitus, ilman patologista kaulavaltimoturvotusta, normaalia kardiologian peruskokeita, mutta korkea BNP, joka voi edustaa CCM: n tapausta.
muista tutkimuksista poiketen ryhmämme ehdottaa edistysaskelta tällä alalla, koska kirroosiin liittyvän sydänsairauden ymmärtäminen voi mahdollistaa diagnosoimattomasta sydänlihaksen vajaatoiminnasta johtuvien komplikaatioiden varhaisen terapeuttisen hoidon. Maksansiirto ja TIPS ovat erityisiä kliinisiä asetuksia, jotka voivat deflagrate sydämen vajaatoiminta näillä potilailla. Koska potilaat selviävät pidempään näiden toimenpiteiden jälkeen, kliinikot joutuisivat kohtaamaan sydänparametrien heikkenemisen .
uskomme, että varhainen terapeuttinen interventio CCM: ssä on lupaava, kun se ilmenee komplikaatioina, kuten refraktaarisena KUUMAHOITONA, ennen kuin ilmenee selvää sydänlihaksen vajaatoiminnasta johtuvaa keuhkojen ruuhkautumista. Kirjallisuus tukee sitä, että piilevään kirroottiseen kardiomyopatiaan liittyvät fyysiset tai farmakologiset stressitilanteet tai infektiot voivat johtaa KUUMAHOITOON, joka voi olla hoitoresistentti tavanomaisiin hoitoihin ja huonompaan ennusteeseen, jos systolinen toimintahäiriö on läsnä .
kokemuksemme viittaa siihen, että HRS: n esittäminen on vihje sydänlihaksen komponentin hoidon aloittamisesta. Tämä eteneminen HRS ymmärretään, koska olemassaolo CCM on laukaista ja ylläpitävä tekijä HRS, joten jos CCM lähestytään aikaisin tässä yhteydessä, HRS voi olla parempi ennuste .
ryhmämme on ollut uranuurtaja hoidettaessa potilaita, joiden kliininen diagnoosi oli CCM ja jotka etenivät tavanomaisiin hoitoihin, joissa dobutamiinin käyttö munuaisten toiminnan pelastushoitona onnistui. Tavoitteena on soveltaa tätä teoriatietoa, joka ennakoi tätä komplikaatiota loppuvaiheen maksasairauspotilailla .
huolimatta siitä, että on hyvin ymmärretty, on puutteellista tietoa kunnolliseen käytännön soveltamiseen. CCM: n tunnistaminen edellyttää suurta kliinistä epäilyä oireettomalla potilaalla, jolla ei ole ilmeisiä toiminnallisia rajoituksia, mutta jolla on subkliininen solu-ja rakenteellinen sydänsairaus.
tutkimuksia tarvitaan sellaisten mahdollisten hoitojen tunnistamiseksi, jotka muuttavat kirroosipotilaiden luonnollista sydänsairaushistoriaa, erityisesti silloin, kun potilaat ovat oireettomia. Tämä on alue, jota ei ole vielä tutkittu, erityisesti tulevien hoitovaihtoehtojen osalta.
eturistiriidat
kirjoittajat ilmoittivat, ettei tämän paperin julkaisemiseen liity eturistiriitoja.
taloudellinen tuki
Ei mitään.
- Sampaio F, Pimenta J (2016) Left ventrikular function assessment in crosis: Current methods and future directions. World J Gastroenterol 22: 112-125.
- Shin WJ, Song JG, Jun IG, Moon YJ, Kwon HM, et al. (2016) Effect of ventriculo-arterial coupling on transplant outcomes in cirrosis: Analysis of pressure-volume curve relations. J Hepatol.
- Carvalheiro F, Rodrigues C, Adrego T,Viana J, Vieira H, et al. (2016) diastolinen toimintahäiriö maksakirroosissa: prognostinen ennustaja Maksansiirrossa? Elinsiirto 48: 128-31.
- Merli M,Torromeo C, Giusto M, Iacovone G, Riggio O, et al. (2016) maksakirroosipotilaiden eloonjäämiseen 2 vuoden kuluttua vaikuttavat vasemman eteisen tilavuus ja vasemman kammion massa. Maksa Int.
- Møller s, Henriksen JH (2002) Cirrhotic cardiomyopathy: a pathophysiological review of circular dysfunction in liver disease. Sydän 87: 9-15.
- Mocarzel LO, Bicca J, Jarske L, Oliveira T, Lanzieri P, et al. (2016) Cirrhotic Cardiomyopatia: toinen tapaus onnistuneen lähestymistavan hoitoon Hepatorenal oireyhtymä. Case Rep Gastroenterol 10: 531-7.
- Timoh T, Protano MA, Wagman G, Bloom M, Vittorio TJ (2011) a perspective on cirrhotic cardiomyopatia. Elinsiirto 43: 1649-1653.
- Ma Z, Lee SS (1996) Cirrhotic cardiomyopathy: getting to the heart of the matter. Hepatology 24: 451-459.
- Zardi EM, Abbate A, Zardi DM, Dobrina a, Margiotta D, et al. (2010) Cirrhotic cardiomyopatia. J Am Coll Cardiol 56: 539-549.
- Myers RP, Lee SS (2000) kirroottinen kardiomyopatia ja maksansiirto. Maksa Transpl 6: S44-52.
- Wiese s, Mortensen C, Gøtze JP, Christensen E,Andersen O, et al. (2014) sydän-ja proinflammatoriset markkerit ennustavat ennustetta kirroosissa. Maksa Int 34: e19-30.
- Fattouh AM, El-Shabrawi MH, Mahmoud EH, Ahmed wo (2016) Evaluation of cardiac functions of cirrhotic children using serum brain natriuretic peptide and tissue Doppler imaging. Ann Pediatr Cardiol 9: 22-8.
- Rahman s, Mallett s V (2015) kirroottinen kardiomyopatia?: Implications for the perioperative management of liver transplant patients 7: 507-20.
- Farr M, Schulze PC (2015) Recent Advances in the Diagnosis and Management of kirroosi-Associated Cardiomyopathy in Liver Transplant Candidates: Advanced Echo Imaging, Heart Biomarkers, and Advanced Heart Failure Therapie. Clin Med Insights Cardiol 8: 67-74.
- Licata A, Corrao S, Petta S,Genco C, Cardillo m, et al. (2013) NT Pro BNP-pitoisuus plasmassa ja eteisen tilavuus ovat yhteydessä maksakirroosin vaikeusasteeseen. PLoS yksi 8: e68364.
- Abbas WA, Kasem Ahmed SM, Abdel Aal AM, Mahmoud AA, Abdelmalek MO, Mekky MA, et al. Galaktiini-3 ja aivojen natriureettinen peptidi verrattuna tavanomaiseen ekokardiografiaan kirroottisen kardiomyopatian varhaisessa toteamisessa. Turk J Gastroenterol 27: 367-74.
- Wong F, Siu s, Liu P, Blendis LM (2001) Brain natriuretic peptide: is it a predictor of cardiomyopatia in kirroosi? Clin Sci (Lond) 101: 621-628.
- Wong F (2009) kirroottinen kardiomyopatia. Hepatol Int 3: 294-304.
- Mimidis K, Papadopoulos V, Thomopoulos K,Tziakas D, Ritis K, et al. (2003) QTc-ajan piteneminen kirroosipotilailla. Ann Gastroenterol 16: 155-8.
- Mozos I (2015) Rytmihäiriöriski maksakirroosissa. World J Hepatol 7: 662-672.
- Mocarzel LO, Bicca J, Jarske L, Oliveira T, Lanzieri P, et al. (2016) Cirrhotic Cardiomyopatia: toinen tapaus onnistuneen lähestymistavan hoitoon Hepatorenal oireyhtymä. Asia Rep Gastroenterol 10: 531-537.
- Batchvarov V, Camm AJ (2014) QT dispersion: Measurement and interpretation.
- Páll A, Czifra A, Vitális Z, Papp M, Paragh G, et al. (2014) Patophysiological and clinical approach to cirrhotic cardiomyopatia. Dis 23: 301-310.
- Castro Hevia J, Antzelevitch C, Tornés Bárzaga F, Dorantes Sánchez M, Dorticós Balea F, et al. (2006) Tpeak-Tend ja Tpeak-Tend dispersio kammiotakykardian/kammiovärinän riskitekijöinä Brugadan oireyhtymää sairastavilla potilailla. J Am Coll Cardiol 47 (9): 1828-34.
- Demir C, Demir M (2013) Evaluation of Tp-e interval and Tp-e/QT ratio in patients with chronic hepatiitti B. Prague Med Rep 114: 239-245.
- Jewell DP (2006) New patients, new lessons, new thinking in inflammatory bowel disease: World Congress of Gastroenterology Symposium, Montreal, Kanada. Kolorektaali Dis 8 Suppl 1 (s1): 1-2.
- Gassanov N, Caglayan E, Semmo N, Massenkeil G, Er F (2014) Cirrhotic cardiomyopathy: a cardiologist ’ s perspective. World J Gastroenterol 20: 15492-15498.
- Chayanupatkul M, Liangpunsakul S (2014) kirroottinen kardiomyopatia: review of pathophysiology and treatment. Hepatol Int 8: 308-315.
- Møller S, Henriksen JH, Bendtsen F (2014) Extrahepatic complications to cirrhosis and portal hypertension: haemodynamic and homeostatic aspects. World J Gastroenterol 20: 15499–517.
- Møller S, Bendtsen F (2015) Cirrhotic Multiorgan Syndrome. Dig Dis Sci 60: 3209-3225.