- Introduction
- materiaalit ja menetelmät
- tutkimussuunnitelma
- Liittymiskriteerit
- diagnoosi
- leikkausryhmä
- Sädehoitoryhmä
- kasvainten luokittelu
- kirurginen ohjelma
- tilastoanalyysi
- tulokset
- leikkausryhmä
- osallistujia
- kasvainten luonne
- leikkaustulokset
- Sädehoitoryhmä
- oireelliset tulokset
- radiologiset tulokset
- jatkohoito
- Keskustelu
- johtopäätös
- tiedon Saatavuuslausunto
- eettinen lausunto
- Tekijäosuudet
- Rahoitus
- eturistiriita
Introduction
Cerebellopontine angle meningioomas account 6-15% of the cerebellopontine angle region (1). Niille on ominaista syvä kasvain sijainti, kapea kirurginen kenttä, ja läheisyys brainstem, useita pareja (V–XI) kallon hermoja (2). Tällä hetkellä kirurginen hoito on ensimmäinen valinta suurten pikkuaivojen kulma meningioomat, kun taas pienet pikkuaivojen kulma meningioomat hoidetaan aina stereotaktinen sädehoito, lääkehoito ja kokeellinen hoito (3). Viime vuosina monissa tutkimuksissa on havaittu, että stereotaktinen sädehoito rajoitti alhaista kasvainkontrollia, hoidon jälkeistä aivojen turvotusta ja kudoksen kiinnittymistä, mikä haittasi jatkohoitoja (4). Siksi yhä useammat pienet pikkuaivopontiinikulman meningeoomapotilaat ovat siirtymässä leikkaushoitoon.
materiaalit ja menetelmät
tutkimussuunnitelma
tehtiin retrospektiivinen analyysi pienistä pikkuaivopontiinikulma meningioomaa sairastavista potilaista. Nämä potilaat leikattiin soochowin yliopiston ensimmäisen sairaalan neurokirurgian osastolla tammikuun 2010 ja joulukuun 2019 välisenä aikana. Nämä potilaat luokiteltiin leikkausryhmään. Kävimme läpi myös pienten pikkuaivojen stereotaktista sädehoitoa koskevaa kirjallisuutta viimeisten 10 vuoden ajalta. Kirjallisuudessa olleet potilaiden kliiniset tiedot kerättiin ja analysoitiin, ja nämä potilaat luokiteltiin sädehoitoryhmään. Analysoimme näiden kahden ryhmän välisiä eroja, mukaan lukien kasvainten luonne, oireet ennen ja jälkeen hoitoja, neurologiset puutteet ja ennuste. Lopuksi selvitimme pienten pikkuaivokulman meningioomien kirurgisia tuloksia ja teimme yhteenvedon kirurgisista kokemuksista.
Liittymiskriteerit
diagnoosi
meningioomien erottamiseksi muista pikkuaivokulmakasvaimista, kuten akustisista neuroomista ja glioomista, kaikki potilaat diagnosoitiin sekä radiologisella että histopatologisella tutkimuksella, mukaan lukien MRI, CT, PET ja SSTR2-ligandit. Sekä dural häntä merkki MRI ja ei laajenemista sisäisen korvakäytävän TT ovat tärkeimmät ero pistettä pikkuaivojen kulma meningiomas ja akustinen neuroomat. Jotta voitaisiin erottaa pikkuaivokulma meningioomat glioomista ja etäpesäkkeistä, potilaat testattiin tavanomaisesti MR-spektroskopialla (5). Histologisten näkökohtien osalta testattiin myös tavanomaisesti immunohistokemiallista analyysia, kuten HE-värjäystä, Vimentinin värjäystä, EMA-värjäystä, Ki-67: ää ja CD56: ta.
leikkausryhmä
(1) potilaat, joilla oli pieni pikkuaivokulma meningiooma, leikattiin tammikuun 2010 ja joulukuun 2019 välisenä aikana, (2) kasvaimen tilavuus ≤ 8 cm3, (3) ei siihen liittyvää hoitoa ennen leikkausta, (4) ei muita hermostosairauksia ja (5) pidettiin yhteyttä seurannan aikana.
Sädehoitoryhmä
(1) pienet pikkuaivopontiinikulma meningiooma – potilaat kerättiin stereotaktista sädehoitoa koskevasta kirjallisuudesta, joka julkaistiin tammikuun 2010 ja joulukuun 2019 välisenä aikana, (2) tutkimukseen osallistuneilla potilailla oli täydelliset tiedot ennen hoitoa ja sen jälkeen, (3) ei muita hermostosairauksia ja (4) pidettiin yhteyttä seurannan aikana.
seuranta koostui rutiininomaisesta potilaskäynnistä ja MRI – tai CT-testeistä 3-6 kuukauden välein ensimmäisten 3 vuoden ajan hoidon jälkeen ja sen jälkeen vierailusta ja testauksesta joka vuosi.
kasvainten luokittelu
duraalin kiinnityskohdan perusteella pikkuaivokulma meningioomat luokiteltiin kolmeen tyyppiin (6): anterioriset kasvaimet olivat ne, jotka olivat peräisin Tentorium-pikkuaivoista tai petroosisesta luusta Dura anteriorisesta sisäisestä korvakäytävästä; keskimmäiset kasvaimet olivat ne, jotka olivat peräisin sisäisestä korvakäytävästä; posterioriset kasvaimet olivat ne, jotka olivat peräisin sigmoidista ja poikittaisista sivuonteloista tai petroosisesta luusta Dura posteriorisesta sisäisestä korvakäytävästä (Kuva 1)).
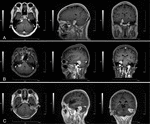
Kuva 1. Kolmenlaisia pieniä pikkuaivopontiini kulma meningiomas. A) Anterior. B) Keskellä. C) Posterior.
tuumoripatologian perusteella pikkuaivopontiinikulman meningioomat luokiteltiin kolmeen luokkaan: WHO: n luokka I (Alhainen uusiutuminen ja alhainen invasiivinen kasvu), WHO: n luokka II (voimakas uusiutuminen ja voimakas invasiivinen kasvu) ja WHO: n luokka III (voimakas uusiutuminen ja metastasoivat systeemisesti).
kasvaimen resektioasteen perusteella potilaat, joilla oli pikkuaivokulma meningiooma, jaettiin viiteen luokkaan: Simpson grade I: yhteensä resektio meningiooma, dural kiinnitys, ja kallo; Simpson luokka II: yhteensä resektio meningiooma ja elektrokoagulaatio tai laser hoito dural kiinnitys; Simpson luokka III: yhteensä resektio meningioomat ja ei hoitoa dural kiinnitys ja kallo; Simpson luokka IV: osittainen resektio meningioomat; Simpson luokka V: dekompressio ja tuumoribiopsia.
kasvaimen etenemiseksi ja regressioksi määriteltiin radiologisessa tutkimuksessa yli 15%: n tilavuusmuutokset.
kirurginen ohjelma
kaikki potilaat käyttivät suboccipitaalista retrosigmoid-lähestymistapaa. Suboccipital retrosigmoid suora viilto noin 8-10 cm tehtiin vaikuttaa puolella. Soikean luuikkunan pitkä halkaisija oli 5 cm ja lyhyt halkaisija 3,5 cm. Luuikkuna poikittaiseen poskionteloon, sivusuunnassa mastoidin juureen, paljasti sigmoidin ja poikittaissuonen välisen kulman. Katkaisi Duran, venytti pikkuaivoja, avasi sisterna Magnan ja vapautti aivo-selkäydinnestettä. Lopuksi, pikkuaivojen kulma meningeooma oli täysin resected, huolehtien suojella petrous laskimoon, kolmoishermon, ja abducens hermo. Leikkauksen aikana elektrofysiologisella seurannalla seurattiin kasvojen ja akustisten hermojen toimintaa.
tilastoanalyysi
kaikki tilastoanalyysit tehtiin SPSS-versiolla 22.0. Parametriset jatkuvat muuttujat ilmoitettiin keskiarvona ± keskihajonta. Ei-parametriset muuttujat raportoitiin vaihteluvälin mukaisena mediaanina. Kliiniset tulokset ja löydökset ja oireet raportoitiin kolmen kategorian tuloksina (paraneminen tai laajentuminen, ei muutoksia, huononemista tai vähenemistä). Riippumaton näytteet t-testi tehtiin kahden luokan tiedot, ja ANOVA tehtiin kolmen luokan tiedot. Khiin neliötesti tehtiin vertailemaan nimellisesti jakautuneita kategorisia muuttujia. Monimuuttuja-analyysejä varten tehtiin logistinen regressioanalyysi. Alle 0, 05: n P-arvoja pidettiin tilastollisesti merkitsevinä.
tulokset
leikkausryhmä
osallistujia
mukana oli yhteensä 162 pientä pikkuaivokulman meningioomaa sairastavaa potilasta, joista 53 oli miehiä ja 109 naisia, joiden keski-ikä oli 54, 85 vuotta (21-89 vuotta). Ennen leikkausta oireina olivat päänsärky ja huimaus (96), kuulon heikkeneminen ja tinnitus (48), kasvojen tunne ja halvaus (29), kävelyn epävakaus ja ataksia (28), käheys, huono yskänrefleksi (16). Potilaista 77: llä oli kaksi tai useampia oireita ja 64: llä ei ollut oireita ennen diagnoosia.
kasvainten luonne
kasvainten tilavuus vaihteli 1, 042-8, 161 cm3, keskimäärin 4, 710 cm3; 72 potilaalla oli etukasvaimia, 41 potilaalla keskimmäisiä kasvaimia ja 49 potilaalla takakasvaimia; 148 potilaalla oli WHO: n I luokan kasvaimia ja 14 potilaalla WHO: n II luokan kasvaimia.
leikkaustulokset
Simpson I-asteen tapauksia oli 152 ja Simpson II-asteen tapauksia 10, leikkauksen jälkeistä oireiden lievitystä 41, merkitsevää muutosta ei tapahtunut 110, pahenemista tai uusia oireita 11.
Sädehoitoryhmä
tutkimukseen osallistui yhteensä 1644 pientä pikkuaivopontiinikulman meningioomaa sairastavaa potilasta, joista 335 oli miehiä ja 1309 naisia (Taulukko 1).
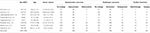
Taulukko 1. Potilaiden ominaisuudet kirjallisuudessa.
sädehoitoryhmästä 971 potilaalla (59, 1%) oireet eivät muuttuneet merkitsevästi hoidon jälkeen, 546 potilaalla (33, 2%) oireet lievenivät ja 127 potilaalla (7, 7%) oireet pahenivat tai heille kehittyi uusia neurologisia oireita.
potilaita oli 151 (9.2%) sädehoitoryhmässä, jossa kasvain uusiutui seurannan aikana.
toista stereotaktista sädehoitoa sai 54 potilasta (3, 3%) ja seurannan aikana leikattiin 62 potilasta (3, 8%).
oireelliset tulokset
leikkausryhmästä 102 potilaalla (63, 0%) oireet eivät muuttuneet merkitsevästi leikkauksen jälkeen, 49 potilaalla (30, 2%) oireet lievenivät ja 11 potilaalla (6, 8%) oireet pahenivat tai heille kehittyi uusia neurologisia oireita. Oireiden pahenemisessa leikkausryhmän ja sädehoitoryhmän välillä ei ollut merkittävää eroa, lukuun ottamatta Andrew ym.tutkimus (taulukko 2). Andrew et al. oli huomattavasti suurempi kuin leikkausryhmällä.
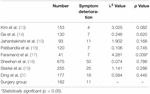
Taulukko 2. Oireiden pahenemisnopeus.
radiologiset tulokset
leikkausryhmässä oli 10 potilasta (6, 2%), joilla kasvain uusiutui seurannan aikana. Emme löytäneet merkittävää eroa kasvaimen laajentumisnopeudessa leikkausryhmän ja sädehoitoryhmän välillä, lukuun ottamatta Robert et al. (Taulukko 3). Kasvaimen laajentumisaste Robert et al. oli huomattavasti suurempi kuin leikkausryhmällä.
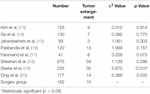
Taulukko 3. Kasvaimen laajentumisnopeus.
jatkohoito
leikkausryhmässä oli yksi potilas (0, 6%), jolle tehtiin toinen resektio, ja 12 potilasta (7, 4%) sai stereotaktista sädehoitoa seurannan aikana. Emme löytäneet merkittävää eroa jatkohoitojen määrässä leikkausryhmän ja sädehoitoryhmän välillä, paitsi Kyung et al. ja Andrew et al. (Taulukko 4). Kyungin ym.jatkohoitoprosentti oli huomattavasti pienempi kuin leikkausryhmän, kun taas jatkohoito määrä Andrew et al. oli huomattavasti suurempi kuin leikkausryhmällä.
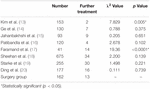
Taulukko 4. Jatkohoito.
LEIKKAUSRYHMÄSSÄ WHO: n luokka II ja Simpsonin luokka II olivat jatkohoidon riskitekijöitä (Taulukko 5).

Taulukko 5. Jatkokäsittelyjen riskitekijät.
Keskustelu
leikkauksen tai stereotaktisen sädehoidon valinta riippuu potilaiden yleisestä tilanteesta ja kasvainten luonteesta (7). Suurin osa pikkuaivokulman meningioomista kuuluu hyvänlaatuisiin kasvaimiin. Pikkuaivokulman meningioomien kirurginen vaikutus on aina tyydytetty, ja sekä leikkauksen jälkeisten oireiden heikkenemisen että kasvaimen laajentumisen määrä on pienempi kuin muilla hermoston kasvaimilla. Kuitenkin, puristus aivorungon ja pikkuaivot on usein esiintyminen pikkuaivojen kulma meningiomas, erityisesti potilailla, joilla on suuri pikkuaivojen kulma meningiomas, korkea kallonsisäinen paine voi johtaa herniation ja akuutti vesipää. Joko täydellinen tai osittainen resektio voi merkittävästi vähentää komplikaatioiden riskiä. Siksi leikkaus on paras valinta potilaille, joilla on suuret pikkuaivokulma meningiomas. Pienten pikkuaivojen meningiomas, stereotaktinen sädehoito, mukaan lukien Gammaveitsi, cyber veitsi ja muunlainen lineaarinen kiihdytin (8), on yleisesti tunnustettu ensimmäinen valinta. Lääkehoidon kehittymisen ja magneettikuvauksen popularisoinnin myötä pikkuaivokulman meningiooman varhainen diagnoosi pienitilavuudessa tai oireettomassa vaiheessa muuttuu mahdolliseksi. Varhainen diagnoosi ja hoito parantaa huomattavasti ennustetta pikkuaivojen kulma meningiooma, sekä tuo sekaannusta valinta leikkaus ja stereotaktinen sädehoito pienten pikkuaivojen kulma meningiooma. Kun otetaan huomioon aivokudoksen turvotus ja kiinnittyminen stereotaktisen sädehoidon jälkeen, mikä haittasi jatkoleikkauksia, yhä useammat tutkimukset ovat tukeneet varhaisia leikkaushoitoja.
leikkausten esioireiden lievittämisen osalta oireiden pahenemisnopeus leikkausryhmässä oli sama tai jopa pienempi kuin sädehoitoryhmässä. Stereotaktiseen sädehoitoon verrattuna leikkaushoito voi joskus johtaa parempiin tuloksiin ennen leikkausta ilmenevien oireiden lievittämisessä. Perifeerisen aivokudoksen turvotus on stereotaktisen sädehoidon yleinen sivuvaikutus. Aivokudoksen turvotus pahentaa hermojen jännitystä ja puristusta, minkä vuoksi oireet pahenevat stereotaktisen sädehoidon jälkeen. Jotta voidaan vähentää hermovaurioita ja lievittää oireiden pahenemista, käyttäjien on suojattava huolellisesti aivokudosta, hermoja ja verisuonia leikkauksen aikana. Verrattuna säännöllisiin pikkuaivokulma meningioomat, kirurginen toimenpide pienten pikkuaivokulma meningioomat vaatii enemmän suojaa hermoja ja verisuonia, ja neuroelektrofysiologista seurantaa koko leikkausprosessin aikana pidetään välttämättömänä, mikä osaltaan vähentää oireiden huononemista leikkausryhmässä. Yleisin kliininen ilmentymä pienten pikkuaivojen kulma meningiomas on toiminnallisia vikoja kasvojen ja kuulohermojen. Siksi kasvojen ja kuulohermojen suojaaminen on keskeinen osa leikkausta. Erilaiset pikkuaivojen kulma meningiomas työntää kasvojen ja kuulon hermoja eri asentoihin (9). Siten, ensimmäinen vaihe pienten pikkuaivojen kulma meningeomas leikkaus on paikallistamiseen kasvojen ja kuulohermot. Anterior kasvaimet yleensä työntää kasvojen ja kuulo hermoja sivusuunnassa tai sivusuunnassa huonompi puoli. Posterior kasvaimet yleensä työntää kasvojen ja kuulo hermoja medial tai medial huonompi puolella. Keskimmäinen kasvaimet yleensä työntää kasvojen ja kuulohermot pystysuoraan (kuva 2). Kasvaimen puristuksen vuoksi kasvojen ja kuulon hermot ovat usein pitkänomaisia ja niistä tulee ohuita ja värimuutoksia.
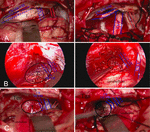
kuva 2. (A) Anterior kasvaimet työntää kasvojen ja kuulohermon sivusuunnassa. (B) Keskimmäinen kasvaimet työntää hermo ventraalinen näkökohta. (C) Posterior kasvaimet työntää hermo medial huonompi puolella.
leikkauksen aikana käyttäjän on vaadittava terävää erottelua erotettaessa kasvain kasvojen ja kuulon hermoista. Kasvojen ja kuulohermojen sekä pikkuaivojen pito tulisi minimoida. Kasvo-ja kuulohermojen ympärillä olevia ravintoastioita tulisi säilyttää mahdollisimman paljon. Vaikka kasvojen ja kuulohermot ovat anatomisesti säilynyt leikkauksen jälkeen, menetys hermotoiminnan edelleen olemassa monilla potilailla, jotka voivat johtua invasiivisia kasvua kasvaimia, intraoperative veto, ja lämmön johtuminen vamman aiheuttama elektrokoagulaatio (10). Tehokas intraoperatiivinen neuroelektrofysiologinen seuranta voi vähentää hermovauriota mahdollistamalla kasvojen ja kuulon hermojen oikea-aikaisen sijainnin, mikä lisää hermotoimintojen säilymisnopeutta.
kasvaimen etenemisen estämisen osalta kasvaimen uusiutumisprosentti leikkausryhmässä on sama tai jopa pienempi kuin sädehoitoryhmässä. Stereotaktiseen sädehoitoon verrattuna kirurginen hoito voi johtaa parempiin tuloksiin kasvaimen etenemisen estämisessä. Stereotaktinen sädehoito, joka viittaa lähinnä Gammaveitseen ja kyberveitseen, estää kasvaimen etenemistä tappamalla kasvainsoluja. Stereotaktisen sädehoidon kohde sijaitsee yleensä kasvainten keskustassa, ja sen annos pienenee, kun kasvainten keskustasta on etäisyyttä. Vaikka perifeerinen annoksen lisälaite tekniikka on syntynyt viime vuosina, ongelma epätäydellinen kasvaimen rajan inaktivointi on edelleen olemassa, mikä johtaa myös kasvainlaajentumisnopeuden kasvuun sädehoitoryhmässä (11). Kirurgiseen hoitoon pienten pikkuaivojen kulma meningiomas, yhteensä resektio kasvain, dural kiinnitys, ja kallo ovat avain estää kasvaimen uusiutumisen. Kirurgisessa periaatteessa käyttäjän on poistettava dural-kiinnitys ja kallo kasvaimen resektion jälkeen Simpson grade I: n saavuttamiseksi. Kun dural kiinnitys ja kallo resektoitiin epätäydellisesti, elektrokoagulaatio on välttämätöntä vähentää kasvaimen uusiutumisen mahdollisuutta ja saavuttaa Simpson grade II. radiotaajuisten laserskalpelien ja muiden mikroinstrumenttien kehittymisen myötä dural-kiinnityksen ja kallon resektion kirurginen hoito on tulossa yhä standardisoidummaksi. Yleinen kasvaimen resektionopeus pienten pikkuaivojen kulma meningeomas kasvaa, ja kasvaimen uusiutumisen määrä vähenee vuosi vuodelta.
monissa sädehoitotutkimuksissa on todettu, että pienten pikkuaivokulman meningioomien uusiutuminen on yhteydessä kasvainten patologiaan. WHO grade II meningioomat uusiutuvat todennäköisemmin kuin WHO grade I meningioomat,mikä liittyy voimakkaaseen invasiiviseen kasvuun. Stereotaktinen sädehoito ei kuitenkaan voi saada kasvainkudosta tutkimaan kasvaimen patologiaa suoraan. Siksi sädehoidolla hoidettujen pikkuaivokulman meningeomien aste päätellään useimmiten kuvantamistutkimuksella, mikä on epävarmaa. Toisin kuin stereotaktinen sädehoito, leikkaus voi suoraan saada kasvainkudosta patologista tutkimusta varten ja ohjata jatkohoitoa tarkan patologisen tutkimuksen tulosten kautta. Tässä tutkimuksessa WHO: n luokka II ja Simpsonin luokka II olivat riskitekijöitä kasvaimen uusiutumiselle leikkauksen jälkeen. Siksi leikkaukseen menevien WHO: n tai Simpsonin luokan II potilaiden on saatava jatkohoitoja varhaisessa vaiheessa sen sijaan, että he odottaisivat kasvainten uusiutumista. Tämä on myös syy siihen, miksi leikkausryhmässä uusiutumisprosentti oli hieman pienempi kuin sädehoitoryhmässä.
jatkohoitojen osalta jatkohoitojen määrä oli leikkausryhmässä sama tai jopa pienempi kuin sädehoitoryhmässä. Stereotaktiseen sädehoitoon verrattuna leikkaushoitoa saavilla potilailla saattaa siis olla pienempi todennäköisyys jatkohoitoihin. Teoksessa Kyung et al.tutkimuksessa koehenkilöt olivat oireettomia potilaita, joilla oli pieniä pikkuaivokulman meningioomia. Oireiden tai suhteellisen lievien oireiden puuttuminen voi merkittävästi vähentää potilaiden subjektiivista halua hoitoon, mikä voi olla syynä Jatkohoitojen määrään Kyung et al-tutkimuksessa. oli pienempi kuin leikkausryhmässä raportoitu. Sädehoitoryhmässä ei ollut merkittävää eroa sädehoidon jatkon valinneiden ja leikkaukseen hakeutuneiden potilaiden välillä. Leikkausryhmässä oli yksi potilas (0, 6%), jolle tehtiin toinen resektio, ja 12 potilasta (7, 4%) sai stereotaktista sädehoitoa seurannan aikana. Syy sädehoidon jatkamiseen leikkausryhmän potilaille oli kasvaimen suuri invasiivisuus ja duraalikiinnityksen ja kallon puutteellinen hoito (12). Kuten muutkin meningiomas, stereotaktinen sädehoito pienten pikkuaivojen kulma meningioomat on todennäköisemmin ylimääräinen hoito estää kasvaimen etenemisen leikkauksen jälkeen.
kirurgisiin komplikaatioihin kuuluivat pääasiassa kasvojen ja kuulon hermojen, kolmoishermon ja takaraivon hermojen toimintahäiriöt sekä vesipää. Kasvohalvaus, kasvojen tunnottomuus ja kuulon heikkeneminen voivat vaikuttaa vakavasti potilaiden elämänlaatuun leikkauksen jälkeen. Takaraivon hermovaurion oireet, kuten käheys, dysartria ja heikentynyt yskänrefleksi, vaikuttavat merkittävästi potilaiden ennusteeseen leikkauksen jälkeen. Koska pieni koko kasvaimen, komplikaatioita, kuten vesipää ja intrakerebraalinen verenvuoto, ovat harvinaisia potilailla, joilla on pieniä pikkuaivojen kulma meningioomat.
johtopäätös
verrattuna stereotaktiseen sädehoitoon pienten pikkuaivojen leikkaushoito voi joskus johtaa parempiin tuloksiin ennen leikkausta ilmenevien oireiden lievittämisessä ja kasvaimen etenemisen estämisessä. Jatkohoitojen osalta verrattuna stereotaktisen sädehoidon epävarmuuteen leikkaushoidolla voidaan saada tarkkoja patologisia tutkimustuloksia, jotka ohjaavat jatkohoitoa. Samanlaisia suuria kasvaimia, leikkaushoito olisi ensimmäinen valinta pienten pikkuaivojen kulma meningiomas, kun taas stereotaktinen sädehoito, lääkehoito ja kokeellinen hoito sopivat paremmin täydentää leikkaushoitoa.
tiedon Saatavuuslausunto
tekijät asettavat tämän artikkelin päätelmiä tukevat raakatiedot ilman aiheetonta varaumaa saataville.
eettinen lausunto
tutkimukset, joihin osallistui ihmisiä, tarkastettiin ja hyväksyttiin Soochowin yliopiston ensimmäisen Liitännäissairaalan institutionaalisessa Arviointilautakunnassa ja eettisessä komiteassa. Potilaat / osallistujat antoivat kirjallisen tietoon perustuvan suostumuksensa osallistua tähän tutkimukseen.
Tekijäosuudet
JW ja GC suunnittelivat tutkimuksen. JB, PP, hy, WG, YL, ZY ja ZW suorittivat kokeet ja analysoivat tiedot. JB kirjoitti käsikirjoituksen. Kaikki kirjoittajat lukivat ja hyväksyivät käsikirjoituksen. JB, PJ ja HY ovat osallistuneet tähän työhön yhtä lailla. Kaikki kirjoittajat osallistuivat artikkelin ja hyväksyi toimitetun version.
Rahoitus
tätä työtä tukivat Jiangsu Provincial Medical Key Talent-apuraha (ZDRCA2016040) ja Suzhoun hallituksen apuraha (SYS2019045).
eturistiriita
kirjoittajat toteavat, että tutkimus tehtiin ilman kaupallisia tai taloudellisia suhteita, joita voitaisiin pitää mahdollisena eturistiriitana.
1. Kankane VK, Warade AC, Misra BK. Nonvestibular schwannoma kasvaimia pikkuaivoissa: yhden kirurgin kokemus. Aasialainen J Neurokirurgi. (2019) 14:154–61. doi: 10.4103 / ajns.ajns_335_17
CrossRef kokoteksti / Google Scholar
2. Faramand A, Kano H, Niranjan A, Park K-J, Flickinger JC, Lunsford LD. Kasvaimen hallinta ja kallon hermo tulokset jälkeen adjuvanttiradiokirurgian Alhainen kallo-base meningioomat. Maailman Neurokirurgi. (2019) 127:e221–9. doi: 10.1016 / j.wneu.2019.03.052
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Spena G, Sorrentino T, Altieri R, Zinis LR, Stefini R, Panciani PP, et al. Varhaisen uran kirurginen käytäntö pikkuaivojen kulma kasvaimia aikakauden radiokirurgian. J Neurol Surg B Skull Base. (2018) 79:269–81. doi: 10.1055 / s-0037-1606826
PubMed Abstrakti / CrossRef kokoteksti / Google Scholar
4. Magill ST, Lee DS, Yen AJ, Lucas CG, Raleigh DR, Aghi MK, et al. Leikkaustulokset uusiutuvien kallonpohjan meningioomien uudelleenavaamisen jälkeen. J Neurokirurgi. (2018) 130:876–83. doi: 10.3171 / 2017.11.jns172278
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Nowosielski M, Galldiks N,Iglseder S, Kickingereder P, Deimling A, Bendszus M, et al. Diagnostisia haasteita meningeoomassa. J Neuro Onkolia. (2017) 19:1588–98.
Google Scholar
6. Magill ST, Rick JW, Chen WC, Haase DA, Ralelgh DR, Aghl MK, et al. Petrous Kasvot meningioomas: luokittelu, kliiniset oireyhtymät, ja kirurgiset tulokset. Maailman Neurokirurgi. (2018) 114:e1266–74. doi: 10.1016 / j.wneu.2018.03.194
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Tomasello F, Angileri FF, Conti a, Scibilia A, Cardali s, Torre DL, et al. Petrosal meningioomat: lopputulokseen vaikuttavat tekijät ja intraoperatiivisen multimodaalisen avun rooli mikrokirurgiassa. Neurokirurgia. (2019) 84:1313–24. doi: 10.1093 / neuros/nyy188
CrossRef kokoteksti / Google Scholar
8. Goldbrunner R, Minniti G, Preusser M, Jenkinson MD, Sallabanda K, Houdart E, et al. Eano guidelines for the diagnosis and treatment of meningioomas. Lancet Onkol. (2016) 17:e383–91. doi: 10.1016 / S1470-2045(16)30321-7
CrossRef Kokoteksti / Google Scholar
9. Ehresman JS, Garzon-Muvdi T, Rogers D, Lim M, Gallia GL, Weingart J, et al. Riski kehittää leikkauksen jälkeisiä alijäämiä, jotka perustuvat kasvaimen sijaintiin kallonsisäisen meningeooman kirurgisen resektion jälkeen. J Neurol Surg B Skull Base. (2019) 80:59–66. doi: 10.1055 / s-0038-1667066
PubMed Abstrakti / CrossRef kokoteksti / Google Scholar
10. D ’ Amico RS, Banu MA, Petridis P, Bercow AS, Malone H, Praver M, et al. Tehokkuutta ja tuloksia kasvojen hermoja säästävä hoito lähestymistapa pikkuaivojen kulma meningiomas. J Neurokirurgi. (2017) 127:1231–41. doi: 10.3171 / 2016.10.JNS161982
CrossRef Full Text | Google Scholar
11. Iwai Y, Yamanaka K, Shimohonji W, Ishibashi K. järjesti gammaveitsiradiokirurgian suurten kallonpohjan meningeomien varalta. Cureus. (2019) 11: e6001. doi: 10.7759/cureus.6001
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Magill ST, Dalle Ore CL, Diaz MA, Jalili DD, Raleigh DR, Aghi MK, et al. Leikkaustulokset toistuvien ei-kallonpohjan meningioomien uudelleen avaamisen jälkeen. J Neurokirurgi. (2018) 1:1–9. doi: 10.3171/2018. 6JNS18118
CrossRef Full Text | Google Scholar
13. Kim KH, Kang SJ, Choi JW, Kong DS, Seol HJ, Nam DH, et al. Proaktiivisen Gammaveitsikirurgian kliiniset ja radiologiset tulokset oireettomien meningeomien osalta verrattuna luonnolliseen kulkuun ilman toimenpiteitä. J Neurokirurgi. (2018) 1:1–10. doi: 10.3171/2017. 12jns171943
CrossRef Full Text | Google Scholar
14. Ge Y, Liu D, Zhang Z, Li Y, Li Y, Wang G, et al. Gammaveitsen radiokirurgia hyvänlaatuisten kallonsisäisten meningioomien hoitoon: seurantatulos 130 potilaalla. Neurokirurgia. (2019) 46: E7. doi: 10.3171 / 2019.3.FOCUS1956
CrossRef Full Text | Google Scholar
15. Jahanbakhshi A, Azar M, Kazemi F, Jalessi M, Chanideh I, Amini E. Gammaveitsi stereotaktinen radiokirurgia pikkuaivojen kulmaan meningiooma. Clin Neurol Neurokirurgi. (2019) 187:105557. doi: 10.1016 / j.clineuro.2019.105557
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Patibandla MR, Lee CC, Tata a, Addagada GC, Sheehan JP. Stereotactic radiosurgery for WHO grade I posterior fossa meningioomas: long-term outcomes with volumetric evaluation. J Neurokirurgi. (2018) 129:1249–59. doi: 10.3171/2017. 6JNS17993
CrossRef Full Text | Google Scholar
17. Faramand a, Kano H, Niranjan a, Johnson SA, Hassib M, Park KJ, et al. Aivohermon tulokset primaarisen stereotaktisen radiokirurgian jälkeen oireisiin kallonpohjan meningioomiin. J Neuroncol. (2018) 139:341–8. doi: 10.1007 / s11060-018-2866-9
PubMed Abstrakti / CrossRef kokoteksti / Google Scholar
18. Sheehan JP, Starke RM, Kano H, Barnett GH, Mathieu D, Chiang V, et al. Gammaveitsi radiosurgery for posterior fossa meningioomas: a multicenter study. J Neurokirurgi. (2015) 122:1479–89. doi: 10.3171/2014. 10JNS14139
CrossRef Full Text | Google Scholar
19. Starke RM, Williams BJ, Hiles C, Nguyen JH, Elsharkawy MY, Sheehan JP. Gammaveitsen leikkaus kallonpohjan meningiomaan. J Neurokirurgi. (2012) 116:588–97.
Google Scholar
20. Ding D, Starke RM, Kano H, Nakaji P, Barnett GH, Mathieu d, et al. Gammaveitsi radiosurgery for cerebellopontine angle meningioomas: a multicenter study. Neurokirurgia. (2014) 75:398-408; tietovisa 408. doi: 10.1227 / NEU.000000000000000480
PubMed Abstract | CrossRef Full Text / Google Scholar