cuvinte cheie
pneumonia cu citomegalovirus; bronhiolitisobliteranii organizarea pneumoniei; imunocompetent
Introducere
manifestările clinice ale citomegalovirusului (CMV)infecția poate fi împărțită în Infecție primară acută Șireactivare. Infecția CMV primară apare cel mai frecventîn timpul alăptării și al copilăriei și este asimptomatică sau prezentă ca un sindrom ușor asemănător mononucleozei la adulții imunocompetenți . Apoi virusul persistă pentru viațăgazda, în general în stadiul latent. Reactivarea Cmvdin latență este bine cunoscută la pacienții imunocompromiși și poate afecta aproape orice organ. Cu toate acestea, pneumonia CMV severă este rară la gazdele imunocompetente . În prezent,mecanismele moleculare și imunologice precise implicate sunt încă necunoscute.
bronșiolita obliterantă organizarea pneumoniei (BOOP) este o afecțiune clinică caracterizată prin tuse, stare generală de rău, febră și dispnee și fără răspuns la antibiotice . Radiograful său este descris ca fiind local, multiplu și difuzează modificări. Poate fi găsit cu alveolită alergică, pneumonită de iradiere, reacții medicamentoase și alte infecții Organizatoare. Cazuri implicate în etiologia virală complicată cu Boofau fost raportate sporadic. Aici, prezentăm un caz de pneumonie cmmv asociată cu BOOP la un pacient imunocompetent prin terapia cu ganciclovir, care esteprimul astfel de caz raportat vreodată din câte știm.
raport de caz
un bărbat de 63 de ani a fost trimis la spitalul nostru din cauza unui istoric de tuse și febră de 10 zile. Avea o tuse paroxistică cu spută galbenă. Febră, cu respirație șuierătoare a apărut în principal îndupă-amiaza și noaptea, iar cea mai mare temperatură a fost39, 3(102, 74). Istoricul său medical anterior a inclus hipertensiune arterială, diabet și gută. Istoria sa anterioară de familieera de neimaginat. Semnele sale vitale au fost următoarele: corptemperatura: 36,5(97,7), ritmul cardiac: 98 bătăi pe minut (BPM), tensiunea arterială: 98/61 mmHg.
la examenul fizic, au fost observate crackle inspiratorii târzii în câmpurile bilaterale pulmonare inferioare. Numărul de celule albe din sânge(WBC) a fost de 14,2 109/l, cu 81,9% neutrofile (NEUTRR), 12,8% limfocite (LYR) și 0,53 109/lmonocite (MONOR) (Figura 1). Nivelul seric al proteinei C reactive (CRP) a fost de 110,67 mg/L.
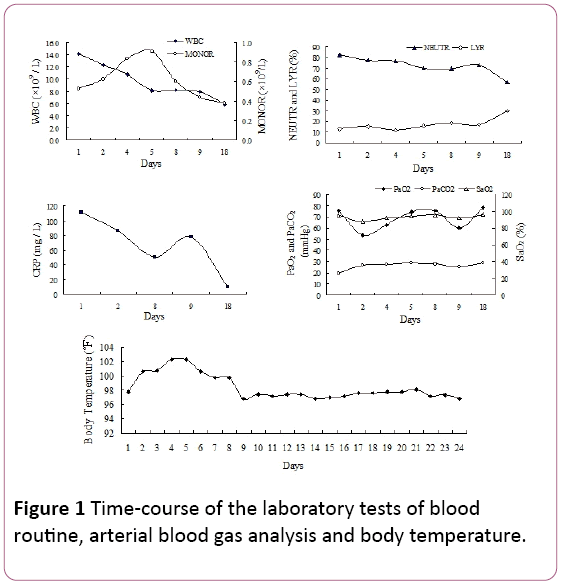
Figura 1: Timpul-cursul testelor de laborator ale sângelui, analiza gazelor arteriale din sânge și temperatura corpului.
presiunea parțială arterială a oxigenului (PaO2) a fost de 75,5 mmHg,cu 25,8 mmHg presiunea parțială arterială a CO2 (PaCO2) și94,7% saturație de oxigen (SaO2, 2 L/min Alimentare cu oxigen canulă vianazală). Din cauza febrei și a semnelor de infecții respiratorii, am început experiențial tratamentul antibiotic cu piperacilină tazobactam. Cu toate acestea, pacientultemperatura nu a redus și scurtarea respirațieidezvoltat în 4 zile persistente de internare în spital.
măsurătorile gazelor arteriale au evidențiat eșecul respirației (PaO2: 53,5 mmHg, PaCO2: 35,6 mmHg, SaO2: 87,7%) cu acidoză metabolică contrabalansată (HCO3 -: 21mmol/l, pH 7,39) atunci când se utilizează 2 L/min oxigen de către canula nazală.Rezultatele investigațiilor de laborator au fost următoarele: anticorp mioplasmapneumonie: 1: 40 (pozitiv), endotoxină bacteriană (conținutul total de lipopolizaharidă a bacteriilor gram negative): 49,14 pg/ mL, fibrinogen plasmatic (Fg): 7,51 g/L, timp de tromboplastină parțială activat (APTT): 45,9 secunde.
electrocardiograma a arătat tahicardie sinusală cu modificări Twave. Radiografia toracică a găsit două infecții pulmonare, nucu excepția leziunilor interstițiale pulmonare (figura 2A). O tomografie computerizată toracic (CT) a evidențiat leziuni interstițiale pulmonare (umbra grilei în ambii plămâni) și mărirea ganglionilor limfatici mediastinali (figura 2D). Apoi, 3,5 L / min oxigen a fost furnizat cu mască de față și tratamentul cu antibiotice a fost trecut la Cefoperazonă sodică șisulbactam sodic plus levofloxacină.
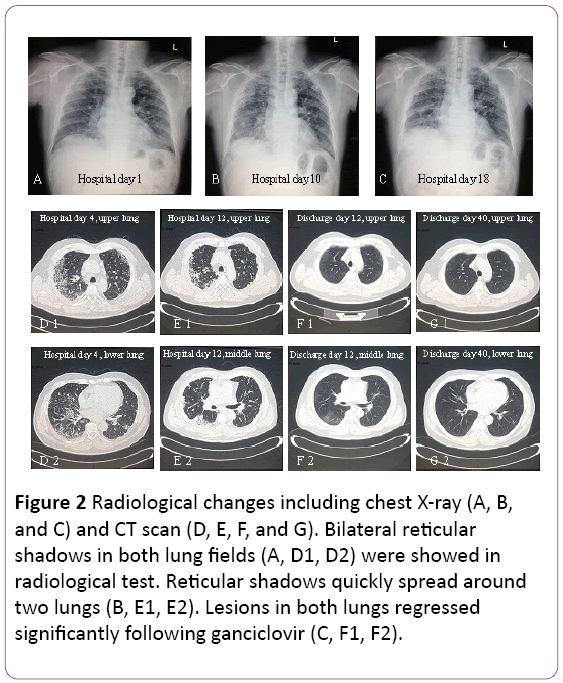
Figura 2: Modificări radiologice, inclusiv radiografia toracică (A, B și C) și scanarea CT (D,E, F și G). În cadrul testului radiologic au fost prezentate umbre reticulare bilaterale în ambele câmpuri pulmonare (A, D1, D2). Umbrele reticulare se răspândesc rapid în jurdoi plămâni (B, E1, E2). Leziunile din ambii plămâni au regresatîn mod semnificativ după ganciclovir (C, F1, F2).
având în vedere diagnosticul unei pneumonii interstițiale, în ziua 5 au fost efectuate teste de laborator relevante și bronhoscopie fibroptică. Rezultatele testelor de laborator au fost următoarele: CMV PCR: negativ, CMV IgM: negativ, imunoglobulină IgG: pozitiv, HIV: negativ, WBC: 7.96 109 / L, NEUTR: 72.4%,LYR: 17%, CRP: 77.51 mg/l, funcție imunologică (celule T, B, NK):normal, subseturi de limfocite T: normal. Markerii pentru bolile autoimune, inclusiv perinuclear-ANCA (p-ANCA),citoplasmatic-Anca (c-ANCA), ANA și anti-dsDNA au fost toate negative.
funcția pulmonară a sugerat disfuncție ventilatorie moderată restrictivă. Scanarea cu raze X și CT au evidențiat leziuni peapulmonarul superior a fost absorbit, dar a fost exacerbat în plămânul inferior drept (figurile 2b și 2e).
o bronhoscopie a arătat bronșită bilaterală (figura 3a).Lichidul de lavaj bronhoalveolar (BAL) a fost formicobacterii negative și pata PAS. Numărul de celule diferențiale a arătat11 % neutrofile, 19% limfocite și 70% macrofage.S-au găsit corpuri de incluziune intranucleară și intracitoplasmicăîn segmentul bazal lateral al țesutului pulmonar transbronchialbiopsy (TBLB) din dreapta jos (figura 3b). Pe baza diagnosticului pneumoniei cu citomegalovirus cu organizare, tratamentul cu ganciclovir (5 mg/kg) prin perfuzie intravenoasă la fiecare 12 ore a fost început în ziua 8. Conform celor de mai susgăsirea combinării cu simptomele clinice (febra dispare),tratamentul cu antibiotice a fost schimbat în moxifloxacină în ziua8. După 1 săptămână de terapie antivirus, tuse persistentă. El a suferit o biopsie pulmonară prin CT-ghidată. O biopsie pulmonară a fost dezvăluităbuclă (figura 3C). Apoi, pacientul trata cu steroid oralhormon. Cu toate acestea, simptomele sale s-au îmbunătățit treptaturmătoarele 1 săptămână. Radiografia toracică a arătat că două afecțiuni pulmonare au fost mai bune decât înainte (figura 2c).
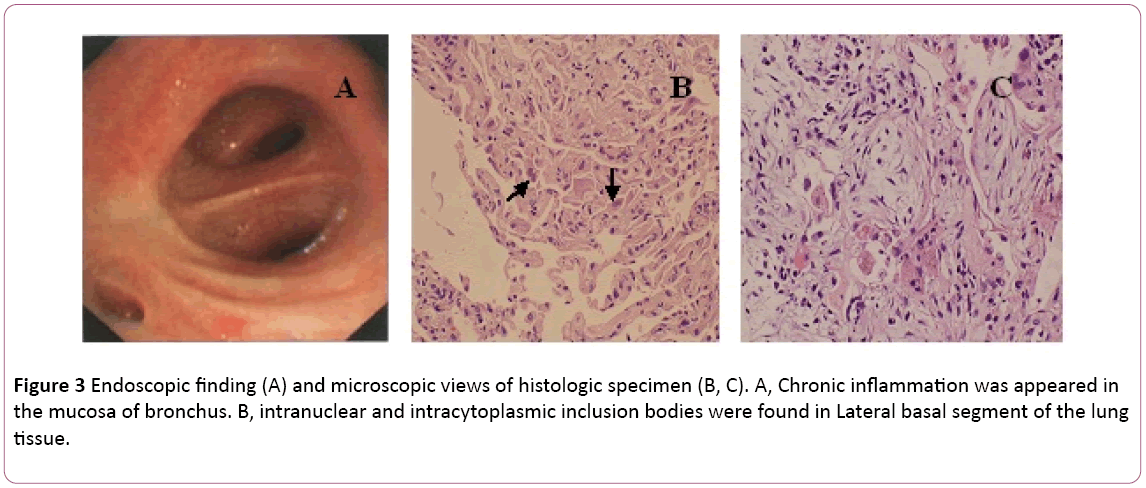
Figura 3: Constatare endoscopică (A) și vederi microscopice ale specimenului histologic (B, C). A, a apărut inflamația Cronicămucoasa bronhiilor. B, corpurile de incluziune intranucleară și intracitoplasmatică au fost găsite în segmentul bazal Lateral al plămânuluițesut.
tratamentul a fost schimbat în ganciclovir oral, 0,6 g/zi (q12h)timp de 7 zile, descărcare. În urmărirea sa, shadow of grid în ambeleplămânii au regresat semnificativ (figura 2f și 2G). El este încăsub urmărire la Clinica de ambulatoriu.
discuție
CMV este un virus ADN din familia Herpesviridae, iar infecția sa este comună. Într-adevăr, 40% până la 100% dintre adulți suntinfectate cu CMV în întreaga lume . Infecții cu CMVÎN populația generală sunt de obicei subclinice. Infecția simptomatică cu CMV a apărut în principal la pacienții imunocompromiși cu disfuncție imună, inclusiv la pacienții cu SIDA, malignitate,pacienți cu transplant și nou-născuți . În cazurile cu imunodeficiență, Cmvinfecția poate provoca pneumonie, retinită,hepatită, encefalită, polineuropatie demielinizantă,miocardită, pancreatită,boli gastro-intestinale și boli suprarenale și așa mai departe . Dimpotrivă, amenințarea gravă a viețiiinfecția indusă de CMV, inclusiv pneumonia CMV, este dificilă la persoanele imunocompetente . În această lucrare descriem un caz de pneumonie CMV, asociat cu BOOPin o gazdă imunocompetentă și tratat eficient cu ganciclovir.
pneumonia CMV se prezintă adesea ca pneumonie virală severă, cu infiltrate interstițiale difuze pe radiografie toracică șiinsuficiență respiratorie . Diagnosticul de laborator poate fidificile și se fac serologic sau patologic.În general, testele serologice pentru detectarea infecției umane cu CMV includ titrul de anticorpi CMV (IgM,IgG), proteina CMVPP65 și CMV PCR . Important, histopatologicdetectarea corpurilor de incluziune CMV pe biopsia transbronhială sau deschisă este patognomonică, deoarece pneumonia CMV la pacienții imunocompetenți reprezintă un eveniment rar .
pacientul nostru a prezentat simptome nespecifice (tuse și febră), care s-au dezvoltat pe parcursul a 10 zile.Simptomele s-au agravat după 2 zile de spitalizare(hipoxemie severă), în ciuda tratamentului empiric cu antibiotice. Diagnosticul pneumoniei CMV s-a bazat pe TBLB, care a fost găsit corpuri de incluziune intranucleară și intracitoplasmatică în celule gigantice ca standard de aur. Mai mult, anticorpul seric CMV IgG pozitiv a fost un alt indice de diagnostic. Imaginea radiologică incluzând radiografia toracică și scanarea CT care arată umbre reticulare bilaterale în ambele câmpuri pulmonare au susținut diagnosticul de pneumonie virală. În cazul nostru, mononucleoza derutina de sânge a fost de asemenea observată (Figura 1). Cu toate acestea, serumIgM CMV a fost negativ în acest caz, ceea ce a fost în conformitate cu raportul Eddleston . CMV PCR a fost, de asemenea, negativ. Poate explica prin rezultate fals negative induse de natura tranzitorie a viremiei .
în timpul spitalizării, rata limfocitelor sale a scăzutîn mod semnificativ. Limfopenia a fost cauzată de infecția cu CMV atât pentru inhibarea directă a creșterii celulelor progenitoare, cât și pentru eșecul auto-reînnoirii celulelor stem . Se poate observa că analiza funcției imune, cum ar fi subsetul celulelor T, celula B și nkcell, au fost normale. În acest caz nu s-au observat anomalii tranzitorii sau subclinice ale celulelor T și o inversare a raportului CD4/CD8 al celulelor T. În boala HIV, o scădere a celulelor CD4 + < 100 10 6/L reprezintă un risc ridicat pentru boala CMV. În plus, pacientul nostru nu a prezentat dovezi ale altor imunodeficiențe (HIV: negativ) și boli autoimune (anticorp autoimun: negativ).
BOOP a fost descris pentru prima dată de Epler și colab. și de atunci a fost investigat pe larg și raportat în întreaga lume . Există mulți agenți infecțioși care pot fiasociate cu BOOP, cum ar fi citomegalovirusul (CMV), virusul herpessimplex (HSV) . De asemenea, au fost raportate infecții parazitare și pneumocystis carinii . Deoarece modul BOOPrepresent în care plămânul poate răspunde la un stimul inflamator, constatările patofiziologice cheie sunt legate de calea inflamatorie. Caracteristici histologiceinclud țesut de granulare în pereții alveolelor șibronhioles sunt semnificative, asociate cu infiltrarea încavitatea interstițială și traheală prin diferite grade decelule mononucleare și celule de spumă. Epitelial alveolar de tip II hiperplazia celulară poate fi, de asemenea, observată . În actualul pacient, BOOP a fost diagnosticat în biopsia pulmonară cu o săptămână mai târziu decât TBLB, sugerând că CMV poate fi cel mai probabilpatogen.
deși nu există o durată standard recomandată pentrutratamentul cuanciclovir pentru pacienții cu pneumonie CMV, medicamentul poate fi început numai după diagnosticul definitiv și este administrat în mod obișnuit timp de două până la trei săptămâni. Cât mai curândtratamentul cu ganciclovir, starea clinică a pacientului nostru a fost îmbunătățită, cu o rezoluție completă a tabloului clinic șidradiologic sub o lună de urmărire.
concluzie
raportăm un caz acut de infecție cu CMV, care a prezentatcu febră, tuse, spută și tahipnee. Acesta din urmădeteriorat rapid și este asociat cu insuficiență respiratorie.Scanarea CT a relevat o mică schimbare de sticlă măcinată la debut, dar schimbarea s-a răspândit rapid în jurul a doi plămâni. În urma examinării patologice (TBLB) s-a confirmat diagnosticul de Cmvpneumonie. Pentru pacienții cu noitulburări de imunodeficiență, este foarte ușor să se diagnosticheze greșit.Raportul actual sugerează că, atunci când arată piept CTLEZIUNI interstițiale,în plus față de a lua în considerare tuberculoza, pneumonie bacteriană și alte boli virale, CMVpneumonia ar trebui să fie incluse la pacienții vârstnici cu avarietate a bolii de bază. Important, acest caz a demonstratcă pneumonia cu citomegalovirus se poate asocia cu BOOP inun pacient imunocompetent. Tratamentul cu Ganciclovir esteeficiente. Sunt necesare studii suplimentare pentru a analizarelațiile și mecanismul său de bază între CMVpneumonia și BOOP.
contribuțiile autorului
CXC a redactat și a scris manuscrisul. Wc, LL și LYH au luatîngrijirea pacientului și a contribuit la coordonareamanescript. XL a efectuat testele microbiologice. Lyhcontribuit la proiectul manuscrisului și revizuit themanuscript. Toți autorii au citit manuscrisul șia aprobat versiunea finală.
mulțumiri
îi suntem recunoscători Prof.Zhiqiang Qin pentru sprijinul său teoretic.
- Hamprecht K, Maschmann J, Vochem M, Dietz K, Speer CP, și colab. (2001) Epidemiologia transmiterii citomegalovirusului de la mamă la sugarul prematur prin alăptare. Lanceta 357: 513-518.
- Carter D, Olchovsky D, Pokroy R, Ezra D (2006) colită asociată cu citomegalovirus care provoacă diaree la un pacient imunocompetent. Lumea J Gastroenterol12: 6898-6899.
- Kralickova P, Mala E, Vokurkova D, Krcmova I, Pliskova L, și colab. (2014) boala citomegalovirusului la pacienții cu imunodeficiență variabilă comună: trei rapoarte de caz. Arhivele internaționale de alergie și Imunologie 163: 69-74.
- Eddleston M, Peacock S, Juniper M, Warrell DA (1997) infecție severă cu citomegalovirus la pacienții imunocompetenți. Clin Infecta Dis 24: 52-56.
- Cunha BA (2010) pneumonia cu citomegalovirus: pneumonie dobândită în comunitate la gazdele imunocompetente. Infecta Dis Clin Nord Am 24: 147-158.
- Cohen JI, Corey GR(1991) Cytomegalovirus infection in the normal host. Medicine 1985; 64:100-114.
- Geddes DM. BOOP and COP. Thorax46:545-547.
- Hansell DM (1992) What are bronchiolitis obliterans organizing pneumonia (BOOP) and cryptogenic organizing pneumonia (COP)? ClinRadiol45:369-70.
- Cunha BA, Syed U, Mickail N(2012) Renal transplant with bronchiolitis obliterans organizing pneumonia (BOOP) attributable to tacrolimus and herpes simplex virus (HSV) pneumonia. Heart & Lung 41:310-315
- Bitzan m, Ouahed JD, Carpineta l, Bernard C, Bell LE(2010) pneumonie Organizatoare criptogenă după terapia cu rituximab pentru presupusa boală limfoproliferativă post-transplant renal. Nefrologie Pediatrică 25: 1163-1167.
- de la Hoz RE, Stephens G, Sherlock C (2002) abordări de diagnostic și tratament ale infecțiilor cu CMV la pacienții adulți. J ClinVirol 25: 1-12.
- Sanadgol N, Ramroodi n, Ahmadi GA, Komijani M, Moghtaderi A, și colab.(2011)prevalența infecției cu citomegalovirus și rolul său în modelul imunoglobulinei totale la pacienții Iranieni cu diferite subtipuri de scleroză multiplă. Noua Microbiologica 34: 263-274.
- Chiotan C, Radu l, Serban R, Cornacel C, Cioboata M, și colab. (2014) retinita cu citomegalovirus la pacienții cu HIV/SIDA. Jurnalul de Medicină și viață 7: 237-240.
- Liu WL, lai CC, Ko WC, Chen YH, Tang HJ, și colab. (2011) caracteristicile clinice și microbiologice ale infecțiilor cauzate de diferite specii de Nocardia din Taiwan: Un studiu multicentric din 1998 până în 2010. Eur J ClinMicrobiol Infecta Dis30: 1341-1347.
- Beam E, Razonable RR(2012)citomegalovirus în transplantul de organe solide: Epidemiologie, prevenire și tratament. Curr Infecta Dis Rep14: 633-641.
- Westman G, Berglund D, Widen J, Ingelsson M, Korsgren O, și colab. (2014) creșterea răspunsului inflamator la pacienții seropozitivi cu citomegalovirus cu boala Alzheimer. PloS one9: 96779.
- Carney WP, Rubin RH, Hoffman RA, Hansen WP, Healey K, și colab. (1981) analiza subseturilor limfocitelor T în mononucleoza citomegalovirusului. J Imunol126: 2114-2116.
- Boeckh M, Leisenring W, Riddell SR, Bowden RA, Huang ML și colab. (2003) boala citomegalovirusului târziu și mortalitatea la beneficiarii transplanturilor de celule stem hematopoietice alogene: importanța încărcăturii virale și a imunității celulelor T. Sânge 101: 407-414.
- Gunthard HF, Aberg JA, Eron JJ, Hoy JF, Telenti a,și colab. (2014) tratamentul Antiretroviral al infecției cu HIV la adulți: 2014 recomandări ale Societății Internaționale antivirale-Panoul SUA. JAMA 312: 410-425.
- Epler GR, Colby TV, McLoud TC, Carrington CB, Gaensler EA (1985) bronchiolitis obliterans organizarea pneumoniei. N Engl J Med 312:152-158.
- Kute VB, Patel MP, Patil SB, Shah PR, Vanikar AV,et al. (2013) Bronchiolitis obliterans organizing pneumonia (BOOP) after renal transplantation. IntUrolNephrol 45:1517-1521.
- White KA, Ruth-Sahd LA (2007) Bronchiolitis obliterans organizing pneumonia. Crit Care Nurse27:53-66.
- Yale SH, Adlakha A, Sebo TJ, Ryu JH(1993)Bronchiolitis obliterans organizing pneumonia caused by Plasmodium vivax malaria. Chest 104:1294-1296.
- Kleindienst R, Fend F, Prior C, Margreiter R, Vogel W(1999)Bronchiolitis obliterans organizing pneumonia associated with Pneumocystis carinii infection in a liver transplant patient receiving tacrolimus. Clin Transplant13:65-67.
- Moore SL (2003)Bronchiolitis obliterans organizing pneumonia: a late complication of stem cell transplantation. Clin J OncolNurs 7:659-662.