weergeven alle weefselcellen zijn afhankelijk van het aerobe metabolisme voor de opwekking van de energie (in de vorm van adenosinetri-fosfaat, ATP) die nodig is voor overleving en functie. Dit fundamenteel vitale mitochondriale proces wordt gekenmerkt door consumptie van zuurstof en productie van kooldioxide, die kan variëren van ongeveer 200 mL/minuut in de rusttoestand tot meer dan vijf keer dit tarief tijdens de oefening.
het uiteindelijke lot van dit kooldioxide is verwijdering uit het lichaam in uitgeademde lucht, en een belangrijke functie van het bloed is het transport van kooldioxide van weefselcellen naar longen.
een begrip van dit transportproces hangt af van een beoordeling van wat wordt bedoeld met partiële druk van een gas en van enkele fundamentele fysische wetten die de oplosbaarheid en beweging (diffusie) van gassen regelen.
- WAT IS PARTIËLE DRUK VAN EEN GAS?
- oplosbaarheid en diffusie van gassen
- TRANSPORT van koolstofdioxide van weefselcellen naar Long
- kooldioxide en de pH van het bloed
- in het laboratorium – definitie van CO2-PARAMETERS
- partiële druk van kooldioxide pCO2
- concentratie bicarbonaat (HCO3-)
- totale KOOLDIOXIDECONCENTRATIE in PLASMA (ctCO2)
- chemische methoden voor het meten van ctCO2
- discordantie tussen gemeten ctCO2 en berekend bicarbonaat
- samenvatting
WAT IS PARTIËLE DRUK VAN EEN GAS?
de hoeveelheid gas in een systeem, met inbegrip van biologische systemen, wordt bepaald door de druk die het uitoefent, traditioneel gemeten als de hoogte van een kolom kwik (mmHg). Dus door te zeggen dat de atmosferische druk 760 mmHg is bedoelen we dat de gassen (zuurstof, stikstof en kooldioxide) in de lucht die we inademen een gecombineerde druk hebben die voldoende is om een standaardkolom van 760 mm hoog te dragen.
deze totale druk is gewoon de som van de partiële druk van elk samenstellende gas. De lucht bevat dus ongeveer 20% zuurstof, 79% stikstof en 0 . 03% koolstofdioxide, de partiële druk van zuurstof (pO2) in geïnspireerde lucht is ongeveer (20 x 760) / 100 = 152 mmHg en partiële druk van koolstofdioxide (pCO2) is (0,03 x 760) / 100 = 0,2 mmHg.
de systeeme internationale (SI) drukeenheid, gebruikt in klinische laboratoria buiten Noord-Amerika, is de kilopascal (kPa). De conversiefactor 0,133 kan worden gebruikt om mmHg om te zetten in kPa.
oplosbaarheid en diffusie van gassen
de wet van Henry bepaalt dat bij evenwicht de hoeveelheid in een vloeistof opgelost gas evenredig is met de partiële druk van dat gas, zolang de temperatuur constant is:
opgelost gas = partiële druk (p) x oplosbaarheidscoëfficiënt (s)
waarbij S een temperatuurafhankelijke constante is voor het betreffende gas. De oplosbaarheidscoëfficiënt (S) voor kooldioxide bij lichaamstemperatuur is 0,23 mmol/l/kPa (of 0,03 mmol/mmHg) . Dus aangezien arteriële pCO2 ongeveer 5 is.3 kPa (40 mmHg), is de hoeveelheid CO2 opgelost in arterieel bloed (dCO2) (5,3 x 0,23) of 40 x 0,03) = 1,2 mmol/L.
de beweging (diffusie) van gassen wordt grotendeels bepaald door concentratiegradiënten. Gas verspreidt van hoge partiële druk naar lage partiële druk .
TRANSPORT van koolstofdioxide van weefselcellen naar Long
het koolstofdioxidetraject (figuur 1a) begint in de mitochondrion van weefselcellen waar het wordt geproduceerd. Door de heersende concentratiegradiënt verspreidt kooldioxide van mitochondriën (waar pCO2 het hoogst is) over het cytoplasma, uit de cel en in het capillaire netwerk.
figuur 1a: CO2 in weefsels
Klik om te vergroten
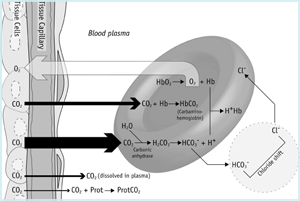
een klein deel van de CO2 die uit weefselcellen in het bloed terechtkomt, blijft fysiek opgelost in bloedplasma (zie hierboven) en een nog kleiner deel bindt zich aan NH2 (amino) terminale groepen plasma-eiwitten, die zogenaamde carbamino-verbindingen vormen. De meeste echter, verspreidt een concentratiegradiënt in rode cellen.
een klein deel hiervan blijft opgelost in het cytoplasma van de rode cel en sommige worden losjes gebonden aan amino terminale groepen van verminderde hemoglobine die carbamino-Hb vormen. Nochtans wordt het grootste deel van het kooldioxide die in rode cellen aankomen snel gehydrateerd tot koolzuur door de rode celisoform van het enzym koolzuuranhydrase. Bij fysiologische pH dissocieert bijna alle koolzuur (≈ 96 %) tot bicarbonaat – en waterstofionen:
vergelijking 1:
![]()
de waterstofionen worden gebufferd door verlaagd hemoglobine en de meeste bicarbonaationen gaan van de rode cel naar plasma in ruil voor chlorideionen (deze zogenaamde ‘chlorideverschuiving’ handhaaft elektrochemische neutraliteit). Uit het bovenstaande blijkt duidelijk dat de meeste kooldioxide als bicarbonaat wordt getransporteerd (voornamelijk in bloedplasma), maar er zijn in totaal vier wijzen van CO2-transport :
- 90 % als bicarbonaat in plasma (65 %) en rode bloedcellen wordt getransporteerd (25 %)
- 5 % fysisch opgelost in plasma wordt getransporteerd en cytoplasma van rode bloedcellen
- 5 % wordt los gebonden aan hemoglobine in rode cellen en
het totale gehalte aan kooldioxide in het bloed is de som van deze vier bestanddelen.
binnen de microvasculatuur van de longen (figuur 1b) bepaalt de partiële drukgradiënt over het alveolaire membraan dat opgeloste CO2 van bloed naar alveoli overgaat. Dit verlies van kooldioxide uit bloed bevordert omkering van de hierboven beschreven rode cel reacties.
bicarbonaat gaat dus van plasma naar de rode cel en buffert waterstofionen die vrijkomen uit hemoglobine, omdat het zuurstofrijk is. De omkering van de koolzuuranhydrasereactie resulteert in de productie van CO2 dat van rode cellen naar plasma en verder naar alveoli verspreidt.
gemengd veneus bloed dat naar de longen komt, heeft een totaal CO2-gehalte van ongeveer 23,5 mmol/l (of 52 mL/dL), terwijl arterieel bloed dat de longen verlaat een totaal CO2-gehalte heeft van 21,5 mmol/l (48 mL / dL).
dit arterioveneuze verschil (2 mmol/L of 4 mL/dL) vertegenwoordigt de hoeveelheid CO2 die aan bloed uit weefselcellen wordt toegevoegd en uit bloed wordt verloren wanneer het door de pulmonale microvasculatuur gaat, en uiteindelijk uit het lichaam wordt uitgescheiden in de uitgeademde lucht.
figuur 1B: CO2 in longen
Klik om te vergroten
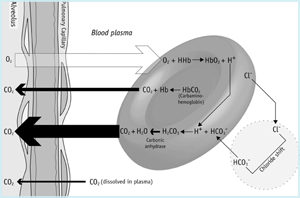
kooldioxide en de pH van het bloed
het zure potentieel van CO2, als gevolg van zijn hydratatiereactie op koolzuur (zie vergelijking 1 hierboven), zorgt ervoor dat de concentratie in het bloed een belangrijke determinant is van de pH van het bloed. Naarmate de CO2-concentratie stijgt, stijgt ook de concentratie van waterstofion (h+). Regulering van het bloed CO2, dat is het afstemmen van de snelheid van de CO2-eliminatie in uitgeademde lucht aan de snelheid van de productie in de mitochondrion van weefselcellen, essentieel voor het handhaven van een normale pH van het bloed, is de zaak van het ademhalingssysteem.
de ademhalingssnelheid (gecontroleerd door pCO2 gevoelige chemoreceptoren in de hersenstam en halsslagader) wordt verhoogd als pCO2 stijgt en neemt af als pCO2 afneemt. Verhoogde ademhalingssnelheid (ademhalingen/min) resulteert in een verhoogde mate van CO2-eliminatie en verminderde ademhalingssnelheid bevordert CO2-retentie.
de relatie tussen pH en koolstofdioxide wordt beschreven door een vorm van De Henderson-Hasselbach vergelijking (vergelijking 2). Dit wordt afgeleid uit de toepassing van de wet van massa-actie op de hydratatie en dissociatie reacties beschreven in vergelijking 1 .
vergelijking 2:
![]()
waarbij
| pK/1 | = | ‘schijnbare dissociatieconstante van koolzuur = 6.1 |
| = | de concentratie van plasma-bicarbonaat (mmol/L) | |
| S | = | de oplosbaarheid van CO2-coëfficiënt voor bij 37 oC (0.23 als pCO2 wordt gemeten in kPa of 0,03 als pCO2 gemeten in mmHg) |
| pCO2 | = | de partiële druk van pCO2 (kPa mmHg of) |
Zoals eerder is uitgelegd, is de noemer in deze vergelijking (S x pCO2) is de hoeveelheid opgeloste kooldioxide (dCO2) mmol/L.
Door het verwijderen van alle constanten in de vergelijking 2 kan worden vereenvoudigd:
vergelijking 3:
pH ∞ / pCO2
de pH van het bloed is dus afhankelijk van de verhouding tussen de plasmaconcentratie van bicarbonaat (de metabole component) en pCO2 (de respiratoire component). Als pCO2 dus toeneemt zonder een gelijkwaardige stijging van bicarbonaat, daalt de pH. Omgekeerd, als pCO2 daalt zonder een gelijkwaardige daling in bicarbonaat, stijgt de pH.
de omgekeerde relatie geldt voor de concentratie bicarbonaat: verhoogde HCO3 – = verhoogde pH; verlaagde bicarbonaat = verlaagde pH.
bicarbonaat is de belangrijkste bloedbuffer en de concentratie ervan op een bepaald moment weerspiegelt het evenwicht tussen de hoeveelheid die wordt geproduceerd door CO2 en de hoeveelheid die wordt verbruikt bij het bufferen van waterstofionen (H+) (zie vergelijking 1).
in het laboratorium – definitie van CO2-PARAMETERS
worden de CO2-parameters gegenereerd door de bloedgasanalysator:
- partiële druk van kooldioxide (pCO2) (kPa/mmHg)
- Plasma bicarbonaatconcentratie (HCO3 -) (mmol/l)
- totale plasmaconcentratie kooldioxide (ctCO2) (mmol/l))
de laatste hiervan, ctCO2, kan ook worden gemeten in plasma of serum door chemische methoden die onafhankelijk zijn van de bloedgasanalysator.
partiële druk van kooldioxide pCO2
deze parameter is een maat voor de druk die wordt uitgeoefend door dat kleine gedeelte (≈ 5 %) van het totale koolstofdioxide in het bloed dat in gasvormige toestand blijft, ‘opgelost’ in de waterfase van plasma-en bloedcelcytoplasma. De meting wordt uitgevoerd met behulp van een CO2 – specifieke pH-elektrode die is opgenomen in bloedgasanalysatoren.
in de gezondheid blijft pCO2 van arterieel bloed binnen het bereik 4,7-6,0 kPa (35-45 mmHg); pCO2 van veneus bloed is iets hoger 5,6-6,8 kPa (41-51 mmHg).
concentratie bicarbonaat (HCO3-)
dit is de hoeveelheid bicarbonaat in volume-eenheid plasma. Zoals eerder opgemerkt, is dit de vorm waarin de meeste kooldioxide (90 %) in bloed wordt getransporteerd. Deze parameter kan niet worden gemeten, maar wordt gegenereerd door berekening tijdens bloedgasanalyse. De gebruikte berekening is een herschikking van vergelijking 2:
vergelijking 4:
log = pH + log (S x pCO2) – pK/1
en hangt af van het hebben van waarden voor pH en pCO2, die beide worden gemeten tijdens bloedgasanalyse.Theoretisch is plasmabicarbonaat het verschil tussen totaal CO2 (ctCO2) en de som van alle andere vormen van CO2 in plasma, d.w.z. opgelost CO2 (dCO2), aan plasma-eiwitten gebonden CO2 (carbamino CO2) en koolzuur (H2CO3).
aldus:
Plasmabicarbonaat (mmol/l) =
ctCO2- (dCO2 + carbamino-CO2 + H2CO3)
in de praktijk wordt, omdat carbamino-CO2 en H2CO3 kwantitatief onbeduidend zijn, aangenomen dat het totale CO2 de som is van enkel bicarbonaat en opgeloste CO2 . Plasma bicarbonaat is dus effectief het verschil tussen plasma totaal CO2 (ctCO2) en plasma opgelost CO2 (dCO2).
in de gezondheid wordt arterieel plasmabicarbonaat (zoals berekend tijdens bloedgasanalyse) binnen het geschatte referentiebereik gehouden: 22-28 mmol/L. veneus bicarbonaat is iets hoger: 24-30 mmol/L.
in sommige laboratoria wordt onderscheid gemaakt tussen ‘feitelijk’ bicarbonaat (de hierboven beschreven parameter) en ‘standaard’ bicarbonaat. Standaardbicarbonaat is een tweede berekende parameter en is de plasmaconcentratie van bicarbonaat in het bloed die is geëquilibreerd met gas met een normale pCO2-spanning (40 mmHg, 5,3 kPa).
in de gezondheid is de werkelijke bicarbonaatconcentratie hetzelfde als de standaard bicarbonaatconcentratie, omdat in beide gevallen pCO2 normaal is. Door het normaliseren van pCO2, de respiratoire component van de zuur-base balans, is standaard bicarbonaat een maat voor alleen de metabole component en wordt daarom als nuttig beschouwd voor het ophelderen van de oorzaak van complexe stoornissen in de zuur-base balans.
totale KOOLDIOXIDECONCENTRATIE in PLASMA (ctCO2)
dit is theoretisch de som van alle vormen van koolstofdioxide in plasma. Het is niet gemeten tijdens de bloed-gas-analyse, maar – zoals bicarbonaat – berekend, ervan uitgaande dat, zoals hierboven reeds dat de totale kooldioxide is de som van bicarbonaat en opgeloste CO2:
Sinds plasma dCO2 mmol/L = (N x pCO2), ctCO2 is dus berekend :
plasma ctCO2 (mmol/L) =
plasma bicarbonaat (mmol/L) + (N x pCO2) (mmol/L)
Opgeloste CO2 (S x pCO2) draagt circa 1.2 mmol/L tot het totale CO2 in het plasma van arterieel bloed (zie hierboven), zodat ctCO2 ongeveer 1,2 mmol hoger is dan plasmabicarbonaat. Het ctCO2-referentiebereik is dus ongeveer 23-29 mmol / L voor arterieel bloed.
opgemerkt wordt dat, net zoals de berekende bicarbonaatwaarde die tijdens de bloedgasanalyse wordt gegenereerd, afhangt van het in vergelijking 2 beschreven verband, ook de berekende waarde voor ctCO2 die tijdens de bloedgasanalyse wordt gegenereerd.
hoewel ctCO2 en bicarbonaat gelijkwaardige klinische informatie leveren, is het in de klinische praktijk steevast bicarbonaat in plaats van ctCO2 dat in combinatie met pH en pCO2 wordt gebruikt om de zuur-base-status te evalueren. De klinische waarde van berekende ctCO2 gegenereerd tijdens bloedgasanalyse is dus beperkt.
chemische methoden voor het meten van ctCO2
in tegenstelling tot bicarbonaat, dat niet kan worden gemeten, is ctCO2 en de assay gewoonlijk een component van het ureum-en elektrolytenprofiel (u&E) van veneus plasma/serum. Aangezien u &E veel vaker geordend is dan arteriële bloedgassen, kan gemeten ctCO2 de eerste aanwijzing zijn voor verstoring van de kooldioxidehomeostase (en dus zuur-base).
het is gebruikelijk dat sommige klinische laboratoria deze gemeten component van het u&e-profiel “plasmabicarbonaat” noemen. Dit is onjuist omdat chemische methoden alle CO2 die vrijkomt uit plasma (of serum) meten door toevoeging van sterk zuur of anders al het bicarbonaat dat wordt geproduceerd als gevolg van de toevoeging van een sterke alkali aan plasma .
omvat dus niet alleen bicarbonaat, maar ook opgeloste CO2 en koolzuur. Als plasma of serum gebruikt in deze tests werden afgeleid van arterieel bloed dan gemeten ctCO2 zou theoretisch ongeveer de berekende ctCO2 waarde gegenereerd tijdens arteriële bloedgasanalyse.
in feite worden de U&e profielen uitsluitend uitgevoerd op plasma of serum teruggevonden uit veneus bloed, zodat er een onvermijdelijk klein theoretisch verschil is van 1-2 mmol/L (gemeten ctCO2 > berekend ctCO2) als gevolg van arterioveneus verschil.
het theoretische verschil tussen gemeten ctCO2 en berekend plasmabicarbonaat is iets hoger (gemeten ctCO2 > berekend plasmabicarbonaat) omdat er, naast het arterioveneuze verschil van 1-2 mmol/L, nog eens 1,5 mmol/l verschil is door de opname van opgeloste CO2 en koolzuur in gemeten ctCO2.
dit verschil veronderstelt echter dat er vóór de analyse geen opgeloste kooldioxide in de atmosfeer verloren gaat. Dit zou niet het geval kunnen zijn omdat u&E monsters niet anaeroob worden behandeld.
sommigen hebben betoogd dat de term “serum/plasmabicarbonaat” voor gemeten ctCO2 gerechtvaardigd is omdat normale laboratoriumpraktijken gepaard gaan met een onvermijdelijk verlies van opgeloste CO2 uit het U&E Monster voorafgaand aan de analyse, in welk geval gemeten ctCO2, in theorie althans, bij benadering het berekende bicarbonaat zou benaderen.
discordantie tussen gemeten ctCO2 en berekend bicarbonaat
ondanks de kleine theoretische verschillen tussen gemeten en berekende waarden die hierboven zijn beschreven, is er algemene acceptatie van het idee dat de gemeten ctCO2 gegenereerd als onderdeel van een u&e-profiel voor alle praktische klinische doeleinden dezelfde is als de plasmaconcentratie van bicarbonaat berekend tijdens de bloedgasanalyse.
dit wordt weerspiegeld in het gebruik van de term ‘plasmabicarbonaat’ om gemeten ctCO2 te beschrijven.
het beste bewijs dat gemeten en berekende resultaten van bicarbonaat in de praktijk klinisch uitwisselbaar kunnen zijn, is te vinden in een zeer recent rapport van de Mayo Clinic . De auteurs van dit rapport recupereerden 17.621 records van gemeten en berekende bicarbonaatconcentratie voor monsters die gelijktijdig werden verzameld bij dezelfde patiënten in 2006/7. De concentratie bicarbonaat in deze enorme database varieerde van 5 tot 49 mmol/l
Het gemiddelde verschil (SD) tussen gemeten en berekende waarden was -0,36 (1,23 mmol/L), en voor 98.5 % van de resultaten van de gepaarde monsters lag binnen 3 mmol / L van elkaar. Hoewel er, zoals in het Mayo-rapport wordt gesuggereerd, over het algemeen aanvaardbare overeenstemming bestaat tussen de twee parameters, is het niet zelden zo dat de resultaten volledig disharmonisch zijn, waarbij gemeten ctCO2 met maar liefst 15 mmol/L verschilt van berekend bicarbonaat .
talrijke studies in de afgelopen veertig jaar hebben getracht de frequentie, de omvang en de oorzaak van de discrepantie tussen berekend bicarbonaat en gemeten ctCO2 vast te stellen.
een vroege focus van dit werk trok de betrouwbaarheid van de bicarbonaatberekening in twijfel, die in belangrijke mate afhangt van de constantheid van pK/1 (zie vergelijking 4). In feite is dit geen echte thermodynamische constante, maar een’ schijnbare ‘ dissociatieconstante experimenteel bepaald uit de meting van pH, pCO2 en opgeloste CO2 met behulp van de volgende relatie afgeleid uit de vergelijking van Henderson-Hasselbach:
pK/1 = pH + log dCO2 – log
verschillende studies toonden voldoende variabiliteit in pK / 1 Aan, met name bij ernstig zieke patiënten, voor een klinisch significante fout in berekend bicarbonaat. In één onderzoek bleek pK/1 bijvoorbeeld te variëren van 5,84 tot 6,29.
de auteurs berekenen dat afwijkingen van pK/1 6.1 van deze omvang zouden resulteren in fouten in berekend bicarbonaat van de orde ± 60 %. Een ander beschrijft het geval van een diabetisch kind in ketoacidose wiens pK/1 varieerde van 5,49 tot 6,02 over een periode van zeven uur.
In een studie met 79 zuigelingen die werden verzorgd op een pediatrische intensive care unit , bleek 25% pK/1 te hebben buiten het ‘normale’ bereik van 6,055-6,195 zoals gedefinieerd in de studie, en in drie gevallen was pK/1 > 6,3, met een ‘verbazingwekkende’ waarde van 7,11. Deze en andere meldingen van klinisch significante variabiliteit in pK/1 zijn betwist en de betrouwbaarheid of anderszins van berekend bicarbonaat blijft een onopgeloste, controversiële kwestie.
de theoretische basis voor de opvatting dat berekend bicarbonaat onbetrouwbaar is bij kritieke ziekte is door Flear uiteengezet . Een even theoretische benadering vergezeld van een schat aan experimenteel bewijs is ingezet door Mass et al om de tegengestelde zaak te maken ter verdediging van berekend bicarbonaat.
auteurs van studies die geen klinisch significante variabiliteit in pK/1 hebben aangetoond, suggereren dat de belangrijkste discordantie tussen berekend bicarbonaat en gemeten ctCO2, die soms in de klinische praktijk wordt waargenomen, hoogstwaarschijnlijk het resultaat is van een combinatie van pre-analytische variabelen, analytisch verschil en willekeurige analytische fout .
meting van ctCO2 is bijzonder gevoelig voor pre-analytische variabiliteit omdat bloed voor u&e profilering universeel wordt verzameld en aëroob wordt verwerkt. De monsters kunnen uren voor analyse niet worden afgetapt. Aangezien de omgevingslucht minder CO2 bevat dan bloed, is er een tendens om opgeloste CO2 uit het monster te verliezen. Naar schatting zal dit gemeten CO2 met een snelheid van 6 mmol/uur verminderen.
daarentegen is berekend bicarbonaat niet geassocieerd met hetzelfde risico op preanalytische variatie, omdat bloed voor bloedgasanalyses routinematig anaeroob worden bemonsterd en er een minimale vertraging is (bijna altijd
een andere bijdragende oorzaak van discordantie tussen gemeten en berekende waarden zou het verschil in het monster kunnen zijn, aangezien arterieel bloed wordt gebruikt om een waarde te berekenen en serum-of plasmamonsters worden gebruikt om een waarde te meten.
wat de oorzaak ook is, studies blijven matige maar klinisch significante discordantie tussen de twee parameters onder ernstig zieke patiënten aantonen . Om de omstreden aard van het debat te bevestigen, blijkt uit de meest recente studie bij ernstig zieke patiënten dat er een aanvaardbare overeenstemming bestaat tussen berekend bicarbonaat en gemeten ctCO2 .
ondanks deze laatste studie is men van mening dat het ten minste voor ernstig zieke patiënten verstandig zou kunnen zijn om het berekende bicarbonaat te verlaten ten gunste van gemeten ctCO2, hoewel moet worden benadrukt dat dit standpunt omstreden is en het klinische effect van verschillen beperkt zou kunnen zijn.
het bewijs van acceptabele overeenstemming dat wordt geleverd door de zeer grote Mayo Clinic studie kan helaas niet worden gebruikt in het specifieke debat dat zich richt op ernstig zieken, omdat de patiëntenpopulatie niet was gedefinieerd.
van de twee parameters heeft berekend bicarbonaat het duidelijke voordeel van gemak ten opzichte van gemeten ctCO2, omdat het alle drie parameters (pH pCO2 en bicarbonaat) die bij de beoordeling van zuur-base worden gebruikt, tegelijkertijd uit één enkel monster beschikbaar maakt.
in de literatuur blijft er geen consensus over veel van de hierboven besproken kwesties. Zo blijft het zelfs onduidelijk of er al dan niet sprake is van discordantie tussen gemeten en berekende CO2, hoewel de balans van het bewijs onlangs is verschoven ten gunste van geen discordantie door de grote Mayo Clinic studie .
voor degenen die geloven dat de balans van de feiten erop wijst dat er onenigheid bestaat, zijn er nog twee onopgeloste kwesties.
dit zijn: de klinische significantie van die discordantie en de oorzaak van die discordantie. Het debat over de oorzaak van discordantie is vooral gericht op de vraag of pKl1 significant varieert tussen patiënten en de mate waarin preanalytische verschillen, analytische verschillen en willekeurige fouten bijdragen tot discordantie.
ten slotte heeft ten minste één commentator vraagtekens geplaatst bij de klinische noodzaak van ofwel berekend bicarbonaat ofwel gemeten ctCO2, wat suggereert dat pH en pCO2 alleen een volledige beoordeling van zuur-base stoornissen mogelijk maken.
samenvatting
kooldioxide is een product van het aerobe celmetabolisme dat in het bloed naar de longen wordt getransporteerd voor excretie in uitgeademde lucht. Een beetje wordt onveranderd opgelost in bloed getransporteerd, maar het meeste wordt getransporteerd als bicarbonaat.
regulering van de hoeveelheid kooldioxide in het bloed, of beter gezegd regulering van de verhouding tussen bicarbonaat en opgeloste kooldioxideconcentratie, is essentieel voor het behoud van de pH van het bloed (normale zuur-base-balans).
klinisch onderzoek naar zuur-base verstoring omvat arteriële bloedgasanalyse, een test die drie parameters van de koolstofdioxidestatus genereert. Hiervan wordt er slechts één, pCO2, gemeten; de andere twee-plasmabicarbonaat en totale kooldioxideconcentratie-worden door berekeningen afgeleid uit gemeten pH en pCO2.
de validiteit van deze berekeningen is in twijfel getrokken en er zijn tegenstrijdige aanwijzingen dat het bij sommige patiëntengroepen klinisch betrouwbaarder zou kunnen zijn om het totale koolstofdioxide met chemische methoden te meten dan om te vertrouwen op berekende waarden.
dit laatste blijft een zeer omstreden kwestie die alleen definitief kan worden opgelost door nader onderzoek.