Nøkkelord
Cytomegalovirus lungebetennelse; Bronkiolitisobliterans organisere lungebetennelse; Immunkompetent
Innledning
de kliniske manifestasjonene av cytomegalovirus (cytomegalovirus)cmv) Infeksjon Kan Deles inn i akutt Primær Infeksjon Ogaktivering. Primær CMV-infeksjon forekommer hyppigstunder amming og barndom, og er asymptomatisk eller tilstede som et mildt mononukleoselignende syndrom iimmunokompetente voksne . Da fortsetter viruset for livet iverten, generelt i latent stadium. Reaktivering Av Cmvfra latens er velkjent hos immunkompromitterte pasienter, og det kan påvirke nesten alle organer. Imidlertid er alvorlig CMV lungebetennelse sjelden i immunkompetente verter . For tiden er de nøyaktige molekylære og immunologiske mekanismerinvolvert er fortsatt ukjente.
Bronchiolitis obliterans organisere lungebetennelse (BOOP) er aklinisk tilstand preget av hoste, sykdomsfølelse, feber, ogdyspnø og ingen respons på antibiotika . Dens brystradiograf beskrevet som lokale, flere og diffunderer endringer. Det kan bli funnet med allergisk alveolitis, bestrålingspneumonitt, narkotikareaksjoner og andre organisasjonsinfeksjoner. Tilfeller involvert i viral etiologi komplisert Med Boophar sporadisk blitt rapportert. Her presenterer vi et tilfelle avcmv lungebetennelse assosiert med BOOP hos en immunkompetent pasient ved behandling av ganciklovir, som er det første slike tilfellet noensinne rapportert så vidt vi kjent.
Saksrapport
En 63 år gammel mann ble henvist til sykehuset på grunn av en 10 dagers historie med hoste og feber. Han hadde en paroksysmal hostemed gul sputum. Feber, med hvesning oppstod hovedsakelig iettermiddagen og natten og den høyeste temperaturen var39.3 (102.74). Hans tidligere medisinske historie inkluderte hypertensjon, diabetes og gikt. Hans tidligere familiehistorie var unremarkable. Hans vitale tegn var som følger: kropptemperatur: 36,5 (97,7), hjertefrekvens: 98 slag per minutt(BPM), blodtrykk: 98/61 mmHg.
ved fysisk undersøkelse ble sen inspiratoriske knitre notert i de bilaterale nedre lungefeltene. Antall hvite blodceller (WBC) var 14,2 × 109 / L, med 81,9% nøytrofile(NØYTR), 12,8% lymfocytter (LYR) og 0,53 × 109 / Lmonocytter (MONOR) (Figur 1). Serum C-reaktivt protein (CRP) nivå var 110,67 mg / L.
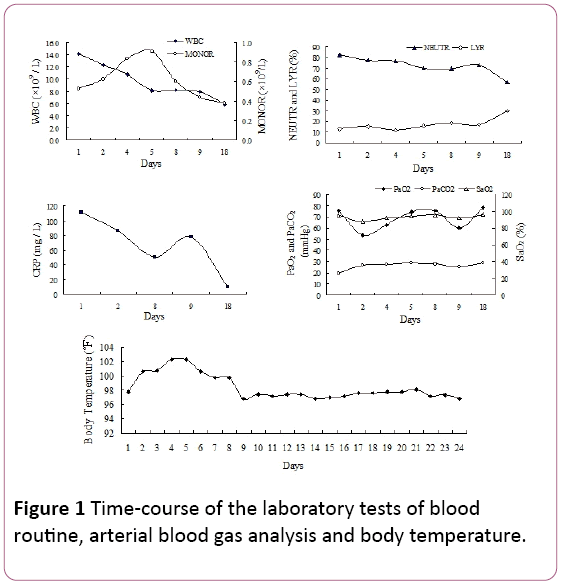
Figur 1: Tid-kurs av laboratorietester av blodrutin, arteriell blodgassanalyse og kroppstemperatur.
Arterielt partialtrykk av oksygen (PaO2) var 75,5 mmHg, med 25,8 mmHg arterielt partialtrykk AV CO2 (PaCO2) og94,7 % oksygenmetning (SaO2, 2 L/min oksygenforsyning vianasal kanyle). På grunn av feber og tegn pååndedrettsinfeksjoner, startet vi erfaringsbasert antibiotikabehandling med piperacillin tazobactam. Imidlertid ble pasiententemperaturen ikke redusert og kortpustetutviklet i vedvarende 4 dager med sykehusopptak.
Arterielle blodgassmålinger viste svikt i respirasjon (PaO2: 53,5 mmHg, PaCO2: 35,6 mmHg, SaO2: 87,7%) med motbalansert metabolsk acidose (HCO3 -: 21mmol / l, pH 7,39) ved bruk av 2 l/min oksygen med nesekanyle.Laboratorieundersøkelsesresultater var som følger: mycoplasmapneumonia antistoff: 1: 40 (positiv), bakteriell endotoksin (det totale innholdet av lipopolysakkarid av gram negative bakterier): 49,14 pg / mL, plasmafibrinogen (Fg): 7,51 g / L, aktivertpartisk tromboplastintid( APTT): 45,9 sekund.
elektrokardiogrammet viste sinus takykardi med Twave endring. Brystrøntgen fant to lungeinfeksjoner, ikkebortsett fra pulmonale interstitiale lesjoner (Figur 2a). En thoraciccomputed tomography (CT) scan avslørte pulmonarinterstitial lesjoner (skygge av rutenett i begge lungene), ogmediastinal lymfeknute utvidelse (Figur 2d). Deretter ble 3,5 L/min oksygen forsynt med ansiktsmaske og antibiotikabehandling ble byttet Til Cefoperazonnatrium ogsulbaktamnatrium pluss Levofloxacin.
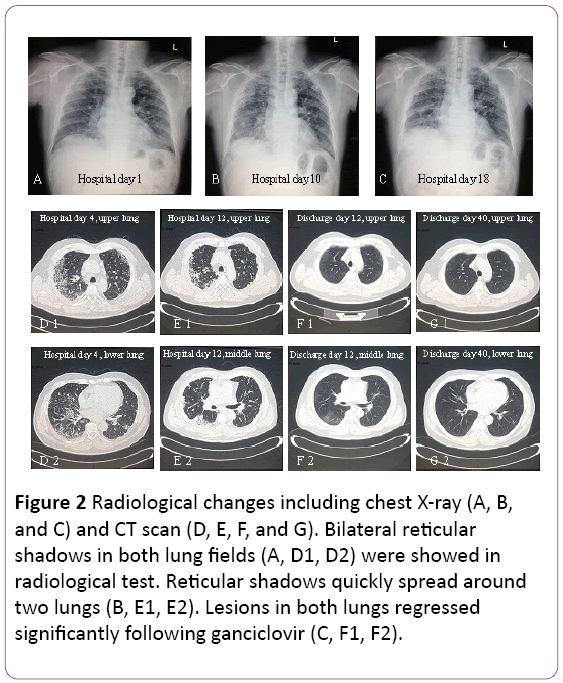
Figur 2: Radiologiske endringer inkludert brystrøntgen (a, B og C) OG CT-skanning (D, E, F og G). Bilaterale retikulærskygger i begge lungefeltene (A, D1, D2) ble vist iradiologisk test. Retikulære skygger sprer seg raskt rundtto lunger (B, E1, E2). Lesjoner i begge lungene regresbetydelig etter ganciklovir (C, F1, F2).
Med tanke på diagnose av interstitial lungebetennelse, relevantlaboratorieprøver og fiberoptisk bronkoskopi ble utførtpå dag 5. Laboratorieprøveresultatene var SOM følger: CMV PCR: negativ, CMV IgM: negativ, immunoglobulin IgG: positiv, HIV: negativ, WBC: 7,96 × 109 / L, NØYTR: 72,4%, LYR: 17%,CRP: 77,51 mg/L, immunologisk funksjon (T, B, nk-celler):normal, undergrupper av t-lymfocytter: normal. Markører for autoimmune sykdommer inkludert perinuclear-ANCA (p-ANCA), cytoplasmisk-ANCA (c-ANCA), ANA og anti-dsDNA var alle negative.
Lungefunksjon foreslo moderat restriktivventilatorisk dysfunksjon. Røntgen-OG CT-skanning avslørte lesjoner påøvre lunge ble absorbert, men det ble forverret iden høyre nedre lungen(Figur 2b OG 2E).
en bronkoskopi viste bilateral bronkitt (Figur 3a).Bronchoalveolar lavage (BAL) væske var negative formykobakterier OG pas flekken. Differensielt celletall vist11 % nøytrofiler, 19% lymfocytter og 70% makrofager.Intranukleære og intracytoplasmatiske inklusjonsorganer ble funneti lateral basal segment av lungevev transbronchialbiopsy (TBLB) av høyre nedre (Figur 3B). Basert på diagnose av cytomegalovirus pneumoni med organisasjon, ble behandling med ganciklovir (5 mg/kg) via intravenøs infusjon hver 12. time påbegynt på dag 8. I følge abovefinding kombinert med kliniske symptomer (feber forsvinner), ble antibiotikabehandlingen endret til Moxifloxacin på dag8. Etter 1 uke med antivirusbehandling, hoste vedvarende. Han gikk lungebiopsi via CT-guidet. En lungebiopsi avslortboop (Figur 3C). Deretter behandles pasienten med oral steroidhormon. Likevel ble hans symptomer gradvis forbedret ifølgende 1 uke. Brystrøntgen viste at to lungelesjoner var bedre enn før (Figur 2c).
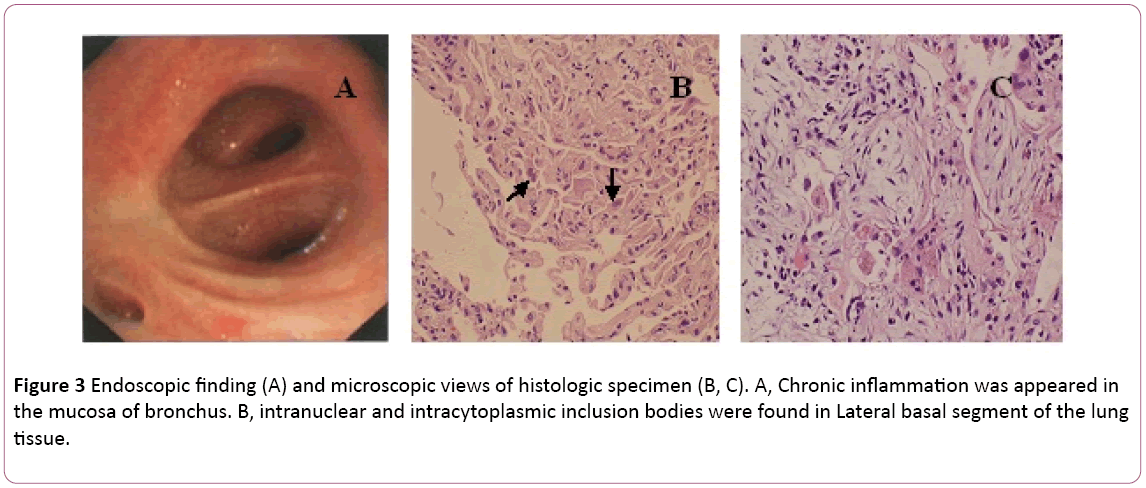
Figur 3: Endoskopisk funn (a) og mikroskopiske visninger av histologiske prøven (B, C). A, Kronisk betennelse ble dukket opp islimhinnen av bronkus. B, intranukleære og intracytoplasmatiske inklusjonsorganer ble funnet I Lateral basal segment av lungevev.
Behandlingen ble endret til oral ganciklovir, 0,6 g / d (q12h)i 7 dager, utskrivning. I sin oppfølging regres shadow of grid i bothlungs betydelig (Figur 2f og 2G). Han er stillunder oppfølging på poliklinikken.
Diskusjon
CMV ER ET DNA-virus i Familien Herpesviridae, og densinfeksjon er vanlig. Faktisk er 40% til 100% av voksne smittet MED CMV over hele verden . CMV-infeksjoneri den generelle befolkningen er vanligvis subklinisk. Den symptomatiske CMV-infeksjonen forekom hovedsakelig iimmunkompromitterte pasienter med immundysfunksjon,inkludert PASIENTER MED AIDS, malignitet,transplantatmottakere og nyfødte . I tilfeller Med immunsvikt Kan Cminfeksjon forårsake lungebetennelse, retinitt, hepatitt, encefalitt,demyeliniserende polyneuropati, myokarditt, pankreatitt,gastrointestinale sykdommer og adrenal sykdommer, og så videre . Tvert imot, alvorlig livstruende infeksjon indusert AV CMV, inkludert CMV lungebetennelse, er god hos immunkompetente individer . I denne artikkelen beskriver VI ET TILFELLE AV CMV pneumoni, assosiert Med BOOPin en immunkompetent vert, og effektivt behandlet medganciklovir.
CMV lungebetennelse presenterer ofte som alvorlig viral lungebetennelse, med diffuse interstitielle infiltrater på brystet X-ray ogrespiratorisk svikt . Laboratoriediagnosen kan værevanskelig, og er laget serologisk eller patologisk.De serologiske analysene for å påvise HUMAN CMV-infeksjon inkluderer VANLIGVIS CMV-antistoffer (IgM,IgG) titer, CMV proteinpp65 og CMV PCR . Det er viktig at histopatologiskdeteksjon AV CMV – inklusjonsorganer på transbronkial eller openlungbiopsi er patognomonisk, siden CMV-pneumoni hos immunkompetente pasienter representerer en sjelden hendelse .
Vår pasient presenterte uspesifikke symptomer (hoste og feber), som hadde utviklet seg i løpet av 10 dager.Symptomene ble forverret etter 2 dager på sykehus (alvorlig hypoksemi), til tross for empirisk antibiotikabehandling. Diagnosen AV CMV lungebetennelse var basert PÅ TBLB, som var funnet intranukleære og intracytoplasmatiske inklusjonsorganer ingiante celler som gullstandarden. VIDERE var serum CMV IgG antistoff positivt en annen diagnostisk indeks. Radiologisk bilde inkludert brystrøntgen og CT-skanning som viser bilaterale retikulære skygger i begge lungefeltene støttet diagnosen viral lungebetennelse. I vårt tilfelle mononukleose avblodrutine ble også observert (Figur 1). SerumIgM CMV var imidlertid negativ i dette tilfellet, som var i samsvar Med Eddleston-rapporten . CMV PCR var også negativ. Det kan kanskje forklares av falske negative resultater indusert av forbigående naturav viremia .
under sykehusinnleggelsen ble hans lymfocytter redusert. betydelig. Lymfopeni ble forårsaket AV CMV-infeksjon for både direkte hemming av stamcellevekst og svikt i stamcellefornyelse . Det kan bemerkes atimmunfunksjonsanalyse som t-celledelmengde, B-celle og NKcell, analyse var normale. Transient eller subklinisk t-celleunormalitet og en inversjon AV CD4 / CD8 T – celleforholdet ble ikke observert i dette tilfellet. VED HIV-sykdom er en reduksjon I CD4+ – celler <100 × 10 6/L en høy risiko for CMV-sykdom. Videre viste vår pasient ingen tegn på andreimmundefekter (HIV: negative) og autoimmune sykdommer(autoimmun antistoff: negativ).
BOOP ble først beskrevet Av Epler et al. og siden dahar blitt grundig undersøkt og rapportert gjennom heleverden . Det er mange smittsomme stoffer som kan væreforbundet MED BOOP, som cytomegalovirus( CMV), herpessimplex virus (HSV) . Parasittiske og pneumocystis cariniiinfeksjoner er også rapportert . Fordi BOOPrepresent måte som lungen kan reagere på aninflammatorisk stimulus, er de viktigste patofysiologiske funnene relatert til den inflammatoriske banen. Histologiske funksjonerinkludere granulasjonsvev i veggene til alveolene ogbronkioler er signifikante, forbundet med infiltrering iinterstitial og trakeal hulrom ved forskjellige grader avmononukleære celler og skumceller. Type II alveolær epitelcellehyperplasi kan også ses . I currentpatient BLE BOOP diagnostisert i lungebiopsi en uke laterenn TBLB, noe SOM tyder PÅ AT CMV kan være det mest sannsynligepatogen.
selv om det ikke er anbefalt standardvarighet for behandling med CMV pneumoni hos pasienter med CMV pneumoni, kan behandlingen kun startes etter endelig diagnose og administreres vanligvis i to til tre uker. Så snart sombehandling med ganciklovir, ble pasientens kliniske tilstand forbedret, med fullstendig oppløsning av det kliniske ogradiologiske bildet under en måneds oppfølging.
Konklusjon
vi rapporterer en akutt CMV infeksjon sak, som presentertmed feber, hoste, sputum og tachypnea. Den sistnevnteforverret seg raskt og er forbundet med respiratorisk svikt.CT-skanning avslørte en liten forandring av bakken glass ved utbruddet, menendringen spredte seg raskt rundt to lunger. Etter patologisk undersøkelse (TBLB) ble Diagnosen Cmvpneumoni bekreftet. For pasienter med noimmundefektilitetsforstyrrelser er det veldig lett å feildiagnose.Den nåværende rapporten antyder at NÅR brystet CT viserinterstitiale lesjoner,i tillegg til å vurdere tuberkulose, bakteriell lungebetennelse og andre virussykdommer, Bør Cmvpneumoni inkluderes hos eldre pasienter med avariety av grunnleggende sykdom. Det er viktig at denne saken viste at cytomegalovirus lungebetennelse kan assosieres MED BOOP i en immunkompetent pasient. Ganciklovir behandling ereffektive. Videre studier er nødvendige for å analyserelasjoner og dens underliggende mekanisme mellom Cmvpneumoni og BOOP.
Forfatterens bidrag
CXC utarbeidet og skrev manuskriptet. WC, LL OG LYH tok vare på pasienten og bidro til å koordinere manuskriptet. XL utførte de mikrobiologiske analysene. Lyhbidro til utkastet til manuskriptet og reviderte manuskriptet. Alle forfattere har lest manuskriptet oggodkjent sin endelige versjon.
Takk
Vi er takknemlige For Prof. Zhiqiang Qin for hans teoretiskestøtte.
- Hamprecht K, Maschmann J, Vochem M, Dietz K, Speer CP, et al. (2001) Epidemiologi av overføring av cytomegalovirus fra mor til prematur spedbarn ved amming. Lancet 357:513-518.
- Carter D, Olchovsky D, Pokroy R, Ezra D (2006) Cytomegalovirus-assosiert kolitt forårsaker diare i en immunkompetent pasient. Verden J Gastroenterol12: 6898-6899.
- Kralickova P, Mala E, Vokurkova D, Krcmova I, Pliskova L, et al. (2014)Cytomegalovirus Sykdom Hos Pasienter Med Vanlig Variabel Immunsvikt: Tre Kasusrapporter. Internasjonale Arkiver For Allergi og Immunologi 163: 69-74.
- Eddleston M, Peacock S, Juniper M, Warrell DA (1997) Alvorlig cytomegalovirusinfeksjon hos immunkompetente pasienter. Clin Smitter Dis 24: 52-56.
- Cunha BA (2010) Cytomegalovirus lungebetennelse: smittsom lungebetennelse hos immunkompetente verter. Infisere Denne Clin Nord Am 24:147-158.
- Cohen JI, Corey GR(1991) Cytomegalovirus infection in the normal host. Medicine 1985; 64:100-114.
- Geddes DM. BOOP and COP. Thorax46:545-547.
- Hansell DM (1992) What are bronchiolitis obliterans organizing pneumonia (BOOP) and cryptogenic organizing pneumonia (COP)? ClinRadiol45:369-70.
- Cunha BA, Syed U, Mickail N(2012) Renal transplant with bronchiolitis obliterans organizing pneumonia (BOOP) attributable to tacrolimus and herpes simplex virus (HSV) pneumonia. Heart & Lung 41:310-315
- Bitzan M, Ouahed JD, Carpineta L, Bernard C, Bell LE(2010) Kryptogen organisering lungebetennelse etter rituximab terapi for antatt post-nyretransplantasjon lymfoproliferativ sykdom. Pediatrisk Nefrologi 25: 1163-1167.
- De La Hoz RE, Stephens G, Sherlock C (2002) Diagnose Og behandlingsmetoder FOR CMV-infeksjoner hos voksne pasienter. J ClinVirol 25:1-12.
- Sanadgol N, Ramroodi N, Ahmadi GA, Komijani M, Moghtaderi A, et al.(2011) Utbredelse av cytomegalovirusinfeksjon og dens rolle i totalt immunoglobulinmønster hos Iranske pasienter med forskjellige subtyper av multippel sklerose. Ny Mikrobiologica 34: 263-274.
- Chiotan C, Radu L, Serban R, Cornacel C, Cioboata M, et al. (2014) Cytomegalovirus retinitt HOS HIV/AIDS-pasienter. Tidsskrift for medisin og liv 7:237-240.
- Liu WL, Lai CC, Ko WC, Chen YH, Tang HJ, et al. (2011) Kliniske og mikrobiologiske egenskaper ved infeksjoner forårsaket Av Ulike nocardia-arter I Taiwan: en multisenterstudie fra 1998 til 2010. Eur J ClinMicrobiol Infisere Dis30:1341-1347.
- Beam E, Razonable RR(2012) Cytomegalovirus i solid organtransplantasjon: epidemiologi, forebygging og behandling. Curr Infisere Dis Rep14: 633-641.
- Westman G, Berglund D, Widen J, Ingelsson M, Korsgren O, Et al. (2014) Økt Inflammatorisk Respons hos Cytomegalovirus Seropositive Pasienter med Alzheimers Sykdom. PloS one9: 96779.
- Carney WP, Rubin RH, Hoffman RA, Hansen WP, Healey K, Et al. (1981) Analyse Av T lymfocytt undergrupper i cytomegalovirus mononukleose. J Immunol126: 2114-2116.
- Boeckh M, Leisenring W, Riddell SR, Bowden RA, Huang ML, Et al. (2003)sent cytomegalovirus sykdom og dødelighet hos mottakere av allogen hematopoietisk stamcelletransplantasjon: betydningen av virusmengde og t-celleimmunitet. Blod 101:407-414.
- Gunthard HF, Aberg JA, Eron JJ, Hoy JF, Telenti A,et al. (2014) Antiretroviral behandling av HIV-infeksjon hos voksne: 2014 anbefalinger Fra International Antiviral Society-USA Panel. JAMA 312: 410-425.
- Epler GR, Colby TV, McLoud TC, Carrington CB, Gaensler EA(1985) Bronkiolitt obliterans organisere lungebetennelse. N Engl J Med 312:152-158.
- Kute VB, Patel MP, Patil SB, Shah PR, Vanikar AV,et al. (2013) Bronchiolitis obliterans organizing pneumonia (BOOP) after renal transplantation. IntUrolNephrol 45:1517-1521.
- White KA, Ruth-Sahd LA (2007) Bronchiolitis obliterans organizing pneumonia. Crit Care Nurse27:53-66.
- Yale SH, Adlakha A, Sebo TJ, Ryu JH(1993)Bronchiolitis obliterans organizing pneumonia caused by Plasmodium vivax malaria. Chest 104:1294-1296.
- Kleindienst R, Fend F, Prior C, Margreiter R, Vogel W(1999)Bronchiolitis obliterans organizing pneumonia associated with Pneumocystis carinii infection in a liver transplant patient receiving tacrolimus. Clin Transplant13:65-67.
- Moore SL (2003)Bronchiolitis obliterans organizing pneumonia: a late complication of stem cell transplantation. Clin J OncolNurs 7:659-662.