a tüdőembólia (PE) a kardiovaszkuláris halál gyakori oka, növekvő gyakorisággal.1-4 a jobb kamrai (RV) utóterhelés akut növekedésének sértése a pulmonalis artériák trombus obstrukciója, hipoxémiás vazokonstrikció és a pulmonalis artéria vazokonstriktorainak felszabadulása RV diszfunkcióhoz és dilatációhoz, valamint csökkent bal kamrai (LV) előterheléshez vezethet, ami a legsúlyosabb esetekben kardiovaszkuláris összeomlást okozhat.5 az antikoaguláció az összes pe kezelésének alapja kiváló eredmények alacsony kockázatú betegeknél.6,7
a közepesen magas és magas kockázatú PE-ben szenvedő betegek egy alcsoportja azonban előnyös lehet a fejlettebb terápiában, beleértve a szisztémás fibrinolízist, a katéter-irányított terápiát (CDT) fibrinolitikumok infúziójával vagy anélkül vagy tüdőembolektómia, mivel ezek a lehetőségek aktívan csökkentik a trombus terhelését az RV utóterhelésének csökkentése érdekében. Azoknál a betegeknél, akik túlélik a kezdeti megjelenést, hosszú távú következmények alakulhatnak ki, beleértve a tartós RV diszfunkciót, a krónikus thromboemboliás pulmonalis hypertoniát, valamint az életminőség és a testmozgási tolerancia csökkenését.8,9
a szisztémás fibrinolízis bizonyítottan gyorsan csökkenti a trombusterhelést és a pulmonalis arteria nyomást. Ez azonban fennáll annak a kockázata, hogy a 20% – ot meghaladó súlyos vérzési arány, az intrakraniális vérzés (ICH) félő szövődménye pedig 3% – ban fennáll.10,11 a vérzéses szövődmények iránti aggodalom a szisztémás fibrinolízis alulfelhasználásához vezetett, a betegek nagy hányada abszolút vagy relatív ellenjavallattal rendelkezik.12 tekintettel a nemkívánatos események arányára, a szisztémás fibrinolízis általában azokra korlátozódott a legnagyobb kockázatú, hemodinamikai kompromisszum vagy kardiogén sokk bizonyítékával. A CDT-t egyre inkább használják az RV utóterhelésének aktív javítására önmagában az antikoaguláción túl, de csökkentett dózissal vagy fibrinolitikus terápia nélkül.
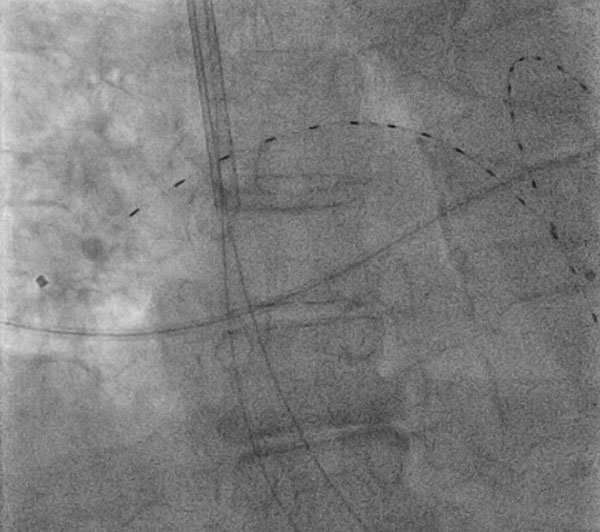 1. Ábra: Katéter-irányított, ultrahanggal megkönnyített, alacsony dózisú fibrinolízis
1. Ábra: Katéter-irányított, ultrahanggal megkönnyített, alacsony dózisú fibrinolízisegy 74 éves nő kétoldali proximális tüdőembólia tartós tachycardiával, katéter-irányított, ultrahang-megkönnyített, alacsony dózisú fibrinolízist kapott fluoroszkópos irányítás alatt a jobb belső jugularis vénán keresztül hozzáférés. A képen látható eszköz az ekosonic endovaszkuláris rendszer (EKOS, Bothell, WA) a kétoldalú tüdőartériákban.
a CDT-k közé tartoznak azok, amelyek fibrinolitikus szereket (pl., szöveti plazminogén aktivátor) ultrahang segítséggel vagy anélkül, valamint olyan eszközök, amelyek különféle mechanikai módszerekkel csökkentik az alvadék terhelését fibrinolitikus szerek nélkül. A legjobban tanulmányozott és egyetlen amerikai Food and Drug Administration által jóváhagyott katéter-irányított eszköz a PE kezelésére az EkoSonic endovaszkuláris rendszer (EKOS, Bothell, WA) (1.ábra). Az 5.4 a francia infúziós katétereket közvetlenül a pulmonalis artériákba helyezik, általában belső jugularis vagy femoralis véna hozzáféréssel, és ultrahangos magot tartalmaznak, amely ultrahanghullámokat bocsát ki a t-PA-t szállító pórusok mellett.
In vitro vizsgálatok kimutatták a t-PA fibrinhez való jobb penetrációját és kötődését ultrahang jelenlétében.13 egy kis vizsgálatban 59 közepes kockázatú PE-ben szenvedő beteg randomizált ultrahanggal megkönnyített, alacsony dózisú fibrinolízis plusz antikoaguláció vs. az antikoaguláció önmagában az intervenciós csoportban nagyobb mértékben csökkent az RV-LV átmérő arány és a pulmonalis artéria szisztolés nyomása, és az RV funkció szignifikánsabb javulása 24 óra elteltével.14 A 90 napos nyomon követés során tendencia mutatkozott az RV méretének nagyobb csökkenése felé az intervenciós csoportban (p = 0,07); a szisztolés artériás nyomásban azonban nem volt különbség.
“a CDT-t egyre inkább használják az RV utóterhelésének aktív javítására önmagában az antikoaguláción túl, de csökkentett dózissal vagy fibrinolitikus terápia nélkül.”
egy nagyobb, egykarú, multicentrikus vizsgálat ultrahanggal megkönnyített, alacsony dózisú fibrinolízist értékelt 150 masszív vagy szubmasszív PE-ben szenvedő betegnél. Szignifikánsan csökkent az RV / LV átmérő arány, a pulmonalis arteria szisztolés nyomása és a thrombus terhelése a 48. órában.15 Volt egy súlyos és 15 közepesen súlyos vérzéses esemény, intracranialis vérzés nélkül. Infúziós katéterek ultrahang nélkül (pl. Cragg-McNamara, pigtail katéter) fibrinolitikus anyagot is kínálnak a pulmonalis artériákba lényegesen kevesebb költséggel, mint az ultrahanggal megkönnyített fibrinolízis. Bár kis retrospektív vizsgálatokra korlátozódik, a katéter által irányított fibrinolízist ultrahanggal és anélkül értékelték, és hasonló eredményeket mutatnak.16,17 ezeket az eredményeket nem validálták randomizált-kontrollos vizsgálatban, bár egy vizsgálat folyamatban van (NCT02758574).18
egy meta-analízis 16 katéter-irányított thrombolysis vizsgálatot értékelt, és 4,7 százalékos komplikációs arányt, 0,35 százalékos intracranialis vérzéses arányt talált.19 a kórházi eredmények közelmúltbeli hajlandóság-megfelelő elemzése a nemzeti visszafogadási adatbázist használta a szisztémás vs. katéterrel irányított fibrinolízis és alacsonyabb kórházi mortalitás és vérzés mutatkozott azoknál a betegeknél, akik katéterrel irányított fibrinolízist kaptak.20 nem voltak prospektív, randomizált vizsgálatok, amelyek összehasonlították a szisztémás katéterrel irányított fibrinolízist.
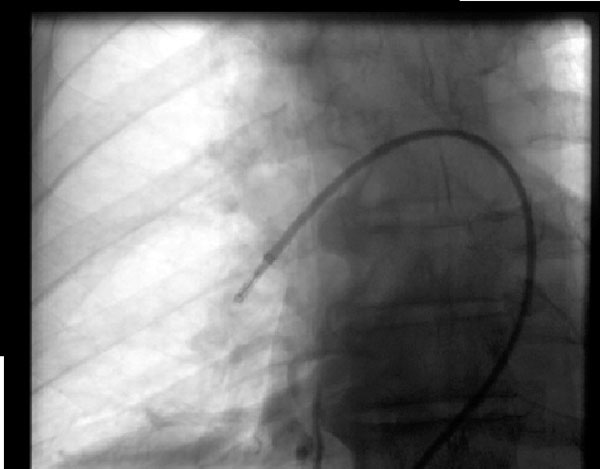 2.ábra: aspirációs thrombectomia
2.ábra: aspirációs thrombectomiaegy 68 éves férfinál egy nappal a gerincműtét után masszív tüdőembólia alakult ki, és nem volt jelölt fibrinolízisre, így fluoroszkópos irányítás alatt aspirációs thrombectomián esett át, hemodinamikájának javulásával. A képen látható eszköz az Indigo embolectomia rendszer (Penumbra, Alameda, CA) A jobb tüdőartériában.
a betegek gyakran indokolják a fejlett terápiát, de ellenjavallatuk van még a t-PA alacsony dózisaira is. Ilyen betegeknél a pulmonalis embolectomia lehetséges lehetőség. Ehhez azonban sternotomia és cardiopulmonalis bypass szükséges nagy dózisú heparinnal. A mechanikus CDT perkután lehetőséget kínál, amely nem használja a fibrinolízist. Különböző mechanikus CDT-k léteznek, beleértve az aspirációs vagy szívó mechanikus thrombectomiát (2.ábra), maceráció pigtail katéterrel, valamint reolitikus thrombectomia.
minden rendelkezésre álló rendszernek különböző korlátai vannak, mint például a katéter mérete miatt a pulmonalis artériákba történő megfelelő manipuláció, az aspiráció során bekövetkező vérveszteség és a trombus eltávolításának korlátozott képessége, különösen, ha idősebb és fibrotikusabb. A kombinált mechanikus és fibrinolitikus terápiának szerepe lehet a thrombus clearance javításában.21 a mechanikus CDT adatai kicsi, egyközpontú toksorozatokra korlátozódnak, bár ésszerű MŰSZAKI sikert mutatnak.A 22-25 CDT mentő kezelési lehetőséget is kínál a szisztémás fibrinolízis ellenére tartós sokkban szenvedő betegek vagy a testen kívüli membrán oxigénellátására helyezett betegek számára.26
“nincsenek magas színvonalú vizsgálatok, amelyek összehasonlítanák a különböző CDT-ket egymással vagy a szisztémás trombolízissel szemben.”
nincsenek magas színvonalú vizsgálatok, amelyek összehasonlítanák a különböző CDT-ket egymással vagy a szisztémás trombolízissel szemben. Tekintettel a CDT közepes kockázatú PE-ben történő alkalmazásának jelenlegi arányára, valamint ezeknek a beavatkozásoknak a lehetséges kockázataira és költségeire, a hosszú távú eredmények értékelése, beleértve a pulmonalis hypertoniát és a terhelési toleranciát, a jobb minőségű rövid távú klinikai eredményadatok mellett.
összefoglalva, a CDT ígéretes kezelési lehetőség akut PE-ben szenvedő betegek számára, és alternatív fejlett terápiát kínál azoknak a betegeknek, akik rosszul jelöltek szisztémás trombolízisre vagy pulmonalis embolectomiára. Továbbra is izgalmas terület az új terápiák gyors fejlődésével, de további kutatásokat igényel a közepes kockázatú PE-ben való széles körű felhasználása előtt.
Brett Carroll, MD, nemrég fejezte be Vascular Medicine ösztöndíját a Brigham and Women ‘ s Hospital-ban, és jelenleg a bostoni Beth Israel Deaconess Medical Center vascularis Medicine igazgatója.
- Jimenez D, De Miguel-Diez J, Guijarro R és mtsai. J Am Coll Cardiol 2016; 67: 162-70.
- Huang W, Goldberg RJ, Anderson FA és mtsai. Am J Med 2014;127: 829-39 e5.
- Cohen AT, Agnelli G, Anderson FA, et al. Thromb Haemost 2007; 98: 756-764.
- Mozaffarian D, Benjamin ej, Go AS, et al. Forgalom 2016;133: e38-360.
- Piazza G, Goldhaber SZ. Circulation 2010;122: 1124-9.
- Aujesky D, Obrosky S, Stone RA, et al. Am J Vagy Crit Ellátás Med 2005;172: 1041-6.
- Kearon C, Akl EA, Ornelas J, et al. Mellkas 2016; 149: 315-52.
- Piazza G, Goldhaber SZ. N Eng J Med 2011; 364: 351-60.
- Sista AK, Miller LE, Kahn SR, Kline JA. Vasc Med 2017;22: 37-43.
- Goldhaber SZ, Haire WD, Feldstein ML, et al. Lancet 1993;341:507-11.
- Goldhaber SZ, Visani L, de Rosa M. Lancet 1999;353:1386-9.
- Stein PD, Mat F. Am J Med 2012;125:465-70.
- Siddiqi F, Odrljin TM, Fay PJ, et al. Vér 1998; 91: 2019-25.
- Kucher N, Boekstegers P, Muller HL, et al. Forgalom 2014;129: 479-86.
- Piazza G, Hohlfelder B, Jaff MR, et al. JACC Cardiovasc Interv 2015; 8:1382-92.
- Liang NL, Avgerinos Szerk, Marone LK, et al. Vasc Endovaszkuláris Surg 2016; 50:405-10.
- Graif A, Grilli CJ, Kimbiris G, et al. J Vasc Interv Radiol 2017;28:1339-47.
- Avgerinos ED, Mohapatra A, Rivera-Lebron B, et al. J Vasc Surg Vénás Nyirokrendszeri Rendellenesség 2018; 6: 126-32.
- Bloomer TL, El-Hayek GE, McDaniel MC, et al. Katéter Cardiovasc Interv 2017; 89: 754-60.
- Arora S, Panaich S, Ainani N és mtsai. Vagyok J Cardiol 2017;120: 1653-61.
- Liu B, Liu M, Yan L és mtsai. J Int Med Res 2017; Január 1;.
- Ciampi-Dopazo JJ, Romeu-Prieto JM, Sanchez-Casado M és mtsai. J Vasc Interv Radiol 2018;29:101-6.
- Tukaye DN, McDaniel M, Liberman H és mtsai. JACC Cardiovasc Interv 2017;10:94-5.
- Hubbard J, Saad WE, Sabri SS, et al. Trombózis 2011;2011: 246410.
- Donaldson CW, Baker JN, Narayan RL, et al. Katéter Cardiovasc Interv 2015; 86: e81-7.
- George B, Parazino M, Omar HR és mtsai. Újraélesztés 2018; 122: 1-5.
klinikai témák: Antikoaguláns kezelés, aritmiák és klinikai EP, szívsebészet, dyslipidaemia, szívelégtelenség és cardiomyopathiák, invazív cardiovascularis angiográfia és beavatkozás, pulmonalis hypertonia és vénás thromboembolia, Érgyógyászat, SCD/ventricularis arrhythmiák, pitvarfibrilláció/supraventricularis arrhythmiák, szívsebészet és arrhythmiák, szívsebészet és szívelégtelenség, Lipid anyagcsere, sztatinok, akut szívelégtelenség, pulmonalis hypertonia, beavatkozások és Érgyógyászat
kulcsszavak: ACC kiadványok, Kardiológiai beavatkozások, Egyesült Államok Food and Drug Administration, vérnyomás, cardiopulmonalis Bypass, dilatáció, embolectomia, testmozgás tolerancia, extracorporalis membrán oxigenizáció, femorális véna, Fibrin, fibrinolízis, fibrinolitikus szerek, nyomon követési vizsgálatok, Heparin, kórházi mortalitás, magas vérnyomás, pulmonalis, indigókármin, intracranialis vérzések, jugularis vénák, beteg visszafogadása, pulmonalis artéria, tüdőembólia, életminőség, retrospektív vizsgálatok, sokk, kardiogén, Sternotomia, szívás, Tachycardia, thrombectomia, thrombolyticus terápia, trombózis, Szöveti plazminogén aktivátor, nagy energiájú lökéshullámok, érszűkület, érszűkítő szerek
< vissza a listákhoz