a fej és a nyak laphámsejtes karcinómája (SCCHN) a hatodik leggyakoribb neoplazma világszerte ~600 000 esetet diagnosztizálnak évente. Az elmúlt 20 év rengeteg klinikai vizsgálati adatot hozott, és ez átalakította az SCCHN kezelésének ellátásának színvonalát. Történelmileg a gyenge helyi betegségkontroll és a teljes túlélés lendületet adott számos klinikai vizsgálathoz, amelyek scchn-ben szenvedő betegek multimodalitási terápiáját értékelték. A fej és a nyak régió bonyolult anatómiája és kritikus funkcionális és társadalmi szerepe kétségtelenül jelentős erőfeszítéseket tett a rosszindulatú daganatok onkológiai reszekciójának alternatíváinak azonosítására ebben a régióban. Ebben az áttekintésben, összefoglaljuk a kombinált kemoradiációs terápia történelmi fejlődését az SCCHN kezelésében, adjon frissítést a legújabb szakirodalomról ezen a területen, valamint megvitassák azokat a kortárs klinikai kérdéseket, amelyeket a jövőbeli tanulmányok megoldhatnak.
egyidejű Kemoradiáció—a kísérleti kezeléstől az előnyben részesített kezelésig
a kombinált kemoradiációs kezelés szerepének klinikai vizsgálata az SCCHN esetében legalább az 1960-as évek végéig, korai vizsgálatokkal, amelyek egyetlen szer, köztük a fluorouracil (5FU), a bleomicin, a ciszplatin, a metotrexát és a mitomicin szekvenciális és egyidejű alkalmazását vizsgálták.1 Az ilyen vizsgálatok gyenge választ mutattak önmagában az egy szeres kemoterápiára, miközben a ciszplatinra mutattak, mint a leghatékonyabb egyetlen szerre, 25-30% – os válaszaránnyal.2-4 későbbi vizsgálat feltárta a multi-ágens kemoterápia szerepét, és a ciszplatin és a bleomycin5 kombinációval 70% – os, a ciszplatin és a folyamatos 5FU infúzió esetén pedig >90% – os válaszarány jelentős javulását mutatta.6,7 fontos, hogy ezek a korai vizsgálatok rámutattak arra, hogy a kemoterápia hozzáadása a hagyományos végleges sugárkezelésekhez és/vagy az SCCHN műtéthez potenciális túlélési előnyt jelent, és további vizsgálatokat indítottak nagyobb randomizált fázis III vizsgálatokban.
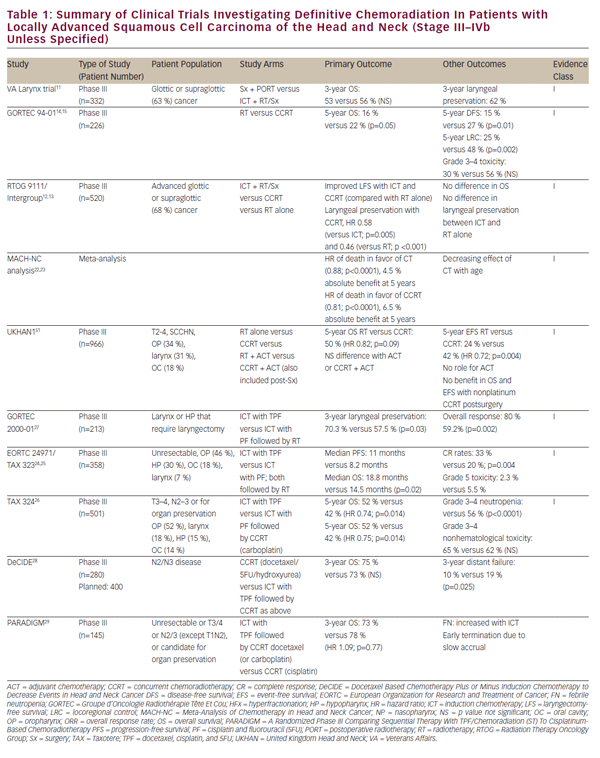
a kemoterápiás kezelések finomításával a lokálisan előrehaladott SCCHN-ben szenvedő betegeknél a végleges és szervmegtakarító kemoradiációs megközelítések lehetőségére fordult a mérlegelés. Ezt a munkát kezdetben egy sor, egyetlen intézményből álló tanulmány támogatta, amelyek bizonyítják a végleges kemoradiáció életképességét a műtét alternatívájaként glottikus és supraglottikus gége daganatok.8-10 a történelmileg fontos Veteránügyi gégerák-tanulmány végül kimutatta, hogy az indukciós kemoterápia (IKT), amelyet sugárzás követ, elérheti a szerv megőrzését SCCHN-ben szenvedő betegeknél kompromisszum nélkül a teljes túlélésben.11 Ez a vizsgálat megalapozta a landmark Radiation Therapy Oncology Group (RTOG) 9111 vizsgálat indoklását, amely a kemoterápia és a sugárzás megfelelő szekvenálásával foglalkozott lokálisan előrehaladott supraglotticus vagy glotticus gégerákban szenvedő betegeknél. A betegeket randomizálták: IKT, majd sugárzás; egyidejű kemoradiáció (CCRT); vagy csak a sugárzás.12,13 az RTOG 9111 eredményei a ccrt jobb voltát mutatták a lokoregionális betegségkontroll és a gége megőrzése szempontjából, míg a teljes túlélésben nem figyeltek meg különbséget a három kar között. Ezt követően a Groupe d ‘Onkologie Radioth (groupe d’ Onkologie Radioth) (Gortec) 94-01 vizsgálatban randomizált, lokálisan előrehaladott oropharyngealis primer tumorokban szenvedő betegek kaptak sugárterápiát vagy ccrt-t karboplatinnal/5FU-val, és javult a helyi betegségkontroll, valamint a teljes túlélés.14,15 a túlélés és a lokoregionális kontroll hasonló javulásáról számoltak be a CCRT-vel kezelt nasopharyngealis betegeknél.16-21 a head and Neck Cancer (Machnc) kemoterápia Meta-analíziséből származó jelentés 6,5% – os teljes túlélési előnyt javasolt 5 év után CCRT-vel, de nem IKT vagy adjuváns kemoterápiával.22,23 a kemoterápia túlélésre gyakorolt hatását ebben a metaanalízisben megfigyelték, hogy az életkor előrehaladtával csökken az 50 évnél idősebbeknél, kimutatható előny nem mutatkozott a 71 éves vagy annál idősebbeknél. Együttesen, bár ezek a vizsgálatok különböznek a befogadási és kizárási kritériumokban, a klinikai végpontokban és a kezelési módszerekben (lásd 1.táblázat), megerősítik a ccrt előnyeit az önmagában alkalmazott sugárterápiával szemben, mint a lokálisan előrehaladott SCCHN végleges kezelését.
A (Kemo) Sugárzást Megelőző Indukciós Kemoterápia-Életképes Stratégia?
bár a fej-fej összehasonlítás a CCRT-vel az IKT alacsonyabbrendűségét jelezte a helyi betegségkontroll szempontjából az RTOG 9111 klinikai vizsgálatban,12 továbbra is érdekes ez a terápiás megközelítés. Az RTOG 9111 adatai e megközelítések egyenértékűségét jelzik a magas fokú toxicitás szempontjából, ami megnehezíti az IKT választásának igazolását a betegek toleranciája alapján. Mindazonáltal az RTOG 9111 nyomon követési tanulmányai arra törekedtek, hogy az IKT platformján fejlődjenek annak érdekében, hogy ez életképesebb kezelési lehetőség legyen. Az EORTC 24971 / TA X 323 trial24,25 jobb teljes túlélést mutatott azzal, hogy docetaxelt (TPF) adtak az RTOG 9111 vizsgálatban alkalmazott ciszplatin és 5FU (PF) ICT sémához inoperábilis SCCHN-ben szenvedő betegeknél. A TA X 324 vizsgálat hasonlóképpen értékelte a TPF-et a PF-hez képest a CCRT beállításában, és ezekben a sémákban a heti karboplatint helyettesítette a ciszplatinnal. Ez a vizsgálat jobb lokoregionális és távoli betegségkontrollt, valamint jobb teljes túlélést mutatott TPF-fel a PF-hez képest.26 egy további követéses vizsgálat (GORTEC 2000-01) lokálisan előrehaladott gégerákban és hypopharyngealis carcinomában igazolta a betegségválasz javulását és a gége megőrzését indukciós TPF mellett a PF-hez képest, de nem mutatott semmilyen hatást a túlélésre.27 Bár ezek a vizsgálatok különböznek a befogadási és kizárási kritériumok, a klinikai végpontok és a kezelési módszerek tekintetében (lásd 1.táblázat), együttesen alátámasztják a TPF fölényét a PF-alapú IKT-vel szemben. Ennek ellenére az IKT közvetlen összehasonlítása a szokásos ciszplatin alapú CCRT-vel hiányzik.
a MACH-NC meta-analízis, amint azt korábban megjegyeztük, az ICT-nek a CCRT-hez viszonyított alacsonyabbrendűségét sugallta a teljes túlélés és a lokoregionális betegségkontroll szempontjából.22 figyelemre méltó azonban, hogy az IKT előnye a távoli áttétek aránya tekintetében kifejezettebb volt, mint a CCRTÉ.22 ez tükrözheti a kemoterápia külön szerepét ezekben a kezelési megközelítésekben. Az egyidejű kemoterápia domináns radioszenzitizáló szerepet játszhat, ami domináns hatást gyakorol a helyi betegségkontrollra, míg a több ágensű IKT hatékony szisztémás kezelést biztosíthat a mikro-metasztatikus betegség számára. Ez a hipotézist generáló megfigyelés e kezelések potenciálisan kiegészítő jellegére utal, és érdeklődést váltott ki kombinációjuk iránt. Eddig az IKT és a CCRT kombinációjának vizsgálatára irányuló erőfeszítések gyenge eredményszemléletű és nem meggyőző eredményeket eredményeztek (döntési és PARADIGMATANULMÁNYOK).28,29 egy folyamatban lévő randomizált fázis III vizsgálat összehasonlítja az IKT-t a PF-vel vagy a TPF-vel, amelyet ciszplatin alapú CCRT követ, szemben a ccrt-vel önmagában, mint elsővonalbeli kezelés lokálisan előrehaladott SCCHN esetén (NCT00261703). A fenti, CCRT-re és IKT-ra vonatkozó vizsgálatok eredményeit az 1. táblázat foglalja össze.
adjuváns Kemoradiáció
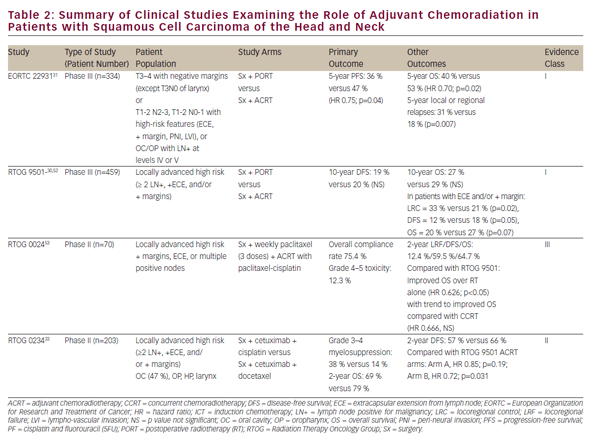
a fent említett klinikai vizsgálatok a ccrt-t életképes végleges kezelésként hozták létre szervmegőrzés lokálisan előrehaladott SCCHN-ben. Mindazonáltal a végleges onkológiai reszekció továbbra is fontos kezelési lehetőség a lokalizált betegség esetén, és a multimodalitás létfontosságú része terápia a szájüreg, a gége és a hypopharynx előrehaladott daganatainál. A kemoradiáció szerepét az onkológiai reszekciót követő adjuváns környezetben nagymértékben meghatározta két III.fázisú randomizált vizsgálat— EORTC 22931 és RTOG 950130,31 (lásd 2. táblázat). Ezek a vizsgálatok megvizsgálták a posztoperatív sugárzás versus adjuváns kemoradiáció ciszplatinnal 3 hetente három cikluson keresztül posztoperatív SCCHN betegeknél. Mindkét vizsgálat javulást mutatott a lokoregionális betegség kontrolljában és a progressziómentes túlélésben, míg az EORTC vizsgálat a teljes túlélés javulását is mutatta. E két vizsgálat post-hoc elemzése arra utalt, hogy az adjuváns CCRT előnye a reszektált nyirokcsomókból származó pozitív műtéti margókkal és/ vagy extracapsularis kiterjesztéssel (ECE) rendelkezőknél volt a legnagyobb.32 az adjuváns CCRT szerepe a szoros műtéti margóval rendelkező betegeknél kevésbé egyértelmű, és ezt az EORTC 22931 is alátámasztotta, amely 5 mm-es műtéti margóval rendelkező betegeket tartalmazott. Másrészt az RTOG 9501 pozitív, de nem közeli margókon alapuló betegeket tartalmazott. A Post-hoc elemzés azt sugallta, hogy a CCRT nem mutat nyilvánvaló előnyt azoknál a betegeknél, akik megfelelnek a belépési kritériumoknak e vizsgálatok közül csak az egyikben.32 hasonló módon az adjuváns CCRT-t idős betegeknél nem vizsgálták kellőképpen, mivel a 70 év felettieket kizárták az EORTC 22931-ből, és az RTOG 9501-ben szenvedő betegeknek csak kis hányadát (5%) teszik ki.30,31
Pursuant to EORTC 22931 and RTOG 9501, adjuvant CCRT has now become standard-of-care treatment in high-risk postoperative SCCHN patients. The phase II RTOG 0234 study has explored alternative adjuvant chemoradiation treatment regimens, randomizing patients with multiple involved lymph nodes, ECE, or positive margins to the epidermal growth factor receptor (EGFR) antibody, cetuximab, plus docetaxel or cetuximab plus cisplatin. This study demonstrated an apparent survival benefit from concurrent adjuvant cetuximab and docetaxel.33 ennek az érdekes II. fázisú vizsgálatnak az eredményei validálást igényelnek egy III. fázisú vizsgálatban a klinikai gyakorlatba való beépítés előtt.
sugárterápiás frakcionálás hatása a Kemoradiációra
a hatékonyság növelése érdekében a korábbi klinikai vizsgálatok alternatív frakcionálási sémákat vizsgáltak sugárterápiás beadásra egyidejű kemoterápiával vagy anélkül SCCHN betegeknél. Az RTOG 9003 és a dán fej-és nyaki Rákcsoport (dahanca) vizsgálatok azt mutatták, hogy a lokoregionális betegség kontrollja javult gyorsított vagy hiperfrakcionált sugárkezeléssel, ha a sugárzást önmagában alkalmazzák.34,35 egy későbbi metaanalízis még szerény túlélési előnyt is javasolt a sugárzás hiper-frakcionálásából, ha egyedüli kezelési módként használják.36 egyidejű kemoterápia esetén azonban az RTOG 0129 és a GORTEC 99-02 vizsgálatok nem mutattak javulást a klinikai kimenetelben az akcelerált és a hagyományos sugárterápia alkalmazása esetén.37,38 a hiper-frakcionált CCRT, összehasonlítva a hiper-frakcionált sugárzással, javította a lokoregionális betegségkontrollt a Duke Egyetem egyetlen intézményi tanulmányában és a Jugoszlávia III.fázisú vizsgálatában, az utóbbi szintén javította az általános túlélést és a távoli metasztázismentes túlélést.39,40 ezek a vizsgálatok azt mutatják, hogy a ccrt előnye továbbra is fennáll hiper-frakcionált sugárterápia esetén. A hagyományos frakcionált CCRT és a hiper-frakcionált ccrt közvetlen összehasonlítását a mai napig nem végezték el. Figyelemre méltó azonban, hogy a Mach-NC metaanalízis nem mutatott ki különbséget az eredményben a ccrt-vel kezelt betegek között hagyományos vagy megváltozott frakcionálási technikákkal.22
toxicitás-a Kemoradiáció költsége
az RTOG 9111 számos, az azt megelőző egyintézményes vizsgálattal egyetértésben jelezte, hogy a kemoterápia előnyei, függetlenül attól, hogy szekvenciálisan vagy egyidejűleg adják-e be a sugárzást, további toxicitás rovására járnak.12 Hasonlóképpen, az adjuváns környezetben mind az EORTC 2291, mind az RTOG 9501 klinikai vizsgálatok azt mutatták, hogy a kemoradiációval járó 3.fokozatú toxicitás hozzávetőlegesen megkétszereződött az önmagában alkalmazott sugárzáshoz képest.30,31 ez a tendencia még a hiper-frakcionált sugárterápia beállításában is fennáll.39 bár a történeti vizsgálatok alapján meghatározott bármely specifikus toxicitás várható aránya valószínűleg túlbecsült az erősen konform sugárterápiás technikák, például az intenzitás modulált sugárterápia (IMRT) jelenlegi korszakában. Két kisebb, randomizált vizsgálat a xerostomia incidenciájának és súlyosságának szignifikáns csökkenéséről számolt be az IMRT alkalmazásával összehasonlítva a fej-és nyakrák hagyományos háromdimenziós konformális sugárterápiájával (parotid-megtakarító intenzitás modulált versus hagyományos sugárterápia a fej-és nyakrák és a Tata Memorial Hospital vizsgálatokban).41,42 a CCRT-t vizsgáló legújabb vizsgálatok lehetővé teszik az IMRT-alapú kezelést standard megközelítésként az SCCHN kezelésében. Még nem látni kell, hogy az IMRT milyen hatással lesz a toxicitási arányokra kemoterápiával kombinálva ezekben a nagyobb randomizált vizsgálatokban.
a továbbfejlesztett sugárterápiás technikák, valamint a támogató és kiegészítő szolgáltatások, például a beszédnyaláb-patológia és a fogászati ellátás növekvő jelentősége és elérhetősége még tovább korlátozza a súlyos, nem hematológiai toxicitások előfordulását. A CCRT-től várható toxicitás azonban várhatóan továbbra is magasabb lesz, mint önmagában a sugárterápia. Ez a tartós toxicitás a kemoterápia és a sugárkezelés kombinálásának klinikai költségét tükrözi. Ebben a környezetben továbbra is kiemelkedő fontosságú, hogy az orvosok átfogóan értékeljék a betegeket annak megállapítására, hogy a CCRT lehetséges előnyei igazolják ezt a költséget. Egyszeri modalitású sugárterápiás alapú kezelések alkalmazása jelentős társbetegségekkel/alacsony kiindulási teljesítmény státusszal vagy alacsony kockázatú, korai stádiumú betegséggel rendelkező betegeknél ésszerű megközelítés lehet a terápiás arány maximalizálása érdekében. Ez a kockázat-haszon elemzés még fontosabbá válik a molekuláris célzott szerek megjelenésével, amelyek életképes alternatívát kínálnak az egyidejű terápiához.
a molekulárisan célzott szerek feltörekvő szerepe
a kemoradiációs kezelés toxicitása, valamint a klinikai eredmények további javításának vágya elősegítette a növekvő érdeklődést a molekuláris célzott szerek szerepe iránt az SCCHN kezelésében. Az EGFR az SCCHN daganatok 80-90% – ában túlexpresszált vagy mutált, és ez a sugárterápiára adott válasz csökkenésével és rosszabb klinikai eredményekkel jár.43-45 2006-ban, Bonner et al. lokálisan előrehaladott SCCHN-ben szenvedő betegeken végzett mérföldkőnek számító vizsgálatról számoltak be, amelyet önmagában vagy az EGFR antitesttel, a cetuximabbal egyidejűleg kezelt sugárzással kezeltek. Ez a vizsgálat kimutatta, hogy az egyidejűleg alkalmazott cetuximab és a sugárzás növelte a lokoregionális betegség kontrollját és a teljes túlélést anélkül, hogy súlyosbította volna a sugárzás gyakori toxicitását.46 Ez a vizsgálat meghatározta az egyidejű cetuximab és sugárkezelés szerepét olyan betegeknél, akik nem jelöltek ciszplatinra.
a későbbi vizsgálatok arra törekedtek, hogy a CCRT-t az egyidejű cetuximabbal hasonlítsák össze a ciszplatinnal. A retrospektív és a korai fázisú vizsgálatok különböztek ebben az értékelésben, és egy randomizált fázis III összehasonlítás folyamatban van az RTOG 1016 – ban. Nevezetesen, az RTOG 0522 vizsgálatban értékelték a cetuximab lehetséges hozzáadott előnyét a ccrt47 ciszplatin alapú sémájához képest. Ez a vizsgálat azt mutatta, hogy a standard platina alapú CCRT-hez adva a cetuximab nem javította tovább a progressziómentes vagy a teljes túlélést. A posztoperatív körülmények között az RTOG 0920 az adjuváns sugárterápiát értékeli cetuximabbal vagy anélkül lokálisan előrehaladott reszekált SCCHN-ben, míg a fázis II/III RTOG 1216 vizsgálat az adjuváns ccrt-t értékeli egyidejű ciszplatin versus docetaxel versus docetaxel és cetuximab a magas kockázatú SCCHN esetén.
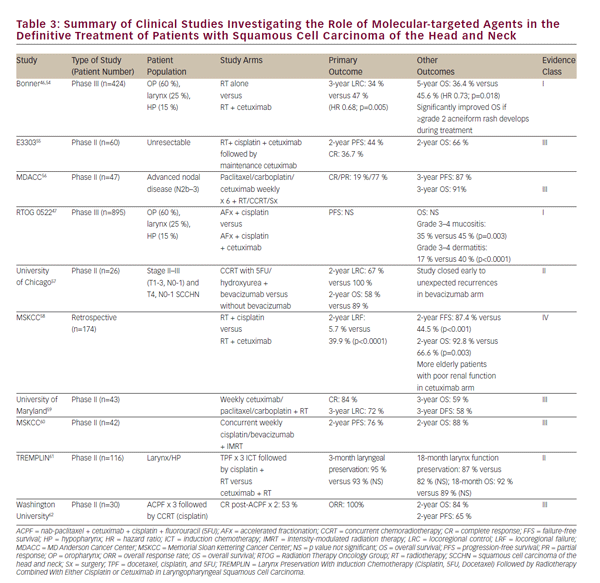
számos korai fázisú klinikai vizsgálat további molekuláris célzott szerekkel együtt sugárzás az SCCHN kezelésére végeztek vagy folyamatban vannak. Ezek kiválasztását az i>3. táblázat foglalja össze. A cetuximabbal végzett vizsgálatok kivételével egyetlen más molekulárisan megcélzott szer sem jutott el olyan pontig, hogy a klinikai vizsgálati környezeten kívül befolyásolja a jelenlegi gyakorlatot. Míg a molekulárisan megcélzott szerek kilátása ígéretes, az egyidejű magas dózisú ciszplatin kemoterápia továbbra is az előnyben részesített, 1.szintű ajánlás A ccrt-re vonatkozó jelenlegi nemzeti átfogó ellátás (NCCN) irányelvei.
Kemoradiációs terápia fej—nyaki rákban-fejlődő paradigma
az elmúlt 20 évben a kemoradiáció megjelenése volt az ellátás standardja az SCCHN végleges kezelésében. Megfelelően kiválasztott betegeknél a kezelés kimutatható túlélési előnye meghaladja a további toxicitások kockázatát. Fontos kérdések maradnak azonban a kemoradiáció optimális alkalmazásával kapcsolatban. Számos klinikai vizsgálat tovább tárta fel az IKT potenciális klinikai hasznosságát lokálisan előrehaladott SCCHN-ben szenvedő betegeknél, és bár ezek a vizsgálatok kimutatták az IKT-kezelések javulását a toxicitás rovására, egyik sem bizonyította meggyőzően jelentős klinikai javulást a ciszplatin alapú CCRT-hez képest.
a jövőbeni vizsgálatok kétségtelenül folytatják az alternatív kemoterápiás kezelések és adagolási ütemtervek, valamint a sugárterápiás frakcionálási, adagolási és szállítási módszerek feltárását a meglévő technikák előmozdítása érdekében. Sőt, az új molekuláris célzott kemoterápiás szerek folyamatos fejlesztésével a jövőbeni tanulmányok szinte biztosan meghatározzák ezeknek a szereknek a növekvő szerepét az SCCHN kezelésében. Különösen érdekes lehet ezeknek a szereknek a használata a CCRT előtti indukciós környezetben, ahol megcélozhatják a mikro-metasztatikus betegséget és csökkenthetik a betegség távoli visszaesését anélkül, hogy toxicitással kapcsolatos korlátozásokat vezetnének be a CCRT befejezési arányára. Míg a CCRT alkalmazása fejlődik, a műtét megfelelő szerepének folyamatos vizsgálata az SCCHN-ben szintén indokolt. Mind a robotsebészet, mind a kemoradiációs kezelési megközelítések fejlődése egyensúlyt biztosít az ilyen vizsgálatokhoz. A jelenlegi gyakorlati Irányelvek adjuváns kemoradiációt javasolnak posztoperatív betegek pozitív margóval vagy ECE-vel, míg adjuváns sugárzás önmagában vagy a kemoradiáció megfontolása ajánlott posztoperatív betegeknél pt3 vagy pT4 primer, pN2 vagy pN3 csomópont betegség, IV.vagy V. szintű nyirokcsomó érintettség, vagy peri-neurális vagy lympho-vaszkuláris invázióval. A korai stádiumú SCCHN-ben szenvedő betegek körében a magas kockázatú állapot preoperatív radiográfiai és klinikai előrejelzőit azonosító további vizsgálatok értékesnek bizonyulnak az ilyen betegek kezelésének irányításában, akiket meg lehet kímélni műtéti beavatkozás előzetes végleges kemoradiációs kezelési megközelítéssel.
a humán papilloma vírus (HPV) fertőzés közelmúltbeli felismerése az OROPHARYNX48-ból és potenciálisan más helyekről származó SCCHN okaként és kedvező prognosztikai tényezőjeként átalakítja az SCCHN mint betegség entitás fogalmát. Az RTOG 0129 retrospektív elemzésében a HPV-re pozitív tumoros betegek 3 éves teljes túlélése 82,4% volt,szemben a HPV-negatív betegség 57%-ával (p49, 50 ennek fényében a jövőbeni vizsgálatokat szükségszerűen a HPV státus szerint rétegzik, vagy a HPV-pozitív vagy-negatív betegek egy részhalmazához igazítják, ami növekvő szakadást vált ki a kezelési megközelítésekben. A már felvetett lehetőség a HPV-pozitív daganatok kevésbé toxikus kezelési megközelítéseinek, valamint a HPV-negatív daganatok agresszívebb végleges kezelésének vizsgálata annak érdekében, hogy figyelembe vegyék a jelenlegi kezelési módokra adott válaszaik közötti éles különbségeket. Az RTOG 1016 egy ilyen vizsgálat, amely kifejezetten a HPV-pozitív betegeket értékeli a kezelés intenzitásának csökkentése érdekében egyidejű cetuximab sugárzással szemben a standard ciszplatin alapú CCRT-vel. A kölcsönhatás a specifikus kezelési rendek és különösen a molekuláris célzott szerek tumor HPV státusz kétségtelenül bizonyítani termékeny talajt a jövőbeli kutatások. Még nem látni kell, hogy a növekvő HPV-járvány és a jelenlegi oltási programok milyen hatással lesznek az SCCHN-ben szenvedő betegek klinikai eredményeire és kezelési megközelítéseire.