Bevezetés
a vénás thromboembolia (VTE), beleértve a mélyvénás trombózist (DVT), a tüdőembóliát (PE) és a splanchnikus vénás trombózist, a rák gyakori szövődménye.1 a rákkal összefüggő VTE kialakulása az életminőség romlásával jár, és jelentős gazdasági terhet ró mind a betegre, mind az egészségügyi rendszerre.2 a VTE a második vezető halálok a kemoterápiában részesülő rákos járóbetegek körében, és kimutatták, hogy független előrejelzője a mortalitásnak a daganatos betegek populációjában.3,4 a rákkal összefüggő VTE kezelése kihívást jelenthet, mivel a VTE és az antikoagulánsokkal összefüggő vérzés kiújulásának kockázata a megfelelő kezelés ellenére magas.5 ezenkívül a Gyógyszerkölcsönhatások és a rákkal összefüggő komorbiditások, mint például a vese-és/vagy májműködési zavar, a csökkent orális bevitel, a kemoterápia által kiváltott hányinger és hányás, valamint a thrombocytopenia szintén növelik a kezelés összetettségét azáltal, hogy korlátozzák az antikoaguláns szer választását.
a kis molekulatömegű heparint értékelő klinikai vizsgálatok a rákhoz társuló VTE kezelésére
az alacsony molekulatömegű heparin (LMWH) hosszú távú alkalmazása a VTE kezelésére aktív daganatos betegeknél első vonalbeli terápiaként ajánlott több nyílt elrendezésű randomizált, kontrollos vizsgálat (RCT) eredményei alapján.6,7 az eddig közzétett két legnagyobb tanulmány, a CLOT (a kis molekulatömegű heparin és az orális antikoaguláns terápia összehasonlítása a visszatérő vénás thromboembolia megelőzésére daganatos betegeknél) és a CATCH (az akut kezelések összehasonlítása a rákos Haemostasisban) vizsgálatok egy LMWH-t hasonlítottak össze a K-vitamin antagonista terápiával aktív daganatos és akut tünetekkel járó proximalis DVT vagy PE-ben szenvedő betegeknél. A kiindulási jellemzőket lásd az 1.táblázatban, a vizsgálati eredményeket pedig a 2. táblázatban.8,9 mindkét vizsgálatban nyílt elrendezésű vizsgálati tervet alkalmaztak, a K-vitamin antagonista kontroll karon ugyanazt a nemzetközi normalizált célarányt (INR), ugyanazt az aktív daganatmeghatározást, azonos kezelési időtartamot és hasonló alkalmassági kritériumokat alkalmaztak.
1. táblázat: a fogási és alvadási vizsgálatok vizsgálati felépítése és kiindulási jellemzői
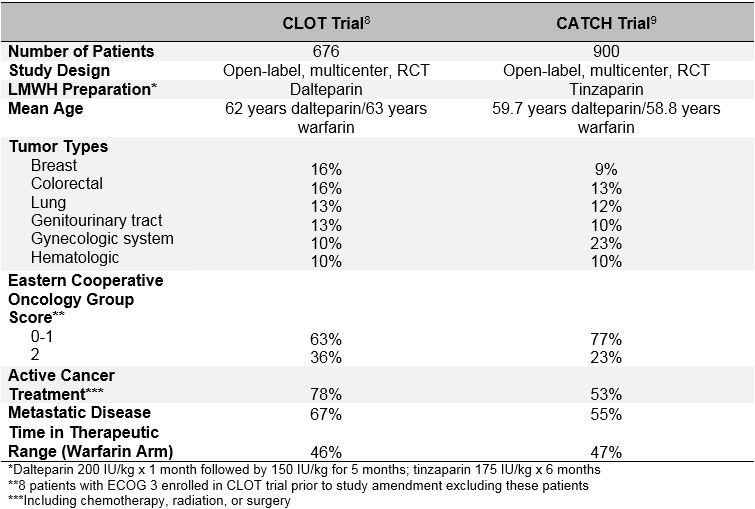
2. táblázat: Az alvadási és fogási vizsgálatok eredményei

a 2003-ban közzétett VÉRRÖGVIZSGÁLAT 676 beteget randomizált dalteparin (napi 200 NE/kg 1 hónapig, majd napi 150 NE/kg 5 hónapig) vagy K-vitamin antagonista (warfarin vagy acenokumarol INR 2,5 célponttal, összesen 6 hónapig, kezdeti 5-7 nap átfedésben a dalteparinnal 200 NE/kg).8 tünetekkel visszatérő DVT-t vagy PE-t, beleértve a PE-vel összefüggő halált is, 27 betegnél (7,0%) figyeltek meg dalteparinra randomizálva, és 53 betegnél (15%), akiket K-vitamin antagonistára randomizáltak (relatív hazárd 0,48; 95% – os konfidencia intervallum , 0,30-0,77; p = 0,002). Nem figyeltek meg különbséget a súlyos vérzés (6 vs.4%; p = 0,27), bármilyen vérzés (15 vs. 19%; p = 0,09) vagy halál (39 vs. 41%; p = 0,53) arányában a 2 csoport között.
a CATCH-vizsgálatban, amelyet több mint 10 évvel később, 2015-ben tettek közzé, 900 beteget randomizáltak tinzaparinra (napi 175 NE/kg dóziscsökkentés nélkül) vagy warfarinra (cél INR 2,0-3,0 kezdeti tinzaparinnal 175 NE/kg átfedés 5-10 napig), összesen 6 hónapig.9 a visszatérő VTE elsődleges összetett végpontja, beleértve az incidenses proximális DVT-t és PE-t, 31 betegnél (6,9%) fordult elő a tinzaparin-karon és 45 betegnél (10%) a warfarin-karon (HR 0,65; 95% CI, 0,41-1,03; p = 0,07). A tünetekkel járó DVT szignifikánsan kevesebb tinzaparinnal kezelt betegnél fordult elő (2, 7 vs.5, 3%; HR 0, 48; 95% CI, 0, 24-0, 96; p = 0, 04). Bár a súlyos vérzések aránya mindkét karon hasonló volt, a klinikailag releváns, nem súlyos vérzés szignifikáns csökkenését figyelték meg a tinzaparin alkalmazásával (10,9 vs.15,3%; HR 0,58; 95% CI, 0,40-0,84; p = 0,004). A mortalitás mindkét csoportban hasonló volt, a betegek körülbelül egyharmada halt meg a vizsgálati időszak alatt (33,4 vs.30,6%; p = 0,54). Bár a tinzaparin nem csökkentette szignifikánsan a visszatérő VTE elsődleges összetett végpontját, a CATCH vizsgálat eredményei alátámasztják a hosszú távú LMWH alkalmazását a rákkal összefüggő VTE előnyben részesített kezeléseként, a klinikailag releváns súlyos vérzés alacsonyabb kockázata és a visszatérő DVT jelentős csökkenése miatt.
a CATCH-próba sikertelensége az elsődleges végpont statisztikai szignifikanciájának elérése a warfarin-karon megfigyelt, a vártnál alacsonyabb visszatérő VTE-aránynak tudható be. Ennek a megfigyelésnek az egyik lehetséges magyarázata lehet A warfarin kezelésének javulása a fogási vizsgálatban. Azonban az INR kontroll hasonló szintjei mindkét vizsgálatban ellentmondanak ennek (a terápiás tartományban az idő 46% volt a vérrögben, szemben a fogás 47% – ával; a terápiás tartomány feletti idő 24% volt a vérrögben, szemben a fogás 27% – ával). Valószínűbb magyarázat a “kevésbé beteg” betegek kiválasztásának elfogultsága a fogási vizsgálatba való beiratkozáshoz. Bár a CATCH és a CLOT vizsgálatok hasonló befogadási és kizárási kritériumokat alkalmaztak, a két betegpopuláció között alapvető különbségek vannak a kiindulási jellemzőkben, különösen a trombotikus és a prognosztikai kockázati tényezők tekintetében. A VÉRRÖGVIZSGÁLATBAN a betegek nagyobb hányada kapott aktív daganatellenes kezelést (72% vérrög vs. 53% fogás), anamnézisében szerepelt korábbi VTE (11% vérrög vs. 6% fogás), metasztatikus betegségre utaló bizonyíték volt (67% vérrög vs. 55% fogás), és volt egy gyengébb teljesítmény állapotát (Keleti kooperatív onkológiai csoport pontszám 2 36% vérrög vs.23% fogás). Ezenkívül a mortalitás a 6 hónapos kezelési periódus alatt is magasabb volt a VÉRRÖGPOPULÁCIÓBAN (39% vérrög vs.32% fogás). Így a fogási betegpopuláció valószínűleg alacsonyabb volt a visszatérő VTE velejáró kockázata a VÉRRÖGVIZSGÁLATI betegekhez képest. Nagyon valószínű, hogy a nyomozók nem vették fel a betegeket a CATCH-be, ha úgy érezték, hogy az LMWH előnyösebb lenne, mint a warfarin, ami olyan betegek szelektív beiratkozását eredményezi, akiknél kevésbé valószínű, hogy visszatérő VTE alakul ki.
a közvetlen orális antikoagulánsokat értékelő vizsgálatok rákkal összefüggő VTE-ben
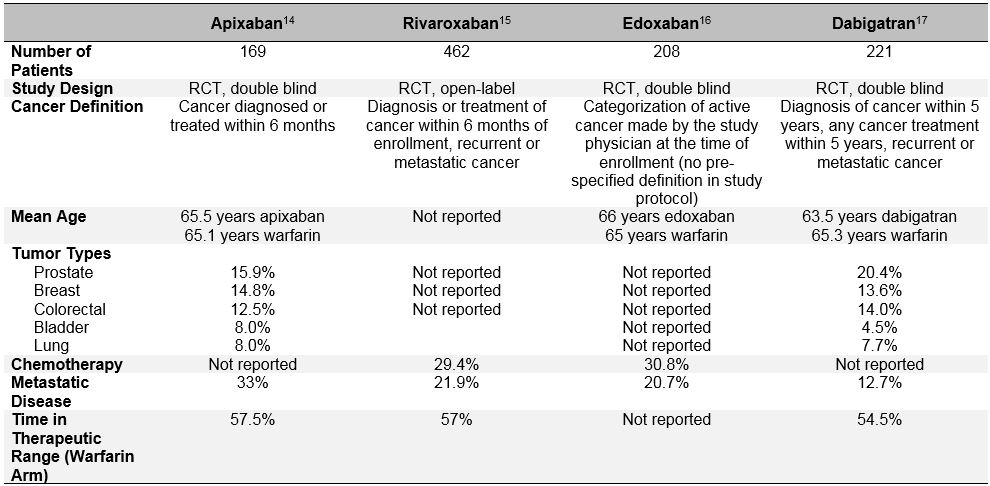
a betegek szelekciós torzulása még nyilvánvalóbb a legutóbbi randomizált vizsgálatokban, amelyek a közvetlen orális antikoagulánsok (DOAC) hatékonyságát és biztonságosságát értékelték az akut VTE kezelésére.10 ezeket az orális antikoagulánsokat az elmúlt évtizedben széles körben tanulmányozták pitvarfibrilláció, VTE kezelés és VTE megelőzés terén. Fázisú klinikai vizsgálatokban következetesen kimutatták, hogy a DOAC-ok nem alacsonyabbak a warfarinnál (összesített relatív kockázat 0,90; 95% CI, 0,77-1.06), és hasonló vagy csökkent a súlyos vérzés kockázata (összesített RR 0,40; 95%-os CI, 0,45-0,83).11 azoknál a betegeknél, akiket ezekben a vizsgálatokban “ráknak” vagy “aktív ráknak” minősítettek, úgy tűnik, hogy a DOAC-k hasonlóan teljesítenek, mint a warfarin.12 de ezeknek a post-hoc adatoknak a mélyebb vizsgálata fontos betegszelekciós torzítást tár fel, és megkérdőjelezi a DOAC vizsgálati eredmények általánosíthatóságát a” valós életben ” VTE-ben szenvedő rákos betegek számára. Az ezekben a vizsgálatokban alkalmazott “aktív rák” heterogén definíciói mellett, amelyek különböztek a vérrög-és fogási vizsgálatoktól, a visszatérő VTE és a vérzés fontos meghatározói szintén nagyon eltérőek voltak a DOAC rákos betegeknél az LMWH rákspecifikus vizsgálatoktól (3.táblázat). Ezek közé tartozik a metasztatikus betegség jelenléte és a daganatellenes kezelés egyidejű alkalmazása. A halálozás hatalmas különbségei a vizsgálati időszak alatt azt is állítják, hogy a “rákos” betegek nagyon különböző csoportjait bevonták a DOAC versus LMWH vizsgálatokba. Továbbá, ellentétben az LMWH-val, amely a visszatérő VTE kockázatának jelentős csökkenésével jár a K-vitamin antagonistákhoz képest (RR 0,52; 95% CI, 0,36-0.74), a DOAC-ok nem csökkentették szignifikánsan ezt a kockázatot az EINSTEIN klinikai vizsgálati programba bevont 1132 rákos beteg meta-analízisében, HOKUSAI-VTE (Edoxaban Versus Warfarin a tüneti vénás thromboembolia kezelésére), helyreáll (a dabigatrán hatásossága és biztonságossága a warfarinnal összehasonlítva az akut tüneti vénás thromboembolia 6 hónapos kezelésére), és AMPLIFIKÁLJÁK (Apixaban a tüdőembólia és a mélyvénás trombózis kezdeti kezelésére első vonalbeli terápiaként) RCT-k (RR 0,66; 95% CI, 0, 39-1, 11).10 mindezek a megfontolások óvatosságra intenek a DOACs nem választott alkalmazása esetén aktív daganatos és akut, tünetekkel járó VTE-ben szenvedő betegeknél.13
3. táblázat: a III. fázisú DOAC-vizsgálatokból származó rákos betegek alcsoportjainak vizsgálati tervezése és kiindulási jellemzői
következtetések
minden jelentős, bizonyítékokon alapuló konszenzusos irányelv az LMWH-t javasolja a rákkal összefüggő VTE kezdeti és hosszú távú kezelésére.6,7,13 ez az ajánlás azon a megfigyelésen alapul, hogy az LMWH nemcsak hatékonyabb, mint a warfarin a visszatérő VTE megelőzésében, hanem további előnyöket is kínál orális szerekkel szemben, beleértve a stabil antikoagulációt a betegek rossz orális bevitel, a gyógyszerkölcsönhatások hiánya, valamint klinikai tapasztalat az invazív eljárásokat körülvevő antikoaguláció kezelésében és thrombocytopenia. Bár a DOAC-K jelenleg nem ajánlottak a VTE kezelésére rákos betegeknél, a rivaroxabánt és az edoxabánt az LMWH-val összehasonlító RCT-k jelenleg folyamatban vannak, és segítenek tisztázni szerepüket a rákkal összefüggő VTE-ben.6,13
- Khorana AA, Dalal M, Lin J, Connolly GC. A vénás thromboembolia (VTE) előfordulása és előrejelzői az ambuláns, magas kockázatú daganatos betegek körében kemoterápiában részesültek az Egyesült Államokban. Rák 2013; 119: 648-55.
- Kourlaba G, Relakis J, Mylonas C és mtsai. A rákos betegek vénás thromboemboliájának humanista és gazdasági terhe: szisztematikus felülvizsgálat. Véralvadási Fibrinolízis 2015; 26: 13-31.
- Kuderer NM, Ortel TL, Francis CW. A vénás thromboembolia és az antikoaguláció hatása a rákra és a rák túlélésére. J Clin Oncol 2009;27: 4902-11.
- Khorana AA, Francis CW, Culakova E, Kuderer NM, Lyman GH. A trombembolia a járóbeteg-kemoterápiában részesülő rákos betegek halálának egyik fő oka. J Thromb Haemost 2007; 5: 632-4.
- Prandoni P, Lensing AW, Piccioli A és mtsai. Recidiváló vénás thromboembolia és vérzéses szövődmények antikoaguláns kezelés során daganatos és vénás thrombosisban szenvedő betegeknél. Vér 2002;100: 3484-8.
- Lyman GH, Bohlke K, Khorana AA, et al. Vénás thromboembolia profilaxis és kezelés daganatos betegeknél: american society of clinical oncology clinical practice guideline update 2014. J Clin Oncol 2015; 33: 654-6.
- Streiff MB, Holmstrom B, Ashrani A és mtsai. Rákkal Összefüggő Vénás Thromboemboliás Betegség, 1.2015 Verzió. J Natl Compr Canc Netw 2015;13:1079-95.
- Lee AY, Levine MN, Baker RI és mtsai. Alacsony molekulatömegű heparin versus kumarin a visszatérő vénás tromboembólia megelőzésére rákos betegeknél. N Engl J Med 2003; 349: 146-53.
- Lee AY, Kamphuisen PW, Meyer G és mtsai. Tinzaparin vs Warfarin akut vénás thromboembolia kezelésére aktív rákos betegeknél: randomizált klinikai vizsgálat. JAMA 2015; 314: 677-86.
- Carrier M, Cameron C, Delluc A, Castellucci L, Khorana AA, Lee AY. Az antikoaguláns terápia hatásossága és biztonságossága az akut, rákkal összefüggő trombózis kezelésében: szisztematikus áttekintés és metaanalízis. Thromb Res 2014;134: 1214-9.
- van Es N, Coppens M, Schulman S, Middeldorp S, B stb. Közvetlen orális antikoagulánsok az akut vénás tromboembólia K-vitamin antagonistáival összehasonlítva: bizonyítékok a 3.fázisú vizsgálatokból. Vér 2014;124: 1968-75.
- Vedovati MC, Germini F, Agnelli G, Becattini C. közvetlen orális antikoagulánsok VTE-ben és rákos betegekben: szisztematikus áttekintés és metaanalízis. Mellkas 2015; 147: 475-83.
- Kearon C, Akl EA, Ornelas J, et al. Antitrombotikus terápia VTE betegség esetén: Mellkasi útmutató és szakértői jelentés. Mellkas 2016; 149: 315-52.
- Agnelli G, B H, Cohen A és mtsai. Orális apixaban vénás thromboembolia kezelésére daganatos betegeknél: az AMPLIFY vizsgálat eredményei. J Thromb Haemost 2015;13: 2187-91.
- Prins MH, Lensing AW, Brighton TA és mtsai. Orális rivaroxaban versus enoxaparin és K-vitamin antagonista a tünetekkel járó vénás thromboembolia kezelésére daganatos betegeknél (EINSTEIN-DVT és EINSTEIN-PE): két randomizált, kontrollos vizsgálat összesített alcsoport-elemzése. Lancet Haematol 2014;1: e37-46.
- Raskob GE, van Es N, Segers a, et al. Edoxaban vénás thromboembolia kezelésére daganatos betegeknél: a Hokusai-VTE randomizált, kettős-vak, kettős hatóanyag nélküli vizsgálat non-inferioritási alcsoport analízisének eredményei. Lancet Haematol 2016; 3: e379-87.
- Schulman S, Goldhaber SZ, Kearon C, et al. Dabigatrán vagy warfarin kezelés vénás thromboemboliás és daganatos betegeknél. Thromb Haemost 2015;114: 150-7.
klinikai témák: Anticoagulation Management, Arrhythmias and Clinical EP, Cardio-Oncology, Pulmonary Hypertension and Venous Thromboembolism, Anticoagulation Management and Atrial Fibrillation, Anticoagulation Management and Venothromboembolism, Atrial Fibrillation/Supraventricular Arrhythmias
Keywords: Kardiotoxinok, kardiotoxicitás, Heparin, kis molekulatömegű, Warfarin, antikoagulánsok, nemzetközi normalizált arány, acenokumarol, Dalteparin, Antitrombinok, vénás thromboembolia, kockázati tényezők, pitvarfibrilláció, járóbetegek, kutató személyzet, életminőség, Piridonok, Pirazolok, piridinek, Tiazolok, vénás trombózis, tüdőembólia, trombózis, Thrombocytopenia, komorbiditás, hemosztázis, daganatok
< vissza a listákhoz