Inleiding
veneuze trombo-embolie (VTE), inclusief diepveneuze trombose (DVT), longembolie (PE) en splanchnische veneuze trombose, is een frequente complicatie van kanker.1 de ontwikkeling van kankergeassocieerde VTE gaat gepaard met een verminderde kwaliteit van leven en legt een aanzienlijke economische last op zowel de patiënt als de gezondheidszorg.2 VTE is de op één na belangrijkste doodsoorzaak bij poliklinische kankerpatiënten die chemotherapie krijgen en is een onafhankelijke voorspeller van mortaliteit in de populatie van kankerpatiënten.3,4 de behandeling van kankergerelateerde VTE-behandeling kan een uitdaging zijn omdat de risico ‘ s van recidiverende VTE-en anticoagulansgerelateerde bloedingen hoog zijn, ondanks de juiste behandeling.Daarnaast vergroten geneesmiddelinteracties en kankergerelateerde comorbiditeiten, zoals nier-en/of leverdysfunctie, verminderde orale inname, door chemotherapie geïnduceerde misselijkheid en braken en trombocytopenie ook de complexiteit van de behandeling doordat de keuze van het anticoagulans wordt beperkt.Klinische studies ter evaluatie van laagmoleculaire heparine voor de behandeling van Kankergeassocieerde VTE
het langdurig gebruik van laagmoleculaire heparine (LMWH) voor de behandeling van VTE bij patiënten met actieve kanker wordt aanbevolen als eerstelijnstherapie op basis van de resultaten van meerdere open-label gerandomiseerde gecontroleerde studies (RCT ‘ s).6,7 in de twee grootste studies die tot op heden zijn gepubliceerd, de CLOT (Comparison of Low-molecular-weight heparine versus orale anticoagulant therapie voor de preventie van recidiverende veneuze trombo-embolie bij patiënten met kanker) en CATCH (Comparison of Acute Treatments in Cancer hemostase) studies, werd een LMWH vergeleken met een vitamine K-antagonist therapie bij patiënten met actieve kanker en acute symptomatische proximale DVT of PE. Zie Tabel 1 Voor uitgangskenmerken en Tabel 2 voor studieresultaten.In beide onderzoeken werd een open-label studieopzet gebruikt, dezelfde target international normalized ratio (INR) in de controlearm met vitamine K-antagonisten, dezelfde actieve kankerdefinitie en dezelfde duur van de behandeling en er waren vergelijkbare criteria voor de geschiktheid van de patiënt.
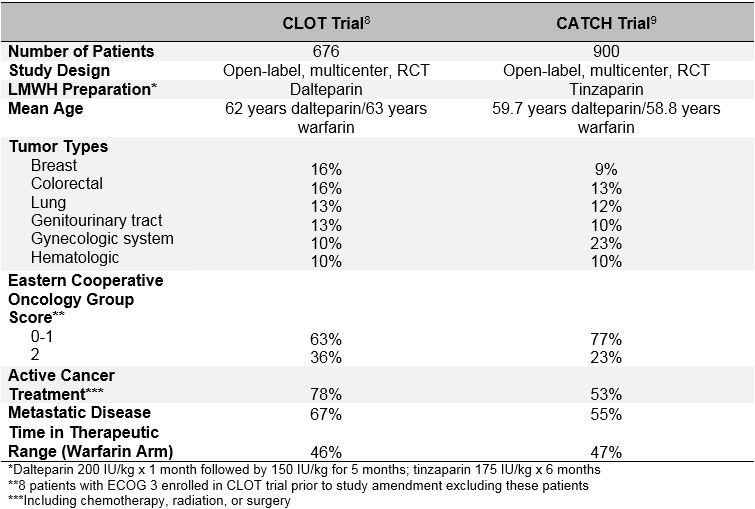
Tabel 1: onderzoeksopzet en Baseline kenmerken van de CATCH and CLOT Trials
Tabel 2: Resultaten in de studies CLOT en CATCH

in het STOLSELONDERZOEK, gepubliceerd in 2003, werden 676 patiënten gerandomiseerd naar dalteparine (200 IE / kg dagelijks gedurende 1 maand gevolgd door 150 IE / kg dagelijks gedurende 5 maanden) of vitamine-K-antagonist (warfarine of acenocoumarol met target INR 2,5 voor een totaal van 6 maanden met een initiële overlapping van 5-7 dagen met dalteparine 200 IE/kg).Symptomatische recidiverende DVT of PE, inclusief overlijden gerelateerd aan PE, werd waargenomen bij 27 patiënten (7,0%) gerandomiseerd naar dalteparine en bij 53 patiënten (15%) gerandomiseerd naar vitamine K-antagonist (hazard ratio 0,48; 95% betrouwbaarheidsinterval, 0,30-0,77; p = 0,002). Er werden tussen de 2 groepen geen verschillen waargenomen in het aantal ernstige bloedingen (6 vs.4%; p = 0,27), enige bloeding (15 VS. 19%; p = 0,09), of overlijden (39 VS. 41%; p = 0,53).
in het CATCH-onderzoek, dat meer dan 10 jaar later in 2015 werd gepubliceerd, werden 900 patiënten gerandomiseerd naar tinzaparine (175 IE/kg per dag zonder dosisverlaging) of warfarine (target INR 2,0-3,0 met initiële tinzaparine 175 IE/kg overlapping gedurende 5-10 dagen) gedurende in totaal 6 maanden.Het primaire samengestelde eindpunt van recidiverende VTE inclusief incidentele proximale DVT en PE kwam voor bij 31 patiënten (6,9%) in de tinzaparinegroep en 45 patiënten (10%) in de warfarinegroep (HR 0,65; 95% BI, 0,41-1,03; p = 0,07). Symptomatische DVT trad op bij significant minder patiënten behandeld met tinzaparine (2,7 vs.5,3%; HR 0,48; 95% BI, 0,24-0,96; p = 0,04). Hoewel het aantal ernstige bloedingen in beide armen vergelijkbaar was, werd een significante afname in klinisch relevante, niet-ernstige bloedingen waargenomen met tinzaparine (10,9 vs.15,3%; HR 0,58; 95% BI, 0,40-0,84; p = 0,004). De mortaliteit was vergelijkbaar in beide groepen, waarbij ongeveer een derde van de patiënten stierf tijdens de studieperiode (33,4 vs.30,6%; p = 0,54). Hoewel tinzaparine het primaire samengestelde eindpunt van recidiverende VTE niet significant verminderde, ondersteunen de resultaten van de CATCH-studie het gebruik van langdurige LMWH als de voorkeursbehandeling voor kankergeassocieerde VTE vanwege een lager risico op klinisch relevante ernstige bloedingen en een significante vermindering van recidiverende DVT.
het niet voldoen aan de statistische significantie van het CATCH-onderzoek voor het primaire eindpunt kan te wijten zijn aan het lager dan verwachte recidiverende VTE-percentage waargenomen in de warfarinegroep. Een mogelijke verklaring voor deze constatering zou een verbetering van de warfarinebehandeling in de VANGSTPROEF kunnen zijn. Vergelijkbare niveaus van INR-controle in beide onderzoeken pleiten hier echter tegen (tijd in therapeutisch bereik was 46% bij stolsel Versus 47% bij CATCH; tijd boven het therapeutisch bereik was 24% bij stolsel Versus 27% bij CATCH). Een meer waarschijnlijke verklaring is een vooroordeel in de selectie van “minder zieke” patiënten voor inschrijving in de CATCH trial. Hoewel in de CATCH-en STOLSELSTUDIES vergelijkbare inclusie-en uitsluitingscriteria werden gebruikt, bestaan er belangrijke verschillen in uitgangskenmerken tussen de twee patiëntenpopulaties, met name met betrekking tot trombotische en prognostische risicofactoren. Een groter deel van de patiënten in het STOLSELONDERZOEK kreeg actieve kankerbehandeling (72% stolsel vs. 53% CATCH), had een voorgeschiedenis van voorafgaande VTE (11% stolsel vs. 6% CATCH), had aanwijzingen voor gemetastaseerde ziekte (67% stolsel vs. 55% CATCH), en had een slechtere performance status (Eastern Cooperative Oncology Group score van 2 op 36% CLOT vs.23% CATCH). Daarnaast was de mortaliteit tijdens de 6 maanden durende behandelingsperiode ook hoger in de STOLPPOPULATIE (39% stolsel Versus 32% CATCH). Daarom had de CATCH-patiëntenpopulatie waarschijnlijk een lager inherent risico op recidiverende VTE in vergelijking met patiënten uit het STOLSELONDERZOEK. Het is zeer waarschijnlijk dat onderzoekers patiënten niet in CATCH hebben ingeschreven als zij van mening waren dat LMWH voordeliger zou zijn dan warfarine, wat resulteerde in de selectieve inschrijving van patiënten die minder waarschijnlijk terugkerende VTE zouden ontwikkelen.
studies ter evaluatie van directe orale anticoagulantia bij Kankergeassocieerde VTE
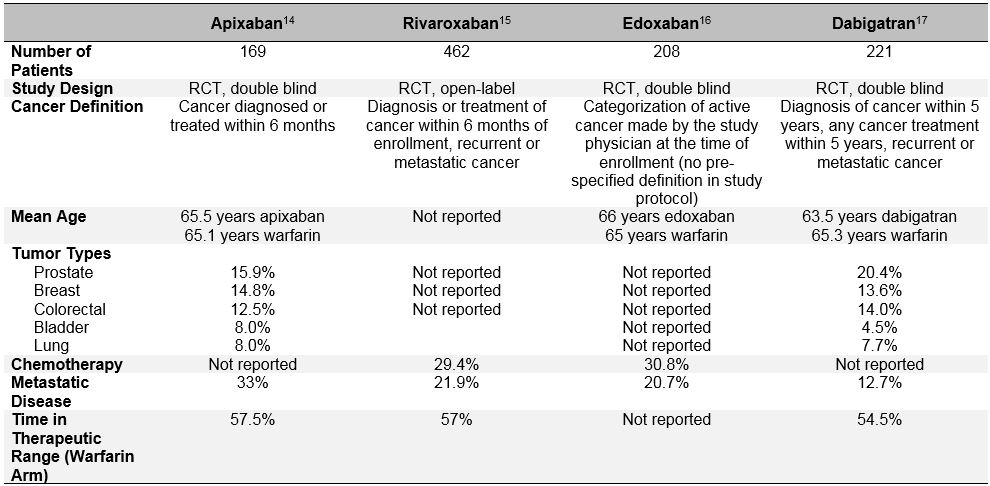
bias voor de selectie van patiënten is nog duidelijker in de recente gerandomiseerde studies ter evaluatie van de werkzaamheid en veiligheid van directe orale anticoagulantia (DOACs) voor de behandeling van acute VTE.Deze orale anticoagulantia zijn de laatste tien jaar uitgebreid bestudeerd op het gebied van atriumfibrilleren, VTE-behandeling en VTE-preventie. In de historische fase III klinische onderzoeken voor acute VTE-behandeling werd consistent aangetoond dat DOACs niet-inferieur zijn aan warfarine (gepoolde relatieve risico 0,90; 95% BI, 0,77-1.06) bij het voorkomen van recidiverende VTE, en ze hebben een vergelijkbaar of verminderd risico op ernstige bloedingen (gepoolde RR 0,40; 95% BI, 0,45-0,83).Onder de patiënten die in deze studies als “kanker” of “actieve kanker” werden geclassificeerd, lijken DOACs ook op dezelfde manier te presteren als warfarine.12 maar een meer diepgaand onderzoek van deze post-hoc gegevens onthult belangrijke voorkeur voor de selectie van patiënten en stelt de generalizability van de DOAC-studieresultaten in vraag voor” real life ” patiënten met kanker met VTE. Naast de heterogene definities van” actieve kanker ” die in deze studies werden gebruikt en die verschilden van de stolsel-en CATCH-studies, waren belangrijke determinanten van recidiverende VTE en bloedingen ook zeer verschillend bij de DOAC-patiënten met kanker van de kankerspecifieke LMWH-studies (Tabel 3). Deze omvatten de aanwezigheid van gemetastaseerde ziekte en het gelijktijdig gebruik van therapie tegen kanker. De enorme verschillen in mortaliteit tijdens de studieperiode beweren ook dat zeer verschillende groepen patiënten met “kanker” werden opgenomen in de DOAC versus LMWH studies. Bovendien, in tegenstelling tot LMWH, die geassocieerd is met een significante vermindering van het risico op recidiverende VTE in vergelijking met vitamine K-antagonisten (RR 0,52; 95% BI, 0,36-0.In een meta-analyse van 1.132 kankerpatiënten die deelnamen aan het EINSTEIN clinical trial program, Hokusai-VTE (Edoxaban Versus warfarine voor de behandeling van symptomatische veneuze trombo-embolie), RECOVER (werkzaamheid en veiligheid van Dabigatran in vergelijking met warfarine voor 6 maanden behandeling van Acute symptomatische veneuze trombo-embolie) en AMPLIFY (Apixaban voor de initiële behandeling van longembolie en diep-veneuze trombose als eerstelijnstherapie) RCT ‘ s (RR 0,66; 95% BI, 0,39-1.11).Al deze overwegingen dienen het niet-geselecteerde gebruik van DOACs bij patiënten met actieve kanker en acute, symptomatische VTE te waarschuwen.13
Tabel 3: onderzoeksopzet en Uitgangskenmerken van de subgroepen van patiënten met kanker uit de Fase III DOAC-onderzoeken
conclusies
alle belangrijke evidence-based consensus guidelines bevelen LMWH aan voor de initiële en langdurige behandeling van kankergeassocieerd VTE.Deze aanbeveling is gebaseerd op de observatie dat LMWH niet alleen effectiever is dan warfarine voor de preventie van recidiverende VTE, maar ook extra voordelen biedt ten opzichte van orale middelen, waaronder stabiele anticoagulatie bij patiënten met een slechte orale inname, een gebrek aan geneesmiddelinteracties en klinische ervaring in de behandeling van anticoagulatie rondom invasieve procedures en trombocytopenie. Hoewel DOAC ’s momenteel niet worden aanbevolen voor VTE-behandeling bij kankerpatiënten, zijn RCT’ s die rivaroxaban en edoxaban vergelijken met LMWH momenteel aan de gang en zullen deze helpen hun rol bij kankergeassocieerde VTE te verduidelijken.6,13
- Khorana AA, Dalal M, Lin J, Connolly GC. Incidentie en voorspellers van veneuze trombo-embolie (VTE) bij ambulante kankerpatiënten met een hoog risico die chemotherapie ondergaan in de Verenigde Staten. Cancer 2013; 119: 648-55.
- Kourlaba G, Relakis J, Mylonas C, et al. De humanistische en economische last van veneuze trombo-embolie bij kankerpatiënten: een systematische herziening. Bloedcoagul Fibrinolyse 2015; 26: 13-31.
- Kuderer NM, Ortel TL, Francis CW. Impact van veneuze trombo-embolie en anticoagulatie op kanker en overleving van kanker. J Clin Oncol 2009; 27: 4902-11.
- Khorana AA, Francis CW, Culakova E, Kuderer NM, Lyman GH. Trombo-embolie is een belangrijke doodsoorzaak bij kankerpatiënten die poliklinische chemotherapie krijgen. J Tromb Hemost 2007;5:632-4.
- Prandoni P, Lensing AW, Piccioli A, et al. Recidiverende veneuze trombo-embolie en bloedingscomplicaties tijdens antistollingsbehandeling bij patiënten met kanker en veneuze trombose. Bloed 2002; 100: 3484-8.
- Lyman GH, Bohlke K, Khorana AA, et al. Veneuze trombo-embolie profylaxe en behandeling bij patiënten met kanker: american society of clinical oncology clinical practice guideline update 2014. J Clin Oncol 2015; 33: 654-6.
- Streiff MB, Holmstrom B, Ashrani A, et al. Veneuze Trombo-Embolische Ziekte Met Kanker, Versie 1.2015. J Natl Compr Canc Netw 2015; 13: 1079-95.
- Lee AY, Levine MN, Baker RI, et al. Laagmoleculaire heparine versus een cumarine voor de preventie van recidiverend veneuze trombo-embolie bij kankerpatiënten. N Engl J Med 2003; 349: 146-53.
- Lee AY, Kamphuisen PW, Meyer G, et al. Tinzaparine vs warfarine voor de behandeling van Acute veneuze trombo-embolie bij patiënten met actieve kanker: een gerandomiseerde klinische studie. JAMA 2015; 314: 677-86.
- Carrier M, Cameron C, Delluc A, Castellucci L, Khorana AA, Lee AY. Werkzaamheid en veiligheid van antistollingstherapie voor de behandeling van acute kankergerelateerde trombose: een systematische beoordeling en meta-analyse. Trombb Res 2014; 134: 1214-9.
- van Es N, Coppens M, Schulman s, Middeldorp s, Büller HR. directe orale anticoagulantia vergeleken met vitamine K-antagonisten voor acute veneuze trombo-embolie: bewijs uit fase 3-onderzoeken. Blood 2014; 124: 1968-75.
- Vedovati MC, Germini F, Agnelli G, Becattini C. Direct oral anticoagulantia in patients with VTE and cancer: a systematic review and meta-analysis. Chest 2015; 147: 475-83.
- Kearon C, Akl EA, Ornelas J, et al. Antitrombotische therapie voor de ziekte van VTE: Borst richtlijn en deskundigenpanel rapport. Chest 2016; 149: 315-52.
- Agnelli G, Büller HR, Cohen A, et al. Orale apixaban voor de behandeling van veneuze trombo-embolie bij kankerpatiënten: resultaten van het AMPLIFY-onderzoek. J Trombh Hemost 2015; 13: 2187-91.
- Prins MH, Lensing AW, Brighton TA, et al. Orale rivaroxaban versus enoxaparine met vitamine K-antagonist voor de behandeling van symptomatische veneuze trombo-embolie bij kankerpatiënten (EINSTEIN-DVT en EINSTEIN-PE): een gepoolde subgroepanalyse van twee gerandomiseerde gecontroleerde onderzoeken. Lancet Haematol 2014; 1: e37-46.
- Raskob GE, Van Es N, Segers A, et al. Edoxaban voor veneuze trombo-embolie bij patiënten met kanker: resultaten van een non-inferioriteits-subgroepanalyse van het gerandomiseerde, dubbelblinde, dubbel-dummy Hokusai-VTE-onderzoek. Lancet Haematol 2016; 3: e379-87.
- Schulman s, Goldhaber SZ, Kearon C, et al. Behandeling met dabigatran of warfarine bij patiënten met veneuze trombo-embolie en kanker. Tromb Hemost 2015; 114: 150-7.
klinische onderwerpen: Anticoagulation Management, Arrhythmias and Clinical EP, Cardio-Oncology, Pulmonary Hypertension and Venous Thromboembolism, Anticoagulation Management and Atrial Fibrillation, Anticoagulation Management and Venothromboembolism, Atrial Fibrillation/Supraventricular Arrhythmias
Keywords: Cardiotoxinen, cardiotoxiciteit, heparine, laag moleculair gewicht, warfarine, anticoagulantia, International Normalized Ratio, Acenocoumarol, dalteparine, Antitrombines, veneuze trombo-embolie, risicofactoren, atriumfibrilleren, poliklinische patiënten, onderzoekspersoneel, kwaliteit van leven, Pyridonen, Pyrazolen, Pyridines, Thiazolen, veneuze trombose, longembolie, trombose, trombocytopenie, comorbiditeit, hemostase, neoplasmata
<