plaveiselcelcarcinoom van het hoofd-halsgebied (SCCHN) is het zesde meest voorkomende neoplasma wereldwijd met jaarlijks ongeveer 600.000 gediagnosticeerde gevallen. De afgelopen 20 jaar hebben een schat aan klinische proefgegevens opgeleverd en dit heeft de normen van zorg voor de behandeling van SCCHN getransformeerd. Historisch gezien hebben slechte lokale ziektecontrole en algehele overleving een impuls gegeven aan een veelheid aan klinische studies die multimodaliteitstherapie bij patiënten met SCCHN evalueerden. De ingewikkelde anatomie en de kritische functionele en sociale rollen van het hoofd-halsgebied hebben zonder twijfel ook belangrijke inspanningen gemotiveerd om alternatieven voor oncologische resectie van kwaadaardige tumoren in dit gebied te identificeren. In dit overzicht vatten we de historische ontwikkeling van gecombineerde chemoradiatietherapie in de behandeling van SCCHN samen, geven we een update van recente literatuur op dit gebied, en bespreken we hedendaagse klinische vragen die toekomstige studies kunnen oplossen.
gelijktijdige Chemoradiatie-van experimentele naar voorkeursbehandeling
klinisch onderzoek naar de rol van gecombineerde chemoradiatiebehandeling voor SCCHN dateert van ten minste eind jaren 1960, met vroege studies waarin sequentieel en gelijktijdig gebruik van enkelvoudige middelen, waaronder fluorouracil (5FU), bleomycine, cisplatine, methotrexaat en mitomycine, werd onderzocht.1 dergelijke studies toonden een slechte respons op monotherapie chemotherapie alleen aan, terwijl cisplatine als het meest effectieve monotherapie met een responspercentage van 25-30% wordt genoemd.2-4 daaropvolgende studies onderzochten de rol van multi-agens chemotherapie en toonden een duidelijke verbetering aan in de respons op de ziekte tot 70% met gecombineerd cisplatine en bleomycine5 en >90% responspercentages met cisplatine en continue infusie 5FU.6,7 belangrijk, deze vroege studies wezen op een potentieel overlevingsvoordeel van de toevoeging van chemotherapie aan traditionele definitieve behandelingen van bestraling en / of chirurgie voor SCCHN en leidden tot verder onderzoek in grotere gerandomiseerde fase III studies.
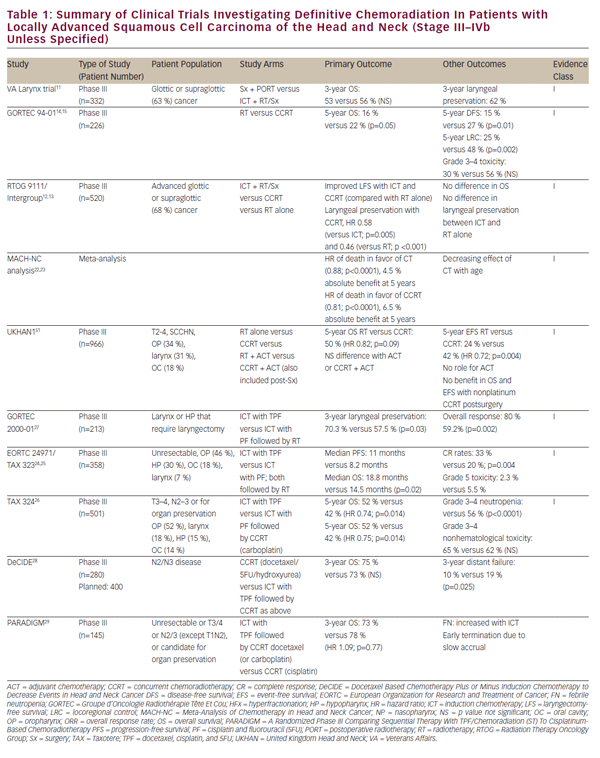
bij de verfijning van chemotherapeutische regimes werd gekeken naar het potentieel voor definitieve en orgaansparende chemoradiatiebenaderingen bij patiënten met lokaal gevorderd SCCHN. Dit werk werd aanvankelijk bevorderd door een reeks studies van één instelling die de levensvatbaarheid van definitieve chemoradiatie als alternatief voor chirurgie voor glottic en supraglottic laryngeal tumors aantonen.8-10 de historisch belangrijke Veteran Affairs Laryngeal Cancer studie toonde uiteindelijk aan dat inductie chemotherapie (ICT) gevolgd door bestraling orgaanbehoud kon bereiken bij SCCHN patiënten zonder compromis in de totale overleving.In dit onderzoek werd een grondgedachte vastgesteld voor het landmark Radiation Therapy Oncology Group (RTOG) 9111-onderzoek, waarin de juiste sequencing van chemotherapie en bestraling werd behandeld bij patiënten met lokaal gevorderde supraglottische of glottische strottenhoofd kanker. Patiënten werden gerandomiseerd naar: ICT gevolgd door straling; gelijktijdige chemoradiatie (CCRT); of straling alleen.De resultaten van RTOG 9111 toonden superioriteit aan van CCRT in termen van locoregionale ziektebestrijding en larynxbehoud, terwijl er geen verschil werd waargenomen in totale overleving tussen de drie armen. Vervolgens werd in het onderzoek Groupe d ‘ oncologie Radiothérapie Tête Et Cou (GORTEC) 94-01 patiënten met lokaal gevorderde orofaryngeale primaire tumoren gerandomiseerd naar bestraling of CCRT met carboplatine/5FU en werd een verbeterde lokale ziektecontrole en algehele overleving aangetoond.Vergelijkbare verbeteringen in overleving en locoregionale controle zijn gemeld voor nasofaryngeale patiënten behandeld met CCRT.Een rapport van de meta-analyse van chemotherapie bij hoofd-halskanker (MACHNC) heeft een algemeen overlevingsvoordeel van 6,5% na 5 jaar met CCRT gesuggereerd, maar niet met ICT of adjuvante chemotherapie.Het effect van chemotherapie op de overleving in deze meta-analyse nam af met de leeftijd voor degenen ouder dan 50 jaar met geen aantoonbaar voordeel aangetoond in die 71 jaar of ouder. Hoewel deze studies verschillen in inclusie-en uitsluitingscriteria, klinische eindpunten en behandelingsmethoden (zie Tabel 1), bevestigen zij gezamenlijk een voordeel van CCRT versus radiotherapie alleen als definitieve behandeling voor lokaal gevorderd SCCHN.
Inductiechemotherapie Voorafgaand Aan (Chemo) Bestraling – Een Haalbare Strategie?
hoewel een directe vergelijking met CCRT in de klinische studie RTOG 9111 wees op inferioriteit van ICT in termen van lokale ziektebestrijding,blijft er interesse in deze therapeutische benadering. Uit gegevens van RTOG 9111 blijkt dat deze benaderingen gelijkwaardig zijn in termen van hoogwaardige toxiciteiten, waardoor het moeilijk is om de keuze voor ICT te rechtvaardigen op grond van de tolerantie van de patiënt. Niettemin hebben follow-upstudies naar RTOG 9111 tot doel gehad het ICT-platform te ontwikkelen om van dit platform een meer haalbare behandelingsoptie te maken. De EORTC 24971/TA x 323 studie24, 25 toonde een verbeterde algehele overleving met de toevoeging van docetaxel (TPF) aan het cisplatine en 5FU (PF) ICT regime gebruikt in de RTOG 9111 studie bij patiënten met inoperabel SCCHN. In het TA X 324-onderzoek werd TPF vergeleken met PF in de setting van CCRT en het vervangen van cisplatine door wekelijks carboplatine in deze regimes. Deze studie toonde een verbeterde locoregionale en verre ziektecontrole aan evenals een verbeterde algehele overleving met TPF vergeleken met PF.Een aanvullend vervolgonderzoek (GORTEC 2000-01) naar lokaal gevorderd laryngeaal en hypofaryngeaal kanker bevestigde een verbeterde respons op de ziekte en het behoud van het strottenhoofd met inductie TPF in vergelijking met PF, maar toonde geen enkel effect op de overleving aan.Hoewel deze studies verschillen in termen van inclusie-en uitsluitingscriteria, klinische eindpunten en behandelingsmethoden (zie Tabel 1), ondersteunen zij gezamenlijk de superioriteit van TPF ten opzichte van op PF gebaseerde ICT. Niettemin ontbreekt het aan een directe vergelijking van ICT met cisplatine-gebaseerde CCRT met standaardzorg.
de MACH-NC meta-analyse, zoals eerder opgemerkt, wees op inferioriteit van ICT in vergelijking met CCRT in termen van totale overleving en locoregionale ziektebestrijding.22 Het is echter opmerkelijk dat het voordeel van ICT groter was dan dat van CCRT in termen van metastase op afstand.Dit kan wijzen op een duidelijke rol van chemotherapie in deze behandelingsbenaderingen. Gelijktijdige chemotherapie kan een overheersende radiosensibiliserende rol spelen, resulterend in een dominant effect op de lokale ziektebestrijding, terwijl multi-agent ICT een effectieve systemische behandeling voor micro-gemetastaseerde ziekte kan bieden. Deze hypothese-genererende observatie suggereert een potentieel complementaire aard van deze behandelingen en heeft geleid tot interesse in hun combinatie. Tot nu toe hebben inspanningen om de combinatie van ICT en CCRT te onderzoeken geleid tot slechte resultaten op transactiebasis en tot onduidelijke resultaten (DeCIDE-en PARADIGMASTUDIES).Een lopende gerandomiseerde fase III-studie vergelijkt ICT met PF of TPF gevolgd door cisplatine-gebaseerde CCRT versus ccrt alleen als eerstelijnsbehandeling voor lokaal gevorderd SCCHN (NCT00261703). De resultaten van bovenstaande studies over CCRT en ICT zijn ook samengevat in Tabel 1.
adjuvante Chemoradiatie
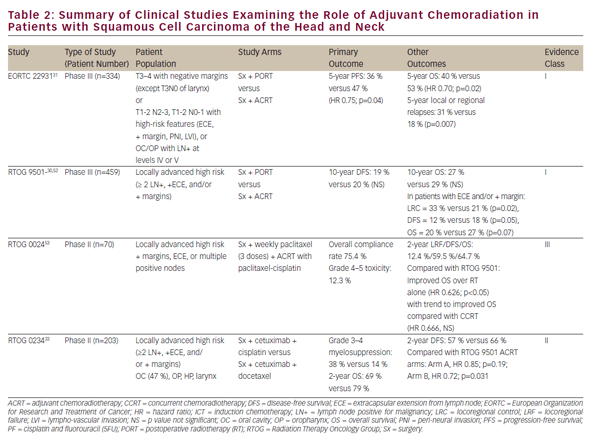
in bovengenoemde klinische studies is ccrt vastgesteld als een levensvatbare definitieve behandeling voor orgaanbehoud in lokaal gevorderd SCCHN. Niettemin, definitieve oncologic resectie blijft een belangrijke behandelingsoptie voor gelokaliseerde ziekte en een essentieel onderdeel van multimodaliteitstherapie voor geavanceerde tumoren van de mondholte, strottenhoofd, en hypopharynx. De rol van chemoradiatie in de adjuvante setting na oncologische resectie is grotendeels gedefinieerd in twee gerandomiseerde fase III— onderzoeken-EORTC 22931 en RTOG 950130,31 (zie Tabel 2). In deze studies werd het gebruik onderzocht van postoperatieve bestraling versus adjuvante chemoradiatie met cisplatine, toegediend om de 3 weken gedurende drie cycli bij postoperatieve SCCHN-patiënten. Beide studies toonden verbetering in locoregionale ziektecontrole en progressievrije overleving aan, terwijl de EORTC-studie ook een verbetering in algehele overleving liet zien. Een post-hoc analyse van deze twee onderzoeken suggereerde dat het voordeel van adjuvante CCRT het grootst was bij patiënten met positieve chirurgische marges en/ of extracapsulaire extensie (ECE) van geresecteerde lymfeklieren.De rol van adjuvante CCRT bij patiënten met nauwe chirurgische marges is minder duidelijk en werd ondersteund door EORTC 22931, die patiënten met ≤5 mm chirurgische marges omvatte. Aan de andere kant omvatte RTOG 9501 patiënten gebaseerd op positieve maar niet nauwe marges. Post-hoc analyse heeft geen duidelijk voordeel van CCRT gesuggereerd voor patiënten die voldoen aan de toelatingscriteria voor slechts één van deze onderzoeken.In een vergelijkbare geest is adjuvante CCRT niet voldoende onderzocht bij oudere patiënten, aangezien degenen ouder dan 70 jaar werden uitgesloten van EORTC 22931 en slechts een kleine minderheid (5%) van de patiënten in RTOG 9501 vormen.30,31
Pursuant to EORTC 22931 and RTOG 9501, adjuvant CCRT has now become standard-of-care treatment in high-risk postoperative SCCHN patients. The phase II RTOG 0234 study has explored alternative adjuvant chemoradiation treatment regimens, randomizing patients with multiple involved lymph nodes, ECE, or positive margins to the epidermal growth factor receptor (EGFR) antibody, cetuximab, plus docetaxel or cetuximab plus cisplatin. This study demonstrated an apparent survival benefit from concurrent adjuvant cetuximab and docetaxel.De resultaten van deze intrigerende fase II studie vereisen validatie in een fase III studie voorafgaand aan integratie in de klinische praktijk.
radiotherapie fractionering Impact op Chemoradiatie
in een poging om de werkzaamheid te verhogen, zijn in eerdere klinische studies alternatieve fractioneringsschema ‘ s onderzocht voor radiotherapie toediening met of zonder gelijktijdige chemotherapie bij SCCHN-patiënten. De rtog 9003 en de Deense hoofd-halskanker Groep (DAHANCA) studies toonden verbetering in locoregionale ziekte controle met versnelde of hyperfractionated radiotherapie regimes wanneer straling alleen wordt gebruikt.34,35 een daaropvolgende meta-analyse heeft zelfs een bescheiden overlevingsvoordeel van hyper-fractionering van straling gesuggereerd wanneer gebruikt als enige behandelingsmodaliteit.In de setting van gelijktijdige chemotherapie hebben de onderzoeken RTOG 0129 en GORTEC 99-02 echter geen verbetering aangetoond in het klinische resultaat bij gebruik van versnelde versus conventionele radiotherapie.37,38 Hyper-gefractioneerde CCRT, vergeleken met hyper-gefractioneerde straling alleen, resulteerde in een verbeterde locoregionale ziektebestrijding in een enkele instelling studie van Duke University en een fase III studie uit Joegoslavië, waarbij de laatste ook verbeterde algehele overleving en verre metastasisvrije overleving liet zien.Deze studies wijzen erop dat het voordeel van CCRT aanhoudt bij hyper-gefractioneerde radiotherapie. Een directe vergelijking van conventioneel gefractioneerde CCRT en hyper-gefractioneerde CCRT is tot op heden niet uitgevoerd. Het is echter opmerkelijk dat de MACH-NC-meta-analyse geen verschil in uitkomst detecteerde bij patiënten die met CCRT werden behandeld met behulp van conventionele of gewijzigde fractioneringstechnieken.22
toxiciteit-de kosten van Chemoradiatie
in overeenstemming met vele studies van één instelling die eraan vooraf gingen, gaf RTOG 9111 aan dat de voordelen van chemotherapie, ongeacht of deze sequentieel of gelijktijdig met bestraling wordt toegediend, ten koste gaan van extra toxiciteit.In de adjuvante setting toonden zowel de klinische studies EORTC 2291 als RTOG 9501 een geschatte verdubbeling van graad 3 toxiciteit bij chemoradiatie in vergelijking met straling alleen.30,31 een dergelijke trend blijft bestaan, zelfs in de setting van hyper-gefractioneerde radiotherapie.Hoewel de verwachte mate van specifieke toxiciteit, zoals bepaald op basis van historische studies, waarschijnlijk wordt overschat in het huidige tijdperk van zeer conformale radiotherapie technieken, zoals intensity gemoduleerde radiotherapie (IMRT). Twee kleine, gerandomiseerde onderzoeken hebben een significante vermindering van de incidentie en ernst van xerostomie gemeld bij gebruik van IMRT in vergelijking met conventionele driedimensionale conformale radiotherapie voor hoofd-halskanker (parotis-sparing intensity gemoduleerd versus conventionele radiotherapie in hoofd-halskanker en Tata Memorial Hospital trials).41,42 de meest recente studies waarin CCRT wordt onderzocht, maken een op IMRT gebaseerde behandeling mogelijk als een standaardbenadering in de behandeling van SCCHN. Het valt nog te bezien welke invloed IMRT zal hebben op de toxiciteitspercentages in combinatie met chemotherapie in deze grotere gerandomiseerde studies.
verbeterde radiotherapie technieken in combinatie met een toenemend belang en beschikbaarheid van ondersteunende zorg en ondersteunende diensten zoals speechswallow pathologie en tandheelkundige zorg beperken de incidentie van ernstige niet-hematologische toxiciteiten nog verder. Er wordt echter nog steeds verwacht dat de toxiciteit van CCRT hoger is dan alleen radiotherapie. Deze persistente toxiciteit weerspiegelt de klinische ‘kosten’ van het combineren van chemotherapie en bestraling. In deze context blijft het van het grootste belang dat artsen patiënten grondig evalueren om te bepalen of de potentiële voordelen van CCRT deze kosten rechtvaardigen. Het gebruik van enkelvoudige modaliteit radiotherapie gebaseerde behandelingen bij patiënten met duidelijke comorbiditeiten/lage baseline performance status of met een laag risico, vroeg stadium van de ziekte kan een redelijke benadering zijn om de therapeutische ratio te maximaliseren. Deze risico-batenanalyse wordt nog belangrijker met de komst van moleculaire gerichte agenten die een levensvatbare alternatieve optie voor gelijktijdige therapie aanbieden.
de opkomende rol van moleculair gerichte middelen
de toxiciteit van chemoradiatiebehandeling en de wens om de klinische resultaten verder te verbeteren, hebben geleid tot een groeiende belangstelling voor de rol van moleculair gerichte middelen voor de behandeling van SCCHN. EGFR is overexpressief of gemuteerd in 80-90% van de scchn tumoren en dit wordt geassocieerd met een verminderde respons op radiotherapie en slechtere klinische resultaten.43-45 in 2006, Bonner et al. gerapporteerd in een baanbrekende studie bij patiënten met lokaal gevorderd SCCHN die behandeld werden met straling alleen of straling gelijktijdig met het EGFR-antilichaam, cetuximab. Dit onderzoek toonde aan dat gelijktijdige cetuximab en straling de locoregionale ziektecontrole en de algehele overleving verhoogden zonder de vaak voorkomende toxiciteit van straling te verergeren.Dit onderzoek definieerde een rol voor gelijktijdige cetuximab en bestraling bij patiënten die geen kandidaat zijn voor cisplatine.
in vervolgstudies is getracht CCRT met gelijktijdig cetuximab te vergelijken met cisplatine. Retrospectieve en vroege fase studies verschillen in deze beoordeling en een gerandomiseerde fase III vergelijking is aan de gang in RTOG 1016. Met name in de RTOG 0522-studie werd het potentiële toegevoegde voordeel van cetuximab beoordeeld op een cisplatine-gebaseerd regime van CCRT47. Dit onderzoek toonde aan dat cetuximab, wanneer het werd toegevoegd aan standaard platina-gebaseerde CCRT, de progressievrije of algehele overleving niet verder verbeterde. In de postoperatieve setting zal RTOG 0920 adjuvante radiotherapie met of zonder cetuximab evalueren in lokaal gevorderd geresecteerd SCCHN, terwijl de fase II / III rtog 1216 studie adjuvante CCRT zal beoordelen met gelijktijdig cisplatine versus docetaxel versus docetaxel en cetuximab voor hoog-risico SCCHN.
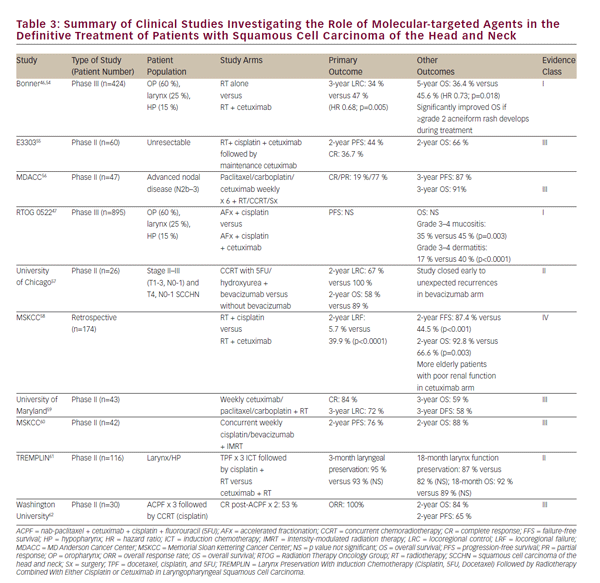
talrijke klinische onderzoeken in de vroege fase met aanvullende moleculair gerichte stoffen in combinatie met bestraling voor de behandeling van SCCHN zijn uitgevoerd of lopen nog. Een selectie hiervan is samengevat in Tabel 3 I>. Met uitzondering van studies met cetuximab, is geen enkel ander moleculair gericht middel zover gevorderd dat het de huidige praktijk beïnvloedt buiten de context van een klinische studie. Hoewel het vooruitzicht van moleculair gerichte middelen veelbelovend is, blijft gelijktijdige hoge dosis cisplatine chemotherapie de voorkeur genieten, niveau 1 aanbeveling van de huidige nationale uitgebreide zorg (NCCN) richtlijnen voor CCRT.
Chemoradiatietherapie bij hoofd—halskanker-een evoluerend paradigma
de laatste 20 jaar is chemoradiatie als standaardbehandeling voor de definitieve behandeling van SCCHN ontstaan. Bij adequaat geselecteerde patiënten weegt het aantoonbare overlevingsvoordeel van deze behandeling op tegen de risico ‘ s voor bijkomende toxiciteiten. Er blijven echter belangrijke vragen over het optimale gebruik van chemoradiatie. In een aantal klinische studies is het potentiële klinische nut van ICT bij lokaal gevorderde SCCHN-patiënten verder onderzocht en hoewel deze studies een verbetering van ICT-regimes ten koste van toxiciteit hebben aangetoond, heeft geen enkele afdoende een significante klinische verbetering aangetoond in vergelijking met cisplatine-gebaseerde CCRT.
toekomstige studies zullen ongetwijfeld alternatieve chemotherapieregimes en doseringsschema ‘ s evenals radiotherapie fractionering, dosering en toediening methoden blijven onderzoeken in een poging om bestaande technieken vooruit te helpen. Bovendien, met de verdere ontwikkeling van nieuwe moleculair gerichte chemotherapeutica, zullen toekomstige studies vrijwel zeker een ontluikende rol definiëren voor deze middelen in de behandeling van SCCHN. Bijzonder intrigerend kan het gebruik van deze middelen in een inductie setting voorafgaand aan CCRT, waar ze micrometastatische ziekte kunnen aanpakken en de terugval van de ziekte op afstand kunnen verminderen zonder toxiciteitsgerelateerde beperkingen op ccrt-voltooiingspercentages op te leggen. Hoewel het gebruik van CCRT evolueert, is verder onderzoek naar de juiste rol van chirurgie bij SCCHN ook gerechtvaardigd. De vooruitgang in zowel robotchirurgie als chemoradiation behandelingsbenaderingen verstrekt equipoise voor dergelijk onderzoek. De huidige praktijkrichtlijnen bevelen adjuvante chemoradiatie aan voor postoperatieve patiënten met positieve marges of ECE, terwijl adjuvante bestraling alleen of overweging van chemoradiatie wordt aanbevolen voor postoperatieve patiënten met een primaire pt3-of pt4 -, pN2-of pN3-nodaalziekte, lymfklierbeïnvloeding van niveau IV of V, of met Peri-neurale of lymfo-vasculaire invasie. Aanvullende studies ter identificatie van preoperatieve radiografische en klinische voorspellers van een hoog risico status bij patiënten met een vroeg stadium SCCHN zal waardevol blijken in het begeleiden van de behandeling van dergelijke patiënten die kunnen worden gespaard van een chirurgische ingreep met een up-front definitieve chemoradiatie behandeling aanpak.
de recente herkenning van infectie met het humaan papillomavirus (HPV) als een oorzaak en gunstige prognostische factor in SCCHN afkomstig van de orofarynx48 en mogelijk andere plaatsen transformeert de conceptie van SCCHN als een ziekte-entiteit. In een retrospectieve analyse van RTOG 0129 was de totale overleving na 3 jaar voor patiënten met tumoren die positief waren voor HPV 82,4% versus 57% voor HPV-negatieve ziekte (p49, 50 in het licht hiervan zullen toekomstige studies noodzakelijkerwijs gestratificeerd worden naar HPV-status of aangepast worden aan een subgroep van HPV-positieve of-negatieve patiënten,wat leidt tot een groeiend schisma in behandelingsbenaderingen. Al wordt verhoogd is het vooruitzicht van het onderzoeken van minder toxische behandeling benaderingen voor HPV-positieve tumoren en agressievere definitieve behandelingen voor HPV-negatieve tumoren om rekening te houden met sterke verschillen in hun respectieve reacties op de huidige behandeling modaliteiten. RTOG 1016 is een dergelijke studie die specifiek HPV-positieve patiënten evalueert voor de intensivering van de behandeling door gebruik van gelijktijdig cetuximab met straling versus standaard cisplatine-gebaseerde CCRT. De interactie van specifieke behandelingsregimes en Specifieke moleculair-gerichte agenten met tumor HPV-status zal ongetwijfeld vruchtbare grond blijken voor toekomstig onderzoek. Het valt nog te bezien welke impact de ontluikende HPV-epidemie en de huidige vaccinatieprogramma ‘ s zullen hebben op klinische resultaten en behandelingsbenaderingen bij patiënten met SCCHN.