Resumen
La miocardiopatía cirrótica es una afección recientemente reconocida que consiste en disfunción miocárdica manifestada en pacientes cirróticos en ausencia de enfermedad cardíaca previa. Los mecanismos patogénicos subyacentes incluyen un entorno «miocardiotóxico» que conduce a una respuesta cardíaca embotada al estrés, ya sea física o farmacológica. Esta condición ahora se comprende mejor y se puede diagnosticar con apoyo clínico, mediante criterios de electrocardiografía y ecocardiografía de laboratorio. Clínicamente, la incompetencia sistólica es más evidente cuando los pacientes cirróticos son sometidos a estrés, ya sea físico o farmacológico. A pesar de ser bien entendido, hay una falta de conocimiento para una aplicación práctica adecuada. Informes de casos recientes han sugerido que la MCC debe tratarse temprano porque puede ser un factor desencadenante de complicaciones de cirrosis. Se necesitan estudios para identificar posibles tratamientos que alteren la historia natural de la enfermedad cardíaca en pacientes cirróticos, especialmente en las fases en las que los pacientes son asintomáticos.
Palabras clave
cirrosis hepática, insuficiencia cardíaca, miocardiopatía
Introducción
La miocardiopatía cirrótica (MCC) es una disfunción cardíaca caracterizada por una respuesta contráctil subóptima al estrés y deterioro de la función diastólica en ausencia de enfermedad cardíaca previa . Hoy en día, la investigación ha propuesto que los pacientes cirróticos tienen una disfunción cardíaca intrínseca que puede influir en el desarrollo de insuficiencia renal en la enfermedad hepática avanzada .
Desde 2002, los hallazgos sobre la disfunción circulatoria en la enfermedad hepática han evolucionado a través de métodos diagnósticos, enfatizando la importancia de la identificación de la MCC en la práctica clínica . Sin embargo, todavía hay una brecha de conocimiento con respecto al manejo de esta condición . La presencia de disfunción miocárdica en la cirrosis aumenta el riesgo de síndrome hepatorrenal (HRS) y eventos cardíacos adversos y se relaciona con una mayor mortalidad .
Revisamos la literatura disponible en PubMed con respecto a los marcadores de complicaciones de cirrosis y las interacciones del corazón y el hígado. El propósito de esta revisión es discutir la necesidad de realizar un seguimiento y tratamiento tempranos de la MCC, ya que puede ser un factor desencadenante de complicaciones de cirrosis, lo que aporta nuevos conocimientos a la práctica clínica.
Definición y prevalencia
La MCC describe la disfunción cardíaca crónica en pacientes cirróticos a pesar de no tener cardiopatía estructural previa . Se define por una o más de las siguientes características: anomalías estructurales en las cámaras cardíacas; disfunción diastólica; función sistólica normal o aumentada en reposo, pero respuesta contráctil deficiente al estrés; y cambios electrofisiológicos . Estas anomalías pueden observarse hasta en el 50% de los pacientes cirróticos .
Fisiopatología
La fisiopatología de la cirrosis se conoce por la sobreproducción de óxido nítrico (NO) en los vasos esplácnicos y la consiguiente vasodilatación sistémica. Este mecanismo desencadena la activación del sistema renina-angiotensina-aldosterona (SRAA) y del sistema nervioso simpático y eleva el nivel de vasopresina sérica, lo que conduce a un estado hiperdinámico que puede repercutir desde el entorno celular hasta el clínico.
Estos pacientes tienen un aumento de monóxido de carbono (CO) sérico secundario a hiperactividad simpática y citoquinas inflamatorias. Hay un aumento del CO, asociado con altos niveles de NO, acumulación de endocannabinoides y otros vasodilatadores. Estas sustancias aumentan los niveles cíclicos de guanosina monofosfato (GMPc), lo que inhibe el monofosfato cíclico de adenosina (AMPc) en cardiomiocitos, responsable de la afluencia de calcio y de una mayor fuerza contráctil (Figura 1,2) . El análisis de células miocárdicas muestra una reducción en la fluidez de la membrana plasmática debido a la deposición de colesterol, lo que dificulta la interacción de sustancias como los receptores beta-adrenérgicos y las proteínas G. La miocita ventricular también puede tener una disminución en la función de los canales de potasio, lo que conduce a una relajación cardíaca subóptima y, consecuentemente, a una disfunción diastólica .
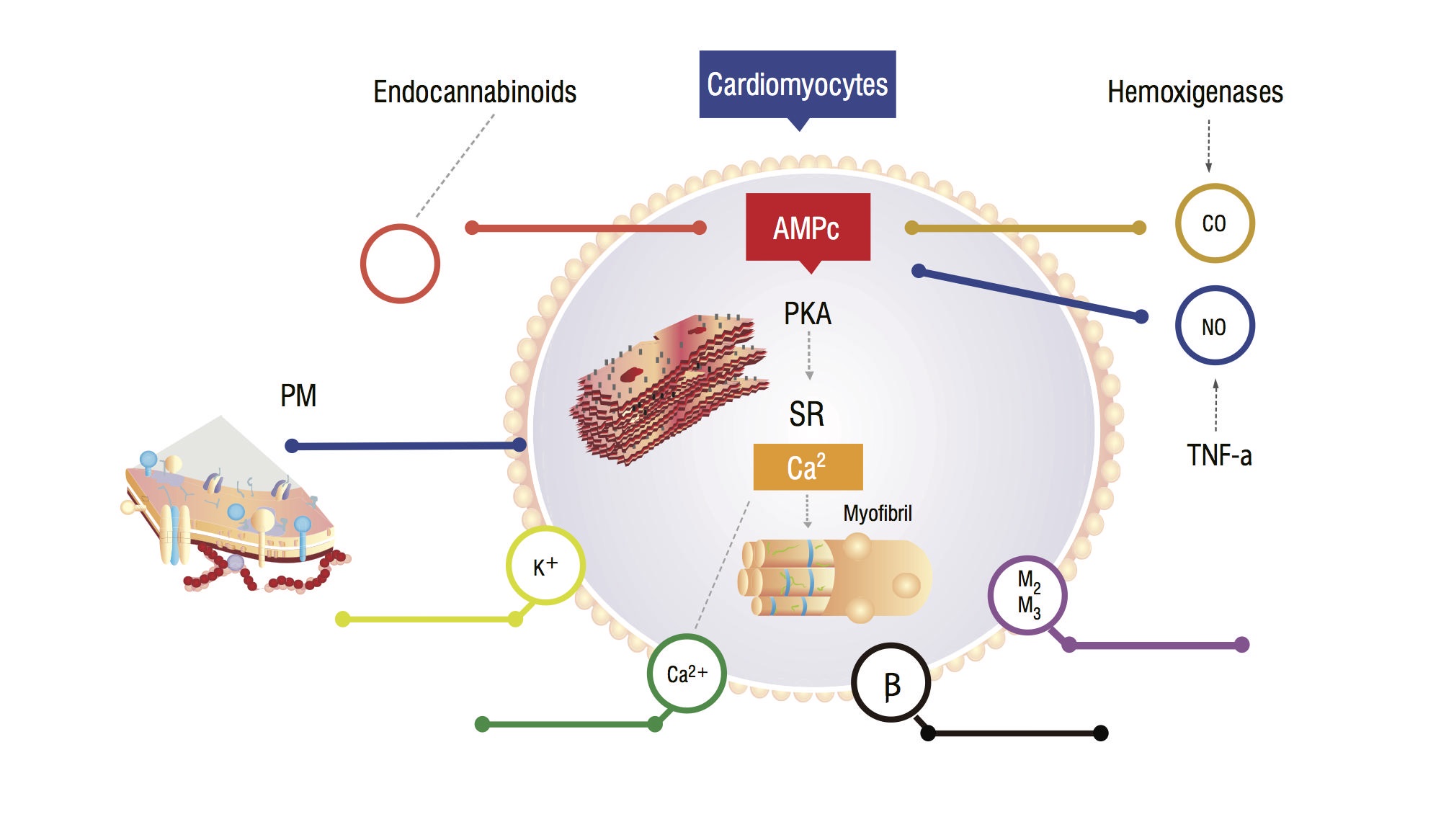
Figura 1. Modelo fisiopatológico de cardiomiocitos que muestra las principales vías de señalización que conducen a una respuesta miocárdica torpe al estrés. PM: Membrana plasmática; CO: Óxido de carbono; NO: óxido nítrico; TNF-a: Factor de necrosis tumoral alfa; SR: Retículo sarcoplasmático; AMPc: Adenosina monofosfato cíclico; PKA: Proteína quinasa A.
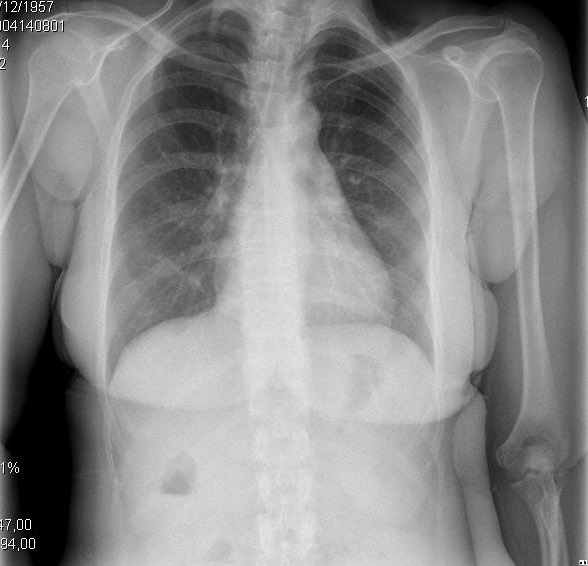
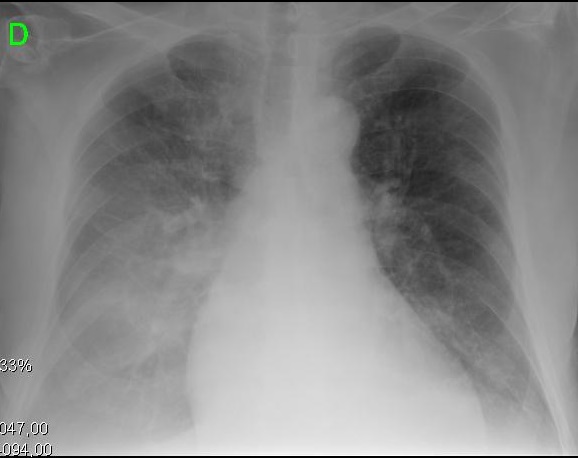
Gráfico 2 Presentaciones clínicas y radiológicas de diferentes etapas evolutivas de la miocardiopatía cirrótica. A. La imagen izquierda muestra derrame pleural pequeño e ICT de 0,50. B. La imagen derecha muestra una congestión pulmonar severa e ICT de 0,67.
Cuadro 1. Criterios clínicos y complementarios para el diagnóstico de MCC. Adaptado de de la referencia 29 con permiso.
Los estímulos beta-adrenérgicos persistentes inducen la regulación descendente y reducen la densidad de los receptores cardíacos, modificando las cascadas de señalización responsables de la activación del canal de calcio ; el resultado es una función contráctil deteriorada . La repercusión clínica de esta vía es una función miocárdica embotada y un aumento de biomarcadores cardíacos .
La identificación de la MCC se basa en características clínicas sutiles que pueden desenmascararse a medida que la enfermedad progresa, o pueden hacerse claramente evidentes en escenarios clínicos específicos de cepa, y se convierten en un desafío con respecto a si tratar y cuándo.
Historia natural y diagnóstico
Los criterios diagnósticos se resumen en la tabla 1 y se basan en marcadores clínicos, de imagen y biomarcadores.
Características clínicas
Las características clínicas de la MCC pueden ocurrir en pacientes con una función cardíaca aparentemente normal, ya que la adaptación crónica del cardiomiocito al entorno cirrótico conduce a todas esas modificaciones celulares .
Los pacientes cirróticos evolucionan con retención de sodio y líquidos, vasodilatación periférica, hiperactividad simpática y acumulación de sustancias «miocardiotóxicas», exigiendo un proceso adaptativo de cardiomiocitos. Este equilibrio continuo se puede romper y desenmascarar una insuficiencia cardíaca latente en situaciones de estrés, como un trasplante de hígado, una derivación portosistémica intrahepática transyugular o infecciones .
Aunque la miocardiopatía cirrótica tiende a ser una afección crónica, los estudios revelan que los signos clínicos de disfunción miocárdica pueden revertirse hasta 15 meses después del trasplante hepático exitoso, así como la prolongación del intervalo QT .
Hallazgos de laboratorio
Dado que la disfunción cardíaca puede reflejarse en biomarcadores inflamatorios, recientemente se están estudiando marcadores cardiacos y proinflamatorios nuevos que se correlacionan con el desarrollo de complicaciones que conducen a un aumento de la mortalidad .
Estudios recientes describen la correlación entre los niveles de pro-hormona de ANP (proANP) y péptido natriurético de tipo B (BNP), copeptina y troponina T de alta sensibilidad (TnT-hs), así como el receptor activador del plasminógeno de tipo uroquinasa soluble (suPAR) y la proteína C reactiva de alta sensibilidad (PCR-hs) y las complicaciones cardiovasculares en cirrosis. Sin embargo, todavía se está evaluando su uso clínico .
El péptido natriurético es secretado por los cardiomiocitos en respuesta a la sobrecarga de volumen o presión, o isquemia miocárdica, para compensar el efecto del SRAA en el equilibrio de sodio y agua . El BNP puede ser uno de los biomarcadores más disponibles que permite un reconocimiento temprano de la afectación cardíaca . Su concentración sérica es mayor cuanto más graves son las enfermedades hepáticas y cardíacas .
Estudios prometedores indican que también se observan niveles altos de adrenomedulina en cirrosis con o sin afectación cardíaca clínica; esta sustancia se libera en el flujo sanguíneo para actuar como vasodilatador y tiene como objetivo reducir la poscarga . Galectina-3, el biomarcador más reciente estudiado elevado en pacientes cirróticos, se ha asociado con fibrosis miocárdica y puede correlacionarse con la gravedad de la cirrosis. Este marcador está demostrando ser más sensible que el BNP en la evaluación de la disfunción diastólica, aunque es menos específico .
Electrocardiograma
Las anomalías electrocardiográficas (ECG) se pueden notar precozmente en un paciente con MCC asintomática y pueden correlacionarse con arritmias ventriculares y muerte súbita . El hallazgo de ECG más frecuente es la prolongación del intervalo QT, que se puede observar en aproximadamente el 30-40% de los pacientes cirróticos, principalmente Child-Pugh B o C, independientemente de la etiología de la cirrosis .
Este patrón de ECG puede ser secundario a anomalías de repolarización de cardiomiocitos en canales de potasio y reducción de la concentración de estos canales en la membrana plasmática, en respuesta a modificaciones menores de la presión portal . Las disfunciones de los canales iónicos, por lo tanto, causan una prolongación del potencial de acción de las células miocárdicas, lo que resulta en una sístole ventricular y un QT más largos . Un tiempo de contracción más largo implica una relajación disminuida, causando disfunción diastólica .
El desacoplamiento electromecánico se describe como una disincronía entre el estímulo eléctrico y la respuesta mecánica sistólica del corazón, que lleva a la pérdida progresiva de la función miocárdica y a la insuficiencia cardíaca congestiva en estos pacientes1 . La incompetencia cronotrópica se caracteriza por la incapacidad del nódulo sinusal para responder a estímulos fisiológicos o farmacológicos , un hecho determinante en la fisiopatología de la MCC. Estos cambios también son secundarios a la hipertensión portal, la disfunción autonómica, la circulación hiperdinámica y la presencia de factores proinflamatorios que afectan al miocardio del paciente .
Ecocardiograma
El ecocardiograma proporciona datos relevantes sobre la función cardíaca y se utiliza como criterio diagnóstico para la miocardiopatía cirrótica .
Los principales hallazgos en estos pacientes son el agrandamiento del ventrículo izquierdo (VI) diastólico final, la reducción de la velocidad máxima y la tasa de deformidad sistólica; aumento de la presión diastólica final del ventrículo izquierdo, sin expansión adecuada de la FEVI. El agrandamiento de la aurícula izquierda (AI) de más de 34 ml/m2 puede indicar disfunción diastólica crónica y, cuando se asocia con una reducción de la masa del VI, puede indicar un peor pronóstico . La evaluación de la AI se puede realizar mediante ecocardiografía de dos dimensiones y seguimiento de manchas .
Los hallazgos comunes observados en la ecocardiografía doppler cardíaca indican alteración de la relajación miocárdica en pacientes cirróticos: disminución de la relación E/A (<1) y tiempo prolongado de desaceleración de la onda E (DT) y tiempo de relajación isovolumétrica (IVRT) > 80 ms .Cuanto más severa es la disfunción diastólica, más corta es la TRIV y la TD mitral, y mayor es la relación de velocidad E/A, caracterizando la disfunción diastólica avanzada, el aumento de la presión de AI y la peor clase funcional.
Estudios recientes con evaluación de strain longitudinal global (GLS) muestran que este puede ser un método útil para la detección temprana de la disfunción cardíaca en el paciente cirrótico, principalmente la disfunción sistólica en reposo .
La relación E/A puede ser un parámetro confiable en el diagnóstico de disfunción diastólica en pacientes cirróticos, incluso con valores influenciados por el grado de hidratación del paciente, aunque puede variar debido a ascitis y sobrecarga de volumen . Mientras tanto, el tiempo de relajación isovolumétrico, aunque altamente sensible, no representa el llenado del VI y varía a medida que cambia la frecuencia cardíaca .
Una disfunción sistólica leve y una disfunción diastólica pueden presentarse independientemente del grado de cirrosis. Sin embargo, la disfunción diastólica se encuentra más comúnmente en pacientes cirróticos y generalmente precede a la primera .
Discusión
Esta revisión aborda una creciente identificación y comprensión de la fisiopatología en la MCC, su correlación con el mal pronóstico en pacientes cirróticos y surge la preocupación sobre el abordaje terapéutico.
Este artículo resume los criterios diagnósticos (Tabla 1) ya establecidos en la literatura médica, con énfasis en los nuevos biomarcadores que se han estudiado para la complementación diagnóstica. Los estudios han demostrado que la disfunción miocárdica existe en varias etapas de la cirrosis hepática. Se ha descrito que si el paciente tiene BNP alto y disfunción ventricular en el ecocardiograma, el tratamiento de la insuficiencia renal es muy difícil; por otro lado, la intervención temprana en pacientes que aún no tienen enfermedad cardíaca establecida es un área que aún no se ha explorado.
Cuadro 1. Criterios clínicos y complementarios para el diagnóstico de MCC. Adaptado de de la referencia 29 con permiso.
Características clínicas
Sin síntomas cardiopulmonares en reposo
Baja reserva cardíaca funcional
Estado hiperadrenérgico con retención de sodio y líquidos
Biomarcadores (troponina I, pro-BNP y BNP, otros)
Eletrocardiografía
Anomalías electrofisiológicas (prolongación del intervalo QT y otras)
Criterios ecocardiográficos
Evaluación diastólica
Relación E/A < 1.0 (edad corregida)
Tiempo de relajación isovolúmica prolongado (> 80mseg)
Tiempo de desaceleración prolongado (> 200mseg)
Hipertrofia ventricular izquierda
Evaluación sistólica
Fracción de eyección en reposo < 55%
Déficit contráctil en el estrés
Los signos y síntomas de la insuficiencia hepática tienden a ser tardíos, con sutiles manifestaciones clínicas y de laboratorio, a veces difíciles de interpretar. El especialista, o incluso el médico general, puede enfrentarse a un paciente con queja de disnea, sin inflamación yugular patológica, exámenes cardiológicos iniciales normales, pero con BNP alto, lo que puede representar un caso de MCC.
A diferencia de otros estudios, nuestro grupo propone un avance en este campo, ya que la comprensión de la cardiopatía concomitante con cirrosis puede permitir una intervención terapéutica temprana de las complicaciones atribuibles a la insuficiencia miocárdica no diagnosticada. El trasplante hepático y las propinas son entornos clínicos especiales que pueden deflagrar la insuficiencia cardíaca en estos pacientes. A medida que los pacientes sobreviven más tiempo después de estos procedimientos, los médicos se enfrentarían a un empeoramiento de los parámetros cardíacos .
Creemos que la intervención terapéutica temprana en la MCC es prometedora, cuando se manifiesta por complicaciones como la HRS refractaria, antes de presentar congestión pulmonar clara atribuible a insuficiencia miocárdica. La literatura apoya que las situaciones de estrés físico o farmacológico, o infecciones, asociadas a cardiomiopatía cirrótica latente pueden resultar en HRS, que puede ser refractario a los tratamientos convencionales y asociado con peor pronóstico si hay disfunción sistólica presente .
Nuestra experiencia sugiere que la presentación de HRS es una pista para iniciar el tratamiento del componente miocárdico. Esta progresión a HRS se entiende ya que la existencia de MCC es un factor desencadenante y perpetuador de la MCC, por lo que si la MCC se aborda tempranamente en este contexto, la MCC puede tener un mejor pronóstico .
Nuestro grupo ha sido pionero en el tratamiento de pacientes con diagnóstico clínico de MCC en progresión a RSH refractaria a tratamientos convencionales, en los que el uso de dobutamina como terapia de rescate para la función renal fue exitoso. El objetivo es aplicar este conocimiento teórico anticipándose a esta complicación en pacientes con enfermedad hepática terminal .
A pesar de ser bien entendido, hay una falta de conocimiento para una aplicación práctica adecuada. Se requiere un alto grado de sospecha clínica para reconocer la MCC en el paciente asintomático sin limitaciones funcionales aparentes, pero con cardiopatía celular y estructural subclínica.
Se necesitan estudios para identificar posibles tratamientos que alteren la historia natural de la cardiopatía en pacientes cirróticos, especialmente en las fases en las que los pacientes son asintomáticos. Esto representa un área de conocimiento que aún no se ha explorado, especialmente en lo que respecta a las opciones terapéuticas futuras.
Conflictos de intereses
Los autores declararon que no existen conflictos de intereses con respecto a la publicación de este artículo.
Apoyo financiero
Ninguno.
- Sampaio F, Pimenta J (2016) Evaluación de la función ventricular izquierda en cirrosis: Métodos actuales y direcciones futuras. World J Gastroenterol 22: 112-125.
- Shin WJ, Song JG, Jun IG, Moon YJ, Kwon HM, et al. (2016) Effect of ventriculoarterial coupling on transplant outcomes in cirrhotics: Analysis of pressure-volume curve relations. J Hepatol.
- Carvalheiro F, Rodrigues C, Adrego T, Viana J, Vieira H, et al. (2016) Disfunción Diastólica en Cirrosis Hepática: ¿Predictor Pronóstico en Trasplante Hepático? Transplant Proc 48: 128-31.
- Merli M, Torromeo C, Giusto M, Iacovone G, Riggio O, et al. (2016) La supervivencia a los 2 años entre los pacientes cirróticos hepáticos está influenciada por el volumen auricular izquierdo y la masa ventricular izquierda. Hígado Int.
- Møller S, Henriksen JH (2002) Cardiomiopatía cirrótica: una revisión fisiopatológica de la disfunción circulatoria en la enfermedad hepática. Corazón 87: 9-15.
- Mocarzel LO, Bicca J, Jarske L, Oliveira T, Lanzieri P, et al. (2016) Cardiomiopatía cirrótica: Otro Caso de un Enfoque Exitoso para el Tratamiento del Síndrome Hepatorrenal. Case Rep Gastroenterol 10: 531-7.
- Timoh T, Protano MA, Wagman G, Bloom M, Vittorio TJ (2011) A perspective on cirrhotic cardiomyopathy. Transplant Proc 43: 1649-1653.
- Ma Z, Lee SS (1996) Cardiomiopatía cirrótica: llegar al corazón de la materia. Hepatology 24: 451-459.
- Zardi EM, Abbate A, Zardi DM, Dobrina A, Margiotta D, et al. (2010) Cardiomiopatía cirrótica. J Am Coll Cardiol 56: 539-549.
- Myers RP, Lee SS (2000) Cardiomiopatía cirrótica y trasplante de hígado. Transpl 6 hepático: S44-52.
- Wiese S, Mortensen C, Gøtze JP, Christensen E, Andersen O, et al. (2014) Los marcadores cardiacos y proinflamatorios predicen el pronóstico en la cirrosis. Hígado Int 34: e19-30.
- Fattouh AM, El-Shabrawi MH, Mahmoud EH, Ahmed WO (2016) Evaluation of cardiac functions of cirrhotic children using serum brain natriuretic peptide and tissue Doppler imaging. Ann Pediatr Cardiol 9: 22-8.
- Rahman S, Mallett S V (2015) ¿Miocardiopatía cirrótica?: Implications for the perioperative management of liver transplant patients 7: 507-20.
- Farr M, Schulze PC (2015) Avances Recientes en el Diagnóstico y Manejo de la Cardiomiopatía Asociada a Cirrosis en Candidatos a Trasplante Hepático: Ecografía Avanzada, Biomarcadores Cardíacos y Terapia Avanzada de Insuficiencia Cardíaca. Clin Med Insights Cardiol 8: 67-74.
- Licata A, Corrao S, Petta S, Genco C, Cardillo M, et al. (2013) El nivel plasmático y el volumen auricular de NT pro BNP están relacionados con la gravedad de la cirrosis hepática. PLoS One 8: e68364.
- Abbas WA, Kasem Ahmed SM, Abdel Aal AM, Mahmoud AA, Abdelmalek MO, Mekky MA, et al. Galactina-3 y péptido natriurético cerebral versus ecocardiografía convencional en la detección temprana de miocardiopatía cirrótica. Turk J Gastroenterol 27: 367-74.
- Wong F, Siu S, Liu P, Blendis LM (2001) Péptido natriurético cerebral: ¿es un predictor de miocardiopatía en cirrosis? Clin Sci (Lond) 101: 621-628.
- Miocardiopatía cirrótica de Wong F (2009). Hepatol Int 3: 294-304.
- Mimidis K, Papadopoulos V, Thomopoulos K, Tziakas D, Ritis K, et al. (2003) Prolongación del intervalo QTc en pacientes con cirrosis. Ann Gastroenterol 16: 155-8.
- Mozos I (2015) Riesgo de arritmia en cirrosis hepática. World J Hepatol 7: 662-672.
- Mocarzel LO, Bicca J, Jarske L, Oliveira T, Lanzieri P, et al. (2016) Cardiomiopatía cirrótica: Otro Caso de un Enfoque Exitoso para el Tratamiento del Síndrome Hepatorrenal. Case Rep Gastroenterol 10: 531-537.
- Batchvarov V, Camm AJ (2014) Dispersión QT: Medición e interpretación.
- Páll A, Czifra A, Vitális Z, Papp M, Paragh G, et al. (2014) Abordaje fisiopatológico y clínico de la miocardiopatía cirrótica. J Gastrointestin Liver Dis 23: 301-310.
- Castro Hevia J, Antzelevitch C, Tornés Bárzaga F, Dorantes Sánchez M, Dorticós Balea F, et al. (2006) Dispersión de Tpeak-Tend y Tpeak-Tend como factores de riesgo para taquicardia ventricular/fibrilación ventricular en pacientes con síndrome de Brugada. J Am Coll Cardiol 47 (9): 1828-34.
- Demir C, Demir M (2013) Evaluación del intervalo Tp-e y la relación Tp-e/QT en pacientes con hepatitis B crónica.Prague Med Rep 114: 239-245.
- Jewell DP (2006) Nuevos pacientes, nuevas lecciones, nuevos pensamientos en la enfermedad inflamatoria intestinal: Simposio del Congreso Mundial de Gastroenterología, Montreal, Canadá. Dis Colorrectal 8 Suppl 1(s1): 1-2.
- Gassanov N, Caglayan E, Semmo N, Massenkeil G, Er F (2014) Cardiomiopatía cirrótica: la perspectiva de un cardiólogo. World J Gastroenterol 20: 15492-15498.
- Chayanupatkul M, Liangpunsakul S (2014) Miocardiopatía cirrótica: review of pathophysiology and treatment. Hepatol Int 8: 308-315.
- Møller S, Henriksen JH, Bendtsen F (2014) Extrahepatic complications to cirrhosis and portal hypertension: haemodynamic and homeostatic aspects. World J Gastroenterol 20: 15499–517.
- Møller S, Bendtsen F (2015) Cirrhotic Multiorgan Syndrome. Dig Dis Sci 60: 3209-3225.