Nombre genérico: fosfato de clindamicina
Forma de dosificación: crema vaginal
Revisado médicamente por Drugs.com. Actualizado por última vez el 1 de marzo de 2020.
- Descripción general
- Efectos secundarios
- Dosis
- Profesional
- Interacciones
- Más
- SOLO PARA USO INTRAVAGINAL, NO PARA USO OFTÁLMICO, DÉRMICO U ORAL
- Crema Vaginal Cleocin-Farmacología clínica
- Mecanismo de acción
- Farmacocinética
- MICROBIOLOGÍA
- Mecanismo de acción
- Resistencia
- Actividad antibacteriana
- Indicaciones y uso para la Crema Vaginal Cleocin
- Contraindicaciones
- Advertencias
- Precauciones
- General
- Información para el paciente
- Interacciones medicamentosas
- Carcinogénesis, Mutagénesis, Alteración de la fertilidad
- Embarazo
- Madres lactantes
- Uso pediátrico
- Uso geriátrico
- Reacciones adversas
- Ensayos clínicos
- Sobredosis
- Dosis y administración de Crema Vaginal Cleocin
- Cómo se suministra la Crema Vaginal de Cleocin
- Ensayos clínicos
- INSTRUCCIONES DE USO
- PANEL DE VISUALIZACIÓN PRINCIPAL – Etiqueta de tubo de 40 g
- PANEL DE VISUALIZACIÓN PRINCIPAL: Caja de tubo de 40 G
- Más información sobre Cleocin Vaginal (clindamycin topical)
- Recursos para el consumidor
- Recursos profesionales
- Otras formulaciones
- Guías de tratamiento relacionadas
SOLO PARA USO INTRAVAGINAL, NO PARA USO OFTÁLMICO, DÉRMICO U ORAL
El fosfato de clindamicina es un éster soluble en agua del antibiótico semisintético producido por una sustitución 7(S)-cloro del grupo 7(R)-hidroxilo del antibiótico original lincomicina. El nombre químico del fosfato de clindamicina es metilo 7-chloro-6,7,8-trideoxy-6-(1-methyl-trans-4-propyl-L-2-pyrrolidinecarboxamido)-1-thio-L-threo-α–D-galacto-octopiranósido 2 – (dihidrogenofosfato). Tiene un peso molecular de 504,96, y la fórmula molecular es C18H34ClN2O8PS. La fórmula estructural se representa a continuación:
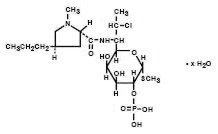
Cleocin Crema Vaginal al 2%, es una crema semisólida blanca, que contiene un 2% de fosfato de clindamicina, USP, a una concentración equivalente a 20 mg de clindamicina por gramo. El pH de la crema está entre 3,0 y 6,0. La crema también contiene alcohol bencílico, alcohol cetoestearílico, ésteres mixtos de ácidos grasos, aceite mineral, polisorbato 60, propilenglicol, agua purificada, monoestearato de sorbitano y ácido esteárico.
Cada aplicador de 5 gramos de crema vaginal contiene aproximadamente 100 mg de fosfato de clindamicina.
Crema Vaginal Cleocin-Farmacología clínica
Mecanismo de acción
La clindamicina es un medicamento antibacteriano (Consulte MICROBIOLOGÍA).
Farmacocinética
Después de administrar una dosis intravaginal de 100 mg de crema vaginal de fosfato de clindamicina al 2% una vez al día a 6 voluntarias sanas durante 7 días, aproximadamente el 5% (intervalo de 0,6% a 11%) de la dosis administrada se absorbió sistémicamente. La concentración sérica máxima de clindamicina observada en el primer día fue de un promedio de 18 ng/ml (intervalo de 4 a 47 ng/ml) y en el día 7 fue de un promedio de 25 ng/ml (intervalo de 6 a 61 ng / ml). Estas concentraciones máximas se alcanzaron aproximadamente 10 horas después de la administración (rango 4-24 horas).
Tras una dosis intravaginal de 100 mg de crema vaginal de fosfato de clindamicina al 2% administrada una vez al día durante 7 días consecutivos a 5 mujeres con vaginosis bacteriana, la absorción fue más lenta y menos variable que la observada en mujeres sanas. Aproximadamente el 5% (intervalo del 2% al 8%) de la dosis se absorbió sistémicamente. La concentración sérica máxima de clindamicina observada el primer día fue de un promedio de 13 ng/ml (intervalo de 6 a 34 ng/ml) y el día 7 fue de un promedio de 16 ng/ml (intervalo de 7 a 26 ng / ml). Estas concentraciones máximas se alcanzaron aproximadamente 14 horas después de la administración (rango 4-24 horas).
Hubo poca o ninguna acumulación sistémica de clindamicina después de la administración vaginal repetida de crema vaginal de fosfato de clindamicina al 2%. La semivida sistémica fue de 1,5 a 2,6 horas.
MICROBIOLOGÍA
Mecanismo de acción
La clindamicina inhibe la síntesis de proteínas bacterianas al unirse al ARN 23S de la subunidad 50S del ribosoma. La clindamicina es predominantemente bacteriostática. Aunque el fosfato de clindamicina es inactivo in vitro, la hidrólisis rápida in vivo lo convierte en clindamicina activa.
Resistencia
La resistencia a la clindamicina es causada con mayor frecuencia por la modificación del sitio diana en el ribosoma, generalmente por modificación química de las bases de ARN por mutaciones puntuales en ARN u ocasionalmente en proteínas. Se ha demostrado resistencia cruzada entre lincosamidas, macrólidos y estreptograminas B en algunos organismos. Se ha demostrado resistencia cruzada entre la clindamicina y la lincomicina.
Actividad antibacteriana
No se realizan rutinariamente pruebas de cultivo y sensibilidad de bacterias para establecer el diagnóstico de vaginosis bacteriana (ver INDICACIONES y USO); metodología estándar para las pruebas de sensibilidad de los patógenos bacterianos potenciales, Gardnerella vaginalis, Mobiluncus spp. o Mycoplasma hominis, no se ha definido.
Se dispone de los siguientes datos in vitro, pero se desconoce su importancia clínica. La clindamicina es activa in vitro frente a la mayoría de los aislados de los siguientes organismos que, según se ha informado, están asociados con vaginosis bacteriana:
- Bacteroides spp.
- Gardnerella vaginalis
- Mobiluncus spp.
- Mycoplasma hominis
- Peptostreptococcus spp.
Indicaciones y uso para la Crema Vaginal Cleocin
La crema Vaginal Cleocin 2%, está indicada en el tratamiento de la vaginosis bacteriana (anteriormente conocida como vaginitis por Haemophilus, vaginitis por Gardnerella, vaginitis inespecífica, vaginitis por Corynebacterium o vaginosis anaeróbica). Cleocin Crema Vaginal al 2%, se puede usar para tratar a mujeres no embarazadas y mujeres embarazadas durante el segundo y tercer trimestre. (Ver ENSAYOS CLÍNICOS.)
NOTA: Para fines de esta indicación, un diagnóstico clínico de vaginosis bacteriana se define generalmente por la presencia de un flujo vaginal homogéneo que (a) tiene un pH superior a 4,5, (b) emite un olor a amina «a pescado» cuando se mezcla con una solución de KOH al 10%, y (c) contiene células clave en el examen microscópico. Los resultados de tinción de Gram consistentes con un diagnóstico de vaginosis bacteriana incluyen (a) morfología de Lactobacilo notablemente reducida o ausente, (b) predominio del morfotipo de Gardnerella, y (c) ausencia o pocos glóbulos blancos.
Se deben descartar otros patógenos comúnmente asociados con vulvovaginitis, por ejemplo, Trichomonas vaginalis, Chlamydia trachomatis, N. gonorrhoeae, Candida albicans y virus del Herpes simple.
Contraindicaciones
Cleocin Crema vaginal al 2%, está contraindicada en personas con antecedentes de hipersensibilidad a la clindamicina, lincomicina o a cualquiera de los componentes de esta crema vaginal. Crema Vaginal Cleocin 2%, también está contraindicada en individuos con antecedentes de enteritis regional, colitis ulcerosa o antecedentes de colitis «asociada a antibióticos».
Advertencias
Se ha notificado colitis pseudomembranosa con casi todos los agentes antibacterianos, incluida la clindamicina, y su gravedad puede variar de leve a potencialmente mortal. La clindamicina administrada por vía oral y parenteral se ha asociado con colitis grave que puede terminar de forma mortal. Se ha informado de diarrea, diarrea con sangre y colitis (incluida la colitis pseudomembranosa) con el uso de clindamicina administrada por vía oral y parenteral, así como con formulaciones tópicas (dérmicas y vaginales) de clindamicina. Por lo tanto, es importante considerar este diagnóstico en pacientes que presentan diarrea posterior a la administración de clindamicina, incluso cuando se administra por vía vaginal, ya que aproximadamente el 5% de la dosis de clindamicina se absorbe sistémicamente de la vagina.
El tratamiento con agentes antibacterianos altera la flora normal del colon y puede permitir el crecimiento excesivo de clostridios.Los estudios indican que una toxina producida por Clostridium difficile es una causa primaria de colitis» asociada a antibióticos».
Una vez establecido el diagnóstico de colitis seudomembranosa, se deben iniciar medidas terapéuticas. Los casos leves de colitis pseudomembranosa generalmente responden a la interrupción del medicamento solo. En casos moderados a graves, se debe considerar el manejo con líquidos y electrolitos, la suplementación de proteínas y el tratamiento con un medicamento antibacteriano clínicamente eficaz contra la colitis por Clostridium difficile.
Pueden aparecer síntomas de colitis seudomembranosa durante o después del tratamiento antimicrobiano.
Precauciones
General
Crema Vaginal Cleocin 2%, contiene ingredientes que causarán ardor e irritación de los ojos. En caso de contacto accidental con el ojo, enjuáguelo con abundante agua fría del grifo.
El uso de Crema Vaginal Cleocin al 2% puede provocar el crecimiento excesivo de organismos no absorbibles en la vagina. En ensayos clínicos en los que participaron 600 mujeres no embarazadas que recibieron tratamiento durante 3 días, se detectó Candida albicans, sintomáticamente o mediante cultivo, en el 8,8% de las pacientes. En el 9% de los pacientes se registró vaginitis. En estudios inclinados en los que participaron 1.325 mujeres no embarazadas que recibieron tratamiento durante 7 días, se detectó Candida albicans, sintomáticamente o mediante cultivo, en el 10,5% de las pacientes. Se registró vaginitis en el 10,7% de los pacientes. En 180 mujeres embarazadas que recibieron tratamiento durante 7 días, se detectó Candida albicans, sintomáticamente o mediante cultivo, en el 13,3% de las pacientes. En el 7,2% de los pacientes se registró vaginitis. Candida albicans, como se informa aquí, incluye los términos: moniliasis vaginal y moniliasis (cuerpo como un todo). La vaginitis incluye los términos: trastorno vulvovaginal, vulvovaginitis, flujo vaginal, vaginitis tricomonal y vaginitis.
Información para el paciente
Se debe indicar a la paciente que no tenga relaciones sexuales vaginales ni utilice otros productos vaginales (como tampones o duchas vaginales) durante el tratamiento con este producto.
También se debe advertir a la paciente que esta crema contiene aceite mineral que puede debilitar los productos de látex o caucho, como los condones o los diafragmas anticonceptivos vaginales. Por lo tanto, no se recomienda el uso de dichos productos dentro de las 72 horas posteriores al tratamiento con Crema Vaginal Cleocin al 2%.
Interacciones medicamentosas
Se ha demostrado que la clindamicina sistémica tiene propiedades bloqueantes neuromusculares que pueden potenciar la acción de otros agentes bloqueantes neuromusculares. Por lo tanto, debe utilizarse con precaución en pacientes que estén recibiendo dichos agentes.
Carcinogénesis, Mutagénesis, Alteración de la fertilidad
No se han realizado estudios a largo plazo con clindamicina en animales para evaluar el potencial carcinogénico.
Las pruebas de genotoxicidad realizadas incluyeron una prueba de micronúcleos en ratas y una prueba de Ames. Ambas pruebas fueron negativas. Los estudios de fertilidad en ratas tratadas por vía oral con hasta 300 mg/kg/día (31 veces la exposición en humanos basada en mg/m2) no revelaron efectos sobre la fertilidad o la capacidad de apareamiento.
Embarazo
Efectos teratogénicos
En ensayos clínicos con mujeres embarazadas, la administración sistémica de clindamicina durante el segundo y tercer trimestre no se ha asociado con un aumento de la frecuencia de anomalías congénitas.
La crema vaginal de clindamicina se debe usar durante el primer trimestre del embarazo solo si es claramente necesario y los beneficios superan los riesgos. No hay estudios adecuados y bien controlados en mujeres embarazadas durante el primer trimestre del embarazo.
La crema vaginal de Cleocin al 2% se ha estudiado en mujeres embarazadas durante el segundo trimestre. En las mujeres tratadas durante siete días, se notificó un parto anormal en 1,1% de las pacientes que recibieron crema vaginal de clindamicina 2% en comparación con 0,5% de las pacientes que recibieron placebo.
Se han realizado estudios de reproducción en ratas y ratones utilizando dosis orales y parenterales de clindamicina de hasta 600 mg/kg/día (62 y 25 veces, respectivamente, la exposición humana máxima basada en la superficie corporal) y no se han revelado indicios de daño al feto debido a la clindamicina. Se observaron paladares hendidos en fetos de una cepa de ratón tratada intraperitonealmente con clindamicina a 200 mg / kg / día (aproximadamente 10 veces la dosis recomendada en función de las conversiones de superficie corporal). Dado que este efecto no se observó en otras cepas de ratones ni en otras especies, el efecto puede ser específico de la cepa.
Madres lactantes
Los datos publicados limitados basados en muestras de leche materna informan que la clindamicina aparece en la leche materna humana en el rango de menos de 0,5 a 3,8 mcg/ml en dosis de 150 mg por vía oral a 600 mg por vía intravenosa. Se desconoce si la clindamicina se excreta en la leche materna tras el uso de fosfato de clindamicina administrado por vía vaginal.
La clindamicina tiene el potencial de causar efectos adversos en la flora gastrointestinal del lactante. Si la clindamicina es requerida por una madre lactante, no es una razón para interrumpir la lactancia, pero se puede preferir un medicamento alternativo. Vigile al lactante en busca de posibles efectos adversos en la flora gastrointestinal, como diarrea, candidiasis (candidiasis bucal, sarpullido del pañal) o, en raras ocasiones, sangre en las heces que indique una posible colitis asociada a antibióticos.
Se deben considerar los beneficios para el desarrollo y la salud de la lactancia materna, junto con la necesidad clínica de clindamicina de la madre y cualquier posible efecto adverso de la clindamicina o de la afección materna subyacente en el lactante.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos.
Uso geriátrico
Los ensayos clínicos para Crema Vaginal de Cleocin al 2% no incluyeron un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes. Otras experiencias clínicas notificadas no han identificado diferencias en las respuestas entre los pacientes de edad avanzada y los más jóvenes.
Reacciones adversas
Ensayos clínicos
Mujeres no embarazadas
En ensayos clínicos en los que participaron mujeres no embarazadas, el 1,8% de 600 pacientes que recibieron tratamiento con Crema Vaginal Cleocin, el 2% durante 3 días y el 2,7% de 1325 pacientes que recibieron tratamiento durante 7 días interrumpieron el tratamiento debido a reacciones adversas relacionadas con el fármaco. Se notificaron eventos médicos considerados relacionados, probablemente relacionados, posiblemente relacionados o de relación desconocida con la crema vaginal de fosfato de clindamicina administrada por vía vaginal 2% en el 20,7% de las pacientes que recibieron tratamiento durante 3 días y en el 21,3% de las pacientes que recibieron tratamiento durante 7 días. Los acontecimientos que ocurrieron en ≥1% de las pacientes que recibieron crema vaginal de fosfato de clindamicina 2% se muestran en la Tabla 1.
| Evento | Cleocin Crema Vaginal | |
|---|---|---|
| 3 Día n = 600 |
7 Día n=1325 |
|
| Urogenital | ||
| Moniliasis vaginal | 7.7 | 10.4 |
| Vulvovaginitis | 6.0 | 4.4 |
| Trastorno vulvovaginal | 3.2 | 5.3 |
| Vaginitis tricomonal | 0 | 1.3 |
| Cuerpo en su Conjunto | ||
| Moniliasis (cuerpo) | 1.3 | 0.2 |
Otros acontecimientos que ocurren en < 1% de los grupos de crema vaginal de clindamicina al 2% incluyen:
Sistema urogenital: flujo vaginal, metrorragia, infección del tracto urinario, endometriosis, trastorno menstrual, vaginitis/infección vaginal y dolor vaginal.
Cuerpo en su conjunto: dolor abdominal localizado, dolor abdominal generalizado, calambres abdominales, halitosis, dolor de cabeza, infección bacteriana, hinchazón inflamatoria, reacción alérgica e infección por hongos.
Sistema digestivo: náuseas, vómitos, estreñimiento, dispepsia, flatulencia, diarrea y trastornos gastrointestinales.
Sistema endocrino: hipertiroidismo.
Sistema nervioso central: mareos y vértigo.
Sistema respiratorio: epistaxis.
Piel: prurito (en el lugar de aplicación), moniliasis, erupción cutánea, erupción maculopapular, eritema y urticaria.
sentidos Especiales: perversión del gusto.
Mujeres embarazadas
En un ensayo clínico en el que participaron mujeres embarazadas durante el segundo trimestre, el 1,7% de 180 pacientes que recibieron tratamiento durante 7 días interrumpieron el tratamiento debido a acontecimientos adversos relacionados con el fármaco. Se notificaron eventos médicos considerados relacionados, probablemente relacionados, posiblemente relacionados o de relación desconocida con la crema vaginal de fosfato de clindamicina administrada por vía vaginal 2% en el 22,8% de las pacientes embarazadas. Los acontecimientos que ocurren en ≥1% de las pacientes que recibieron crema vaginal de fosfato de clindamicina al 2% o placebo se muestran en la Tabla 2.
| Evento | CLEOCIN Crema vaginal |
Placebo |
|---|---|---|
| 7 DÍA n = 180 |
7 DÍA n=184 |
|
| Urogenital | ||
| Moniliasis vaginal | 13.3 | 7.1 |
| Trastorno vulvovaginal | 6.7 | 7.1 |
| Parto anormal | 1.1 | 0.5 |
| Cuerpo en su Conjunto | ||
| Infección fúngica | 1.7 | 0 |
| Piel | ||
| Prurito en el lugar de no aplicación | 1.1 | 0 |
Otros acontecimientos que ocurren en < 1% del grupo de crema vaginal de clindamicina 2% incluyen:
Sistema urogenital: disuria, metrorragia, dolor vaginal y vaginitis tricomonal.
Cuerpo en su conjunto: infección de las vías respiratorias superiores.
Piel: prurito (lugar de aplicación tópica) y eritema.
Experiencia postcomercialización
Dado que estas reacciones se notifican voluntariamente en una población de tamaño incierto, no siempre es posible estimar de forma fiable su frecuencia o establecer una relación causal con la exposición al medicamento.
En el período postcomercialización, se han notificado casos de colitis pseudomembranosa con el uso de crema vaginal de fosfato de clindamicina.
Otras formulaciones de clindamicina
La crema vaginal de clindamicina proporciona niveles séricos máximos mínimos y exposición sistémica (AUCs) de clindamicina en comparación con la dosis oral de 100 mg de clindamicina. Aunque es menos probable que estos niveles más bajos de exposición produzcan las reacciones comunes observadas con la clindamicina oral, la posibilidad de estas y otras reacciones no puede excluirse en la actualidad. No se dispone de datos de ensayos bien controlados que comparen directamente la clindamicina administrada por vía oral con la clindamicina administrada por vía vaginal.
Se han notificado las siguientes reacciones adversas y alteraciones de las pruebas de laboratorio con el uso oral o parenteral de la clindamicina:
Gastrointestinal: Dolor abdominal, esofagitis, náuseas, vómitos, diarrea y colitis pseudomembranosa. (Ver ADVERTENCIAS.Hematopoyético: Se han notificado neutropenia (leucopenia) transitoria, eosinofilia, agranulocitosis y trombocitopenia. En ninguno de estos informes se pudo establecer una relación etiológica directa con el tratamiento simultáneo con clindamicina.
Reacciones de hipersensibilidad: Se ha observado erupción maculopapular y urticaria durante el tratamiento farmacológico. Las erupciones cutáneas de tipo morbiliforme generalizadas de leves a moderadas son las reacciones adversas notificadas con mayor frecuencia. Casos raros de eritema multiforme, algunos parecidos al síndrome de Stevens-Johnson, se han asociado con la clindamicina. Se han notificado algunos casos de reacciones anafilactoides. Si se produce una reacción de hipersensibilidad, se debe suspender el medicamento.
Hígado: Durante el tratamiento con clindamicina se han observado ictericia y anomalías en las pruebas de la función hepática.
Musculoesquelético: Se han notificado casos raros de poliartritis.
Renal: Aunque no se ha establecido una relación directa de la clindamicina con el daño renal, en raras ocasiones se ha observado disfunción renal, evidenciada por azotemia, oliguria y/o proteinuria.
Sobredosis
La crema vaginal de fosfato de clindamicina aplicada vaginalmente al 2% podría absorberse en cantidades suficientes para producir efectos sistémicos. (Ver ADVERTENCIAS.)
Dosis y administración de Crema Vaginal Cleocin
La dosis recomendada es de un aplicador de crema vaginal de fosfato de clindamicina al 2% (5 gramos que contienen aproximadamente 100 mg de fosfato de clindamicina) por vía intravaginal, preferiblemente a la hora de acostarse, durante 3 o 7 días consecutivos en pacientes no embarazadas y durante 7 días consecutivos en pacientes embarazadas. (Ver ENSAYOS CLÍNICOS.)
Cómo se suministra la Crema Vaginal de Cleocin
La Crema Vaginal de Cleocin al 2% (crema vaginal de fosfato de clindamicina) se suministra de la siguiente manera:
tubo de 40 g (con 7 aplicadores desechables) NDC 0009-3448-01
Almacenar a temperatura ambiente controlada de 20° a 25° C (68° a 77° F) . Proteger de la congelación.
Ensayos clínicos
En dos ensayos clínicos en los que participaron 674 mujeres no embarazadas evaluables con vaginosis bacteriana, en los que se comparó la Crema Vaginal de Cleocina al 2% durante 3 ó 7 días, las tasas de curación clínica, determinadas a un mes de la terapia, oscilaron entre el 72% y el 81% para el tratamiento de 3 días y entre el 84% y el 86% para el tratamiento de 7 días.
| CLEOCIN 3 Días | CLEOCIN 7 Días | |||
|---|---|---|---|---|
| Estudio en los Estados Unidos | 94/131 | 72% | 110/128 | 86% |
| Estudio Europeo | 161/199 | 81% | 181/216 | 84% |
En un ensayo clínico en el que participaron 249 pacientes embarazadas evaluables en el segundo y tercer trimestre tratadas durante 7 días, la tasa de curación clínica, determinada al mes de tratamiento, fue del 60% (77/129) en el grupo de clindamicina y del 9% (11/120) en el grupo de brazo del vehículo. La determinación de la cura clínica se basó en la ausencia de un olor a amina» a pescado » cuando el flujo vaginal se mezcló con una solución de KOH al 10% y la ausencia de células clave en el examen microscópico.
Solo Rx
La etiqueta de este producto puede haber sido actualizada. Para obtener información completa sobre la prescripción actual, visite www.pfizer.com.

LAB-0043-12.0
Revisado 03/2020
INSTRUCCIONES DE USO
Este paquete incluye aplicadores de plástico desechables. Están diseñados para permitir la administración vaginal adecuada de la crema.
Retire la tapa del tubo de crema. Enrosque un aplicador de plástico en el extremo roscado del tubo.
Tubo rodante desde la parte inferior, apriete suavemente y fuerce el medicamento en el aplicador. El aplicador se llena cuando el émbolo alcanza su punto de parada predeterminado.
Desenrosque el aplicador del tubo y vuelva a colocar la tapa.
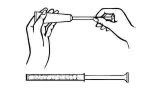
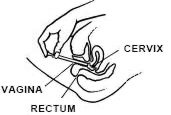
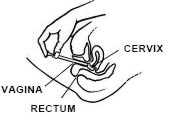
Mientras está acostado boca arriba, sujete firmemente el barril del aplicador e insértelo en la vagina en la medida de lo posible sin causar molestias.
Slowly push the plunger until it stops.
Carefully withdraw applicator from vagina, and discard applicator.
REMEMBER TO APPLY ONE APPLICATORFUL EACH NIGHT BEFORE BEDTIME, OR AS PRESCRIBED BY YOUR DOCTOR.
INSTRUCCIONES PARA LA PACIENTE
Este envase contiene aplicadores de plástico desechables. Los aplicadores están diseñados para la administración apropiada de la crema en la vagina.
Remueva la tapa del tubo de crema y enrosque el aplicador de plástico al tubo.
Exprima el tubo suavemente desde el extremo inferior y fuerce el medicamento al aplicador. El aplicador estará lleno cuando el émbolo llega a su máxima longitud.
Desenrosque el aplicador del tubo y vuelva a poner la tapa.
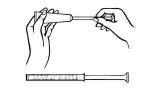
Acuéstese de espalda y agarrando firmemente el aplicador, introdúzcalo en la vagina tanto como sea posible sin causar molestias.
Empuje lentamente el émbolo hasta que se detenga.
Saque el aplicador cuidadosamente de la vagina y descártelo.
RECUERDE APLICARSE UN APLICADOR LLENO TODAS LAS NOCHES AL ACOSTARSE, O DE ACUERDO CON LAS INDICACIONES DE SU MEDICO.
LAB-1058-1.0
PANEL DE VISUALIZACIÓN PRINCIPAL – Etiqueta de tubo de 40 g
NDC 0009-3448-01
40 Gramos
Solo Rx
Cleocin®
fosfato de clindamicina
crema vaginal, USP
Para Utilizar Únicamente
2%*
PANEL DE VISUALIZACIÓN PRINCIPAL: Caja de tubo de 40 G
NDC 0009-3448-01
40 Gramos Con 7 Aplicadores
solo Rx
Cleocin®
fosfato de clindamicina
crema vaginal, USP
Solo Para uso Intravaginal
2%*
Pfizer
Distribuido por
Pharmacia & Upjohn Co
División de Pfizer Inc, NY, NY 10017
| CLEOCINA crema de fosfato de clindamicina |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Etiquetadora – Pharmacia y Upjohn Company LLC (618054084)
| Establecimiento | |||
| Nombre de | Dirección | ID/FEI | Operaciones |
| Pharmacia y Upjohn Company LLC | 618054084 | ANÁLISIS(0009-3448), la API de FABRICACIÓN(0009-3448), ETIQUETA(0009-3448), FABRICACIÓN(0009-3448), PACK(0009-3448) | |
Más información sobre Cleocin Vaginal (clindamycin topical)
- Efectos Secundarios
- Durante el embarazo o la lactancia
- Información de dosificación
- Interacciones con medicamentos
- Precios & Cupones
- Disponibilidad genérica
- Clase de medicamentos: antiinfecciosos vaginales
Recursos para el consumidor
- Lectura avanzada
Recursos profesionales
- Información de prescripción
- Crema Vaginal de Clindamicina (FDA)
Otras marcas Clindamax, Clindagel, Clindesse, Clindacin ETZ, … +4 más
Otras formulaciones
- Cleocin
- … + 4 más
Guías de tratamiento relacionadas
- Vaginitis bacteriana
Descargo de responsabilidad médica