Es wird erwartet, dass die sechsgliedrigen Ringe von Decalin, wie die von Cyclohexan, in der Stuhlform am stabilsten sind. Es gibt jedoch zwei Möglichkeiten, wie zwei Stühle verbunden werden können (Abbildung 12-21). Die Ringübergangswasserstoffe können sich entweder auf derselben Seite des Moleküls (Cis-Decalin) oder auf gegenüberliegenden Seiten (Trans-Decalin) befinden. Wenn die beiden Ringe durch zwei äquatoriale Bindungen verbunden sind, ergibt sich Trans-Decalin, während eine axial-äquatoriale Vereinigung Cis-Decalin ergibt. Beide Isomere sind bekannt, und das Trans-Isomer ist etwa \ (2 \: \ text {/ mol} ^{-1}\) stabiler als das Cis-Isomer, hauptsächlich wegen relativ ungünstiger nicht gebundener Wechselwirkungen innerhalb des konkaven Bereichs von cis-Decalin (siehe Abbildung 12-22).
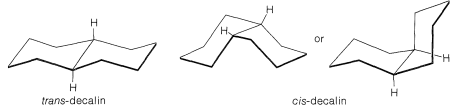
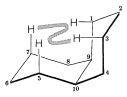
Es ist von historischem Interesse festzustellen, dass die Baeyer-Stammtheorie mit ihren planaren Ringen nur eine Form von Decalin mit den Ringübergangswasserstoffen auf derselben Seite des Moleküls vorhersagt (Abbildung 12-23). Das Sachse-Mohr-Konzept der verzogenen spannungsfreien Ringe ermöglicht zwei Isomere. Tatsächlich sagte Mohr voraus, dass die beiden Isomere von Decalin vor W existieren sollten. Hückel (1925) gelang es, sie vorzubereiten. Beide Isomere kommen im Erdöl vor.
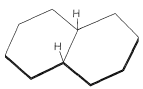
An dieser Stelle wird es wahrscheinlich hilfreich sein, Modelle von Cis- und Trans-Decalinen zu konstruieren, um Folgendes zu verstehen: (a) Die beiden Verbindungen können sich nicht miteinander verbinden, es sei denn, \(\ ce {CC}\) oder \(\ce {C-H}\) Bindungen werden zuerst gebrochen. (b) Trans-Decalin ist ein relativ starres System, und im Gegensatz zu Cyclohexan können die beiden Ringe nicht von einer Stuhlform in eine andere übergehen. Dementsprechend ist die Orientierung des Substituenten in der Stuhl-Stuhl-Konformation von Trans-Decalin festgelegt. (c) Die Stuhl-Stuhl-Formen von Cis-Decalin sind relativ flexibel, und die Inversion beider Ringe auf einmal tritt ziemlich leicht auf (die Barriere für die Inversion ist etwa \(14 \: \ text {kcal mol} ^{-1}\)). Ein Substituent kann daher zwischen axialen und äquatorialen Konformationen interkonvertieren (Abbildung 12-24).
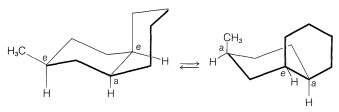
Die Auswirkungen der Konformationsanalyse von flexiblen und starren Ringsystemen sind von erheblicher Bedeutung für das Verständnis von Stabilität und Reaktivität in polyzyklischen Systemen. Dies wird in späteren Diskussionen immer deutlicher werden.
Mitwirkende und Zuschreibungen
- John D. Robert und Marjorie C. Caserio (1977) Grundprinzipien der organischen Chemie, zweite Auflage. W. A. Benjamin, Inc. In : Menlo Park, CA. ISBN 0-8053-8329-8. Dieser Inhalt ist unter den folgenden Bedingungen urheberrechtlich geschützt: „Sie erhalten die Erlaubnis zur individuellen, pädagogischen, forschungsbezogenen und nichtkommerziellen Reproduktion, Verbreitung, Anzeige und Aufführung dieser Arbeit in jedem Format.“