klíčová slova
Cytomegalovirová pneumonie; Bronchiolitisobliterans organizující pneumonii; imunokompetentní
Úvod
klinické projevy infekce cytomegalovirem (CMV)lze rozdělit na akutní primární infekce aaktivace. Primární infekce CMV se vyskytuje nejčastějiběhem kojení a dětství a je asymptomatická nebo je přítomna jako mírný syndrom podobný mononukleózěimunokompetentní dospělí . Pak virus přetrvává po celý živothostitel, obvykle v latentní fázi. Reaktivace Cmvz latence je u imunokompromitovaných pacientů dobře známa a může ovlivnit téměř jakýkoli orgán. Těžká CMV pneumonie je však u imunokompetentních hostitelů vzácná . V současné době,přesné molekulární a imunologické mechanismyinvolved jsou stále neznámé.
Bronchiolitis obliterans organizující pneumonii (BOOP) je aklinický stav charakterizovaný kašlem, malátností, horečkou adyspnoe a žádná odpověď na antibiotika . Jeho chestradiograf je popsán jako lokální, vícenásobné a difúzní změny. Může se vyskytnout u alergické alveolitidy, ozařovací pneumonitidy, lékových reakcí a dalších organizujících infekcí. Případy spojené s virovou etiologií komplikovanou přípravkem Boofy byly hlášeny sporadicky. Zde uvádíme případcmv pneumonie spojená s BOOPEM u imunokompetentního pacienta terapií ganciklovirem, což jeprvní takový případ, který byl kdy hlášen, pokud je nám známo.
kazuistika
63letý muž byl předán do naší nemocnice kvůli 10denní anamnéze kašle a horečky. Měl paroxysmální kašel se žlutým sputem. Horečka, s pískotem se objevila hlavně vobodně a v noci a nejvyšší teplota byla 39,3 (102,74). Jeho dřívější anamnéza zahrnovala hypertenzi, cukrovku a dnu. Jeho předchozí rodinná historiebyl pozoruhodný. Jeho vitální funkce byly následující: těloteplota: 36,5 (97,7), srdeční frekvence: 98 úderů za minutu(BPM), krevní tlak: 98/61 mmHg.
při fyzikálním vyšetření byly v bilaterálních dolních plicních polích zaznamenány pozdní inspirační praskání. Počet bílých krvinek(WBC) byl 14,2 × 109 / L, s 81,9% neutrofilů (NEUTR), 12,8% lymfocytů (LYR) a 0,53 × 109 / Lmonocytů (MONOR) (Obrázek 1). Hladina C-reaktivního proteinu v séru(CRP) byla 110,67 mg / L.
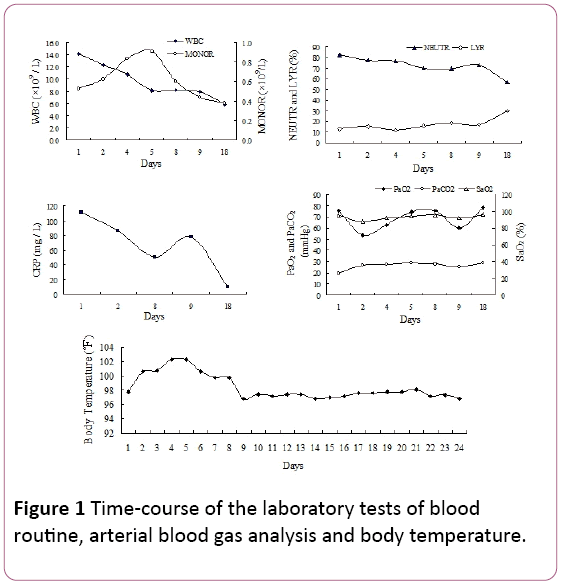
Obrázek 1: Časový průběh laboratorních testů krverutin, analýza arteriálních krevních plynů a tělesná teplota.
arteriální parciální tlak kyslíku (PaO2) byl 75,5 mmHg, s 25,8 mmHg arteriální parciální tlak CO2 (PaCO2) a 94, 7% saturace kyslíkem (SaO2, 2 L / min přívod kyslíku vianasal kanyla). Kvůli horečce a známkám respiračních infekcí jsme začali s antibiotickou léčbou piperacilinem tazobaktamem. Nicméně, pacientova teplota se nesnížila a dušnostse vyvinula v přetrvávajících 4 dnech hospitalizace.
měření arteriálních krevních plynů odhalilo selhánírespirace (PaO2: 53,5 mmHg, PaCO2: 35,6 mmHg, SaO2: 87,7%) s vyváženou metabolickou acidózou (HCO3 -: 21 mmol/ l, pH 7,39) při použití 2 L/min kyslíku nosní kanylou.Výsledky laboratorního výzkumu byly následující: protilátka mykoplazmapneumonie: 1: 40 (pozitivní), bakteriální endotoxin (celkový obsah lipopolysacharidu gramnegativních bakterií): 49,14 pg/ mL, plazmatický fibrinogen (Fg): 7,51 g/L, aktivovanýčástečný tromboplastinový čas (APTT): 45,9 sekundy.
elektrokardiogram ukázal sinusovou tachykardii se změnou Twave. Rentgen hrudníku našel dvě plicní infekce, kromě plicních intersticiálních lézí (obrázek 2A). Hrudní počítačová tomografie (CT) odhalila plicní intersticiální léze (stín mřížky v obou plicích) a zvětšení mediastinálních lymfatických uzlin (obrázek 2D). Poté byl s obličejovou maskou dodán kyslík 3,5 L/min a antibiotikaléčba byla převedena na sodnou sůl cefoperazonu asulbaktamu sodného plus levofloxacinu.
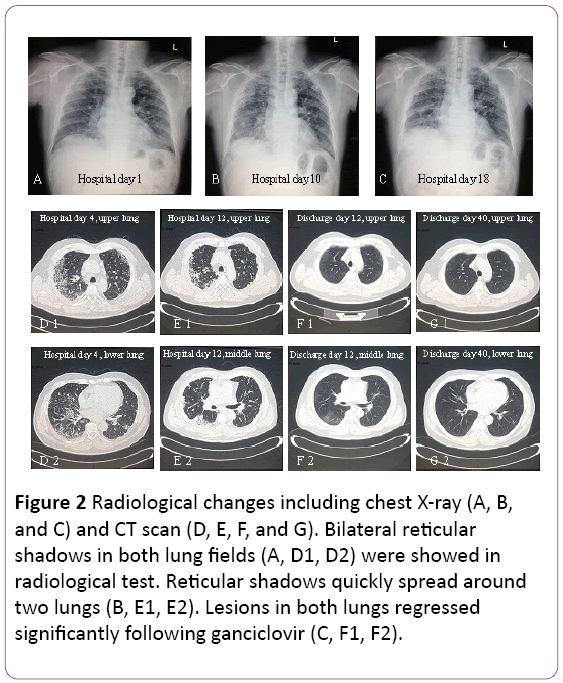
Obrázek 2: Radiologické změny včetně rentgenového vyšetření hrudníku (A ,B A C) a CT vyšetření (D, E, F A G). Bilaterální retikulárnístíny v obou plicních polích (A, D1, D2) byly prokázány vradiologický test. Retikulární stíny se rychle rozšířilydvě plíce (B, E1, E2). Léze v obou plicích ustoupilyvýrazně po gancikloviru (C, F1, F2).
vzhledem k diagnóze intersticiální pneumonie byly provedeny relevantnílaboratorní testy a fiberoptická bronchoskopie 5. den. Výsledky laboratorních testů byly následující: CMV PCR: negativní, CMV IgM: negativní, imunoglobulin IgG: pozitivní, HIV: negativní, WBC: 7,96 × 109 / L, NEUTR: 72,4%, LYR: 17%, CRP: 77,51 mg / L, imunologická funkce (T, B, NK buňky): normální, podmnožiny T-lymfocytů: normální. Markery proautoimunitní onemocnění včetně perinukleární ANCA (p-ANCA), cytoplazmatické ANCA (c-ANCA), ANA a anti-dsDNA byly všenegativní.
plicní funkce naznačovala mírnou restriktivníventilační dysfunkci. Rentgenové a CT vyšetření odhalilo lézehorní plicní byly absorbovány, ale zhoršilypravé dolní plíce (obrázek 2B a 2E).
bronchoskopie ukázala bilaterální bronchitidu (obrázek 3A).Bronchoalveolární výplach (Bal) tekutina byla negativní formycobacteria a pas skvrna. Diferenciální počet buněk byl ukázán11 % neutrofilů, 19% lymfocytů a 70% makrofágů.Byly nalezeny intranukleární a intracytoplazmatické inkluzní tělav laterálním bazálním segmentu transbronchialbiopsie plicní tkáně (TBLB) pravého dolního (obrázek 3B). Na základědiagnostika cytomegalovirové pneumonie s organizací, léčba ganciklovirem (5 mg / kg) intravenózní infuzíkaždých 12 hodin byla zahájena 8.den. Podle výše uvedenéhozjistění kombinace s klinickými příznaky (horečka zmizí) byla antibiotická léčba změněna na Moxifloxacin8. Po 1 týdnu antivirové terapie přetrvává kašel. Prošel plicní biopsií pomocí CT. Byla odhalena plicní biopsieboop (obrázek 3C). Pak pacient léčí perorálním steroidemhormon. Nicméně jeho příznaky se postupně zlepšovalynásledující 1 týden. Rentgen hrudníku odhalil, že dvě plíce byly lepší než dříve (obrázek 2C).
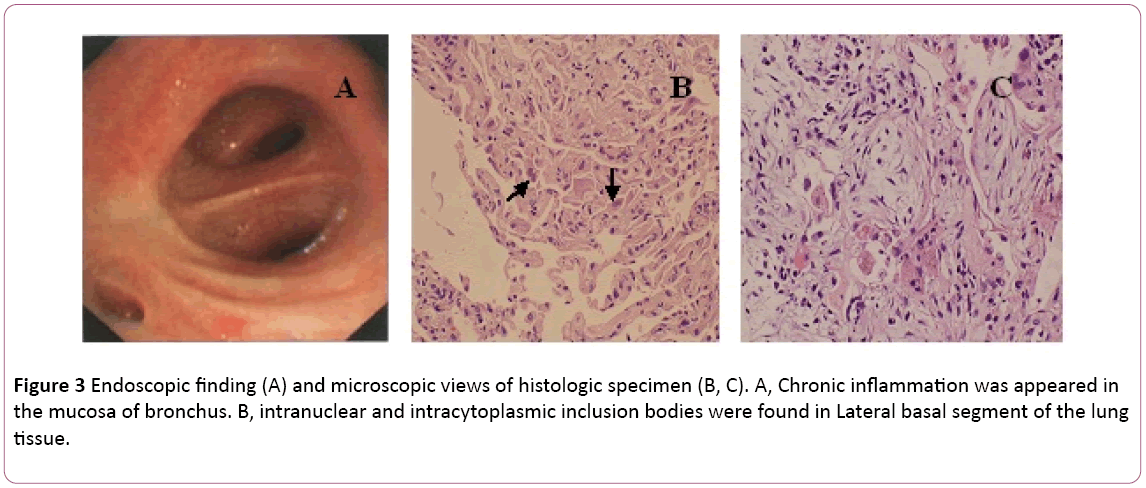
obrázek 3: Endoskopické nálezy (A) a mikroskopické pohledy na histologický vzorek (B, C). A objevil se chronický zánětsliznice průdušek. B, intranukleární a Intracytoplazmatická inkluzní těla byla nalezena v laterálním bazálním segmentu plic.
léčba byla změněna na perorální ganciklovir, 0, 6 g / d (q12h) po dobu 7 dnů, výtok. Ve svém následném sledování shadow of grid v obýchplic významně ustoupil (obrázek 2F a 2G). Na ambulanci je stále pod dohledem.
CMV je DNA virus z čeledi Herpesviridae a jeho infekce je běžná. Ve skutečnosti je 40% až 100% dospělýchinfikovaných CMV po celém světě . Infekce CMVV běžné populaci jsou obvykle subklinické. Asymptomatická infekce CMV se vyskytla hlavně uimunokompromitovaných pacientů s imunitní dysfunkcí, včetně pacientů s AIDS, malignitou,příjemci transplantátů a novorozenci . V případech s imunodeficiencí může Cmvinfekce způsobit pneumonii, retinitidu,hepatitidu, encefalitidu, demyelinizační polyneuropatii,myokarditidu, pankreatitidu,gastrointestinální onemocnění a nadledviny atd. Naopak, těžká život ohrožujícíinfekce vyvolaná CMV, včetně pneumonie CMV, je u imunokompetentních jedinců nebezpečná . V tomto článku popisujeme případ CMV pneumonie, spojené s Boopinem imunokompetentním hostitelem a účinně léčenyganciklovirem.
CMV pneumonie se často projevuje jako závažná virová pneumonie s difúzními intersticiálními infiltráty na rentgenovém snímku hrudníku arespirační selhání . Laboratorní diagnóza může býtobtížné a jsou prováděny sérologicky nebo patologicky.Obecně platí, že sérologické testy k detekci lidské infekce CMV zahrnují titr CMV protilátek (IgM, IgG), CMV proteinpp65 a CMV PCR . Důležité je histopatologickédetekce inkluz CMV na transbronchiální nebo openlung biopsii je patognomonická, protože pneumonie CMV vimunokompetentních pacientů představuje vzácnou událost .
náš pacient vykazoval nespecifické příznaky (kašel a horečka), které se vyvinuly v průběhu 10 dnů.Příznaky se zhoršily po 2 dnech v nemocnici (těžká hypoxemie), a to i přes empirickou léčbu antibiotiky. Adiagnostika CMV pneumonie byla založena na TBLB, což bylonašel intranukleární a intracytoplazmatické inkluzní tělíska vobří buňky jako zlatý standard. Navíc pozitivní protilátka CMV IgG v séru byla dalším diagnostickým indexem. Diagnostiku virové pneumonie podpořil theradiologický snímek zahrnující rentgen hrudníku a CT zobrazující bilaterální retikulární stíny v obou plicních polích. V našem případě mononukleózabyla také pozorována rutina krve (Obrázek 1). Sérum CMV však bylo v tomto případě negativní, což bylo v souladu s eddlestonovou zprávou . CMV PCR byla také negativní. Může to být vysvětleno falešně negativními výsledky vyvolanými přechodnou povahou virémie .
během hospitalizace se jeho počet lymfocytů snížilvýrazně. Lymfopenie byla způsobena infekcí CMV jak přímou inhibicí růstu progenitorových buněk, tak selhánímobnovení kmenových buněk . Je možné poznamenat, žeimunitní analýza funkcí, jako je podmnožina T buněk, B buňka a analýza NKcell, byla normální. V tomto případě nebyla pozorována přechodná nebo subklinická t buněkanormalita a inverze poměru T-buněk CD4/CD8. U onemocnění HIV pokles CD4 + buněk <100 × 106 / L představuje vysoké riziko onemocnění CMV. Kromě toho náš pacient nevykazoval žádné známky jinýchimunodeficience (HIV: negativní) a autoimunitní onemocnění (autoimunitní protilátka: negativní).
BOOP byl poprvé popsán Eplerem a kol. a od té doby byla rozsáhle zkoumána a hlášena po celém světě . Existuje mnoho infekčních agens může býtspojené s BOOP, jako je cytomegalovirus (CMV), herpesimplex virus (HSV). Byly také hlášeny parazitární a pneumocystis cariniiinfekce . Protože Boopreprezentují způsob, jakým mohou plíce reagovat na zánětlivý stimul, klíčové patofyziologické nálezy jsourelatované na zánětlivou cestu. Histologické rysyzahrnují granulační tkáň ve stěnách alveol abronchioly jsou významné, spojené s infiltrací vintersticiální a tracheální dutině různými stupněmimononukleárních buněk a pěnových buněk. Alveolární epitel typu II může být také pozorována hyperplazie buněk . V současném pacientovi byl BOOP diagnostikován v plicní biopsii o týden později než TBLB, což naznačuje, že CMV může být nejpravděpodobnějším patogenem.
ačkoli pro léčbu pacientů s CMV pneumonií není doporučeno standardní trváníléčba by mohla být zahájena až po definitivní diagnóze a běžně se podává po dobu dvou až tří týdnů. Jakmile léčba ganciklovirem, klinický stav našeho pacientabylo zlepšeno, s úplným rozlišením klinického andradiologického obrazu do jednoho měsíce sledování.
závěr
hlásíme případ akutní infekce CMV, který se projevils horečkou, kašlem, sputem a tachypnoe. Posledně jmenovanérychle se zhoršila a je spojena s respiračním selháním.CT vyšetření odhalilo malou změnu broušeného skla při nástupu, ale změna se rychle rozšířila kolem dvou plic. Po patologickém vyšetření (TBLB) byla potvrzena diagnóza Cmvpneumonie. U pacientů s poruchami noimunodeficience je velmi snadné špatně diagnostikovat.Současná zpráva naznačuje, že při zobrazování CT hrudníkuintersticiální léze, kromě zvážení tuberkulózy, bakteriální pneumonie a dalších virových onemocnění, by měla být Cmvpneumonie zahrnuta u starších pacientů s rozmanitostí základního onemocnění. Důležité je, že tento případ prokázalže cytomegalovirová pneumonie se může spojit s BOOPEM v imunokompetentním pacientovi. Léčba ganciklovirem jeúčinná. Další studie jsou nezbytné pro analýzuvztahy a jeho základní mechanismus mezi Cmvpneumonií a BOOPEM.
autorské příspěvky
CXC vypracoval a napsal rukopis. O pacientku se postaraly nemocnice, LL a LYH a přispěly k jejich koordinaci. XL provedl mikrobiologické testy. Lyhpřispěl k návrhu rukopisu a revidoval jeanuscript. Všichni autoři přečetli rukopis aschválil jeho konečnou verzi.
poděkování
jsme vděčni Prof. Zhiqiang Qin za jeho teoretické podpory.
- Hamprecht K, Maschmann J, Vochem M, Dietz K, Speer CP, et al. (2001) epidemiologie přenosu cytomegaloviru z matky na předčasně narozené dítě kojením. Lancet 357: 513-518.
- Carter D, Olchovsky D, Pokroy R, Ezra D (2006) kolitida spojená s cytomegalovirem způsobující průjem u imunokompetentního pacienta. Svět J Gastroenterol12: 6898-6899.
- Kralickova P, Mala E, Vokurkova D, Krcmova I, Pliskova L, et al. (2014)cytomegalovirové onemocnění u pacientů se společnou variabilní imunodeficiencí: tři kazuistiky. Mezinárodní archiv alergie a imunologie 163: 69-74.
- Eddleston M, Peacock S, Juniper M, Warrell DA (1997) těžká cytomegalovirová infekce u imunokompetentních pacientů. Clintonová 24: 52-56.
- Cunha BA (2010) Cytomegalovirová pneumonie: komunitní pneumonie u imunokompetentních hostitelů. Infect Dis Clin North Am 24: 147-158.
- Cohen JI, Corey GR(1991) Cytomegalovirus infection in the normal host. Medicine 1985; 64:100-114.
- Geddes DM. BOOP and COP. Thorax46:545-547.
- Hansell DM (1992) What are bronchiolitis obliterans organizing pneumonia (BOOP) and cryptogenic organizing pneumonia (COP)? ClinRadiol45:369-70.
- Cunha BA, Syed U, Mickail N(2012) Renal transplant with bronchiolitis obliterans organizing pneumonia (BOOP) attributable to tacrolimus and herpes simplex virus (HSV) pneumonia. Heart & Lung 41:310-315
- Bitzan M, Ouahed JD, Carpineta L, Bernard C, Bell LE (2010) kryptogenní organizující pneumonie po léčbě rituximabem pro předpokládané lymfoproliferativní onemocnění po transplantaci ledvin. Dětská Nefrologie 25: 1163-1167.
- de la Hoz RE, Stephens G, Sherlock C (2002) diagnostika a léčebné přístupy infekcí CMV u dospělých pacientů. Jičín 25: 1-12.
- Sanadgol N, Ramroodi N, Ahmadi GA, Komijani M, Moghtaderi A, et al.(2011) Prevalence cytomegalovirové infekce a její role v celkovém imunoglobulinovém vzoru u íránských pacientů s různými podtypy roztroušené sklerózy. New Microbiologica 34: 263-274.
- Chiotan C, Radu L, Serban R, Cornacel C, Cioboata M, et al. (2014)Cytomegalovirová retinitida u pacientů s HIV / AIDS. Žurnál medicíny a života 7: 237-240.
- Liu WL, Lai CC, Ko WC, Chen YH, Tang HJ, et al. (2011) klinické a mikrobiologické charakteristiky infekcí způsobených různými druhy Nocardie na Tchaj-wanu: multicentrická studie od roku 1998 do roku 2010. Eur J ClinMicrobiol Infect Dis30: 1341-1347.
- paprsek E, Razonable RR (2012)Cytomegalovirus při transplantaci pevných orgánů: epidemiologie, prevence a léčba. Curris 14: 633-641.
- Westman G, Berglund D, Widen J, Ingelsson M, Korsgren O, et al. (2014) zvýšená zánětlivá odpověď U cytomegalovirových séropozitivních pacientů s Alzheimerovou chorobou. PloS one9: 96779.
- Carney WP, Rubin RH, Hoffman RA, Hansen WP, Healey K, et al. (1981) analýza podmnožin T lymfocytů v mononukleóze cytomegaloviru. Jaromír Jágr 126: 2114-2116.
- Boeckh M, Leisenring W, Riddell SR, Bowden RA, Huang ML, et al. (2003) pozdní cytomegalovirové onemocnění a mortalita u příjemců alogenních transplantací hematopoetických kmenových buněk: význam virové zátěže a imunity T-buněk. Krev 101: 407-414.
- Gunthard HF, Aberg JA, Eron JJ, Hoy JF, Telenti A, et al. (2014)antiretrovirová léčba infekce HIV u dospělých: 2014 doporučení panelu mezinárodní antivirové společnosti-USA. JAMAOVÁ 312: 410-425.
- Epler GR, Colby TV, McLoud TC, Carrington CB, Gaensler EA (1985) Bronchiolitis obliterans organizující pneumonii. N Engl J Med 312:152-158.
- Kute VB, Patel MP, Patil SB, Shah PR, Vanikar AV,et al. (2013) Bronchiolitis obliterans organizing pneumonia (BOOP) after renal transplantation. IntUrolNephrol 45:1517-1521.
- White KA, Ruth-Sahd LA (2007) Bronchiolitis obliterans organizing pneumonia. Crit Care Nurse27:53-66.
- Yale SH, Adlakha A, Sebo TJ, Ryu JH(1993)Bronchiolitis obliterans organizing pneumonia caused by Plasmodium vivax malaria. Chest 104:1294-1296.
- Kleindienst R, Fend F, Prior C, Margreiter R, Vogel W(1999)Bronchiolitis obliterans organizing pneumonia associated with Pneumocystis carinii infection in a liver transplant patient receiving tacrolimus. Clin Transplant13:65-67.
- Moore SL (2003)Bronchiolitis obliterans organizing pneumonia: a late complication of stem cell transplantation. Clin J OncolNurs 7:659-662.