Holger J Schünemann, Julian PT Higgins, Gunn e Vist, Paul Glasziou, Elie A Akl, Nicole Skoetz, Gordon h Guyatt; namens de Cochrane GRADEing Methods Group (voorheen Applicability and Recommendations Methods Group) en de Cochrane Statistical Methods Group
- :
- 14.1 ‘samenvatting van bevindingen’ tabellen
- 14.1.1 Inleiding tot’ samenvatting van bevindingen’tabellen
- 14.1.2 het selecteren van resultaten voor de tabellen “samenvatting van bevindingen”
- 14.1.3 Algemene template voor de tabellen “samenvatting van bevindingen”
- 14.1.4 het opstellen van “Samenvatting van de bevindingen” tabellen
- 14.1.5 statistische overwegingen in de tabellen “samenvatting van bevindingen”
- 14.1.5.1 dichotome uitkomsten
- 14.1.5.2 uitkomsten van tijd tot gebeurtenis
- 14.1.6 gedetailleerde inhoud van een tabel “samenvatting van bevindingen”
- 14.1.6.1 titel en kop van de tabel
- 14.1.6.2 resultaten
- 14.1.6.3 beste schatting van het risico met een vergelijkingsinterventie
- 14.1.6.4 risico met interventie
- 14.1.6.5 Risicoverschil
- 14.1.6.6 relatief effect (95% BI)
- 14.1.6.7 aantal deelnemers (studies)
- 14.1.6.8 zekerheid van het bewijs (graad)
- 14.1.6.9 opmerkingen
- 14.1.6.10 toelichtingen
- 14.2 Assessing the security or quality of a body of evidence
- 14.2.1 the GRADE approach
:
- een tabel met “samenvatting van de bevindingen” voor een gegeven vergelijking van interventies levert belangrijke informatie op over de omvang van de relatieve en absolute effecten van de onderzochte interventies, de hoeveelheid beschikbaar bewijsmateriaal en de zekerheid (of kwaliteit) van beschikbaar bewijsmateriaal.
- ‘samenvatting van bevindingen’ tabellen bevatten een rij voor elk belangrijk resultaat (tot een maximum van zeven). Geaccepteerde formaten van’ Summary of findings ‘- tabellen en interactieve ‘Summary of findings’ – tabellen kunnen worden geproduceerd met behulp van GRADE ‘ s software GRADEpro GDT.Cochrane heeft de GRADE approach (Grading of Recommendations Assessment, Development and Evaluation) gebruikt om de zekerheid (of kwaliteit) van een verzameling bewijsmateriaal te beoordelen.
- de GRADENBENADERING specificeert vier niveaus van zekerheid voor een verzameling bewijsmateriaal voor een bepaald resultaat: hoog, matig, laag en zeer laag.
- Grade assessments of certainity worden bepaald aan de hand van vijf domeinen: risico van vertekening, inconsistentie, onrechtmatigheid, onnauwkeurigheid en vertekening van publicatie. Voor bewijs uit niet-gerandomiseerde studies en zelden gerandomiseerde studies, kunnen beoordelingen dan worden opgewaardeerd door overweging van drie andere domeinen.
citeer dit hoofdstuk Als: Schünemann HJ, Higgins JPT, Vist GE, Glasziou P, Akl EA, Skoetz N, Guyatt GH. Hoofdstuk 14: Het invullen van de tabellen “samenvatting van de bevindingen” en het beoordelen van de zekerheid van het bewijsmateriaal. In: Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, Page MJ, Welch VA (editors). Cochrane Handbook for Systematic Reviews of Interventions version 6.2 (bijgewerkt februari 2021). Cochrane, 2021. Beschikbaar op www.opleiding.cochrane.org/handbook.
14.1 ‘samenvatting van bevindingen’ tabellen
14.1.1 Inleiding tot’ samenvatting van bevindingen’tabellen
‘ samenvatting van bevindingen ‘ tabellen geven de belangrijkste bevindingen van een overzicht in een transparante, gestructureerde en eenvoudige tabelvorm. Zij verstrekken met name essentiële informatie over de zekerheid of de kwaliteit van het bewijsmateriaal (d.w.z. het vertrouwen of de zekerheid in het bereik van een effectschatting of een verband), de omvang van het effect van de onderzochte interventies en de som van de beschikbare gegevens over de belangrijkste resultaten. Cochrane Reviews dient tijdens de planning en publicatie tabellen ‘samenvatting van bevindingen’ te bevatten en dient ten minste één belangrijke tabel ‘samenvatting van bevindingen’ te bevatten die de belangrijkste vergelijkingen weergeeft. Sommige beoordelingen kunnen meer dan één tabel met “samenvatting van bevindingen” bevatten, bijvoorbeeld als de beoordeling betrekking heeft op meer dan één belangrijke vergelijking, of substantieel verschillende populaties omvat die afzonderlijke tabellen vereisen (bijvoorbeeld omdat de effecten verschillen of het belangrijk is om de resultaten afzonderlijk weer te geven). In de Cochrane Database of Systematic Reviews (CDSR) staat aan het begin, vóór de Background sectie, de belangrijkste ‘Summary of findings’ tabel van een review. Tussen de resultaten en het Discussiegedeelte staan andere tabellen met “samenvatting van de bevindingen”.
14.1.2 het selecteren van resultaten voor de tabellen “samenvatting van bevindingen”
het plannen van de tabel “samenvatting van bevindingen” begint vroeg in de systematische evaluatie, waarbij de selectie van de resultaten moet worden opgenomen in: i) de evaluatie; en ii) de tabel “samenvatting van bevindingen”. Dit is een cruciale stap, en een die recensie auteurs moeten zorgvuldig aanpakken.
om de productie van optimaal bruikbare informatie te garanderen, beginnen Cochrane Reviews met het ontwikkelen van een beoordelings-vraag en met een opsomming van alle belangrijke resultaten die belangrijk zijn voor patiënten en andere besluitvormers (zie hoofdstuk 2 en hoofdstuk 3). De GRADENBENADERING om de zekerheid van het bewijs te beoordelen (zie paragraaf 14.2) definieert en operationaliseert een beoordelingsproces dat helpt om de resultaten te scheiden in die welke van cruciaal belang zijn, belangrijk of niet belangrijk voor de besluitvorming. Raadpleging en feedback over het herzieningsprotocol, onder meer van consumenten en andere besluitvormers, kunnen dit proces verbeteren.
kritieke resultaten omvatten waarschijnlijk duidelijk belangrijke eindpunten; typische voorbeelden zijn mortaliteit en ernstige morbiditeit (zoals beroertes en myocardinfarct). Nochtans, kunnen zij ook frequente kleine en zeldzame belangrijke bijwerkingen, symptomen, kwaliteit van leven, lasten verbonden aan behandeling, en hulpbronkwesties (kosten) vertegenwoordigen. Lasten vertegenwoordigen de impact van de zorgbelasting op de functie en het welzijn van de patiënt, en omvatten de eisen van het vasthouden aan een interventie die patiënten of verzorgers (bijvoorbeeld familie) kunnen verafschuwen, zoals het ondergaan van meer frequente tests, of de beperkingen op levensstijl die bepaalde interventies vereisen (Spencer-Bonilla et al 2017).
bij het formuleren van vragen die alle patiëntbelangrijke uitkomsten voor de besluitvorming omvatten, zullen de auteurs van de review vaak geconfronteerd worden met rapporten van studies die niet al deze uitkomsten bevatten. Dit geldt met name voor negatieve resultaten. Randomized trials kunnen bijvoorbeeld bewijs leveren over beoogde effecten en over frequente, relatief kleine bijwerkingen, maar rapporteren niet over zeldzame nadelige resultaten zoals zelfmoordpogingen. Hoofdstuk 19 bespreekt strategieën om negatieve effecten aan te pakken. Om gegevens te verkrijgen voor alle belangrijke resultaten kan het nodig zijn de resultaten van niet-gerandomiseerde studies te onderzoeken (zie hoofdstuk 24). Cochrane heeft, in samenwerking met anderen, richtlijnen ontwikkeld voor recensie auteurs om hun beslissing te ondersteunen over wanneer te zoeken naar en omvatten niet-gerandomiseerde studies (Schünemann et al 2013).
als een review alleen gerandomiseerde trials omvat, zijn deze trials mogelijk niet op alle belangrijke resultaten gericht en is het mogelijk dat het niet mogelijk is deze resultaten binnen de beperkingen van de review aan te pakken. Recensie-auteurs moeten deze beperkingen erkennen en ze transparant maken voor lezers. De auteurs van de beoordeling worden aangemoedigd om niet-gerandomiseerde studies op te nemen om zeldzame of op lange termijn nadelige gevolgen te onderzoeken die niet adequaat in gerandomiseerde studies kunnen worden bestudeerd. Dit verhoogt de mogelijkheid dat schade-resultaten kunnen komen uit studies waarin de deelnemers verschillen van die in studies gebruikt in de analyse van de voordelen. Recensie auteurs zullen dan moeten overwegen hoeveel dergelijke verschillen waarschijnlijk van invloed zijn op de bevindingen, en dit zal van invloed zijn op de zekerheid van bewijs vanwege bezorgdheid over de onrechtmatigheid gerelateerd aan de populatie (zie paragraaf 14.2.2).
niet-gerandomiseerde onderzoeken kunnen belangrijke informatie verschaffen, niet alleen wanneer gerandomiseerde onderzoeken geen resultaat rapporteren of wanneer gerandomiseerde onderzoeken lijden aan ondirectheid, maar ook wanneer het bewijs van gerandomiseerde onderzoeken als zeer laag wordt beoordeeld en niet-gerandomiseerde onderzoeken bewijzen van hogere zekerheid bieden. Verdere bespreking van deze kwesties is ook te vinden in hoofdstuk 24.
14.1.3 Algemene template voor de tabellen “samenvatting van bevindingen”
verschillende alternatieve standaardversies van de tabellen “samenvatting van bevindingen” zijn ontwikkeld om consistentie en gebruiksgemak te garanderen bij alle beoordelingen, de opname van de belangrijkste informatie die de besluitvormers nodig hebben en een optimale presentatie (zie voorbeelden in Figuur 14.1.a en 14.1.b). Deze formaten worden ondersteund door onderzoek dat gericht is op een beter begrip van de informatie die ze willen overbrengen (Carrasco-Labra et al 2016, Langendam et al 2016, Santesso et al 2016). Ze zijn beschikbaar via het officiële softwarepakket van GRADE dat is ontwikkeld om de GRADE-aanpak te ondersteunen: GRADEpro GDT (www.gradepro.org).
standaard Cochrane ‘Summary of findings’ – tabellen bevatten de volgende elementen aan de hand van een van de aanvaarde formaten. Verdere richtsnoeren voor elk van deze worden gegeven in punt 14.1.6.
- een korte beschrijving van de populatie en de omgeving waarop de beschikbare gegevens betrekking hebben (die enigszins kunnen verschillen van of smaller kunnen zijn dan die welke in de toetsingsvraag worden gedefinieerd).
- een korte beschrijving van de vergelijking in de tabel “samenvatting van de bevindingen”, met inbegrip van zowel de experimentele als de vergelijkingsinterventies.
- een lijst van de meest kritische en/of belangrijke gezondheidsresultaten, zowel wenselijk als ongewenst, beperkt tot zeven of minder resultaten.
- een maat voor de typische belasting van elk resultaat (bv. illustratief risico, of illustratief gemiddelde, bij een vergelijkingsinterventie).
- de absolute en relatieve omvang van het effect gemeten voor elk (indien beide geschikt zijn).
- het aantal deelnemers en studies die bijdragen tot de analyse van elk resultaat.
- een beoordeling van de Algemene zekerheid van het bewijsmateriaal voor elke uitkomst (die kan variëren per resultaat).
- ruimte voor opmerkingen.
- toelichting (voorheen voetnoten genoemd).
idealiter worden de tabellen “samenvatting van de bevindingen” ondersteund door meer gedetailleerde tabellen (bekend als “bewijsprofielen”) waaraan het overzicht kan worden gekoppeld, die meer gedetailleerde uitleg geven. De bewijsprofielen omvatten dezelfde belangrijke gezondheidsresultaten en geven meer details dan de tabellen “samenvatting van bevindingen” van zowel de individuele overwegingen die aan de beoordeling van de zekerheid ten grondslag liggen als de resultaten van de studies (Guyatt et al 2011a). Zij zorgen ervoor dat een gestructureerde aanpak wordt gebruikt om de zekerheid van bewijs te beoordelen. Hoewel ze zelden worden gepubliceerd in Cochrane Reviews, bewijs profielen worden vaak gebruikt, bijvoorbeeld, door Richtlijn ontwikkelaars bij het overwegen van de zekerheid van het bewijs om richtlijn aanbevelingen te ondersteunen. Recensie auteurs zullen het gemakkelijker vinden om de ‘samenvatting van bevindingen’ tabel te ontwikkelen door het invullen van de beoordeling van de zekerheid van bewijs in het bewijs profiel eerst in GRADEpro GDT. Ze kunnen dit dan automatisch converteren naar een van de’ samenvatting van bevindingen ‘formaten in GRADEpro GDT, inclusief een interactieve’ samenvatting van bevindingen ‘ voor publicatie.
als maat voor de omvang van het effect voor dichotome uitkomsten moet de tabel “samenvatting van bevindingen” een relatieve maat voor het effect (bv. risicoverhouding, odds ratio, gevaar) en metingen van het absolute risico bevatten. Voor andere soorten gegevens kan alleen een absolute maat (zoals een verschil in middelen voor continue gegevens) voldoende zijn. Het is belangrijk dat de omvang van het effect op een zinvolle manier wordt gepresenteerd, wat een transformatie van het resultaat van een meta-analyse kan vereisen (zie ook hoofdstuk 15, paragraaf 15.4 en paragraaf 15.5). Beoordelingen met meer dan één hoofdvergelijking moeten voor elke vergelijking een afzonderlijke “samenvatting van bevindingen” – tabel bevatten.
figuur 14.1.a geeft een voorbeeld van een “samenvatting van de bevindingen” tabel. Figuur 15.1.b voorziet in een alternatief formaat dat het begrip en de interpretatie van de bevindingen van de evaluatie door de gebruikers verder kan vergemakkelijken. Uit gegevens die verschillende formaten evalueren, blijkt dat in de tabel “samenvatting van bevindingen” een risicoverschil moet worden opgenomen als maatstaf voor het absolute effect en dat de auteurs bij voorkeur een formaat moeten gebruiken dat een risicoverschil bevat .
een gedetailleerde beschrijving van de inhoud van een tabel “samenvatting van de bevindingen” is te vinden in Paragraaf 14.1.6.
figuur 14.1.een Voorbeeld van een ‘Overzicht bevindingen’ table
Samenvatting van de bevindingen (voor interactieve versie klik hier)
|
Compressie kousen in vergelijking met geen compressie kousen voor mensen die lange vluchten |
||||||
|
Patiënten of de bevolking: iedereen die een lange vlucht (langer dan 6 uur) Instellingen: international air reizen Interventie: compressie stockingsa Vergelijking: zonder kousen |
||||||
|
Resultaten |
Illustratief vergelijkende risico ‘ s* (95% CI) |
Relatieve effect (95% CI) |
Aantal deelnemers (studies) |
Zekerheid van het bewijs (GRADE) |
||
|
aanvaard risico |
Bijbehorende risico |
|||||
|
Zonder kousen |
Met kousen |
|||||
|
Symptomatische diepe veneuze trombose (DVT) |
Zie reactie |
Zie reactie |
Niet meetbaar |
(9 studies) |
Zie reactie |
0 deelnemers ontwikkeld symptomatische DVT in deze studies |
|
Symptomless DVT |
Laag risico populationb |
RR 0.10 (0.04 0.26) |
(9 studies) |
⊕⊕⊕⊕ Hoog |
||
|
10 per 1000 |
1 per 1000 (0 tot 3) |
|||||
|
Hoog risico populationb |
||||||
|
20 per 1000 |
2 per 1000 (1 tot 8) |
|||||
|
Oppervlakkige veneuze trombose |
13 per 1000 |
6 per 1000 (2 tot 15) |
RR 0.45 (0.18 1.13) |
(8 studies) |
⊕⊕⊕◯ Moderatec |
|
|
Oedeem na de vlucht waarden gemeten op een schaal van 0, geen oedeem, 10, maximum oedeem |
De gemiddelde oedeem score varieerde in de controle groepen van 6 9 |
De gemiddelde oedeem score in de interventie groepen gemiddeld 4.7 lagere (95% CI -4.9 tot -4.5) |
(6 studies) |
⊕⊕◯◯ Lowd |
||
|
longembolie |
Zie reactie |
Zie reactie |
Niet meetbaar |
(9 studies) |
Zie reactie |
0 deelnemers ontwikkeld longembolie in deze studiese |
|
Dood |
Zie reactie |
Zie reactie |
Niet inschatbaar |
(9 studies) |
Zie reactie |
0 deelnemers stierven in deze studies |
|
Negatieve effecten |
Zie reactie |
Zie reactie |
Niet meetbaar |
(4 studies) |
Zie reactie |
De verdraagbaarheid van de kousen werd beschreven als zeer goed geen klachten van bijwerkingen in 4 studiesf |
|
*De basis voor de veronderstelde risico is bepaald in voetnoot. Het overeenkomstige risico (en het 95% betrouwbaarheidsinterval) is gebaseerd op het veronderstelde risico in de interventiegroep en het relatieve effect van de interventie (en het 95% CI). BI: betrouwbaarheidsinterval; RR: risicoratio; graad: graad werkgroep cijfers van bewijs (zie toelichting). |
||||||
a Alle kousen in de negen studies opgenomen in dit overzicht waren onder-knie compressiekousen. In vier studies was de compressiesterkte 20 mmHg tot 30 mmHg bij de enkel. Het was 10 mmHg tot 20 mmHg in de andere vier studies. Kousen zijn er in verschillende maten. Als een kous is te strak rond de knie kan voorkomen dat essentiële veneuze terugkeer waardoor het bloed te zwembad rond de knie. Steunkousen moeten goed worden gemonteerd. Een kous die te strak is, kan tijdens een lange vlucht in de huid snijden en mogelijk zweren en een verhoogd risico op DVT veroorzaken. Sommige kousen kunnen iets dikker zijn dan normale beenbedekking en kunnen potentieel beperkend zijn met strakke voetslijtage. Het is een goed idee om kousen te dragen rond het huis voorafgaand aan de reis om te zorgen voor een goede, comfortabele pasvorm. Deelnemers trekken hun kousen twee tot drie uur voor de vlucht aan in de meeste studies. De beschikbaarheid en kosten van kousen kunnen variëren.
b in twee studies werden deelnemers met een hoog risico opgenomen, gedefinieerd als deelnemers met eerdere episodes van DVT, stollingsstoornissen, ernstige obesitas, beperkte mobiliteit als gevolg van bot-of gewrichtsproblemen, neoplastische ziekte in de afgelopen twee jaar, grote spataderen of, in een van de studies, deelnemers groter dan 190 cm en zwaarder dan 90 kg. De incidentie voor de zeven onderzoeken waarbij deelnemers met een hoog risico werden uitgesloten was 1.45% en de incidentie voor de twee onderzoeken waarbij deelnemers met een hoog risico werden aangeworven (met ten minste één risicofactor) bedroeg 2,43%. We hebben 10 en 30 per 1000 gebruikt om verschillende risicostrata uit te drukken, respectievelijk.
c het betrouwbaarheidsinterval overschrijdt geen verschil en sluit geen kleine toename uit.
d de meting van oedeem werd niet gevalideerd (ondirectheid van de uitkomst) of geblindeerd voor de interventie (risico op bias).
e indien er zeer weinig of geen gebeurtenissen zijn en het aantal deelnemers groot is, kan een oordeel over de zekerheid van bewijs (met name uitspraken over onnauwkeurigheid) gebaseerd zijn op het absolute effect. Hier kan de zekerheidsscore als ‘hoog’ worden beschouwd als de uitkomst naar behoren werd beoordeeld en de gebeurtenis in feite niet plaatsvond bij 2821 onderzochte deelnemers.
f in geen van de andere studies werden bijwerkingen gemeld, met uitzondering van vier gevallen van oppervlakkige veneuze trombose in spataderen in het kniegebied die in één studie gecomprimeerd werden door de bovenrand van de kous.
figuur 14.1.b Voorbeeld van een alternatief ‘Overzicht bevindingen’ tabel
|
Samenvatting van de bevindingen (voor interactieve versie klik hier): |
||||||
|
Probiotica, vergeleken met geen probiotica als een aanvulling op antibiotica bij kinderen |
||||||
|
de Patiënt of populatie: kinderen die antibiotica Instellingen: ziekenhuizen en extramurale Interventie: probiotica Vergelijking: geen probiotica |
||||||
|
Resultaten Geen van de deelnemers (studies) |
Relatieve effecten |
de Verwachte absolute effecten* (95% CI) |
Zekerheid van het bewijs |
|||
|
Zonder probiotica |
Met probiotica |
Verschil |
||||
|
de Incidentie van diarree: Probiotische dosis 5 miljard CFU/dag Follow-up: 10 dagen tot 3 maanden kinderen < 5 jaar |
kinderen < 5 jaar |
⊕⊕⊕⊝ moderateb vanwege risico op vertekening |
vermindert waarschijnlijk de incidentie van diarree. |
|||
|
1474 (7 studies) |
RR 0,41 (0,29 tot 0.55) |
22.3%a |
8.9% (6.5 aan 12.2) |
13.4% minder kinderen (10,1 tot 15.8 minder) |
||
|
kinderen > 5 jaar |
kinderen > 5 jaar |
⊕⊕⊝⊝ lowb, c vanwege risico op vertekening en onnauwkeurigheid |
kan de incidentie van diarree verminderen. |
|||
|
624 (4 studies) |
RR 0,81 (0,53 tot 1.21) |
11.2%a |
9% (5.9 aan 13.6) |
2.2% minder kinderen (5,3 minder tot 2.4 meer) |
||
|
Negatieve eventsd Follow-up: 10 44 dagen 1575 (11 studies) |
1.8%een |
2.3% (0.8 naar 3.8) |
0.5% meer nadelige eventse (1 minder 2 meer) |
⊕⊕⊝⊝ lowf, g Door het risico van de afwijking en de inconsistentie |
Er kan weinig of geen verschil in bijwerkingen. |
|
|
duur van diarree Follow-up: 10 dagen tot 3 maanden 897 (5 onderzoeken) |
de gemiddelde duur van diarree zonder probiotica was 4 dagen. |
0.6 minder dagen (1,18 tot 0,02 minder dagen) |
⊕⊕⊝⊝ lowh, i vanwege onnauwkeurigheid en inconsistentie |
kan de duur van diarree verminderen. |
||
|
ontlasting per dag Follow-up: 10 dagen tot 3 maanden 425 (4 onderzoeken) |
de gemiddelde ontlasting per dag zonder probiotica was 2,5 ontlasting per dag. |
0.3 minder ontlasting per dag (0,6 tot 0 minder) |
⊕⊕⊝⊝ lowj, k vanwege onnauwkeurigheid en inconsistentie |
er kan weinig of geen verschil in ontlasting per dag. |
||
|
*de basis voor het risico in de controlegroep (bijvoorbeeld het mediane risico van de controlegroep in alle onderzoeken) is opgenomen in voetnoten. Het risico in de interventiegroep (en het 95% betrouwbaarheidsinterval) is gebaseerd op het veronderstelde risico in de vergelijkingsgroep en het relatieve effect van de interventie (en het 95% BI). BI: betrouwbaarheidsinterval; RR: risicoratio. |
||||||
|
toelichting risicoschattingen van een controlegroep komen uit gepoolde schattingen van controlegroepen. Relatief effect op basis van beschikbare casusanalyse B hoog risico op bias als gevolg van hoge loss to follow-up. c onnauwkeurigheid ten gevolge van enkele voorvallen en betrouwbaarheidsintervallen omvatten merkbaar voordeel of schade. d bijwerkingen: huiduitslag, misselijkheid, flatulentie, braken, toegenomen slijm, pijn op de borst, constipatie, smaakstoornissen en lage eetlust. de risico ‘ s werden berekend op basis van gepoolde risicoverschillen. f hoog risico op bias. Slechts 11 van de 16 onderzoeken rapporteerden over bijwerkingen, wat wijst op een selectieve rapportage bias. g ernstige inconsistentie. Talrijke probiotica en doses werden geëvalueerd in een relatief klein aantal studies, waardoor ons vermogen om conclusies te trekken over de veiligheid van de vele probiotica en doses toegediend werd beperkt. h ernstige onverklaarde inconsistentie (grote heterogeniteit I2 = 79%, p-waarde , puntschattingen en betrouwbaarheidsintervallen variëren aanzienlijk). I ernstige onnauwkeurigheid. De bovengrens van 0,02 dagen diarree minder wordt niet als belangrijk voor de patiënt beschouwd. J ernstige onverklaarde inconsistentie (grote heterogeniteit I2 = 78%, p-waarde , puntschattingen en betrouwbaarheidsintervallen variëren aanzienlijk). K ernstige onnauwkeurigheid. Het 95% betrouwbaarheidsinterval omvat geen effect en de ondergrens van 0,60 ontlasting per dag is van twijfelachtig belang voor de patiënt. |
||||||
14.1.4 het opstellen van “Samenvatting van de bevindingen” tabellen
de software van de GRADE Working Group, GRADEpro GDT (www.gradepro.org), met inbegrip van het interactieve handboek van GRADE, is beschikbaar om recensiefauteurs te helpen bij het opstellen van “Samenvatting van de bevindingen” – tabellen. GRADEpro kan gegevens over het risico van de vergelijkingsgroep en de effectschatting (ingevoerd door de auteurs van de beoordeling of geïmporteerd uit bestanden die in RevMan zijn gegenereerd) gebruiken om de relatieve Effecten en absolute risico ‘ s te produceren die samenhangen met experimentele interventies. Daarnaast leidt het de gebruiker door het proces van een GRADE assessment, en produceert het een tabel die kan worden gebruikt als een standalone tabel in een beoordeling (inclusief door directe import in software zoals RevMan of integratie met RevMan Web), of een interactieve ‘samenvatting van bevindingen’ tabel (zie help resources in GRADEpro).
14.1.5 statistische overwegingen in de tabellen “samenvatting van bevindingen”
14.1.5.1 dichotome uitkomsten
de tabellen “samenvatting van bevindingen” moeten zowel absolute als relatieve maatstaven van het effect voor dichotome uitkomsten bevatten. Risicoratio ‘s, odds-ratio’ s en risicoverschillen zijn verschillende manieren om twee groepen te vergelijken met dichotoom uitkomstgegevens (zie hoofdstuk 6, paragraaf 6.4.1). Bovendien zijn er twee verschillende risicoratio ‘s, afhankelijk van welke gebeurtenis (bv.” ja ” of “nee”) de focus van de analyse is (zie hoofdstuk 6, punt 6.4.1.5). In de aanwezigheid van een niet-nulinterventie-effect loopt elke variatie tussen de studies in de vergelijkingsgroep risico ‘ s (d.w.z. variatie in het risico van het gebeuren zonder tussenkomst van belang, bijvoorbeeld in verschillende populaties) maakt het onmogelijk dat meer dan één van deze maatregelen in elk onderzoek werkelijk hetzelfde zijn.
in de epidemiologie is lange tijd aangenomen dat relatieve effectmetingen consistenter zijn dan absolute effectmetingen van het ene scenario naar het andere. Er is empirisch bewijs om deze aanname te ondersteunen (Engels et al 2000, Deeks and Altman 2001, Furukawa et al 2002). Om deze reden moeten meta-analyses over het algemeen ofwel een risico-ratio ofwel een odds-ratio gebruiken als maat voor het effect (zie hoofdstuk 10, paragraaf 10.4.3). Dienovereenkomstig is een enkele schatting van het relatieve effect waarschijnlijk een geschiktere samenvatting dan een enkele schatting van het absolute effect. Als een relatief effect inderdaad consistent is in alle studies, dan zullen verschillende risico ‘ s van de vergelijkingsgroep verschillende implicaties hebben voor het absolute voordeel. Bijvoorbeeld, als de risicoratio consequent 0 is.75, dan zou de experimentele interventie een risico van de vergelijkingsgroep van 80% tot 60% in de interventiegroep verminderen (een absolute risicoreductie van 20 procentpunten), maar ook een risico van de vergelijkingsgroep van 20% tot 15% in de interventiegroep (een absolute risicoreductie van 5 procentpunten).
de tabellen “samenvatting van bevindingen” zijn gebaseerd op de aanname van een consistent relatief effect. Het is daarom belangrijk om rekening te houden met de implicaties van dit effect voor de verschillende risico ‘ s van de vergelijkingsgroep (deze kunnen uit een aantal bronnen worden afgeleid of geschat, zie rubriek 14.1.6.3), die een beoordeling van de zekerheid van bewijs voor prognostisch bewijs kan vereisen (Spencer et al 2012, Iorio et al 2015). Voor elk risico van een vergelijkingsgroep is het mogelijk een overeenkomstig risico van de interventiegroep (d.w.z. het absolute risico met de interventie) te schatten aan de hand van de meta-analytische risicoratio of odds ratio. De cijfers in de kolom “overeenstemmend risico” zijn specifiek voor de ” risico ‘s” in de aangrenzende kolom.
voor de meta-analytische risicoratio (RR) en het veronderstelde comparatorrisico (ACR) wordt het overeenkomstige interventierisico verkregen als:
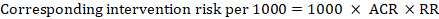 .
.
als voorbeeld, in Figuur 14.1.a is de meta-analytische risicoratio voor symptomloze diepveneuze trombose (DVT) RR = 0,10 (95% BI 0,04 tot 0,26). Uitgaande van een vergelijkingsrisico van ACR = 10 per 1000 = 0,01, krijgen we:
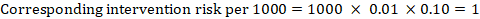 .
.
voor de meta-analytische odds ratio (OR) en het veronderstelde vergelijkingsrisico, ACR, wordt het overeenkomstige interventierisico verkregen als:
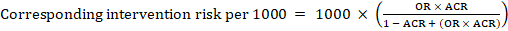 .
.
bovenste en onderste betrouwbaarheidsgrenzen voor het overeenkomstige interventierisico worden verkregen door RR respectievelijk of door hun bovenste en onderste betrouwbaarheidsgrenzen te vervangen (bv. door 0.10 met 0,04, dan met 0,26, in het voorbeeld). Dergelijke betrouwbaarheidsintervallen houden geen rekening met onzekerheid in de veronderstelde risico ‘ s van een vergelijkingsmiddel.
bij de behandeling van risicoratio ’s is het van cruciaal belang dat dezelfde definitie van “gebeurtenis” wordt gebruikt als voor de meta-analyse. Bijvoorbeeld, als de meta-analyse zich richtte op’ dood ‘(in tegenstelling tot overleving) als de gebeurtenis, dan moeten overeenkomstige risico’ s in de tabel ‘samenvatting van bevindingen’ook verwijzen naar ‘dood’.
In (zeldzame) omstandigheden waarin er een duidelijke reden is om in de meta-analyse een consistent risicoverschil aan te nemen, is het in principe mogelijk om dit voor relevante ” veronderstelde risico ‘s” en de bijbehorende risico’ s te presenteren, en om de overeenkomstige (verschillende) relatieve effecten voor elk aangenomen risico te presenteren.
het risicoverschil geeft het verschil weer tussen de ACR en het overeenkomstige interventierisico (of het verschil tussen de experimentele en de vergelijkingsinterventie).
voor de meta-analytische risicoratio (RR) en het veronderstelde vergelijkingsrisico (ACR) wordt het overeenkomstige risicoverschil verkregen als (merk op dat risico ‘ s ook kunnen worden uitgedrukt met behulp van percentages of procentpunten):
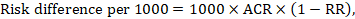
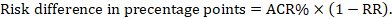
als voorbeeld, in Figuur 14.1.b de meta-analytische risicoratio is 0,41 (95% BI 0,29 tot 0,55) voor diarree bij kinderen jonger dan 5 jaar. Uitgaande van een comparator Groep risico van 22,3%:
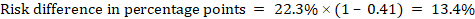 .
.
Voor de meta-analyse odds ratio (or) en nam de comparator risico (ACR) is het absolute risico verschil is verkregen als (percentage punten):
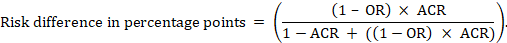
Bovenste en onderste betrouwbaarheidsgrenzen voor het absolute risico verschil zijn verkregen door het opnieuw uitvoeren van de bovenstaande berekening, terwijl het vervangen van RR of door hun bovenste en onderste betrouwbaarheidsinterval, respectievelijk (bijvoorbeeld het vervangen van 0.41 met 0,28, dan met 0.55, in het voorbeeld). Dergelijke betrouwbaarheidsintervallen houden geen rekening met onzekerheid in de veronderstelde risico ‘ s van een vergelijkingsmiddel.
14.1.5.2 uitkomsten van tijd tot gebeurtenis
uitkomsten van tijd tot gebeurtenis meten of en wanneer een bepaalde gebeurtenis (bijvoorbeeld overlijden) optreedt (van Dalen et al 2007). Het effect van de experimentele interventie ten opzichte van de vergelijkingsgroep op de resultaten van de tijd tot het voorval wordt gewoonlijk gemeten met behulp van een hazard ratio (HR) (zie hoofdstuk 6, paragraaf 6.8.1).
een hazard ratio geeft een schatting van het relatieve effect weer. Het kan op verschillende manieren worden gebruikt om absolute risico ‘ s en andere interpreteerbare hoeveelheden voor een specifieke populatie te verkrijgen. Hier beschrijven we hoe hazard ratio ‘ s opnieuw kunnen worden uitgedrukt in termen van: (I) absoluut risico van gebeurtenisvrije overleving binnen een bepaalde periode; (ii) absoluut risico van een gebeurtenis binnen een bepaalde periode; en (iii) mediane tijd tot het voorval. Alle methoden zijn gebaseerd op een aanname van consistente relatieve effecten (dat wil zeggen dat de hazard ratio niet varieert in de tijd).
(i) Het Absolute risico op gebeurtenisvrije overleving binnen een bepaalde periode van tijd Gebeurtenisvrije overleving (bijvoorbeeld totale overleving) wordt vaak gerapporteerd door individuele onderzoeken. Om absolute effecten te verkrijgen voor de resultaten van tijd tot gebeurtenis, gemeten als gebeurtenisvrije overleving, kan de samenvatting HR worden gebruikt in combinatie met een verondersteld deel van de patiënten die gebeurtenisvrij zijn in de vergelijkingsgroep (Tierney et al 2007). Dit percentage patiënten zal specifiek zijn voor een periode van observatie. Het is echter niet strikt noodzakelijk deze termijn te specificeren. Zo kan een deel van 50% van de gebeurtenisvrije patiënten van toepassing zijn op patiënten met een hoog gebeurtenispercentage dat gedurende 1 jaar wordt waargenomen, of op patiënten met een laag gebeurtenispercentage dat gedurende 2 jaar wordt waargenomen.

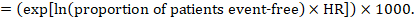
stel bijvoorbeeld dat de meta-analytische hazard ratio 0,42 is (95% BI 0,25 tot 0,72). Uitgaande van het risico van een comparatorgroep op gebeurtenisvrije overleving (bijvoorbeeld bij mensen die overall survival leven) na 2 jaar van ACR = 900 per 1000 = 0,9, krijgen we:

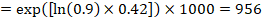
zodat die 956 per 1000 mensen zullen leven met de experimentele interventie op 2 jaar. De afleiding van het risico moet worden toegelicht in een opmerking of voetnoot.
(ii) absoluut risico van een gebeurtenis binnen een bepaalde periode om dit absolute effect te verkrijgen, kan ook de samenvatting HR worden gebruikt (Tierney et al. 2007):

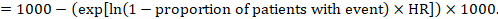
in het voorbeeld, stel dat we aannemen een comparator Groep risico van gebeurtenissen (bijvoorbeeld voor mortaliteit, mensen die dood zijn) op 2 jaar van ACR = 100 per 1000 = 0,1. Wij verkrijgen:

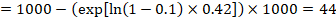
zodat die 44 per 1000 mensen dood zullen zijn met de experimentele interventie op 2 jaar.
(iii) mediane tijd tot het voorval in plaats van absolute aantallen kan de tijd tot het voorval in de interventie-en vergelijkingsgroepen worden uitgedrukt als mediane overlevingstijd in maanden of jaren. Om de mediane overlevingstijd te verkrijgen kan de gepoolde HR worden toegepast op een veronderstelde mediane overlevingstijd in de comparatorgroep (Tierney et al. 2007):
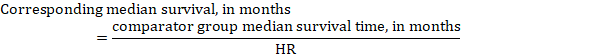
in het voorbeeld, uitgaande van een vergelijkingsgroep mediane overlevingstijd van 80 maanden, krijgen we:
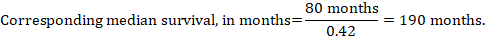
voor alle drie deze opties voor het opnieuw uitdrukken van de resultaten van tijd-tot-gebeurtenis analyses worden de bovenste en onderste betrouwbaarheidsgrenzen voor het overeenkomstige interventierisico verkregen door HR te vervangen door respectievelijk de bovenste en de onderste betrouwbaarheidsgrenzen (bijvoorbeeld door 0,42 te vervangen door 0,25, vervolgens door 0,72 in het voorbeeld). Nogmaals, zoals voor dichotome uitkomsten, bevatten dergelijke betrouwbaarheidsintervallen geen onzekerheid in de veronderstelde risico ‘ s van de vergelijkingsgroep. Dit is van bijzonder belang voor de overleving op lange termijn met een laag of matig sterftecijfer en een overeenkomstig hoog aantal gecensureerde patiënten (d.w.z. een laag aantal patiënten onder risico en een hoog censuurpercentage).
14.1.6 gedetailleerde inhoud van een tabel “samenvatting van bevindingen”
14.1.6.1 titel en kop van de tabel
in de titel van elke tabel “samenvatting van bevindingen” moet de zorgvraag worden gespecificeerd, in termen van de populatie en moet duidelijk worden gemaakt welke vergelijking van interventies wordt gemaakt. In Figuur 14.1.a, de bevolking is mensen die lange vluchten vliegen, de interventie is steunkousen, en de controle is geen steunkousen.
de eerste rijen van elke tabel “samenvatting van bevindingen” moeten de volgende “header” – informatie bevatten:
patiënten of populatie dit verduidelijkt verder de populatie (en mogelijk de subpopulaties) van belang en idealiter de omvang van het risico van de meest cruciale nadelige uitkomst waarop een interventie is gericht. Mensen op een langeafstandsvlucht kunnen bijvoorbeeld verschillende risico ‘ s lopen voor DVT; degenen die selectieve serotonineheropnameremmers (SSRI ‘ s) gebruiken, kunnen een ander risico lopen op bijwerkingen; terwijl degenen met atriumfibrilleren een laag (< 1%), matig (1% tot 4%) of hoog (> 4%) jaarlijks risico op beroerte kunnen hebben.
instelling hier moeten specifieke kenmerken van de instellingen van de zorgvraag worden vermeld die de toepasbaarheid van de samenvatting van de bevindingen kunnen beperken tot andere instellingen (bijvoorbeeld eerstelijnszorg in Europa en Noord-Amerika).
interventie de experimentele interventie.
vergelijking de vergelijkingsinterventie (inclusief geen specifieke interventie).
14.1.6.2 resultaten
de rijen van een tabel “samenvatting van bevindingen” moeten alle gewenste en ongewenste gezondheidsresultaten (gerangschikt in volgorde van belangrijkheid) bevatten die essentieel zijn voor de besluitvorming, tot maximaal zeven resultaten. Als er meer resultaten in de herziening zijn, zullen de auteurs van de herziening de minder belangrijke resultaten uit de tabel moeten weglaten, en de beslissing om te kiezen welke resultaten cruciaal Of belangrijk zijn voor de herziening moet worden gemaakt tijdens de ontwikkeling van het protocol (zie hoofdstuk 3). De auteurs van de beoordeling moeten termijnen verstrekken voor het meten van de resultaten (bv. 90 dagen of 12 maanden) en het type instrumentscores (bv. variërend van 0 tot 100).
merk op dat de auteurs van de beoordeling De vooraf gespecificeerde kritische en belangrijke resultaten in de tabel moeten opnemen, ongeacht of gegevens beschikbaar zijn of niet. Zij moeten echter alert zijn op de mogelijkheid dat het belang van een resultaat (bijvoorbeeld een ernstig negatief effect) pas bekend wordt nadat het protocol is geschreven of de analyse is uitgevoerd, en moeten passende maatregelen nemen om deze op te nemen in de tabel “samenvatting van bevindingen”.
de tabel ‘samenvatting van bevindingen’ kan effecten in subgroepen van de populatie voor verschillende vergelijkingsrisico ‘ s en effectgroottes afzonderlijk bevatten. Bijvoorbeeld in Figuur 14.1.B effecten worden afzonderlijk gepresenteerd voor kinderen jonger en ouder dan 5 jaar. Recensie auteurs kunnen er ook voor kiezen om afzonderlijke ‘samenvatting van bevindingen’ tabellen voor verschillende populaties te produceren.
de auteurs van de beoordeling dienen ernstige bijwerkingen op te nemen, maar het zou mogelijk kunnen zijn om kleine bijwerkingen te combineren als één enkele uitkomst, en beschrijven dit in een verklarende voetnoot (merk op dat het niet passend is om voorvallen bij elkaar op te tellen, tenzij ze onafhankelijk zijn, dat wil zeggen dat een deelnemer die één bijwerking heeft ervaren een onaangetaste kans heeft om de andere bijwerking te ervaren).
resultaten gemeten op meerdere tijdstippen vormen een bijzonder probleem. In het algemeen, om de tabel eenvoudig te houden, recensie auteurs moeten MEERDERE tijdpunten alleen presenteren voor resultaten die cruciaal zijn voor de besluitvorming, waar ofwel het resultaat of de genomen beslissing waarschijnlijk variëren in de tijd. De rest moet waar mogelijk op een gemeenschappelijk tijdstip worden gepresenteerd.
auteurs van de Review kunnen continue resultaatmetingen presenteren in de tabel “samenvatting van Bevindingen” en moeten trachten deze voor de doelgroep te interpreteren. Dit vereist dat de eenheden duidelijk en gemakkelijk te interpreteren zijn, bijvoorbeeld dagen van pijn of frequentie van hoofdpijn, en de naam en de schaal van de gebruikte meetinstrumenten moeten worden vermeld (bijvoorbeeld een visuele analoge schaal, variërend van 0 tot 100). Echter, veel meetinstrumenten zijn niet gemakkelijk te interpreteren door niet-gespecialiseerde artsen of patiënten, bijvoorbeeld punten op een Beck depressie inventaris of kwaliteit van leven score. Voor deze, een meer interpreteerbare presentatie zou kunnen bestaan uit het omzetten van een continue naar een dichotoom resultaat, zoals >50% verbetering (zie hoofdstuk 15, paragraaf 15.5).
14.1.6.3 beste schatting van het risico met een vergelijkingsinterventie
de auteurs van de beoordeling moeten maximaal drie typische risico ‘ s verstrekken voor deelnemers die de vergelijkingsinterventie ontvangen. Voor dichotome uitkomsten raden we aan deze te presenteren in de vorm van het aantal mensen dat de gebeurtenis ervaart per 100 of 1000 mensen (natuurlijke frequentie) afhankelijk van de frequentie van de uitkomst. Voor continue resultaten zou dit worden vermeld als een gemiddelde of mediane waarde van het gemeten resultaat.
Geschatte of veronderstelde risico ’s van vergelijkende interventie kunnen gebaseerd zijn op beoordelingen van typische risico’ s in verschillende patiëntengroepen die zijn afgeleid van de beoordeling zelf, individuele representatieve studies in de beoordeling, of risico ‘ s die zijn afgeleid van een systematische beoordeling van prognostische studies of andere bronnen van bewijs, die op hun beurt een beoordeling van de zekerheid voor het prognostische bewijs kunnen vereisen (Spencer et al 2012, Iorio et al 2015). Idealiter zouden risico ‘ s groepen weerspiegelen die artsen gemakkelijk kunnen identificeren op basis van hun presentatiekenmerken.
in een verklarende voetnoot moet de bron of motivering voor elk risico van de vergelijkingsgroep worden vermeld, met inbegrip van de periode waarmee het in voorkomend geval overeenkomt. In Figuur 14.1.a, kunnen clinici gemakkelijk individuen met risicofactoren voor diepe veneuze trombose onderscheiden van die zonder. Als bekend is dat er weinig variatie is in het baseline-risico, kunnen de auteurs van de beoordeling het mediane risico van de vergelijkingsgroep voor alle studies gebruiken. Als de typische risico ‘ s niet bekend zijn, is een optie om het risico te kiezen uit de opgenomen studies, waarbij de tweede hoogste voor een hoog en de tweede laagste voor een laag risico populatie.
14.1.6.4 risico met interventie
voor dichotome uitkomsten moeten de auteurs van de review een overeenkomstig absoluut risico voor elk risico van de vergelijkingsgroep geven, samen met een betrouwbaarheidsinterval. Dit absolute risico met de (experimentele) interventie zal gewoonlijk worden afgeleid uit het meta-analyseresultaat weergegeven in de kolom relatieve effecten (zie paragraaf 14.1.6.6). Formules worden gegeven in punt 14.1.5. De auteurs van de beoordeling moeten het absolute effect in dezelfde vorm presenteren als de risico ‘ s met een vergelijkingsinterventie (zie paragraaf 14.1.6.3), bijvoorbeeld als het aantal mensen dat de gebeurtenis ervaart per 1000 mensen.
voor continue resultaten moet een verschil in gemiddelden of een gestandaardiseerd verschil in gemiddelden worden weergegeven met het betrouwbaarheidsinterval. Deze worden doorgaans direct verkregen uit een meta-analyse. Ter verduidelijking van de Betekenis dient een verklarende tekst te worden gebruikt, zoals in Figuur 14.1.a en 14.1.
14.1.6.5 Risicoverschil
voor dichotome uitkomsten kan het risicoverschil worden verstrekt met behulp van een van de tabelformaten “samenvatting van bevindingen” als een aanvullende optie (zie figuur 14.1.b). Dit risicoverschil geeft het verschil weer tussen de experimentele en de vergelijkingsinterventie en zal gewoonlijk worden afgeleid uit het meta-analyseresultaat in de kolom relatieve effecten (Zie Rubriek 14.1.6.6). Formules worden gegeven in punt 14.1.5. De auteurs van de beoordeling moeten het risicoverschil presenteren in hetzelfde formaat als de veronderstelde en overeenkomstige risico ’s met een vergelijkingsinterventie (zie paragraaf 14.1.6.3); bijvoorbeeld als het aantal personen dat de gebeurtenis per 1000 personen ervaart of als procentpunten als de veronderstelde en overeenkomstige risico’ s in percentage worden uitgedrukt.
voor continue resultaten kan, indien de tabel “samenvatting van bevindingen” deze optie bevat, het gemiddelde verschil hier worden weergegeven en de kolom “overeenstemmend risico” blanco worden gelaten (zie figuur 14.1.b).
14.1.6.6 relatief effect (95% BI)
het relatieve effect is doorgaans een risico-of odds-ratio (of soms een hazard ratio) met het bijbehorende 95% betrouwbaarheidsinterval, verkregen uit een meta-analyse uitgevoerd op basis van dezelfde effectmaat. Risicoratio ’s en odds-ratio’ s zijn vergelijkbaar wanneer de risico ’s van de vergelijkingsinterventie laag zijn en de effecten klein, maar kunnen aanzienlijk verschillen wanneer de risico’ s van de vergelijkingsgroep toenemen. De meta-analyse kan een aanname inhouden van vaste of willekeurige effecten, afhankelijk van wat de auteurs van de beoordeling passend achten, en impliceert dat het relatieve effect ofwel een schatting is van het effect van de interventie, ofwel een schatting van het gemiddelde effect van de interventie over studies, respectievelijk.
14.1.6.7 aantal deelnemers (studies)
deze kolom moet het aantal deelnemers bevatten dat in de opgenomen studies voor elk resultaat werd beoordeeld en het overeenkomstige aantal studies dat deze deelnemers heeft bijgedragen.
14.1.6.8 zekerheid van het bewijs (graad)
auteurs van het onderzoek dienen commentaar te leveren op de zekerheid van het bewijs (ook bekend als kwaliteit van het bewijsmateriaal of vertrouwen in de effectschattingen). Auteurs van de beoordeling moeten gebruik maken van het specifieke evidence grading system dat is ontwikkeld door de GRADE Working Group (Atkins et al 2004, Guyatt et al 2008, Guyatt et al 2011a), dat in detail wordt beschreven in Paragraaf 14.2. De GRADENBENADERING categoriseert de zekerheid in een bewijsmateriaal als’ hoog’,’ matig’,’ laag ‘of’ zeer laag ‘ naar resultaat. Dit is het resultaat van een oordeel, maar het beoordelingsproces werkt binnen een transparante structuur. Als voorbeeld zou de zekerheid “hoog” zijn als de samenvatting van verschillende gerandomiseerde proeven met een laag risico op vertekening zou zijn, maar de beoordeling van zekerheid wordt lager als er bezorgdheid bestaat over het risico op vertekening, inconsistentie, onrechtmatigheid, onnauwkeurigheid of vertekening van publicatie. Andere oordelen dan die met “hoge” zekerheid moeten transparant worden gemaakt met behulp van verklarende voetnoten of de kolom “opmerkingen” in de tabel “samenvatting van de bevindingen” (zie punt 14.1.6.10).
14.1.6.9 opmerkingen
het doel van het veld “Opmerkingen” is om de in de rij vermelde informatie of gegevens te helpen interpreteren. Dit kan bijvoorbeeld betrekking hebben op de geldigheid van de uitkomstmaat of de aanwezigheid van variabelen die geassocieerd zijn met de omvang van het effect. Belangrijke kanttekeningen over de resultaten moeten hier worden gemarkeerd. Niet alle rijen hebben opmerkingen nodig en het is het beste om een lege ruimte achter te laten als er niets is dat een opmerking rechtvaardigt.
14.1.6.10 toelichtingen
gedetailleerde toelichtingen dienen als voetnoten te worden opgenomen ter ondersteuning van de oordelen in de tabel “samenvatting van de bevindingen”, zoals de Algemene beoordeling van de rang. In de toelichting moet de motivering voor belangrijke aspecten van de inhoud worden beschreven. Tabel 14.1.een lijst van richtlijnen voor nuttige uitleg. De uitleg moet beknopt, informatief, relevant, gemakkelijk te begrijpen en nauwkeurig zijn. Indien de toelichting in de voetnoten niet voldoende kan worden beschreven, dienen de auteurs van de beoordeling nadere bijzonderheden over de kwesties in de resultaten en de Discussieonderdelen van de beoordeling te verstrekken.
tabel 14.1.een leidraad voor het verstrekken van nuttige toelichtingen in de tabellen “samenvatting van bevindingen” (SoF). Aangepast van Santesso et al (2016)
algemene richtsnoeren
- Voer de informatie voor lezers zo mogelijk rechtstreeks in de tabel in (bv. informatie over de duur van de follow-up of de gebruikte schaal).
- vermeld in het algemeen geen verwijzingen in de toelichting, tenzij er specifieke redenen zijn, bijvoorbeeld, voor het verstrekken van informatie over bronnen van basisrisico ‘ s (zie punt 3).
- Geef de bron van informatie over de basisrisico ‘ s die worden gebruikt om de absolute effecten te berekenen.
- na voltooiing van de tabel, bekijk alle verklaringen om te bepalen of er meerdere keren naar kan worden verwezen indien deze worden herschreven of gecombineerd.
- geef redenen voor het upgraden en downgraden van het bewijs (zie domeinspecifieke richtlijnen hieronder) en gebruik GRADEpro GDT-software om zich te houden aan GRADE guidance.
- het bewijsmateriaal voor een bepaalde uitkomst kan worden vastgesteld dat er ernstige of zeer ernstige problemen zijn voor het betrokken domein (of ernstig ernstig voor het risico van vertekening wanneer ROBINS-I wordt gebruikt). Het kan dus nuttig zijn om het aantal niveaus voor downgrading aan te geven (bijvoorbeeld een niveau voor risico op vertekening), maar om herhaling van wat in de tabel staat (en de indruk van formulaïsche of algoritmische rapportage) te vermijden. In bewijs profielen, deze informatie is al in de cellen van de tabel.
- hoewel uitleg over de zekerheid in het bewijsmateriaal in de eerste plaats vereist is wanneer zij de zekerheid veranderen, overweeg dan een verklaring toe te voegen wanneer de zekerheid in het bewijsmateriaal niet is gewijzigd, maar wanneer dit besluit door anderen kan worden betwist. Dit zal helpen om redenen voor onenigheid te begrijpen.
- ervoor zorgen dat de tabel niet wordt gebruikt als een beschrijving van de methoden van de herziening (geef bijvoorbeeld geen beschrijving van de redenen voor de statistische analyse).
- voer resultaten in voor resultaten die niet statistisch konden worden gecombineerd in een meta-analyse (d.w.z. narratieve uitkomsten) direct in de SoF-tabel in de resultatenkolommen. Het is mogelijk dat een toelichting niet nodig is om deze resultaten mee te delen. Voeg aanvullende schattingen van de interventie-effecten (bv. aantal dat nodig is om te behandelen voor voordeel en schade, risicoverschil uitgedrukt als percentage, continu resultaat uitgedrukt in minimale belangrijke verschileenheden) toe in de kolom opmerkingen.
- gebruik de informatie in de toelichting bij het beoordelingsproces om andere belangrijke onderdelen van de beoordeling te informeren, waaronder samenvattende versies en de discussie.
domeinspecifieke richtsnoeren voor het schrijven van nuttige toelichtingen
risico op vertekening
- beschrijf het aantal studies, of de hoeveelheid informatie die zij in de meta-analyse verstrekken, die een hoog risico op vertekening hadden en voor welk criterium.
- gebruik termen als meerderheid, minderheid, Alle, sommige of geen; of het aantal studies als x / X studies.
- vermeld voor gerandomiseerde onderzoeken de specifieke criteria, waaronder het verbergen van de toewijzingsvolgorde, het rapporteren van selectieve resultaten, enz. Voor niet-gerandomiseerde studies, beschrijf het criterium in de gebruikte tool (bijvoorbeeld met behulp van de ROBINS-I tool).
- geef aan of het effect van het risico op bias is onderzocht in een gevoeligheidsanalyse. Vermeld in voorkomend geval de bijdrage van de studies met een hoog risico op vertekening aan de ramingen.
- informatie over de studieopzet kan in de toelichting worden opgenomen, met name in de SoF wanneer verschillende studieopzetstukken worden opgenomen.
inconsistentie
- geef aan welke maatstaf wordt gebruikt om inconsistentie te beoordelen, zoals de statistische test of maatstaf (I2, Chi2, Tau), of de overlapping van betrouwbaarheidsintervallen, of gelijkenis van puntschattingen.
- indien de inconsistentie gebaseerd is op I2, beschrijf deze dan als aanzienlijk, substantieel, matig of niet belangrijk.
- vermeld indien van toepassing of heterogeniteit is onderzocht in subgroepanalyses door PICO (patiënten, interventie, vergelijking, resultaat) en of er andere mogelijke redenen zijn voor de heterogeniteit.
- in het geval van een enkel onderzoek voor een resultaat, zeggen dat er “geen” is in plaats van “niet van toepassing”.
onnauwkeurigheid
- geef aan waar de steekproefgrootte of het aantal gebeurtenissen niet voldoet aan de optimale informatiegrootte zoals berekend, of aan de “vuistregels” (bv. 400 gebeurtenissen). Vermijd verwijzing naar het aantal studies als reden voor onnauwkeurigheid.
- geef aan of de betrouwbaarheidsintervallen de mogelijkheid bevatten van een klein of geen effect en belangrijke voordelen of schade. Vermeld, indien bekend, de numerieke waarde van de drempel van belangrijk voordeel.
- vermijd het rapporteren van het resultaat als statistisch of niet-statistisch significant.
Upgrading
- vermeld de reden voor upgrading: vanwege groot effect; een dosis-respons gradiënt; of plausibele resterende tegengestelde verstorende verhoogt de zekerheid van bewijs.
- voor grote effecten, rapporteren als het relatieve effect > 2 of >5 is. Geef Voor dosis-responsgradiënten de mate van interventie en het effect op het resultaat. Beschrijf voor het domein ‘plausible residual opposing confounding’ het effect van de confounding factor op de schatting.
14.2 Assessing the security or quality of a body of evidence
14.2.1 the GRADE approach
the Grades of Recommendation, Assessment, Development and Evaluation Working Group (GRADE Working Group) has developed a system for grading the security of evidence (Schünemann et al 2003, Atkins et al 2004, Schünemann et al 2006, Guyatt et al 2008, Guyatt et al 2011a). Meer dan 100 organisaties, waaronder de Wereldgezondheidsorganisatie (WHO), het American College of Physicians, de American Society of Hematology( ASH), het Canadian Agency for Drugs and Technology in Health (CADTH) en de National Institutes of Health and Clinical Excellence (NICE) in het Verenigd Koninkrijk hebben het GRADE system (www.gradeworkinggroup.org).
Cochrane heeft ook formeel voor deze aanpak gekozen, en bij alle Cochrane-beoordelingen moet GRADE worden gebruikt om de zekerheid van bewijs voor belangrijke resultaten te evalueren (zie Mecir kader 14.2.een).
Mecir kader 14.2.een relevante verwachting voor het uitvoeren van interventiebeoordelingen
|
C74: beoordeling van de zekerheid van het bewijsmateriaal (verplicht) |
|
|
gebruik de vijf overwegingen (risico van vertekening, consistentie van het effect, onnauwkeurigheid, onrechtmatigheid en publicatie vertekening) om de zekerheid van het bewijsmateriaal voor elke uitkomst te beoordelen en conclusies te trekken over de zekerheid van het bewijsmateriaal in de tekst van het onderzoek. |
GRADE is de meest gebruikte benadering voor het samenvatten van het vertrouwen in de effecten van interventies door de uitkomst van de studies. Het verdient de voorkeur om de online GRADEpro tool te gebruiken, en om het te gebruiken zoals beschreven in het help-systeem van de software. Dit moet ertoe bijdragen dat auteursteams toegang krijgen tot dezelfde informatie om hun oordeel te informeren. Idealiter zouden twee personen die onafhankelijk werken, de zekerheid van het bewijsmateriaal moeten beoordelen en een consensus moeten bereiken over beslissingen tot verlaging van de rangorde. De vijf RANGOVERWEGINGEN moeten worden behandeld, ongeacht of de evaluatie een tabel met “samenvatting van de bevindingen” bevat. Het is nuttig om deze informatie te gebruiken in de discussie, in de conclusies van de auteurs en om de zekerheid in het bewijs over te brengen in de abstracte en eenvoudige taal samenvatting. |
|
C75: rechtvaardiging van de beoordeling van de zekerheid van de bewijselementen (verplicht) |
|
|
onderbouw en documenteer alle beoordelingen van de zekerheid van het bewijsmateriaal (bijvoorbeeld downgrading of upgrading met GRADE). |
de invoering van een gestructureerde aanpak zorgt voor transparantie bij het formuleren van een interpretatie van het bewijsmateriaal, en het resultaat is meer informatief voor de gebruiker. |
voor systematische beoordelingen definieert de GRADENBENADERING de zekerheid van een bewijsstuk als de mate waarin men er zeker van kan zijn dat een schatting van het effect of de associatie dicht bij de hoeveelheid van specifiek belang ligt. De beoordeling van de zekerheid van een lichaam van bewijs houdt de overweging van binnen – en over-studie het risico van bias (beperkingen in de onderzoeksopzet en de uitvoering of de methodologische kwaliteit), – inconsistentie (of heterogeniteit), indirectness van bewijs, onnauwkeurigheid van het effect van ramingen en risico van publicatie bias (zie Paragraaf 14.2.2), evenals de domeinen die kunnen verhogen ons vertrouwen in het effect schatten (zoals beschreven in Paragraaf 14.2.3). Het rangsysteem houdt een beoordeling in van de zekerheid van een bewijsstuk voor elke individuele uitkomst. Oordelen over de domeinen die de zekerheid van bewijs bepalen, moeten worden beschreven in de resultaten of discussie sectie en als onderdeel van de ‘samenvatting van bevindingen’ tabel.
de GRADENBENADERING specificeert vier niveaus van zekerheid (figuur 14.2.een). Voor interventies, met inbegrip van diagnostische en andere tests die als interventies worden beoordeeld (Schünemann et al 2008b, Schünemann et al 2008a, Balshem et al 2011, Schünemann et al 2012), is het uitgangspunt voor het beoordelen van de zekerheid van bewijs in twee typen ingedeeld. :
- gerandomiseerde onderzoeken; en
- niet-gerandomiseerde studies van interventies (NRSI), met inbegrip van observationele studies (met inbegrip van maar niet beperkt tot cohortstudies, en case-control studies, transversale studies, case series en case reports, hoewel niet al deze ontwerpen gewoonlijk worden opgenomen in Cochrane Reviews).
er zijn veel gevallen waarin auteurs van reviews vertrouwen op informatie van NRSI, met name om potentiële schade te evalueren (zie hoofdstuk 24). Bovendien kunnen de auteurs van de beoordeling relevante gegevens uit zowel gerandomiseerde studies als NRSI verkrijgen, waarbij elk type bewijs de andere aanvult (Schünemann et al 2013).
in graad begint een verzameling bewijsmateriaal uit gerandomiseerde onderzoeken met een hoge-zekerheid rating, terwijl een verzameling bewijsmateriaal uit NRSI begint met een lage-zekerheid rating. De lagere rating met NRSI is het resultaat van de potentiële bias veroorzaakt door het ontbreken van randomisatie (dwz verstorende en selectie bias).
echter, wanneer gebruik wordt gemaakt van de nieuwe tool Risk Of Bias In Non-randomized Studies of Interventions (ROBINS-I) (Sterne et al 2016), een beoordelingsinstrument dat het risico van bias door gebrek aan randomisatie dekt, kunnen alle studies beginnen als hoge zekerheid van het bewijs (Schünemann et al 2018). De benadering om alle onderzoeksontwerpen (met inbegrip van NRSI) als hoge zekerheid te starten, is niet in strijd met de initiële benadering om de beoordeling van NRSI als bewijs van lage zekerheid te starten. De reden hiervoor is dat een hoeveelheid bewijsmateriaal uit NRSI over het algemeen met twee niveaus moet worden verlaagd vanwege het inherente risico van bias geassocieerd met het ontbreken van randomisatie, namelijk verstorende en selectie bias. Het niet verlagen van NRSI van hoge naar lage zekerheid vereist transparante en gedetailleerde rechtvaardiging voor wat de zorgen over verstorende en selectie bias verzacht (Schünemann et al 2018). Er bestaan momenteel zeer weinig voorbeelden van gevallen waarin niet met twee niveaus kan worden verlaagd.
de hoogste zekerheidsscore is een bewijsstuk wanneer er geen problemen zijn in een van de in Figuur 14.2 vermelde CIJFERFACTOREN.a. recensie auteurs vaak downgraden bewijs tot matige, lage of zelfs zeer lage zekerheid bewijs, afhankelijk van de aanwezigheid van de vijf factoren in Figuur 14.2.A. Gewoonlijk zal de zekerheidsscore met één niveau voor elke factor dalen, tot maximaal drie niveaus voor alle factoren. Als er zeer ernstige problemen zijn voor een domein (bijv. bij de beoordeling van het risico op bias werden alle onderzoeken niet verhuld, gedeblokkeerd en verloren meer dan 50% van hun patiënten voor follow-up), het bewijs kan dalen met twee niveaus als gevolg van die factor alleen. Het is niet mogelijk om minder te beoordelen dan “zeer lage zekerheid” bewijs.
de auteurs van de Review beoordelen in het algemeen bewijs uit gedegen niet-gerandomiseerde studies als lage zekerheid, zelfs als ROBINS-I wordt gebruikt. Indien dergelijke studies echter grote effecten opleveren en er geen duidelijke vooringenomenheid is die deze effecten verklaart, kunnen de auteurs van de review het bewijs beoordelen als matig of – als het effect groot genoeg is-zelfs als hoge zekerheid (figuur 14.2.een). Het zeer lage betrouwbaarheidsniveau is geschikt voor, maar is niet beperkt tot, studies met kritieke problemen en onsystematische klinische observaties (bv. casusreeksen of casusrapporten).