todas as células tecidulares dependem do metabolismo aeróbico para a geração da energia (sob a forma de trifosfato de adenosina, ATP) necessária para a sobrevivência e a função. Este processo mitocondrial fundamental é caracterizado pelo consumo de oxigênio e produção de dióxido de carbono, que pode variar de cerca de 200 mL/minuto no estado de repouso para mais de cinco vezes esta taxa durante o exercício.
o destino final deste dióxido de carbono é a eliminação do corpo no ar expirado, e uma função importante do sangue é o transporte de dióxido de carbono das células dos tecidos para os pulmões.
uma compreensão deste processo de transporte depende de uma apreciação do que se entende por pressão parcial de um gás, bem como algumas leis físicas básicas que regem a solubilidade e movimento (difusão) de gases.
- QUAL É A PRESSÃO PARCIAL DE UM GÁS?
- SOLUBILIDADE E DIFUSÃO DE GASES
- transporte de dióxido de carbono das células tecidulares para o pulmão
- DIÓXIDO de CARBONO E do PH do SANGUE
- IN the LABORATORY-DEFINITION OF CO2 PARAMETERS
- pressão parcial do dióxido de carbono pCO2
- concentração de bicarbonato (HCO3-)
- concentração total de dióxido de carbono no PLASMA (ctCO2)
- métodos químicos para medir ctCO2
- discordância entre o ctCO2 medido e o bicarbonato calculado
- resumo
QUAL É A PRESSÃO PARCIAL DE UM GÁS?
a quantidade de gás em um sistema, incluindo sistemas biológicos, é definida pela pressão que ele exerce, tradicionalmente medida como a altura de uma coluna de mercúrio (mmHg). Assim, ao dizer que a pressão atmosférica é de 760 mmHg, queremos dizer que os gases (oxigênio, nitrogênio e dióxido de carbono) no ar que respiramos têm uma pressão combinada suficiente para suportar uma coluna padrão de mercúrio de 760 mm de altura.
esta pressão total é simplesmente a soma das pressões parciais de cada gás constituinte. Assim, uma vez que o ar compreende aproximadamente 20% de oxigénio, 79% de azoto e 0.03% de dióxido de carbono, a pressão parcial de oxigênio (pO2) no ar inspirado é de aproximadamente (20 x 760) / 100 = 152 mm hg e a pressão parcial de dióxido de carbono (pCO2) é (0,03 x 760) / 100 = 0.2 mm hg.
a unidade de pressão systeme internationale (SI), utilizada em laboratórios clínicos fora da América do Norte, é o kilopascal (kPa). O Fator de conversão 0.133 pode ser usado para converter mmHg em kPa.
SOLUBILIDADE E DIFUSÃO DE GASES
lei de Henry afirma que, no equilíbrio, a quantidade de gás dissolvido em um líquido é proporcional à pressão parcial desse gás, desde que a temperatura é constante:
de gás Dissolvido = pressão parcial (p) x coeficiente de solubilidade (S)
Onde S é a uma temperatura dependente constante para o gás em particular. O (s) coeficiente (s) de solubilidade para o dióxido de carbono à temperatura corporal é de 0, 23 mmol/L/kPa (ou 0, 03 mmol/mmHg). Assim, uma vez que o pCO2 arterial é aproximadamente 5.3 kPa (40 mmHg), a quantidade de CO2 dissolvido no sangue arterial (dCO2) é (5,3 x 0.23) ou 40 x 0,03) = a 1,2 mmol/L.
O movimento (difusão) de gases é determinado em grande parte por gradientes de concentração. O gás difunde-se de alta pressão parcial para baixa pressão parcial .
transporte de dióxido de carbono das células tecidulares para o pulmão
a viagem de dióxido de carbono (figura 1a) começa na mitocôndria das células tecidulares onde é produzido. Devido ao gradiente de concentração prevalecente, o dióxido de carbono difunde-se da mitocôndria (onde pCO2 é mais alto) através do citoplasma, fora da célula e para a rede capilar.
FIGURA 1a: CO2 nos tecidos
Clique para ampliar
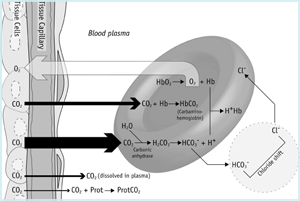
Um pouco de CO2, chegando no sangue a partir de células do tecido permanece fisicamente dissolvido no plasma de sangue (ver acima) e uma proporção ainda menor se liga ao NH2 (amino) terminal de grupos de proteínas plasmáticas, formando os denominados carbamino compostos. No entanto, a maioria difunde um gradiente de concentração para os glóbulos vermelhos.
um pouco destes restos dissolvidos no citoplasma da célula vermelha e alguns estão vagamente ligados a grupos aminoácidos terminais de hemoglobina reduzida formando carbamino-Hb. No entanto, a maior parte do dióxido de carbono que chega aos glóbulos vermelhos é rapidamente hidratada ao ácido carbónico pela isoforma dos glóbulos vermelhos da enzima anidrase carbónica. A pH fisiológico quase todos (≈96 %) deste ácido carbónico dissocia-se a bicarbonato e íons de hidrogénio:
equação 1:
![]()
os íons de hidrogênio são tamponados pela redução da hemoglobina e a maioria dos íons de bicarbonato passam da célula vermelha para o plasma em troca de íons cloreto (este chamado “desvio de cloreto” mantém a neutralidade eletroquímica). Do exposto resulta claramente que a maior parte do dióxido de carbono é transportado como bicarbonato (predominantemente no plasma sanguíneo), mas existem no total quatro modos de transporte de CO2 :
- 90 % é transportado como bicarbonato no plasma (65 %) e de glóbulos vermelhos (25 %)
- 5 % é transportado fisicamente dissolvido no plasma e glóbulos vermelhos citoplasma
- 5 % é transportado frouxamente ligado à hemoglobina nos glóbulos vermelhos e
> Total de dióxido de carbono do sangue de conteúdo é a soma desses quatro componentes.
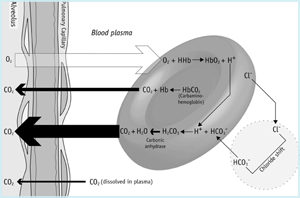
na microvasculatura dos pulmões (figura 1b), o gradiente de pressão parcial através da membrana alveolar determina que o CO2 dissolvido passa do sangue para os alvéolos. Esta perda de dióxido de carbono do sangue favorece a reversão das reações dos glóbulos vermelhos descritas acima.Deste modo, o bicarbonato passa do plasma para os glóbulos vermelhos, libertando íons de hidrogénio da hemoglobina, uma vez que é oxigenado. A reversão da reacção anidrase carbónica resulta na produção de CO2 que se difunde dos glóbulos vermelhos para o plasma e em diante para os alvéolos.
o sangue venoso misto que chega aos pulmões tem um teor total de CO2 de aproximadamente 23, 5 mmol/L (ou 52 mL/dL), enquanto o sangue arterial que sai dos pulmões tem um teor total de CO2 de 21, 5 mmol/L (48 mL / dL).
esta diferença arterio-venosa (2 mmol/L ou 4 mL/dL) representa a quantidade de CO2 adicionada ao sangue das células dos tecidos e perdida do sangue à medida que passa pela microvasculatura pulmonar, a ser eventualmente excretada do corpo no ar expirado.
FIGURA 1b: CO2 nos pulmões
Clique para ampliar
DIÓXIDO de CARBONO E do PH do SANGUE
O ácido potencial do CO2, devido à sua hidratação reação ao ácido carbônico (ver equação 1 acima), garante que a sua concentração no sangue é um dos principais determinantes do pH do sangue. À medida que aumenta a concentração de CO2, também aumenta a concentração de íon hidrogênio (H+). A regulação do CO2 no sangue, que corresponde à taxa de eliminação do CO2 no ar expirado à taxa de produção na mitocôndria de células de tecidos, essencial para manter o pH normal no sangue, é o negócio do sistema respiratório.
a taxa respiratória (controlada por quimiorreceptores sensíveis pCO2 localizados no tronco cerebral e na artéria carótida) é aumentada se o pCO2 estiver a subir e diminuir se o pCO2 estiver a diminuir. O aumento da frequência respiratória (respiração/min) resulta no aumento da taxa de eliminação de CO2 e diminuição da taxa respiratória promove a retenção de CO2.
a relação entre pH e dióxido de carbono é descrita por uma forma da equação de Henderson-Hasselbach (equação 2). Isto é derivado da aplicação da lei da ação da massa às reações de hidratação e dissociação descritas na equação 1 .
Equação 2:
![]()
onde
| pK/1 | = | ‘aparente’ constante de dissociação do ácido carbônico = 6.1 |
| = | concentração plasmática de bicarbonato (mmol/L) | |
| S | = | solubilidade coeficiente de CO2 a 37 oC (de 0,23 se pCO2 é medido, em kPa ou 0.03 se pCO2 medida em mmHg) |
| pCO2 | = | a pressão parcial de pCO2 (kPa mm hg ou) |
Como explicado anteriormente, o denominador na equação (S x pCO2) é a quantidade de dissolução de dióxido de carbono (dCO2) mmol/L.
removendo todas as constantes, a equação 2 pode ser simplificado para:
equação 3:
pH ∞ / pCO2
portanto, o pH do sangue depende da razão entre a concentração plasmática de bicarbonato (o componente metabólico) e o pCO2 (o componente respiratório). Assim, se o pCO2 aumenta sem um aumento equivalente no bicarbonato, o pH cai. Inversamente, se pCO2 cai sem uma queda equivalente em bicarbonato, o pH sobe.
a relação inversa mantém– se para a concentração de bicarbonato viz aumentou HCO3 – = pH aumentado; diminuição do bicarbonato = diminuição do pH.
bicarbonato é o principal tampão sanguíneo e a sua concentração em determinado momento reflecte o equilíbrio entre o que é produzido a partir do CO2 e o que é consumido em íons de hidrogénio tamponados (H+) (ver equação 1).
IN the LABORATORY-DEFINITION OF CO2 PARAMETERS
The CO2 parameters generated by the blood gas analyzer are:
- pressão Parcial de dióxido de carbono (pCO2) (kPa/mmHg)
- Plasma concentração de bicarbonato (HCO3-) (mmol/L)
- Plasma total concentração de dióxido de carbono (ctCO2) (mmol/L)
O último deles, ctCO2, também pode ser medida no plasma ou no soro por métodos químicos independente de sangue analisador de gás.
pressão parcial do dióxido de carbono pCO2
este parâmetro é uma medida da pressão exercida por essa pequena porção (≈ 5 %) de dióxido de carbono total no sangue que permanece no estado gasoso, “dissolvido” na fase aquosa do citoplasma e células sanguíneas. A medição é feita utilizando um eletrodo de pH específico de CO2 incorporado nos analisadores de gases sanguíneos.
In health pCO2 of arterial blood is maintained within the range 4.7-6.0 kPa (35-45 mmHg); pCO2 of venous blood is a little higher 5.6-6.8 kPa (41-51 mmHg).
concentração de bicarbonato (HCO3-)
esta é a quantidade de bicarbonato no volume unitário do plasma. Como já foi referido, esta é a forma em que a maioria do dióxido de carbono (90 %) é transportado no sangue. Este parâmetro não pode ser medido, mas é gerado pelo cálculo durante a análise dos gases sanguíneos. O cálculo utilizado é um rearranjo da equação 2:
Equação 4:
log = pH + log (S x pCO2) – pK/1
e depende de se ter valores de pH e pCO2, ambos os quais são medidos durante gasometria.
Teoricamente plasmáticas de bicarbonato é a diferença entre o total de CO2 (ctCO2) e a soma de todas as outras formas de CO2 no plasma, por exemplo, o CO2 dissolvido (dCO2), CO2 às proteínas plasmáticas (carbamino CO2) e o ácido carbônico (H2CO3).
Assim:
Plasma bicarbonato (mmol/L) =
ctCO2 – (dCO2 + carbamino-CO2 + H2CO3)
Na prática, uma vez carbamino-CO2 e H2CO3 são quantitativamente insignificante uma suposição é feita de que o total de CO2 é a soma de apenas bicarbonato e o CO2 dissolvido . Assim, o bicarbonato plasmático é efetivamente a diferença entre o CO2 total plasmático (ctCO2) e o CO2 dissolvido plasmático (dCO2).
Em saúde arterial plasma bicarbonato (como calculado durante a gasometria) é mantido dentro aproximada do intervalo de referência: 22-28 mmol/L. Venosa bicarbonato é um pouco maior: 24-30 mmol/L.
Em alguns laboratórios é feita uma distinção entre ‘real’ bicarbonato (o parâmetro descrito acima) e ‘padrão’ de bicarbonato. O bicarbonato padrão é um segundo parâmetro calculado e é a concentração plasmática de bicarbonato de sangue que foi equilibrada com gás de tensão normal de pCO2 (40 mmHg, 5, 3 kPa).
na saúde então a concentração real de bicarbonato é a mesma que a concentração padrão de bicarbonato porque em ambos os casos pCO2 é normal. Ao normalizar o pCO2, o componente respiratório do equilíbrio ácido-base, o bicarbonato padrão é uma medida apenas do componente metabólico e é, portanto, considerado útil para elucidar a causa de distúrbios complexos no equilíbrio ácido-base.
concentração total de dióxido de carbono no PLASMA (ctCO2)
esta é teoricamente a soma de todas as formas de dióxido de carbono no plasma. Ele não é medido durante a gasometria, mas – assim como o bicarbonato de – calculada, assumindo-se como acima, que o total de dióxido de carbono é a soma do bicarbonato e o CO2 dissolvido:
Desde plasma dCO2 mmol/L = (S x pCO2), ctCO2 é calculado assim :
plasma ctCO2 (mmol/L) =
plasma bicarbonato (mmol/L) + (S x pCO2) (mmol/L)
o CO2 Dissolvido (S x pCO2) contribui com aproximadamente 1.2 mmol/L para o CO2 total no plasma do sangue arterial (ver acima), de modo que o ctCO2 é cerca de 1, 2 mmol superior ao bicarbonato plasmático. O intervalo de referência ctCO2 é, portanto, aproximadamente 23-29 mmol / L para o sangue arterial.
note-se que assim como o valor calculado do bicarbonato gerado durante a análise dos gases sanguíneos depende da relação descrita na equação 2, também o valor calculado para o ctCO2 gerado durante a análise dos gases sanguíneos.
embora ctCO2 e bicarbonato forneçam informação clínica equivalente, na prática clínica é invariavelmente bicarbonato em vez de ctCO2 que é usado em conjunto com pH e pCO2 para avaliar o estado ácido-base. O valor clínico do ctCO2 calculado gerado durante a análise dos gases sanguíneos é, portanto, limitado.
métodos químicos para medir ctCO2
ao contrário do bicarbonato, que não pode ser medido, ctCO2 pode e o ensaio é normalmente um componente do perfil ureia e electrólito (U&e) do plasma/soro venoso. Uma vez que o U&e é ordenado muito mais frequentemente do que os gases sanguíneos arteriais, o ctCO2 medido pode ser a primeira indicação de perturbação na homeostase do dióxido de carbono (e, portanto, ácido-base).É prática corrente de alguns laboratórios clínicos referirem-se a este componente medido do perfil U&e como “bicarbonato plasmático”. Isto é errado porque os métodos químicos medem todo o CO2 libertado do plasma (ou soro) por adição de ácido forte ou, alternativamente, todos os bicarbonato produzido como resultado da adição de um alcalino forte ao plasma .Assim, inclui não só bicarbonato, mas também CO2 dissolvido e ácido carbónico. Se o plasma ou o soro utilizado nestes ensaios foram derivados do sangue arterial, então o ctCO2 seria teoricamente aproximado do valor calculado ctCO2 gerado durante a análise dos gases sanguíneos arteriais.
de facto, os Perfis U&e são realizados exclusivamente no plasma ou no soro recuperado do sangue venoso, de modo que existe uma diferença teórica inevitável de 1-2 mmol/L (ctCO2 medido > calculado ctCO2) devido a uma diferença arterio-venosa.
A diferença teórica entre a medida ctCO2 e calculado plasma bicarbonato é um pouco superior (medido ctCO2 > calculado plasma bicarbonato) porque, além de o artério-venosa diferença de 1-2 mmol/L, há mais de 1,5 mmol/L diferença devido à inclusão de CO2 dissolvido e o ácido carbônico na medida ctCO2.
no entanto, esta diferença pressupõe que nenhum dióxido de carbono dissolvido é perdido para a atmosfera antes da análise. Pode não ser esse o caso, uma vez que as amostras de U&e não são manuseadas anaeróbicamente.
Alguns têm argumentado que o termo ‘soro/plasma bicarbonato’ para medido ctCO2 é justificado em razão de que o normal práticas de laboratório está associado a uma inevitável perda de CO2 dissolvido do U&E amostra antes da análise, caso em que medida ctCO2 seria, teoricamente pelo menos, aproximada para calculado bicarbonato.
discordância entre o ctCO2 medido e o bicarbonato calculado
não obstante as ligeiras diferenças teóricas entre os valores medidos e calculados acima, existe uma aceitação geral da noção de que o ctCO2 medido gerado como parte de um perfil U&e é, para todos os efeitos clínicos, a mesma concentração plasmática de bicarbonato calculada durante a análise dos gases sanguíneos.Este facto reflecte-se na utilização do termo “bicarbonato plasmático” para descrever o ctCO2 medido.
a melhor evidência até à data de que os resultados medidos e calculados do bicarbonato podem, na prática, ser clinicamente permutáveis vem de um relatório muito recente da Clínica Mayo . Os autores deste relatório recuperaram 17.621 registros da concentração medida e calculada de bicarbonato para amostras coletadas simultaneamente dos mesmos pacientes durante 2006/7. A concentração de bicarbonato nesta enorme base de dados variou entre 5 e 49 mmol/L.
a diferença média (DP) entre os valores medidos e calculados foi de-0, 36 (1, 23 mmol/L) e para 98.5 % dos resultados das amostras emparelhadas encontravam-se num intervalo de 3 mmol/L entre si. Embora, como sugere o relatório Mayo, exista geralmente um acordo aceitável entre os dois parâmetros, não é de modo algum raro os resultados serem totalmente discordantes, com o ctCO2 medido diferindo do bicarbonato calculado em até 15 mmol/l.
numerosos estudos nos últimos quarenta anos procuraram estabelecer a frequência, a magnitude e a causa da discrepância entre o bicarbonato calculado e o ctCO2 medido.
An early focus of this work questioned the reliability of the bicarbonate calculation, which depends crucialmente on the constancy of pK/1 (see equation 4). Na verdade, esta não é uma verdadeira constante termodinâmica, mas uma constante de dissociação’ aparente ‘ determinada experimentalmente a partir da medição do pH, pCO2 e CO2 dissolvido usando a seguinte relação derivada da equação de Henderson-Hasselbach:
pK/1 = pH + log dCO2 – log
vários estudos revelaram uma variabilidade suficiente na pK/1, particularmente entre os doentes críticos, por erro clinicamente significativo no bicarbonato calculado. Por exemplo, num estudo, verificou-se que a pK/1 variava entre 5, 84 e 6, 29.
os autores calculam que desvios de pK / 1 6.1 desta magnitude resultariam em erros no bicarbonato calculado da ordem ± 60%. Outro descreve o caso de uma criança diabética em cetoacidose cuja pK/1 variou de 5, 49 a 6, 02 durante um período de sete horas.
Em um estudo de 79 crianças sendo cuidadas no pediátrica, unidade de terapia intensiva , 25 % foram encontrados para ter pK/1 fora do ‘normal’ intervalo 6.055-6.195 definido pelo estudo, e em três casos pK/1 > 6.3, com um ‘surpreendente’ valor de 7.11. Estes e outros relatórios de variabilidade clinicamente significativa na pK/1 foram contestados e a fiabilidade ou não do bicarbonato calculado continua a ser uma questão controversa e não resolvida.
the theoretical basis for the view that calculated bicarbonato is unreliable in critical illness has been set out by Flear . Uma abordagem igualmente teórica, acompanhada por uma riqueza de evidências experimentais, foi implantada por Mass et al para fazer o caso oposto em defesa do bicarbonato calculado.
Autores de estudos que não demonstraram clinicamente significativa variabilidade na pK/1 sugerem que a principal discordância entre o calculado de bicarbonato e medido ctCO2, ocasionalmente visto na prática clínica, é mais provável que o resultado de uma combinação de pré-as variáveis analíticas, analíticas diferença aleatório e erro analítico .
a medição do ctCO2 é particularmente propensa à variabilidade pré-analítica porque o sangue para U&e o perfil é universalmente recolhido e processado aerobicamente. As amostras podem ser deixadas por limpar durante horas antes da análise. Uma vez que o ar ambiente contém menos CO2 do que o sangue, há uma tendência para o CO2 dissolvido a ser perdido a partir da amostra. Estima-se que este valor reduza o CO2 medido à taxa de 6 mmol/h.
Por contraste calculado bicarbonato não está associado com o mesmo risco de pré-analíticas variação porque o sangue para o sangue, a análise dos gases, são rotineiramente amostrados de forma anaeróbica, e não há o mínimo de atraso (quase invariavelmente
Outro contributiva causa da discordância entre o medido e o valor calculado pode ser exemplo de diferença, desde que o sangue arterial é usado para calcular um valor e amostras de plasma ou soro são utilizados para medir um valor.
qualquer que seja a causa, os estudos continuam a demonstrar discórdia moderada mas clinicamente significativa entre os dois parâmetros entre os doentes criticamente . No entanto, como se para confirmar a natureza controversa do debate, o estudo mais recente de pacientes criticamente doentes fornece evidência de acordo aceitável entre o bicarbonato calculado e ctCO2 medido .
Apesar de que este último estudo, existe um corpo de opinião que, para pacientes criticamente doentes, pelo menos, pode ser prudente abandonar calculado bicarbonato em favor de medida ctCO2 , embora ele deve ser enfatizado que esta visão é controversa e pode ser que o impacto clínico das diferenças é limitado.
a evidência de acordo aceitável fornecida pelo estudo clínico Mayo muito grande não pode, infelizmente, ser usado no debate particular que se centra nos doentes críticos, porque a população de pacientes não foi definida.
dos dois parâmetros, o bicarbonato calculado tem a vantagem distinta de conveniência sobre o ctCO2 medido porque permite que todos os três parâmetros (pH pCO2 e bicarbonato) utilizados na avaliação da base ácida estejam disponíveis ao mesmo tempo a partir de uma única amostra.
não existe consenso na literatura sobre muitas das questões discutidas acima. Assim, ainda não é claro se há ou não discordância entre o CO2 medido e calculado, embora o equilíbrio de evidências tenha recentemente mudado em favor de nenhuma discordância pelo grande estudo da Clínica Mayo .
para aqueles que acreditam que o equilíbrio de evidências sugere que há discordância, há mais duas questões por resolver.
estes são: o significado clínico dessa discórdia e a causa dessa discordância. O Debate sobre a causa da discórdia centrou-se principalmente na questão de saber se a pKl1 varia significativamente entre os doentes e em que medida as diferenças pré-analíticas, as diferenças analíticas e os erros aleatórios contribuem para a discórdia.
finalmente, pelo menos um comentador questionou a necessidade clínica de bicarbonato calculado ou ctCO2 medido, sugerindo que o pH e o pCO2, por si só, permitem uma avaliação completa das perturbações ácido-base.
resumo
dióxido de carbono é um produto do metabolismo aeróbico das células que é transportado no sangue para os pulmões por excreção no ar expirado. Um pouco é transportado inalterado dissolvido em sangue, mas a maioria é transportado como bicarbonato.
a regulação da quantidade de dióxido de carbono no sangue, ou, mais precisamente, a regulação da relação entre a concentração de bicarbonato e a concentração de dióxido de carbono dissolvido, é essencial para a manutenção do pH sanguíneo (equilíbrio ácido-base normal).
a investigação clínica da perturbação ácido-base inclui a análise dos gases sanguíneos arteriais, um teste que gera três parâmetros de Estado do dióxido de carbono. Destes apenas um, pCO2, é realmente medido; os outros dois-bicarbonato de plasma e concentração total de dióxido de carbono – são derivados por cálculos a partir de pH medido e pCO2.
a validade destes cálculos foi questionada e há evidências conflitantes de que em alguns grupos de pacientes pode ser mais clinicamente confiável medir o dióxido de carbono total por métodos químicos, do que confiar em valores calculados.
esta última continua a ser uma questão altamente controversa que só pode ser finalmente resolvida através de um estudo mais aprofundado.