一般名:clonidineの塩酸塩
適量形態:タブレット
医学的に見直されるDrugs.com最終更新日は2020年10月1日です。
- 概要
- 副作用
- 投与量
- プロフェッショナル
- ヒント
- 相互作用
- 詳細
塩酸クロニジン-塩酸クロニジン錠
- マレックスファーマシューティカルズ株式会社
- 塩酸クロニジン錠説明
- クロニジン錠-臨床薬理学
- 薬物動態
- クロニジン錠の適応症と使用法
- 禁忌
- 警告
- 離脱
- 使用上の注意
- 一般
- 周術期使用
- 患者のための情報
- 薬物相互作用
- 毒性
- 発癌、変異誘発、不妊障害
- 妊娠
- 授乳中の母親
- 小児の使用
- 副作用
- 過剰投与
- 投与量および投与量
- 初回投与量
- 維持用量
- 腎機能障害
- クロニジン錠の供給方法
- PRINCIPAL DISPLAY PANEL
- PRINCIPAL DISPLAY PANEL
- PRINCIPAL DISPLAY PANEL
- PRINCIPAL DISPLAY PANEL
- PRINCIPAL DISPLAY PANEL
- 主な表示パネル
- クロニジンについての詳細
- 消費者リソース
- 専門的リソース
- 関連の処置ガイド
マレックスファーマシューティカルズ株式会社
塩酸クロニジン錠
塩酸クロニジン錠、USP経口降圧薬
0.1mg、0.2mgおよび0.3mg Rxのみ
処方情報
塩酸クロニジン錠説明
塩酸クロニジン、USPは3つの適量の強さで経口投与のためにタブレットとして利用できるアゴニストのhypotensive代理店:
0.1Mg、0.2MGおよび0.3Mg。 0.1mg錠剤は、遊離塩基の0.087mgに相当する。
不活性成分は、コロイド状二酸化ケイ素、コーンスターチ、リン酸カルシウム二塩基性、ヒドロキシプロピルセルロース、微結晶セルロース、乳糖一水和物およびステアリン酸マグネシウムである。 また、0.1mg錠剤はFD&C赤色40号を含有し、0.2mg錠剤および0.3mg錠剤は、それぞれFD&C黄色6号を着色添加剤として含有する。
塩酸クロニジンはイミダゾリン誘導体であり、メソマー化合物として存在する。 化学名は2-(2,6-ジクロロフェニルアミノ)-2-イミダゾリン塩酸塩です。 以下は構造式である:
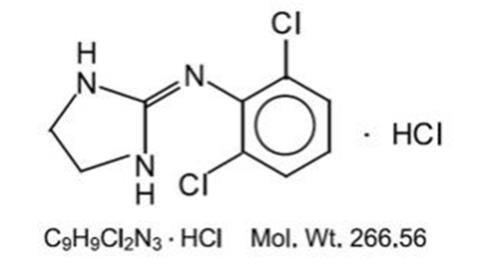
clonidineの塩酸塩は水およびアルコールの無臭、苦い、白い、結晶の物質のsolubleです。
クロニジン錠-臨床薬理学
クロニジンは脳幹のα-アドレナリン受容体を刺激する。 この作用は、中枢神経系からの交感神経流出の減少、および末梢抵抗、腎血管抵抗、心拍数および血圧の減少をもたらす。 クロニジン塩酸塩錠剤は比較的急速に作用する。 患者の血圧は、経口投与後30〜60分以内に低下し、最大減少は2〜4時間以内に起こる。 腎臓の血の流れおよび糸球体のろ過率は本質的に変わらない残ります。 正常な状態の反射はそのままです;従って、orthostatic徴候は穏やか、まれです。
ヒトにおける塩酸クロニジンを用いた急性研究では、末梢抵抗の変化なしに仰臥位における心拍出量の中等度の減少(15%から20%)が示されている: 45’傾きで心拍出量のより小さい減少および周辺抵抗の減少がある。 長期治療中、心拍出量は対照値に戻る傾向があり、末梢抵抗は減少したままである。 脈拍数の減速はclonidineを与えられたほとんどの患者で観察されましたが、薬剤は練習への正常な血行力学の応答を変えません。
降圧効果に対する耐性が一部の患者で発症する可能性があり、治療の再評価が必要である。
患者を対象とした他の研究では、血漿レニン活性の低下およびアルドステロンおよびカテコールアミンの排泄の証拠が提供されている。 クロニジンの降圧効果に対するこれらの薬理学的作用の正確な関係は完全には解明されていない。
クロニジンは小児と成人の両方で成長ホルモンの放出を急性に刺激するが、長期使用では慢性的な成長ホルモンの上昇を生じない。
薬物動態
クロニジンの薬物動態は、100~600mcgの範囲で用量比例する。 経口投与のclonidineの絶対生物学的利用能は70%から80%です。 ピーク血しょうclonidineのレベルはおよそ1から3時間に達成されます。
静脈内投与後、クロニジンは約20分の分布半減期と12から16時間の範囲の除去半減期を有する二相性性素因を示す。 重度の腎機能障害を有する患者では、半減期は41時間まで増加する。 クロニジンは胎盤の障壁を交差させます。 ラットの血頭脳の障壁を交差させることを示しました。
経口投与後、吸収された用量の約40%から60%が未変化薬物として尿中に24時間で回収される。 吸収された用量の約50%が肝臓で代謝される。 食物も患者の人種もクロニジンの薬物動態に影響を与えない。
正常な排泄機能を有する患者では、降圧効果は約0.2ng/mLと2.0ng/mLの血漿濃度で達成される。 血漿レベルのさらなる上昇は、降圧効果を増強しない。
クロニジン錠の適応症と使用法
クロニジン塩酸塩錠、USPは高血圧の治療に適応されます。 クロニジン塩酸塩錠剤、USPは、単独で、または他の降圧剤と同時に使用することができる。
禁忌
塩酸クロニジン錠は、クロニジンに対する過敏症が知られている患者には使用しないでください(注意事項を参照)。
警告
離脱
患者は医師に相談せずに治療を中止しないように指示されるべきである。 クロニジンの処置の突然の停止は緊張、激越、頭痛および振戦のような徴候で、場合によっては、血圧の急速な上昇および血しょうの上げられたカテコールアミンの集中に先行して伴われるか、または起因しました。 従ってクロニジン療法の停止へのそのような反作用の可能性は大量服用の管理の後でより大きいようですまたは付随のベータ遮断薬の処置および特 高血圧性脳症、脳血管障害および死亡のまれな例は、クロニジンの離脱後に報告されている。 クロニジンによる治療を中止する場合、医師は禁断症状を避けるために2-4日にわたって徐々に用量を減らすべきである。
クロニジン療法の中止後の血圧の過度の上昇は、塩酸クロニジン経口投与またはフェントラミン静脈内投与によって逆転させることができる。 Β遮断薬とクロニジンを同時に投与されている患者で治療を中止する場合は、クロニジンの徐々の中止の数日前にβ遮断薬を中止する必要があります。
子供たちは一般的に嘔吐につながる胃腸疾患を持っているため、薬物を服用することができないことに起因する高血圧のエピソードに特に影響を受けやすくなる可能性があります。
使用上の注意
一般
経皮クロニジンに対する局所的な接触感作を発症した患者では、経皮クロニジンの継続または経口クロニジン塩酸塩療法の置換が、全身性皮膚発疹の発症と関連している可能性がある。
経皮クロニジンに対するアレルギー反応を発症する患者では、経口クロニジン塩酸塩の置換はまた、アレルギー反応(全身性発疹、蕁麻疹、または血管性浮腫を含む)を誘発する可能性がある。)
クロニジンの交感神経溶解作用は、特に他の交感神経溶解薬を服用している患者では、洞結節機能不全および房室(AV)ブロックを悪化させる可能性がある。 クロニジンを服用中にIVアトロピン、IVイソプロテレノールおよび一時的な心臓ペーシングを必要とする重度の徐脈を発症した伝導異常および/または他のsympatholytic薬を服用している患者の市販後の報告がある。
褐色細胞腫による高血圧症では、塩酸クロニジン錠の治療効果は期待できません。
周術期使用
塩酸クロニジン錠の投与は、手術後四時間以内に継続し、その後できるだけ早く再開する必要があります。 血圧は外科の間に注意深く監視され、血圧を制御する付加的な手段は必要であれば利用できるべきです。
患者のための情報
患者は彼らの医者の助言なしでclonidineの塩酸塩のタブレット療法の中断に対して警告されるべきです。
患者はクロニジンの使用により鎮静効果、めまい、または宿泊障害を経験する可能性があるため、車両の運転や家電製品や機械の操作などの活動に従事することに注意してください。 また、この鎮静効果は、アルコール、バルビツール酸塩、または他の鎮静薬の併用によって増加する可能性があることを患者に知らせる。
コンタクトレンズを着用している患者は、塩酸クロニジン錠による治療は目の乾燥を引き起こす可能性があることに注意する必要があります。
薬物相互作用
クロニジンは、アルコール、バルビツール酸塩または他の鎮静薬のCNS抑うつ効果を増強する可能性があります。 塩酸クロニジンを投与されている患者も三環系抗うつ薬を服用している場合、クロニジンの降圧効果が低下し、クロニジン用量の増加が必要になる クロニジンを受けている患者も神経弛緩薬を服用している場合、起立性調節障害(例えば、起立性低血圧、めまい、疲労)が誘発されるか、または悪化するこ
ジギタリス、カルシウムチャネル遮断薬、β遮断薬など、洞結節機能またはAV結節伝導に影響を与えることが知られている薬剤と同時にクロニジンを受けている患者の心拍数を監視する。 入院およびペースメーカーの挿入に終って湾曲の徐脈はdiltiazemまたはverapamilと同時にclonidineの使用と関連付けて報告されました。
アミトリプチリンとクロニジンの組み合わせは、ラットの角膜病変の発現を増強する(毒物学を参照)。
アルコール性せん妄状態の患者の観察に基づいて、クロニジンの高静脈内投与量は、ハロペリドールの高静脈内投与量の不整脈発生能(QT延長、心室細動)を増加させる可能性があることが示唆されている。 クロニジン経口錠剤の因果関係および関連性は確立されていない。
毒性
経口クロニジン塩酸塩を用いたいくつかの研究では、6ヶ月以上治療されたアルビノラットで自発的な網膜変性の発生率と重症度の用量依存的な増加が見られた。 イヌおよびサルにおける組織分布の研究では、脈絡膜中のクロニジンの濃度を示した。
ラットに見られる網膜変性を考慮して、クロニジン療法の開始前および開始後に定期的に908人の患者の臨床試験中に眼検査を行った。 これらの353人の908人の患者では、目の検査は24か月またはより長い期間にわたって遂行されました。 眼の一部の乾燥を除いて,薬物関連の異常眼科所見は記録されず,網膜電図や黄斑眩暈などの特殊な検査では網膜機能は変化しなかった。
アミトリプチリンと組み合わせて、塩酸クロニジン投与は5日以内にラットの角膜病変の発症につながった。
発癌、変異誘発、不妊障害
クロニジンの慢性食餌療法投与は、それぞれラット(132週)またはマウス(78週)に対して発癌性がなく、最大推奨日用量のmg/kg(9または6回のMG/m2ベースでMRDHD)で46または70倍まで投与された。 変異原性のためのエイムズ試験またはクラスト原性のためのマウス小核試験で遺伝毒性の証拠はなかった。
雄または雌のラットの生殖能力は、150mcg/kg(約3倍のMRDHD)と高いクロニジン用量によって影響されなかった。 別の実験では、雌ラットの繁殖力は、500〜2000mcg/kg(mg/kgベースで経口MRDHDの10〜40倍、mg/m’ベースでMRDHDの2〜8倍)の用量レベルで影響を受けるように見えた。)
妊娠
催奇形性効果:妊娠カテゴリー C.クロニジン塩酸塩錠剤の経口最大推奨一日ヒト用量(MRDHD)の約3倍までの用量でウサギで行われた生殖研究は、ウサギの催奇形性または胚毒性の可能性の証拠をもたらさなかった。 ラットでは、しかし、クロニジンの1/3経口MRDHD(1/15mg/m2ベースでMRDHD)として低い用量は、ダムが交配する前に2ヶ月から継続的に治療された研究では、再吸収 ダムが妊娠6日目から15日目に治療されたとき、再吸収の増加は、同時にまたはより高い用量レベル(経口MRDHDの3倍まで)での治療と関連していなかった。
再吸収の増加は、はるかに高い用量レベル(mg/kgベースで経口MRDHDの40倍)で観察された; 妊娠1〜1 4日目に処置したマウスおよびラットにおいて、MRDHDをmg/m2ベースで4〜8倍にした(この試験で用いた最低用量は5 0 0mcg/kgであった)。
妊婦を対象とした十分に制御された研究は実施されていない。 クロニジンは胎盤障壁を横切る(CLINICAL PHARMACOLOGY,,Pharmacokineticsを参照)。 動物の生殖研究は必ずしも人間の反応を予測するものではないため、この薬は明らかに必要な場合にのみ妊娠中に使用する必要があります。
授乳中の母親
塩酸クロニジンは母乳中に排泄されるため、授乳中の女性に塩酸クロニジン錠剤を投与する場合は注意が必要です。
小児の使用
小児患者の安全性と有効性は、適切かつ十分に制御された試験では確立されていません(警告、撤退を参照)。
副作用
ほとんどの副作用は軽度であり、治療を続けると減少する傾向があります。 最も頻繁に(用量に関連しているように見える)は口渇であり、約40の100人の患者に発生する。; 眠気、約33in100;めまい、約16in100;便秘および鎮静、それぞれ約10in100。
塩酸クロニジン錠を投与された患者では、以下の副作用の頻度が低いことも報告されていますが、多くの場合、併用薬を投与されており、因果関係は確立されていません。
体全体:疲労、発熱、頭痛、蒼白、衰弱、離脱症候群。 また、クームスの試験が弱く陽性であり、アルコールに対する感受性が増加したと報告されている。
: 徐脈、うっ血性心不全、心電図異常(すなわち、洞結節停止、接合性徐脈、高度AVブロックおよび不整脈)、起立性症状、動悸、レイノー現象、失神、および頻脈。
副鼻腔徐脈および房室ブロックの症例が、付随するジギタリスの使用の有無にかかわらず報告されている。
中枢神経系: 動揺、心配、せん妄、妄想の認識、幻覚(を含む視覚および聴覚)、不眠症、精神不況、緊張、他の行動の変更、感覚異常、落ち着きのなさ、睡眠障害および鮮やかな夢か悪夢。
皮膚科:脱毛症、血管神経性浮腫、蕁麻疹、そう痒症、発疹、蕁麻疹。<551><2781>胃腸:腹痛、食欲不振、便秘、肝炎、倦怠感、肝機能検査における軽度の一過性異常、悪心、耳下腺炎、偽閉塞(結腸偽閉塞を含む)、唾液腺痛、嘔吐。
尿生殖器:性的活動の減少、排尿困難、勃起不全、性欲の喪失、夜間頻尿、および尿閉。
血液学的:血小板減少症。
代謝:女性化乳房、血中グルコースまたは血清クレアチンホスホキナーゼの一時的な上昇、および体重増加。
筋骨格系:脚のけいれんおよび筋肉または関節の痛み。
Oro-otolaryngeal:鼻粘膜の乾燥。
眼科:調節障害、視力のぼけ、目の灼熱感、涙液漏れの減少、目の乾燥。
過剰投与
高血圧は早期に発症することがあり、その後に低血圧、徐脈、呼吸抑制、低体温、眠気、反射の減少または不在、衰弱、過敏症および縮瞳が続く CNSうつ病の頻度は、成人よりも子供の方が高い可能性があります。 大量の過剰摂取は、可逆的な心臓伝導欠損または不整脈、無呼吸、昏睡および発作を引き起こす可能性がある。 過剰摂取の徴候および症状は、一般的に暴露後30分から2時間以内に起こる。 クロニジンの0.1mgは子供の毒性の印を作り出しました少し。
クロニジンの過剰投与に対する特異的な解毒剤はない。 クロニジンの過剰投与はCNSの不況の急速な開発で起因するかもしれません;従って、ipecacシロップとの嘔吐の誘導は推薦されません。 胃洗浄は最近のおよび/または大きいingestionsの後で示されるかもしれません。 活性炭および/またはカタルシス剤の投与は有益であり得る。 支持療法には、徐脈のための硫酸アトロピン、静脈内液および/または低血圧のための昇圧剤および高血圧のための血管拡張剤が含まれ得る。 Naloxoneはclonidine誘発の呼吸の不況、低血圧や昏睡状態の管理のための有用な付加物であるかもしれません;naloxoneの管理が逆説的な高血圧で時折起因したので血圧
トラゾリン投与は一貫性のない結果をもたらしており、第一選択療法としては推奨されていない。 透析はかなりclonidineの除去を高めて本当らしくないです。
これまでに報告された最大の過剰摂取には、塩酸クロニジン粉末100mgを摂取した28歳の男性が関与していました。 この患者は高血圧を発症し,低血圧,徐脈,無呼吸,幻覚,セミコーマ,および早期心室収縮が続いた。 患者は集中治療後に完全に回復した。 血漿クロニジンレベルは、1時間後に60ng/mL、1.5時間後に190ng/mL、2時間後に370ng/mL、および5.5および6.5時間後に120ng/mLであった。 マウスおよびラットでは、クロニジンの経口LD50はそれぞれ206および465mg/kgである。
投与量および投与量
成人
塩酸クロニジン錠剤の投与量は、患者の個々の血圧応答に応じて調整する必要があります。 以下は、その管理への一般的なガイドです。
初回投与量
0.1mg錠一日二回(朝と就寝時)。 年配の患者はより低い最初の線量から寄与するかもしれません。
維持用量
所望の応答が達成されるまで、必要に応じて週間隔で0.1mg/日のさらなる増分を行うことができる。 就寝時に経口日用量の大部分を摂取すると、口渇や眠気の一時的な調整効果が最小限に抑えられる可能性があります。 最も一般に用いられる治療上の線量は分けられた線量で与えられる1日あたりの0.2mgから0.6mgまで及びました。
の研究では、2.4mgが最大有効日用量であることが示されていますが、これほど高い用量はめったに採用されていません。
腎機能障害
腎機能障害を有する患者は、より低い初期用量の恩恵を受ける可能性がある。 患者は慎重に監視する必要があります。 日常的な血液透析中に最小限の量のクロニジンのみが除去されるので、透析後に補足的なクロニジンを与える必要はない。
クロニジン錠の供給方法
塩酸クロニジン錠、USPは以下のように供給されています:
0.1mg:ピンクの錠剤、 “の形をしています。 NDC10135-0708-01(ボトル100)
“の形をしています。 NDC10135-0708-01(ボトル100)
NDC10135-0708-05(ボトル500)
0.2mg:オレンジ色の錠剤で、「 」の形をしています。 NDC10135-0709-01(100本入)
」の形をしています。 NDC10135-0709-01(100本入)
NDC10135-0709-05(500本入)
0.3mg: “ “の形をした明るいオレンジ色のタブレット。 NDC10135-0710-01(ボトル100)
“の形をした明るいオレンジ色のタブレット。 NDC10135-0710-01(ボトル100)
NDC10135-0710-05(ボトル500)
25°C(77°F)で保管し、15°C-30°C(59°F-86°F)までの遠足を許可します。 堅く、耐光性の容器で分配して下さい。
Marlex Pharmaceuticals,Inc.
Marlex Pharmaceuticals,Inc.
Marlex Pharmaceuticals,Inc.
ニューキャッスル、デ19720
Rev. 9/20 MP
PRINCIPAL DISPLAY PANEL
NDC 10135-0708-01
CLONIDINE
HYDROCHLORIDE
TABLETS, USP
Rx Only
100 Tablets

PRINCIPAL DISPLAY PANEL
NDC 10135-0708-05
CLONIDINE
HYDROCHLORIDE
TABLETS, USP
0.1mg
Rx Only
500 Tablets

PRINCIPAL DISPLAY PANEL
NDC 10135-0709-01
CLONIDINE
HYDROCHLORIDE
TABLETS, USP
0.2mg
Rx Only
100 Tablets

PRINCIPAL DISPLAY PANEL
NDC 10135-0709-05
CLONIDINE
HYDROCHLORIDE
TABLETS, USP
0.2mg
Rx Only
500 Tablets

PRINCIPAL DISPLAY PANEL
NDC 10135-0710-01
CLONIDINE
HYDROCHLORIDE
TABLETS, USP
0.3mg
Rxのみ
100錠

主な表示パネル
NDC10135-0710-05
クロニジン
塩酸塩
錠剤、USP
0.3mg
Rxのみ
500錠

改訂版: 10/2020
| CLONIDINE HYDROCHLORIDE clonidine hydrochloride tablet |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| 塩酸クロニジン 塩酸クロニジン錠 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| 塩酸クロニジン 塩酸クロニジン錠 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
ラベラー-マーレックス-ファーマシューティカルズ株式会社(782540215)
クロニジンについての詳細
- 副作用
- 妊娠中または授乳中
- 投与量情報
- 患者のヒント
- 薬物画像
- 薬物相互作用
- 代替案の比較
- サポートグループ
- 価格&クーポン
- 619レビュー
- 薬物クラス:抗Adrenergicエージェント、集中作用
- Fdaアラート(1)
消費者リソース
- 患者情報
- 。.. +5その他
専門的リソース
- 処方情報
- クロニジン(専門的な患者のアドバイス)
- クロニジン(FDA)
- クロニジン延長放出錠(FDA)
- クロニジン注射(FDA)
- クロニジン注射(FDA)
- クロニジン注射(FDA)
- クロニジン注射(FDA)
- クロニジン注射(FDA)
- クロニジン注射(FDA)
- クロニジン注射(FDA)
- クロニジンパッチ(fda)
他のブランドcatapres、kapvay、catapres-Tts、Duraclon、Nexiclon Xr
関連の処置ガイド
- 心配
- Adhd
- アルコール回収
- 心房
- .. +19より
医療免責事項