一般名:クリンダマイシンリン酸
剤形:膣クリーム
医学的にレビュー Drugs.com最終更新日は2020年3月1日です。
- 概要
- 副作用
- 投与量
- プロフェッショナル
- 相互作用
- 詳細
- 膣内使用のみ眼科、皮膚、または経口使用には使用できません
- クレオシン膣クリーム-臨床薬理学
- 作用機序
- 薬物動態
- 微生物学
- 作用機序
- 耐性
- 抗菌活性
- Cleocinの腟のクリームのための徴候そして使用法
- 禁忌
- 警告
- 使用上の注意
- 一般
- 患者のための情報
- 薬物相互作用
- 発癌、突然変異誘発、生殖能力の障害
- 妊娠
- 授乳中の母親
- 小児使用
- 高齢者の使用
- 副作用
- 臨床試験
- 過量投与
- クレオシン膣クリームの投与量および投与
- クレオシン膣クリームの供給方法
- 臨床試験
- 使用方法
- 主な表示パネル-40gチューブラベル
- 主要な表示パネル-40gの管のカートン
- クレオシン膣(クリンダマイシン局所)についての詳細)
- 消費者資源
- プロフェッショナルリソース
- その他の製剤
- 関連治療ガイド
膣内使用のみ眼科、皮膚、または経口使用には使用できません
クリンダマイシンリン酸は、親抗生物質リンコマイシンの7(R)-ヒドロキシル基の7(S)-クロロ-置換によって生成される半合成抗生物質の水溶性エ リン酸クリンダマイシンの化学名はメチルです7-chloro-6,7,8-trideoxy-6-(1-methyl-trans-4-propyl-L-2-pyrrolidinecarboxamido)-1-thio-L-threo-α–D-galacto-オクトピラノシド2-(リン酸二水素)。 それに504.96の分子量があり、分子方式はC18H34Cln2O8Psです。 構造式は以下の通りである。:
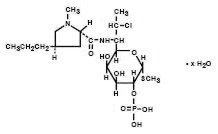
Cleocinの腟のクリーム2%は、グラムごとの20mgのクリンダマイシンと同等の集中で2%のクリンダマイシンの隣酸塩、USPを、含んでいる半固体、白いクリームです。 クリームのpHは3.0と6.0の間です。 クリームにはベンジルアルコール、セトステアリルアルコール、混合脂肪酸エステル、鉱油、ポリソルベート60、プロピレングリコール、精製水、モノステアリン酸ソルビタン、ステアリン酸も含まれています。
各アプリケーター5グラムの膣クリームには、約100mgのクリンダマイシンリン酸が含まれています。
クレオシン膣クリーム-臨床薬理学
作用機序
クリンダマイシンは抗菌薬です(微生物学を参照)。
薬物動態
100mgのクリンダマイシンリン酸膣クリーム2%を一日一回膣内投与し、6人の健康な女性ボランティアに7日間投与した後、投与用量の約5%(0.6%から11%の範囲)が全身的に吸収された。 最初の日に観察されたピーク血清クリンダマイシン濃度は平均1 8ng/ml(4〜4 7ng/mlの範囲)であり、7日目には平均2 5ng/ml(6〜6 1ng/mlの範囲)であった。 これらのピーク濃度は、投与後約1 0時間(4〜2 4時間の範囲)に達成された。
100mgのクリンダマイシンリン酸膣クリーム2%を一日一回膣内投与し、細菌性膣炎の女性5人に7日間連続して投与した後、吸収は健康な女性よりも遅く、可変性は低かった。 用量の約5%(2%〜8%の範囲)を全身的に吸収した。 最初の日に観察されたピーク血清クリンダマイシン濃度は平均1 3ng/ml(6〜3 4ng/mlの範囲)であり、7日目には平均1 6ng/ml(7〜2 6ng/mlの範囲)であった。 これらのピーク濃度は、投与後約1 4時間(4〜2 4時間の範囲)に達成された。
クリンダマイシンリン酸膣クリーム2%の繰り返し膣投与後、クリンダマイシンの全身蓄積はほとんどまたは全くなかった。 全身半減期は1.5-2.6時間であった。
微生物学
作用機序
クリンダマイシンは、リボソームの23Sサブユニットの50S RNAに結合することにより、細菌のタンパク質合成を阻害する。 クリンダマイシンは主に静菌性である。 リン酸クリンダマイシンはin vitroでは不活性であるが、in vivoでの迅速な加水分解はそれを活性クリンダマイシンに変換する。
耐性
クリンダマイシンに対する耐性は、ほとんどの場合、リボソーム上の標的部位の修飾によって引き起こされ、通常はRNAの点突然変異によるRNA塩基の化学的修飾によって、または場合によってはタンパク質中で引き起こされる。 交差抵抗はある有機体のlincosamides、マクロライドおよびstreptogramins B間で示されました。 クリンダマイシンとリンコマイシンの間で交差抵抗が実証されている。
抗菌活性
細菌性膣炎の診断を確立するために、細菌の培養および感受性試験は日常的に行われていない(適応症および使用法を参照)。、またはmycoplasma hominisは、定義されていない。
以下のin vitroデータが入手可能であるが、その臨床的意義は不明である。 クリンダマイシンは細菌のvaginosisと関連付けられるために報告される次の有機体のほとんどの隔離集団に対して生体外で活動的です:
- Bacteroides spp.
- Gardnerella vaginalis
- Mobiluncus spp.
- Mycoplasma hominis
- Peptostreptococcus spp.
Cleocinの腟のクリームのための徴候そして使用法
Cleocinの腟のクリーム2%は細菌のvaginosis(以前Haemophilusのvaginitis、Gardnerellaのvaginitis、非特異的なvaginitis、Corynebacteriumのvaginitis、または嫌気性のvaginosisと言われる)の処置で、示されます。 Cleocinの腟のクリーム2%が第2および第3学期の間に非妊婦および妊婦を扱うのに、使用することができます。 (臨床研究を参照してください。)<1333><7211>注: この徴候の目的のために、細菌の膣炎の臨床診断は通常(a)4.5より大きいのpHがあり、(b)10%KOHの解決と混合されたとき”魚のような”アミン臭気を出し、(c)顕微鏡検査の糸口の細胞を含んでいる同質なおり分泌物の存在によって定義されます。 細菌性膣炎の診断と一致するグラムの染色結果には、(a)著しく減少したか存在しない乳酸菌の形態、(b)Gardnerella形態型の優位性、および(c)存在しないか、または少数の白血球が含まれる。
一般的に外陰膣炎に関連する他の病原体、例えば、Trichomonas vaginalis、Chlamydia trachomatis、n.gonorrhoeae、Candida albicans、および単純ヘルペスウイルスは除外されるべきである。
禁忌
クレオシン膣クリーム2%は、クリンダマイシン、リンコマイシン、またはこの膣クリームのいずれかの成分に対する過敏症の病歴を有する個人には禁忌である。 クレオシン膣クリーム2%は、局所腸炎、潰瘍性大腸炎、または”抗生物質関連”大腸炎の病歴を有する個人にも禁忌である。
警告
偽膜性大腸炎は、クリンダマイシンを含むほぼすべての抗菌剤で報告されており、重症度は軽度から生命を脅かすものまでの範囲である可能性 経口的および非経口的に投与されたクリンダマイシンは、致命的に終了する可能性のある重度の大腸炎と関連している。 下痢、血まみれの下痢および大腸炎(を含むpseudomembranous大腸炎)はclindamycinの項目(皮膚および腟の)公式と同様、口頭でおよび非経口的に管理されたclindamycinの使用と、報告されました。 したがって、クリンダマイシン投与後に下痢を呈する患者では、クリンダマイシン投与量の約5%が膣から全身的に吸収されるため、膣経路で投与されていても、この診断を考慮することが重要である。
抗菌剤による治療は、結腸の正常な細菌叢を変化させ、クロストリジウムの過増殖を可能にする可能性がある。調査はClostridiumのdifficileによって作り出される毒素が「抗生物質準の」大腸炎の第一次原因であることを示します。
偽膜性大腸炎の診断が確立された後、治療措置を開始すべきである。 偽膜性大腸炎の軽度の症例は、通常、薬物単独の中止に応答する。 中等度から重度の症例では,クロストリジウム-ディフィシル大腸炎に対して臨床的に有効な抗菌薬による体液や電解質の管理,蛋白質の補給,抗菌薬による治療に配慮すべきである。
偽膜性大腸炎の症状の発症は、抗菌治療中または抗菌治療後に起こることがあります。
使用上の注意
一般
クレオシン膣クリーム2%には、火傷や目の刺激の原因となる成分が含まれています。 偶発的に目に接触した場合は、多量の冷たい水道水で目をすすいでください。
クレオシン膣クリーム2%の使用は、膣内の非感受性生物の過増殖を引き起こす可能性があります。 3日間の治療を受けた600人の非妊娠女性を含む臨床研究では、カンジダ-アルビカンスは、症状または培養のいずれかで、患者の8.8%で検出された。 患者の9%において、膣炎が記録された。 1325日間の治療を受けた非妊娠女性を含む臨床研究では、カンジダアルビカンスは、患者の10.5%において、症候的または文化によって検出された。 膣炎は患者の10.7%に記録された。 180日間の治療を受けた妊婦では、カンジダ-アルビカンスは、患者の13.3%において、症候的または培養によって検出された。 患者の7.2%において、膣炎が記録された。 ここで報告されているように、カンジダ-アルビカンスには、膣moniliasisおよびmoniliasis(体全体)という用語が含まれています。 膣炎には、外陰膣障害、外陰膣炎、膣分泌物、trichomonal vaginitis、およびvaginitisという用語が含まれます。
患者のための情報
患者は、この製品の治療中に膣性交に従事したり、他の膣製品(タンポンやdouchesなど)を使用しないように指示する必要があります。
このクリームには、コンドームや膣避妊用ダイアフラムなどのラテックスやゴム製品を弱める可能性のある鉱油が含まれていることもお勧めします。 したがって、クレオシン膣クリーム2%での治療後72時間以内にそのような製品を使用することは推奨されません。
薬物相互作用
全身性クリンダマイシンは、他の神経筋遮断剤の作用を増強する可能性のある神経筋遮断特性を有することが示されている。 したがって、そのような薬剤を受けている患者には注意して使用する必要があります。
発癌、突然変異誘発、生殖能力の障害
発癌性を評価するためにクリンダマイシンを用いた動物の長期研究は行われていない。
実施された遺伝毒性試験には、ラット小核試験およびエイムズ試験が含まれていた。 両方のテストは陰性であった。 最大300mg/kg/日(mg/m2に基づくヒト曝露の31倍)で経口投与されたラットの生殖能力研究は、生殖能力または交配能力に影響を及ぼさないことを明らかにした。
妊娠
催奇形性効果
妊婦を対象とした臨床試験では、第二および第三学期のクリンダマイシンの全身投与は、先天性異常の頻度の増加と関連していない。
クリンダマイシン膣クリームは、明確に必要とされ、利点がリスクを上回る場合にのみ、妊娠の最初の学期の間に使用する必要があります。 妊娠の最初の学期の間に妊娠中の女性には適切で十分に制御された研究はありません。
クレオシン膣クリーム2%は妊娠後期の妊婦で研究されています。 7日間扱われた女性では異常な労働は偽薬を受け取った患者の0.5%と比較されるクリンダマイシンの腟のクリーム2%を受け取った患者の1.1%で報告
ラットおよびマウスにおいて、クリンダマイシンの経口および非経口用量を用いて600mg/kg/日まで(それぞれ62回および25回、体表面積に基づく最大ヒト曝露)、クリンダマイシンによる胎児への害の証拠は明らかにされていない。 口蓋裂は、200mg/kg/日(体表面積変換に基づいて推奨用量の約10倍)でクリンダマイシンで腹腔内に処理された一つのマウス株から胎児で観察された。 この効果は他のマウス株または他の種では観察されなかったので、効果は株特異的であり得る。
授乳中の母親
クリンダマイシンは、ヒトの母乳中に0.5-3.8mcg/mL未満の範囲で、経口150mgから静脈内600mgの用量で現れるという母乳サンプリング それはクリンダマイシンが腟に管理されたクリンダマイシンの隣酸塩の使用に続く人間の母乳で排泄されるかどうか知られていません。
クリンダマイシンは、授乳中の乳児の胃腸内細菌叢に悪影響を及ぼす可能性があります。 クリンダマイシンが授乳中の母親によって必要とされる場合、母乳育児を中止する理由ではありませんが、代替薬が好ましい場合があります。 下痢、カンジダ症(ツグミ、おむつかぶれ)、またはまれに、抗生物質関連大腸炎の可能性を示す便中の血液などの胃腸細菌叢に悪影響を及ぼす可能性があ
母乳育児の発達上および健康上の利点は、母親のクリンダマイシンに対する臨床的必要性およびクリンダマイシンまたは根底にある母親の状態
小児使用
小児患者における安全性と有効性は確立されていない。
高齢者の使用
クレオシン膣クリームの臨床研究2%には、65歳以上の被験者が若年者と異なる反応を示すかどうかを判断するのに十分な数が含まれていませんでした。 他の報告された臨床経験は、高齢者と若年患者の間の反応の違いを同定していない。
副作用
臨床試験
非妊娠女性
非妊娠女性を対象とした臨床試験では、クレオシン膣クリームによる治療を受けた600人の患者の1.8%が2%3日間、1325人の患者の2.7%が7日間の治療を受けたが、薬物関連の有害事象により治療を中止した。 関連する、おそらく関連する、おそらく関連する、または膣投与されたクリンダマイシンリン酸膣クリーム2%との未知の関係であると判断された医学的事象は、20.7%の3日間の治療を受けている患者の21.3%の7日間の治療を受けている患者のために報告された。 クリンダマイシンリン酸膣クリーム2%を受けている患者の≥1%で発生する事象を表1に示す。
| イベント | クレオシン膣クリーム | |
|---|---|---|
| 3 7日目 n=600 |
7日目 n=600 |
7日目 n=600=1325 |
| 泌尿生殖器 | ||
| 膣モニリア症 | 7.7 | 10.4 |
| 外陰膣炎 | 6.0 | 4.4 |
| 外陰膣障害 | 3.2 | 5.3 |
| 三毛性膣炎 | 0 | 1.3 |
| 全体としての体 | ||
| モニリアシス(ボディ) | 1.3 | 0.2 |
クリンダマイシン膣クリーム2%群の<1%で発生するその他の事象には、
泌尿生殖器系:おりもの、metrorrhagia、尿路感染症、子宮内膜症、月経障害、膣炎/膣感染症、および膣痛
体全体として: 限局性腹痛、全身性腹痛、腹部痙攣、口臭、頭痛、細菌感染、炎症性腫脹、アレルギー反応、および真菌感染症。
消化器系:悪心、嘔吐、便秘、消化不良、鼓腸、下痢、および胃腸障害。
内分泌系:甲状腺機能亢進症。
中枢神経系:めまいとめまい。
呼吸器系:鼻出血。<1333><7211>皮膚:そう痒症(非適用部位)、モニリア症、発疹、黄斑丘疹、紅斑、蕁麻疹。
: 倒錯を味わう。
妊婦
妊娠後期の妊婦を対象とした臨床試験では、7日間の治療を受けた180人の患者の1.7%が薬物関連の有害事象のために治療を中止した。 関連する、おそらく関連する、おそらく関連する、または膣投与されたクリンダマイシンリン酸膣クリーム2%との未知の関係であると判断された医療イベン クリンダマイシンリン酸膣クリーム2%またはプラセボのいずれかを受けている患者の≥1%で発生する事象を表2に示す。
| イベント | クレオシン 膣クリーム |
プラセボ |
|---|---|---|
| 7 日 n=180 |
7日 n=180 |
7日 n=180 |
| 泌尿生殖器 | ||
| 膣モニリア症 | 13.3 | 7.1 |
| 外陰膣障害 | 6.7 | 7.1 |
| 異常労働 | 1.1 | 0.5 |
| 全体としての体 | ||
| 真菌感染症 | 1.7 | 0 |
| 皮 | ||
| 掻痒、非適用部位 | 1.1 | 0 |
クリンダマイシン膣クリーム2%群の<1%で発生するその他の事象には、
泌尿生殖器系:排尿障害、月経過多、膣痛、および三毛性膣炎が含まれる。
身体全体:上気道感染症。<1333><7211>皮膚:掻痒(局所適用部位)および紅斑。
市販後の経験
これらの反応は不確実な大きさの集団から自発的に報告されているため、その頻度を確実に推定したり、薬物曝露との因果関係を確
市販後の期間に、クリンダマイシンリン酸膣クリームを使用した偽膜性大腸炎の症例報告がありました。
その他のクリンダマイシン製剤
クリンダマイシン膣クリームは、100mgの経口クリンダマイシン投与と比較して、クリンダマイシンのピーク血清レベルおよび全身暴露(AUCs)を最小限に抑えます。 これらの低レベルの暴露は、経口クリンダマイシンで見られる一般的な反応を生成する可能性は低いが、これらおよび他の反応の可能性は現在排除 経口投与されたクリンダマイシンと膣内投与されたクリンダマイシンとを直接比較した十分に対照された試験からのデータは入手できない。
クリンダマイシンの経口または非経口使用により、以下の副作用および実験室試験の変更が報告されている:
胃腸:腹痛、食道炎、悪心、嘔吐、下痢、偽膜性 (警告を参照してください。)
造血:一過性好中球減少症(白血球減少症)、好酸球増加症、無顆粒球症、および血小板減少症が報告されている。 これらの報告のいずれにおいても、同時クリンダマイシン療法との直接的な病因学的関係はない。
: 薬物療法中に黄斑丘疹および蕁麻疹が観察されている。 一般化された穏やかから適当なmorbilliformそっくりの皮膚発疹はすべての不利な反作用の最も頻繁に報告されます。 多形性紅斑のまれな例は、いくつかのスティーブンス-ジョンソン症候群に似ているが、クリンダマイシンと関連している。 アナフィラキシー様反応のいくつかの症例が報告されている。 過敏反応が起こる場合は、薬物を中止する必要があります。
肝臓:クリンダマイシン治療中に黄疸および肝機能検査の異常が観察されている。
: 多発性関節炎のまれな例が報告されている。
腎:クリンダマイシンと腎障害との直接的な関係は確立されていないが、まれに高窒素血症、乏尿、および/またはタンパク尿によって証明される腎機能不全が観察されている。
過量投与
膣に適用されたクリンダマイシンリン酸膣クリーム2%は、全身効果を生み出すのに十分な量で吸収することができた。 (警告を参照してください。)
クレオシン膣クリームの投与量および投与
推奨用量は、クリンダマイシンリン酸膣クリーム2%(約100mgのクリンダマイシンリン酸を含む5グラム)を膣内、好ましくは就寝時、非妊娠患者では3または7日間連続し、妊娠患者では7日間連続して投与する。 (臨床研究を参照してください。)
クレオシン膣クリームの供給方法
クレオシン膣クリーム2%,(クリンダマイシンリン酸膣クリーム)は以下のように供給されています:
40gチューブ(7個の使い捨てアプリケーター付き)NDC0009-3448-01
制御された室温20°25°C(68°77°F)で保管してください。 凍結から保護します。
臨床試験
細菌性膣炎を有する674人の評価可能な非妊娠女性を含む二つの臨床試験では、クレオシン膣クリーム2%を3または7日間比較し、治療後1ヶ月で決定された臨床治癒率は、72%から81%の3日間治療、84%から86%の7日間治療の範囲であった。
| クレオシン3日目 | クレオシン7日目 | |||
|---|---|---|---|---|
| 米国の研究 | 94/131 | 72% | 110/128 | 86% |
| ヨーロッパ留学 | 161/199 | 81% | 181/216 | 84% |
249評価可能な妊娠中の患者を含む臨床研究では、第二および第三期の7日間治療され、1ヶ月posttherapyで決定された臨床治癒率は、クリンダマイシンアームで60%(77/129)、9%(11/120)であった。 車の腕。 臨床治癒の決定は、おりものを10%KOH溶液と混合したときの”魚のような”アミン臭の欠如および顕微鏡検査での手がかり細胞の不在に基づいていた。
Rxのみ
この製品のラベルが更新されている可能性があります。 現在の完全な処方情報については、をご覧くださいwww.pfizer.com.

LAB-0043-12.0
改訂03/2020
使用方法
使い捨てプラスチック製アプリケーターがこのパッケージに付属しています。 彼らはクリームの適切な膣投与を可能にするように設計されています。
クリームチューブからキャップを外します。 管の通された端のプラスチックアプリケーターをねじで締めて下さい。
下からチューブを転がし、優しく絞って薬をアプリケータに押し込みます。 アプリケータは、プランジャが所定の停止点に達すると充填される。
アプリケータをチューブから外し、キャップを交換します。
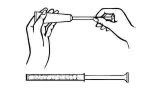
あなたの背中に横たわっている間、しっかりとアプリケータバレルを把握し、不快感を引き起こすことなく、可能な限り膣に挿入します。
ゆっくりとプランジャーを停止するまで押します。
慎重に膣からアプリケータを引き出し、アプリケータを破棄します。
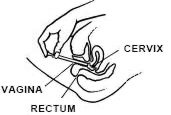
就寝前に毎晩、または医師の指示に従って、1つのアプリケータフルを適用することを忘れないでください。
患者の指示
このパックには使い捨てのプラスチック製アプリケーターが含まれています。 アプリケーターは膣へのクリームの適切な管理のために設計されています。
クリームチューブからキャップを取り外し、プラスチックアプリケータをチューブにねじ込みます。
チューブを下端から静かに絞って、薬をアプリケータに押し込みます。 アプリケーターはプランジャーが最大長に達する場合完全です。
アプリケータをチューブから外し、キャップを交換します。
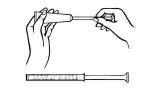
あなたの背中に横になり、アプリケータをしっかりと保持し、不快感を引き起こすことなくできるだけ膣に挿入してください。
ゆっくりとプランジャーを停止するまで押します。
慎重に膣からアプリケータを取り出し、それを捨てます。
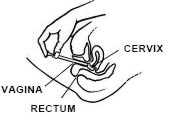
就寝時に、またはあなたの医者によって指示されるように完全なアプリケーターを毎晩加えることを忘れないで下さい。
ラボ-1058-1.0
主な表示パネル-40gチューブラベル
NDC0009-3448-01
40グラム
Rxのみ
クレオシン®
クリンダマイシンリン酸
膣クリーム、USP
膣内使用のみ
2%*
主要な表示パネル-40gの管のカートン
NDC0009-3448-01
7つのアプリケーターとの40グラム
Rxだけ
Cleocin®
クリンダマイシンの隣酸塩
腟のクリーム、USP
膣内
2%*
ファイザー
ファーマシア&アップジョン Co
ファイザー株式会社の事業部,NY,NY10017
| クレオシン リン酸クリンダマイシンクリーム |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
ラベラー -ファーマシアとアップジョン会社合同会社(618054084)
| 設立 | |||
| 名前 | アドレス | ID/FEI | 操作 |
| ファーマシア-アップジョン-カンパニー合同会社 | 618054084 | 分析(0009-3448)、APIの製造(0009-3448)、ラベル(0009-3448)、製造(0009-3448)、パック(0009-3448) | |
クレオシン膣(クリンダマイシン局所)についての詳細)
- 副作用
- 妊娠中または授乳中
- 投与量情報
- 薬物相互作用
- 価格&クーポン
- 一般的な可用性
- 薬物クラス:膣抗infectives
消費者資源
- 高度な読書
プロフェッショナルリソース
- 処方情報
- クリンダマイシン膣クリーム(Fda)
その他のブランドClindamax、Clindagel、clindesse、clindacin etz、。.. +4その他
その他の製剤
- クレオシン
- 。.. +4その他
関連治療ガイド
- 細菌性膣炎
医療免責事項