Nome generico: clindamycin phosphate
Forma di dosaggio: vaginal cream
Medicamente recensito da Drugs.com. Ultimo aggiornamento marzo 1, 2020.
- Panoramica
- Effetti Collaterali
- Dosaggio
- Professional
- Interazioni
- Più
- PER USO INTRAVAGINALE ONLYNOT OFTALMICI, per via CUTANEA, O USO ORALE
- Cleocin Vaginal Cream-Farmacologia clinica
- Meccanismo d’azione
- Farmacocinetica
- MICROBIOLOGIA
- Meccanismo d’azione
- Resistenza
- Attività antibatterica
- Indicazioni e utilizzo per la crema vaginale Cleocin
- Controindicazioni
- Avvertenze
- Precauzioni
- Generale
- Informazioni per il paziente
- Interazioni farmacologiche
- Carcinogenesi, mutagenesi, compromissione della fertilità
- Gravidanza
- Madri che allattano
- Uso pediatrico
- Uso geriatrico
- Reazioni avverse
- Studi clinici
- Sovradosaggio
- Cleocin Crema Vaginale il Dosaggio e la Somministrazione
- Come viene fornita la crema vaginale Cleocin
- Studi clinici
- ISTRUZIONI PER L’USO
- PRINCIPALE del PANNELLO DISPLAY – 40 g Tubo Etichetta
- PRINCIPALE del PANNELLO DISPLAY – 40 g Tubo di Cartone
- Maggiori informazioni Cleocin Vaginale (clindamicina topica)
- risorse per i Consumatori
- risorse Professionali
- Altre formulazioni
- Guide di trattamento correlate
PER USO INTRAVAGINALE ONLYNOT OFTALMICI, per via CUTANEA, O USO ORALE
Clindamicina fosfato è solubile in acqua estere di semi-sintetico antibiotico prodotto da un 7(S)-chloro-sostituzione di 7(R)-gruppo dell’idrossile di padre antibiotico lincomicina. Il nome chimico per il fosfato di clindamicina è metile 7-chloro-6,7,8-trideoxy-6-(1-methyl-trans-4-propyl-L-2-pyrrolidinecarboxamido)-1-thio-L-threo-α–D-galacto-octopiranoside 2 – (diidrogeno fosfato). Ha un peso molecolare di 504,96 e la formula molecolare è C18H34ClN2O8PS. La formula strutturale è rappresentata di seguito:
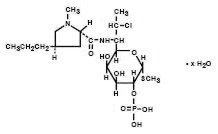
Cleocin Vaginal Cream 2%, è una crema bianca semi-solida, che contiene il 2% di clindamicina fosfato, USP, ad una concentrazione equivalente a 20 mg di clindamicina per grammo. Il pH della crema è compreso tra 3,0 e 6,0. La crema contiene anche alcool benzilico, alcool cetostearilico, esteri misti di acidi grassi, olio minerale, polisorbato 60, glicole propilenico, acqua purificata, monostearato di sorbitan e acido stearico.
Ogni applicatoreful di 5 grammi di crema vaginale contiene circa 100 mg di fosfato di clindamicina.
Cleocin Vaginal Cream-Farmacologia clinica
Meccanismo d’azione
La clindamicina è un farmaco antibatterico (vedi MICROBIOLOGIA).
Farmacocinetica
Dopo una dose intravaginale di 100 mg di clindamicina fosfato crema vaginale 2%, somministrata una volta al giorno a 6 volontarie sane per 7 giorni, circa il 5% (range 0,6% – 11%) della dose somministrata è stato assorbito a livello sistemico. Il picco di concentrazione sierica di clindamicina osservato il primo giorno era in media di 18 ng/mL (intervallo da 4 a 47 ng/mL) e il giorno 7 era in media di 25 ng/mL (intervallo da 6 a 61 ng/mL). Queste concentrazioni di picco sono state raggiunte circa 10 ore dopo la somministrazione (intervallo 4-24 ore).
A seguito di una dose intravaginale una volta al giorno di 100 mg di clindamicina fosfato crema vaginale 2%, somministrata per 7 giorni consecutivi a 5 donne con vaginosi batterica, l’assorbimento è stato più lento e meno variabile di quello osservato nelle femmine sane. Circa il 5% (range dal 2% all ‘ 8%) della dose è stato assorbito a livello sistemico. Il picco di concentrazione sierica di clindamicina osservato il primo giorno era in media di 13 ng/mL (intervallo da 6 a 34 ng/mL) e il giorno 7 era in media di 16 ng/mL (intervallo da 7 a 26 ng/mL). Queste concentrazioni di picco sono state raggiunte circa 14 ore dopo la somministrazione (intervallo 4-24 ore).
C’è stato poco o nessun accumulo sistemico di clindamicina dopo ripetute dosi vaginali di clindamicina fosfato crema vaginale 2%. L ‘ emivita sistemica era compresa tra 1,5 e 2,6 ore.
MICROBIOLOGIA
Meccanismo d’azione
La clindamicina inibisce la sintesi proteica batterica legandosi all’RNA 23S della subunità 50S del ribosoma. La clindamicina è prevalentemente batteriostatica. Sebbene il fosfato di clindamicina sia inattivo in vitro, la rapida idrolisi in vivo lo converte in clindamicina attiva.
Resistenza
La resistenza alla clindamicina è più spesso causata dalla modifica del sito bersaglio sul ribosoma, di solito dalla modifica chimica delle basi di RNA mediante mutazioni puntiformi nell’RNA o occasionalmente nelle proteine. In alcuni organismi è stata dimostrata resistenza crociata tra lincosamidi, macrolidi e streptogramine B. È stata dimostrata resistenza crociata tra clindamicina e lincomicina.
Attività antibatterica
I test di coltura e sensibilità dei batteri non vengono eseguiti di routine per stabilire la diagnosi di vaginosi batterica (vedi INDICAZIONI E UTILIZZO); metodologia standard per i test di suscettibilità dei potenziali patogeni batterici, Gardnerella vaginalis, Mobiluncus spp., o Mycoplasma hominis, non è stato definito.
Sono disponibili i seguenti dati in vitro, ma il loro significato clinico non è noto. La clindamicina è attiva in vitro contro la maggior parte degli isolati dei seguenti organismi segnalati per essere associati a vaginosi batterica:
- Bacteroides spp.
- Gardnerella vaginalis
- Mobiluncus spp.
- Mycoplasma hominis
- Peptostreptococcus spp.
Indicazioni e utilizzo per la crema vaginale Cleocin
La crema vaginale Cleocin 2% è indicata nel trattamento della vaginosi batterica (precedentemente denominata vaginite Haemophilus, vaginite Gardnerella, vaginite aspecifica, vaginite Corynebacterium o vaginosi anaerobica). Cleocin Crema vaginale 2%, può essere usato per trattare le donne non gravide e le donne incinte durante il secondo e terzo trimestre. (Vedere STUDI CLINICI.)
NOTA: Ai fini di questa indicazione, una diagnosi clinica di vaginosi batterica è solitamente definita dalla presenza di una scarica vaginale omogenea che (a) ha un pH superiore a 4,5, (b) emette un odore di ammina “pesce” quando miscelato con una soluzione KOH al 10% e (c) contiene cellule indizio all’esame microscopico. I risultati delle macchie di Gram coerenti con una diagnosi di vaginosi batterica includono (a) morfologia del Lactobacillus marcatamente ridotta o assente, (b) predominanza del morfotipo di Gardnerella e (c) globuli bianchi assenti o pochi.
Altri agenti patogeni comunemente associati a vulvovaginite, ad esempio, Trichomonas vaginalis, Chlamydia trachomatis, N. gonorrhoeae, Candida albicans e Herpes simplex virus dovrebbero essere esclusi.
Controindicazioni
Cleocin Crema vaginale 2%, è controindicato nei soggetti con una storia di ipersensibilità alla clindamicina, lincomicina, o uno qualsiasi dei componenti di questa crema vaginale. Cleocin Crema vaginale 2%, è anche controindicato in individui con una storia di enterite regionale, colite ulcerosa o una storia di colite “associata agli antibiotici”.
Avvertenze
La colite pseudomembranosa è stata riportata con quasi tutti gli agenti antibatterici, inclusa la clindamicina, e può variare in gravità da lieve a pericolosa per la vita. La clindamicina somministrata per via orale e parenterale è stata associata a colite grave che può terminare fatalmente. Diarrea, diarrea sanguinolenta e colite (compresa la colite pseudomembranosa) sono state riportate con l’uso di clindamicina somministrata per via orale e parenterale, nonché con formulazioni topiche (dermiche e vaginali) di clindamicina. Pertanto, è importante considerare questa diagnosi nei pazienti che presentano diarrea successiva alla somministrazione di clindamicina, anche se somministrata per via vaginale, poiché circa il 5% della dose di clindamicina viene assorbita sistemicamente dalla vagina.
Il trattamento con agenti antibatterici altera la normale flora del colon e può consentire una crescita eccessiva dei clostridi.Gli studi indicano che una tossina prodotta da Clostridium difficile è una causa primaria di colite “associata agli antibiotici”.
Dopo che è stata stabilita la diagnosi di colite pseudomembranosa, devono essere avviate misure terapeutiche. I casi lievi di colite pseudomembranosa di solito rispondono alla sospensione del farmaco da solo. Nei casi da moderati a gravi, si deve prendere in considerazione la gestione con fluidi ed elettroliti, la supplementazione di proteine e il trattamento con un farmaco antibatterico clinicamente efficace contro la colite da clostridium difficile.
I sintomi della colite pseudomembranosa possono verificarsi durante o dopo il trattamento antimicrobico.
Precauzioni
Generale
Cleocin Vaginal Cream 2%, contiene ingredienti che causano bruciore e irritazione agli occhi. In caso di contatto accidentale con l’occhio, sciacquare l’occhio con abbondante acqua di rubinetto fredda.
L’uso di Cleocin Vaginal Cream 2% può causare la crescita eccessiva di organismi non sensibili nella vagina. Negli studi clinici che hanno coinvolto 600 donne non gravide che hanno ricevuto un trattamento per 3 giorni, Candida albicans è stata rilevata, sintomaticamente o per coltura, nell ‘ 8,8% dei pazienti. Nel 9% dei pazienti è stata registrata vaginite. In studi clinici condotti su 1325 donne non gravide che hanno ricevuto un trattamento per 7 giorni, Candida albicans è stata rilevata, in modo sintomatico o per coltura, nel 10,5% dei pazienti. La vaginite è stata registrata nel 10,7% dei pazienti. In 180 donne in gravidanza che hanno ricevuto un trattamento per 7 giorni, Candida albicans è stata rilevata, sintomaticamente o per coltura, nel 13,3% dei pazienti. Nel 7,2% dei pazienti è stata registrata vaginite. Candida albicans, come riportato qui, include i termini: moniliasi vaginale e moniliasi (corpo nel suo complesso). Vaginite comprende i termini: disturbo vulvovaginale, vulvovaginite, perdite vaginali, vaginite trichomonal e vaginite.
Informazioni per il paziente
Il paziente deve essere istruito a non avere rapporti sessuali vaginali o ad usare altri prodotti vaginali (come tamponi o docce) durante il trattamento con questo prodotto.
Il paziente deve anche essere informato che questa crema contiene olio minerale che può indebolire prodotti in lattice o gomma come preservativi o diaframmi contraccettivi vaginali. Pertanto, l’uso di tali prodotti entro 72 ore dopo il trattamento con Cleocin Vaginal Cream 2%, non è raccomandato.
Interazioni farmacologiche
La clindamicina sistemica ha dimostrato di avere proprietà bloccanti neuromuscolari che possono migliorare l’azione di altri agenti bloccanti neuromuscolari. Pertanto, deve essere usato con cautela nei pazienti che ricevono tali agenti.
Carcinogenesi, mutagenesi, compromissione della fertilità
non sono stati condotti studi a lungo termine su animali con clindamicina per valutare il potenziale cancerogeno.
I test di genotossicità effettuati comprendevano un test del micronucleo nel ratto e un test di Ames. Entrambi i test erano negativi. Studi sulla fertilità in ratti trattati per via orale fino a 300 mg/kg/die (31 volte l’esposizione umana in base a mg/m2) non hanno rivelato effetti sulla fertilità o sulla capacità di accoppiamento.
Gravidanza
Effetti teratogeni
Negli studi clinici con donne in gravidanza, la somministrazione sistemica di clindamicina durante il secondo e terzo trimestre non è stata associata ad un aumento della frequenza di anomalie congenite.
La crema vaginale alla clindamicina deve essere utilizzata durante il primo trimestre di gravidanza solo se chiaramente necessaria e i benefici superano i rischi. Non ci sono studi adeguati e ben controllati in donne in gravidanza durante il primo trimestre di gravidanza.
Cleocin Vaginal Cream 2% è stato studiato in donne in gravidanza durante il secondo trimestre. Nelle donne trattate per sette giorni, il travaglio anormale è stato riportato nell ‘ 1,1% dei pazienti che hanno ricevuto la crema vaginale clindamicina 2% rispetto allo 0,5% dei pazienti che hanno ricevuto placebo.
Studi sulla riproduzione sono stati condotti su ratti e topi utilizzando dosi orali e parenterali di clindamicina fino a 600 mg/kg/die (62 e 25 volte, rispettivamente, l’esposizione umana massima in base alla superficie corporea) e non hanno rivelato alcuna prova di danno al feto a causa della clindamicina. Palati di schisi sono stati osservati nei feti di un ceppo di topo trattati per via intraperitoneale con clindamicina a 200 mg / kg / die (circa 10 volte la dose raccomandata in base alle conversioni della superficie corporea). Poiché questo effetto non è stato osservato in altri ceppi murini o in altre specie, l’effetto può essere specifico del ceppo.
Madri che allattano
Dati pubblicati limitati basati sul campionamento del latte materno riportano che la clindamicina appare nel latte materno umano nell’intervallo da meno di 0,5 a 3,8 mcg/mL a dosaggi da 150 mg per via orale a 600 mg per via endovenosa. Non è noto se la clindamicina sia escreta nel latte materno umano dopo l ‘ uso di clindamicina fosfato somministrata per via vaginale.
La clindamicina può causare effetti avversi sulla flora gastrointestinale del neonato allattato al seno. Se la clindamicina è richiesta da una madre che allatta, non è un motivo per interrompere l’allattamento al seno, ma un farmaco alternativo può essere preferito. Monitorare il bambino allattato al seno per possibili effetti avversi sulla flora gastrointestinale, come diarrea, candidosi (mughetto, dermatite da pannolino) o raramente, sangue nelle feci che indica possibile colite associata agli antibiotici.
I benefici per lo sviluppo e la salute dell’allattamento al seno devono essere considerati insieme alla necessità clinica della madre per la clindamicina e qualsiasi potenziale effetto negativo sul bambino allattato dalla clindamicina o dalla condizione materna sottostante.
Uso pediatrico
La sicurezza e l’efficacia nei pazienti pediatrici non sono state stabilite.
Uso geriatrico
Gli studi clinici per Cleocin Vaginal Cream 2% non hanno incluso un numero sufficiente di soggetti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso rispetto ai soggetti più giovani. Altre esperienze cliniche riportate non hanno identificato differenze nelle risposte tra pazienti anziani e pazienti più giovani.
Reazioni avverse
Studi clinici
Donne non gravide
Negli studi clinici che hanno coinvolto donne non gravide, l ‘ 1,8% dei 600 pazienti trattati con Cleocin Vaginal Cream 2% per 3 giorni e il 2,7% dei 1325 pazienti trattati per 7 giorni hanno interrotto la terapia a causa di eventi avversi correlati al farmaco. Eventi medici giudicati correlati, probabilmente correlati, possibilmente correlati o di relazione sconosciuta con la crema vaginale di clindamicina fosfato somministrata per via vaginale 2%, sono stati riportati per il 20,7% dei pazienti che hanno ricevuto il trattamento per 3 giorni e il 21,3% dei pazienti che hanno ricevuto il trattamento per 7 giorni. Gli eventi che si verificano in ≥1% dei pazienti trattati con clindamicina fosfato crema vaginale 2% sono riportati nella Tabella 1.
| Evento | Cleocin Crema Vaginale | |
|---|---|---|
| 3 Giorno n=600 |
7 Giorni n=1325 |
|
| Urogenitale | ||
| moniliasi Vaginale | 7.7 | 10.4 |
| Vulvovaginiti | 6.0 | 4.4 |
| Vulvovaginale disturbo | 3.2 | 5.3 |
| Trichomonal vaginite | 0 | 1.3 |
| Corpo Intero | ||
| Moniliasi (corpo) | 1.3 | 0.2 |
Altri eventi che si verificano in <1% della clindamicina crema vaginale 2% gruppi includono:
sistema Urogenitale: perdite vaginali, metrorragia, infezione del tratto urinario, endometriosi, disordine mestruale, vaginite/infezione vaginale e dolore vaginale.
Corpo nel suo complesso: dolore addominale localizzato, dolore addominale generalizzato, crampi addominali, alitosi, mal di testa, infezione batterica, gonfiore infiammatorio, reazione allergica e infezione fungina.
Apparato digerente: nausea, vomito, stitichezza, dispepsia, flatulenza, diarrea e disturbi gastrointestinali.
Sistema endocrino: ipertiroidismo.
Sistema nervoso centrale: capogiri e vertigini.
Apparato respiratorio: epistassi.
Cute: prurito (non sito di applicazione), moniliasi, rash, rash maculopapulare, eritema e orticaria.
Sensi speciali: perversione del gusto.
Donne in gravidanza
In uno studio clinico che ha coinvolto donne in gravidanza durante il secondo trimestre, l ‘ 1,7% dei 180 pazienti trattati per 7 giorni ha interrotto la terapia a causa di eventi avversi correlati al farmaco. Nel 22,8% delle pazienti gravide sono stati riportati eventi medici giudicati correlati, probabilmente correlati, possibilmente correlati o di relazione sconosciuta con clindamicina fosfato vaginale crema 2% somministrata per via vaginale. Gli eventi che si verificano in ≥1% dei pazienti trattati con clindamicina fosfato crema vaginale 2% o placebo sono riportati nella Tabella 2.
| Evento | CLEOCIN Crema Vaginale |
Placebo |
|---|---|---|
| 7 GIORNO n=180 |
7 GIORNI n=184 |
|
| Urogenitale | ||
| moniliasi Vaginale | 13.3 | 7.1 |
| Vulvovaginale disturbo | 6.7 | 7.1 |
| Anormale di lavoro | 1.1 | 0.5 |
| Corpo Intero | ||
| infezione Fungina | 1.7 | 0 |
| Pelle | ||
| Prurito, camere non-sito di applicazione | 1.1 | 0 |
Altri eventi che si verificano in <1% della clindamicina crema vaginale 2% gruppo:
sistema Urogenitale: disuria, metrorragia, dolore vaginale, e trichomonal vaginite.
Corpo nel suo complesso: infezione delle vie respiratorie superiori.
Pelle: prurito (sito di applicazione topica) ed eritema.
Esperienza post-marketing
Poiché queste reazioni sono segnalate volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l’esposizione al farmaco.
Nel periodo post-marketing, ci sono stati casi di colite pseudomembranosa con l’uso di clindamicina fosfato crema vaginale.
Altre formulazioni di clindamicina
La crema vaginale di clindamicina offre livelli sierici di picco minimi e esposizione sistemica (AUC) di clindamicina rispetto al dosaggio orale di 100 mg di clindamicina. Sebbene questi livelli più bassi di esposizione abbiano meno probabilità di produrre le reazioni comuni osservate con clindamicina orale, la possibilità di queste e altre reazioni non può essere esclusa attualmente. Non sono disponibili dati provenienti da studi ben controllati che confrontano direttamente la clindamicina somministrata per via orale con la clindamicina somministrata per via vaginale.
Con l’uso orale o parenterale di clindamicina sono state riportate le seguenti reazioni avverse e alterate analisi di laboratorio:
Gastrointestinale: dolore addominale, esofagite, nausea, vomito, diarrea e colite pseudomembranosa. (Vedere AVVERTENZE.)
Ematopoietico: sono stati riportati neutropenia transitoria (leucopenia), eosinofilia, agranulocitosi e trombocitopenia. Nessuna relazione eziologica diretta con la terapia concomitante di clindamicina potrebbe essere fatta in nessuno di questi rapporti.
Reazioni di ipersensibilità: Durante la terapia farmacologica sono stati osservati rash maculopapulare e orticaria. Le eruzioni cutanee generalizzate da lievi a moderate di tipo morbilliforme sono le reazioni avverse più frequentemente riportate. Rari casi di eritema multiforme, alcuni simili alla sindrome di Stevens-Johnson, sono stati associati alla clindamicina. Sono stati riportati alcuni casi di reazioni anafilattoidi. Se si verifica una reazione di ipersensibilità, il farmaco deve essere interrotto.
Fegato: ittero e anomalie nei test di funzionalità epatica sono stati osservati durante la terapia con clindamicina.
Muscolo-scheletrico: Sono stati riportati rari casi di poliartrite.
Renale: Sebbene non sia stata stabilita alcuna relazione diretta tra clindamicina e danno renale, in rari casi è stata osservata disfunzione renale come evidenziato da azotemia, oliguria e/o proteinuria.
Sovradosaggio
Clindamycin phosphate Vaginally applied Vaginally phosphate cream 2% potrebbe essere assorbito in quantità sufficienti a produrre effetti sistemici. (Vedere AVVERTENZE.)
Cleocin Crema Vaginale il Dosaggio e la Somministrazione
La dose raccomandata è di una applicatorful di clindamicina fosfato crema vaginale 2%, (5 grammi, che contiene circa 100 mg di clindamicina fosfato) intravaginale, preferibilmente al momento di coricarsi, per 3 o 7 giorni consecutivi in pazienti non in gravidanza e per 7 giorni consecutivi nelle pazienti in gravidanza. (Vedere STUDI CLINICI.)
Come viene fornita la crema vaginale Cleocin
La crema vaginale Cleocin 2%, (clindamycin phosphate vaginal cream) viene fornita come segue:
Tubo da 40 g (con 7 applicatori monouso) NDC 0009-3448-01
Conservare a temperatura ambiente controllata da 20° a 25° C (da 68° a 77° F) . Proteggere dal congelamento.
Studi clinici
In due studi clinici condotti su 674 donne non gravide valutabili con vaginosi batterica, confrontando Cleocin Vaginal Cream 2% per 3 o 7 giorni, le percentuali di guarigione clinica, determinate a 1 mese di post-terapia, variavano dal 72% all ‘81% per il trattamento di 3 giorni e dall’ 84% all ‘ 86% per il trattamento di 7 giorni.
| CLEOCIN Giorno 3 | CLEOCIN 7 Giorni | |||
|---|---|---|---|---|
| NOI di Studio | 94/131 | 72% | 110/128 | 86% |
| Studio europeo | 161/199 | 81% | 181/216 | 84% |
In uno studio clinico che coinvolge 249 valutabili pazienti in gravidanza nel secondo e terzo trimestre di gravidanza trattati per 7 giorni, il tasso di guarigione clinica, determinato a 1 mese posttherapy, è stata del 60% (77/129) nel clindamycin braccio e il 9% (11/120) per il braccio del veicolo. La determinazione della cura clinica si basava sull’assenza di un odore di ammina “pesce” quando la scarica vaginale veniva miscelata con una soluzione KOH al 10% e l’assenza di cellule indizio all’esame microscopico.
Solo Rx
L’etichetta di questo prodotto potrebbe essere stata aggiornata. Per informazioni aggiornate sulla prescrizione completa, si prega di visitare www.pfizer.com.

LAB-0043-12.0
Revised 03/2020
ISTRUZIONI PER L’USO
Gli applicatori di plastica monouso sono forniti con questo pacchetto. Sono progettati per consentire una corretta somministrazione vaginale della crema.
Rimuovere il tappo dal tubo crema. Avvitare un applicatore di plastica sull’estremità filettata del tubo.
Tubo di rotolamento dal basso, spremere delicatamente e forzare il farmaco nell’applicatore. L’applicatore viene riempito quando lo stantuffo raggiunge il suo punto di arresto predeterminato.
Svitare l’applicatore dal tubo e sostituire il tappo.
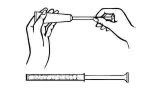
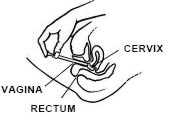
Mentre si è sdraiati sulla schiena, afferrare saldamente la canna dell’applicatore e inserirla nella vagina il più lontano possibile senza causare disagio.
Spingere lentamente lo stantuffo finché non si arresta.
Prelevare con cautela l’applicatore dalla vagina e scartare l’applicatore.
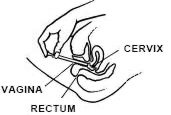
RICORDARSI DI APPLICARE UN APPLICATORFUL OGNI SERA PRIMA DI CORICARSI, O COME PRESCRITTO DAL MEDICO.
ISTRUZIONI PER IL PAZIENTE
Questa confezione contiene applicatori monouso in plastica. Gli applicatori sono progettati per una corretta somministrazione della crema nella vagina.
Rimuovere il tappo dal tubo crema e avvitare l’applicatore di plastica sul tubo.
Spremere delicatamente il tubo dall’estremità inferiore e forzare il farmaco nell’applicatore. L’applicatore sarà pieno quando lo stantuffo raggiunge la sua lunghezza massima.
Svitare l’applicatore dal tubo e sostituire il tappo.
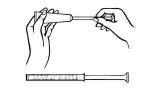
Sdraiati sulla schiena e tenendo saldamente l’applicatore, inseriscilo nella vagina il più possibile senza causare disagio.
Spingere lentamente lo stantuffo finché non si arresta.
Rimuovere con cautela l’applicatore dalla vagina e scartarlo.
RICORDARSI DI APPLICARE UN APPLICATORE COMPLETO OGNI SERA PRIMA DI CORICARSI, O COME INDICATO DAL MEDICO.
LAB-1058-1.0
PRINCIPALE del PANNELLO DISPLAY – 40 g Tubo Etichetta
NDC 0009-3448-01
40 Grammi
Rx solo
Cleocin®
clindamicina fosfato
crema vaginale, USP
Per Intravaginale Utilizzare Solo
2%*
PRINCIPALE del PANNELLO DISPLAY – 40 g Tubo di Cartone
NDC 0009-3448-01
40 Grammi Con 7 Applicatori
Rx solo
Cleocin®
clindamicina fosfato
crema vaginale, USP
Per Intravaginale Utilizzare Solo
2%*
Pfizer
Distribuito da
Pharmacia & Upjohn Co
Divisione di Pfizer Inc, NY, NY 10017
| CLEOCIN clindamicina fosfato crema |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Pharmacia e Upjohn Company LLC (618054084)
| Struttura | |||
| Nome | Indirizzo | ID/FEI | Operazioni |
| Pharmacia e Upjohn Company LLC | 618054084 | ANALISI(0009-3448), API FABBRICAZIONE(0009-3448), ETICHETTA(0009-3448), PRODUZIONE(0009-3448), PACK(0009-3448) | |
Maggiori informazioni Cleocin Vaginale (clindamicina topica)
- Effetti Collaterali
- Durante la Gravidanza o l’Allattamento al seno
- Dosaggio di Informazioni
- interazioni Farmacologiche
- Prezzi & Coupon
- Disponibilità Generico
- classe di Droga: vaginale anti-infettivi
risorse per i Consumatori
- Avanzate di Lettura
risorse Professionali
- Informazioni prescrittive
- Clindamicina Crema Vaginale (FDA)
Altre marche Clindamax, Clindagel, Clindesse, Clindacin ETZ, … + 4 più
Altre formulazioni
- Cleocin
- … + 4 più
Guide di trattamento correlate
- Vaginite batterica
Disclaimer medico