introduktion
venös tromboembolism (VTE), inklusive djup ventrombos (DVT), lungemboli (PE) och splanchnic venetrombos, är en frekvent komplikation av cancer.1. utvecklingen av cancerassocierad VTE är förknippad med minskad livskvalitet och lägger en betydande ekonomisk börda på både patienten och sjukvården.2 VTE är den näst ledande dödsorsaken hos cancerpatienter som får kemoterapi och har visat sig vara en oberoende prediktor för dödlighet i populationen av patienter med cancer.3,4 hanteringen av cancerassocierad VTE-behandling kan vara utmanande eftersom riskerna för återkommande VTE och antikoagulantrelaterad blödning är höga trots lämplig hantering.5 dessutom ökar läkemedelsinteraktioner och cancerrelaterade komorbiditeter, såsom njur-och/eller leverdysfunktion, minskat oralt intag, kemoterapiinducerad illamående och kräkningar och trombocytopeni också behandlingskomplexiteten genom att begränsa valet av antikoagulantmedel.
kliniska prövningar som utvärderar lågmolekylärt Heparin för behandling av Cancerassocierad VTE
långvarig användning av lågmolekylärt heparin (LMWH) för behandling av VTE hos patienter med aktiv cancer rekommenderas som förstahandsbehandling baserat på resultaten från flera öppna randomiserade kontrollerade studier (RCT).6,7 de två största studierna som hittills publicerats, CLOT (jämförelse av heparin med låg molekylvikt jämfört med Oral antikoagulantbehandling för förebyggande av återkommande venös tromboembolism hos patienter med Cancer) och CATCH (jämförelse av akuta behandlingar i Cancerhemostas), jämförde en LMWH med vitamin K-antagonistbehandling hos patienter med aktiv cancer och akut symtomatisk proximal DVT eller PE. Se Tabell 1 för baslinjeegenskaper och Tabell 2 för studieresultat.8,9 båda studierna använde en öppen studiedesign, samma target international normalized ratio (INR) i vitamin K-antagonistkontrollarmen, samma aktiva cancerdefinition och samma behandlingstid och hade jämförbara kriterier för patientberättigande.
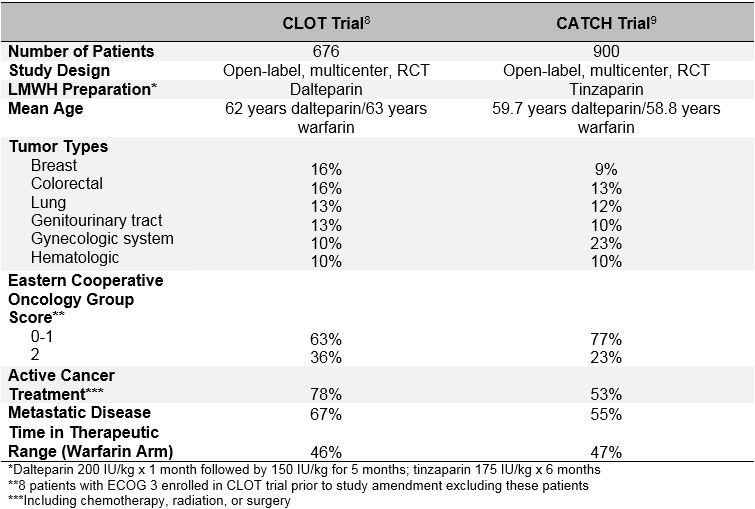
Tabell 1: studiedesign och Baslinjekarakteristika för CATCH and CLOT-studierna
Tabell 2: Resultat i koagulations-och FÅNGSTSTUDIERNA

CLOT-studien, publicerad 2003, randomiserade 676 patienter för att få dalteparin (200 IE/kg dagligen i 1 månad följt av 150 IE/kg dagligen i 5 månader) eller vitamin K-antagonist (warfarin eller acenokumarol med mål INR 2, 5 under totalt 6 månader med en initial 5-7 dagar överlappning med dalteparin 200 IE/kg).8 symtomatisk återkommande DVT eller PE, inklusive död relaterad till PE, observerades hos 27 patienter (7, 0%) randomiserade till dalteparin och hos 53 patienter (15%) randomiserade till vitamin K-antagonist (hazard ratio 0, 48; 95% konfidensintervall, 0,30-0,77; p = 0,002). Ingen skillnad i frekvensen av större blödningar (6 mot 4%; p = 0,27), någon blödning (15 mot 19%; p = 0,09) eller död (39 mot 41%; p = 0,53) observerades mellan de 2 grupperna.
I CATCH-studien, publicerad över 10 år senare 2015, randomiserades 900 patienter till tinzaparin (175 IE/kg dagligen utan dosreduktion) eller warfarin (target INR 2,0-3,0 med initial tinzaparin 175 IE/kg överlappning i 5-10 dagar) under totalt 6 månader.9 det primära sammansatta effektmåttet för recidiverande VTE inklusive Incident proximal DVT och Le förekom hos 31 patienter (6,9%) i tinzaparinarmen och 45 patienter (10%) i warfarinarmen (HR 0,65; 95% ki, 0,41-1,03; p = 0,07). Symtomatisk DVT inträffade hos signifikant färre patienter behandlade med tinzaparin (2,7 mot 5,3%; HR 0,48; 95% ki, 0,24-0,96; p = 0,04). Även om större blödningsfrekvenser var likartade i båda armarna observerades en signifikant minskning av kliniskt relevant, icke-större blödning med tinzaparin (10,9 mot 15,3%; HR 0,58; 95% ki, 0,40-0,84; p = 0,004). Mortaliteten var likartad i båda grupperna, med ungefär en tredjedel av patienterna som dör under studieperioden (33,4 mot 30,6%; p = 0,54). Även om tinzaparin inte signifikant minskade det primära sammansatta effektmåttet för återkommande VTE, stöder CATCH – studieresultaten användningen av långvarig LMWH som den föredragna behandlingen för cancerassocierad VTE på grund av en lägre risk för kliniskt relevant större blödning och en signifikant minskning av återkommande DVT.
FÅNGSTFÖRSÖKETS misslyckande att uppfylla statistisk signifikans för det primära effektmåttet kan bero på den lägre än förväntad återkommande VTE-frekvens som observerats i warfarinarmen. En möjlig förklaring till denna observation kan vara en förbättring av warfarinhanteringen i FÅNGSTFÖRSÖKET. Liknande nivåer av INR-kontroll i båda studierna argumenterar emellertid mot detta (tiden i terapeutiskt intervall var 46% i koagel mot 47% i fångst; tiden över det terapeutiska intervallet var 24% i koagel mot 27% I fångst). En mer sannolik förklaring är en bias i valet av” mindre sjuka ” patienter för inskrivning i FÅNGSTFÖRSÖKET. Även om CATCH and CLOT-studierna använde liknande inkluderings-och uteslutningskriterier, finns det viktiga skillnader i baslinjekarakteristika mellan de två patientpopulationerna, särskilt med avseende på trombotiska och prognostiska riskfaktorer. En högre andel av patienterna i PROPPSTUDIEN fick aktiv cancerbehandling (72% propp mot 53% fångst), hade tidigare haft VTE (11% propp mot 6% fångst), hade bevis på metastatisk sjukdom (67% propp mot. 55% fångst) och hade en sämre prestationsstatus (Eastern Cooperative Oncology Group-poäng på 2 i 36% koagel mot 23% fångst). Dessutom var mortaliteten under 6 månaders behandlingsperiod också högre i KOAGELPOPULATIONEN (39% koagel mot 32% fångst). Således hade FÅNGSTPATIENTPOPULATIONEN sannolikt en lägre inneboende risk för återkommande VTE jämfört med patienter med BLODPROPPSSTUDIER. Det är mycket troligt att utredare inte registrerade patienter i fångst om de kände att LMWH skulle vara mer fördelaktigt än warfarin, vilket resulterade i selektiv registrering av patienter som var mindre benägna att utveckla återkommande VTE.
försök som utvärderar direkta orala antikoagulantia i Cancerassocierad VTE
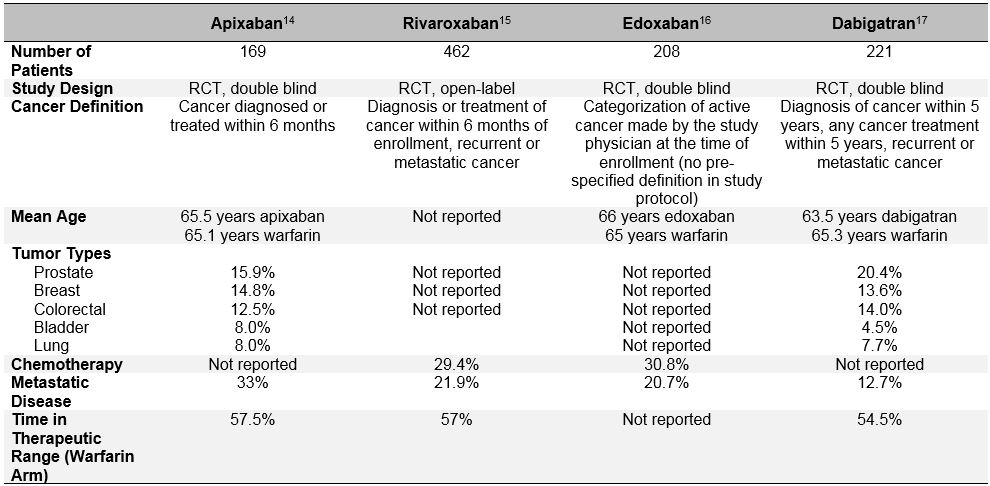
patientval bias är ännu tydligare i de senaste randomiserade studierna som utvärderar effekten och säkerheten av direkta orala antikoagulantia (DOACs) för behandling av akut VTE.10 dessa orala antikoagulantia har studerats omfattande under det senaste decenniet vid förmaksflimmer, VTE-behandling och VTE-förebyggande. I landmark fas III kliniska prövningar för akut VTE-behandling visades det konsekvent att DOACs inte är sämre än warfarin (poolad relativ risk 0,90; 95% CI, 0,77-1.06) för att förhindra återkommande VTE, och de har en liknande eller minskad risk för större blödningar (poolad RR 0,40; 95% CI, 0,45-0,83).11 Bland de patienter som klassificerades som ”cancer” eller ”aktiv cancer” i dessa studier verkar DOACs också fungera på samma sätt som warfarin.12 Men en mer djupgående undersökning av dessa post-hoc-data avslöjar viktig patientvalförspänning och ifrågasätter generaliserbarheten av doac-försöksresultaten till ”verkliga” patienter med cancer med VTE. Förutom de heterogena definitionerna av” aktiv cancer ” som användes i dessa studier som skilde sig från blodpropps-och FÅNGSTFÖRSÖK, var viktiga determinanter för återkommande VTE och blödning också mycket olika hos DOAC-patienter med cancer från LMWH-cancerspecifika studier (tabell 3). Dessa inkluderar förekomst av metastatisk sjukdom och samtidig användning av cancer mot cancer. De stora skillnaderna i dödlighet under studieperioden hävdar också att mycket olika grupper av patienter med ”cancer” inkluderades i doac kontra LMWH-studierna. Dessutom, till skillnad från LMWH, vilket är förknippat med en signifikant minskning av risken för återkommande VTE jämfört med vitamin K-antagonister (RR 0,52; 95% CI, 0,36-0.74), doacs minskade inte signifikant denna risk i en metaanalys av 1 132 patienter med cancer inskrivna i Einsteins kliniska prövningsprogram, HOKUSAI-VTE (Edoxaban kontra Warfarin för behandling av symptomatisk venös tromboembolism), RECOVER (effekt och säkerhet för Dabigatran jämfört med Warfarin för 6-månaders behandling av akut symptomatisk venös tromboembolism) och AMPLIFY (Apixaban för Initial hantering av lungemboli och djup ventrombos som förstahandsbehandling) RCT (RR 0,66; 95% ki, 0,39-1,11).10 alla dessa överväganden bör varna den omarkerade användningen av DOACs hos patienter med aktiv cancer och akut, symptomatisk VTE.13
tabell 3: studiedesign och Baslinjekarakteristika för subgrupperna av patienter med Cancer från fas III DOAC-studierna
slutsatser
alla viktiga evidensbaserade konsensusriktlinjer rekommenderar LMWH för initial och långvarig behandling av cancerassocierad VTE.6,7,13 denna rekommendation är baserad på observationen att LMWH inte bara är effektivare än warfarin för förebyggande av återkommande VTE, men erbjuder också ytterligare fördelar jämfört med orala medel inklusive stabil antikoagulation hos patienter med dåligt oralt intag, brist på läkemedelsinteraktioner och klinisk erfarenhet av hantering av antikoagulation kring invasiva procedurer och trombocytopeni. Även om DOACs för närvarande inte rekommenderas för VTE-behandling hos patienter med cancer, RCT som jämför rivaroxaban och edoxaban med LMWH pågår för närvarande och kommer att bidra till att klargöra deras roll i cancerassocierad VTE.6,13
- Khorana AA, Dalal M, Lin J, Connolly GC. Förekomst och prediktorer för venös tromboembolism (VTE) bland ambulerande högriskcancerpatienter som genomgår kemoterapi i USA. Cancer 2013; 119: 648-55.
- Kourlaba G, Relakis J, Mylonas C, et al. Den humanistiska och ekonomiska bördan av venös tromboembolism hos cancerpatienter: en systematisk översyn. Blodkoagulfibrinolys 2015; 26: 13-31.
- Kuderer NM, Ortel TL, Francis CW. Påverkan av venös tromboembolism och antikoagulation på cancer och canceröverlevnad. J Clin Oncol 2009; 27: 4902-11.
- Khorana AA, Francis CW, Culakova E, Kuderer NM, Lyman GH. Tromboembolism är en ledande dödsorsak hos cancerpatienter som får poliklinisk kemoterapi. J Thromb Hemost 2007; 5: 632-4.
- Prandoni P, Linsing AW, Piccioli A, et al. Återkommande venös tromboembolism och blödningskomplikationer vid antikoagulantbehandling hos patienter med cancer och venös trombos. Blod 2002; 100: 3484-8.
- Lyman GH, Bohlke K, Khorana AA, et al. Venös tromboembolism profylax och behandling hos patienter med cancer: american society of clinical oncology klinisk praxis riktlinje uppdatering 2014. J Clin Oncol 2015; 33: 654-6.
- Streiff MB, Holmström B, Ashrani A, et al. Cancerassocierad Venös Tromboembolisk Sjukdom, Version 1.2015. J Natl Compr Canc Netw 2015; 13: 1079-95.
- Lee AY, Levine MN, Baker RI, et al. Heparin med låg molekylvikt kontra kumarin för förebyggande av återkommande venös tromboembolism hos patienter med cancer. N Engl J Med 2003; 349: 146-53.
- Lee AY, Kamphuisen PW, Meyer G, et al. Tinzaparin vs Warfarin för behandling av akut venös tromboembolism hos patienter med aktiv Cancer: En randomiserad klinisk studie. JAMA 2015; 314: 677-86.
- bärare M, Cameron C, Delluc A, Castellucci L, Khorana AA, Lee AY. Effekt och säkerhet av antikoagulant terapi för behandling av akut cancerassocierad trombos: en systematisk granskning och metaanalys. Thromb Res 2014; 134: 1214-9.
- van Es N, Coppens M, Schulman S, Middeldorp S, B Acabller HR. direkta orala antikoagulantia jämfört med vitamin K-antagonister för akut venös tromboembolism: bevis från fas 3-studier. Blod 2014; 124: 1968-75.
- Vedovati MC, Germini F, Agnelli G, Becattini C. direkta orala antikoagulantia hos patienter med VTE och cancer: en systematisk granskning och metaanalys. Bröst 2015; 147: 475-83.
- Kearon C, Akl EA, Ornelas J, et al. Antitrombotisk behandling för VTE-sjukdom: Bröst riktlinje och Expert Panel rapport. Bröst 2016; 149: 315-52.
- Agnelli G, B Obbller HR, Cohen A, et al. Oral apixaban för behandling av venös tromboembolism hos cancerpatienter: resultat från AMPLIFY-studien. J Thromb Hemost 2015; 13: 2187-91.
- Prins MH, Lensing AW, Brighton TA, et al. Oral rivaroxaban kontra enoxaparin med vitamin K-antagonist för behandling av symtomatisk venös tromboembolism hos patienter med cancer (EINSTEIN-DVT och EINSTEIN-PE): en poolad subgruppsanalys av två randomiserade kontrollerade studier. Lancet Hematol 2014; 1: e37-46.
- Raskob GE, van Es N, Segers A, et al. Edoxaban för venös tromboembolism hos patienter med cancer: resultat från en non-inferiority subgruppsanalys av Hokusai-VTE randomiserad, dubbelblind, dubbelblind studie. Lancet Hematol 2016; 3: e379-87.
- Schulman S, Goldhaber SZ, Kearon C, et al. Behandling med dabigatran eller warfarin hos patienter med venös tromboembolism och cancer. Thromb Hemost 2015; 114: 150-7.
kliniska ämnen: Anticoagulation Management, Arrhythmias and Clinical EP, Cardio-Oncology, Pulmonary Hypertension and Venous Thromboembolism, Anticoagulation Management and Atrial Fibrillation, Anticoagulation Management and Venothromboembolism, Atrial Fibrillation/Supraventricular Arrhythmias
Keywords: Kardiotoxiner, kardiotoxicitet, Heparin, lågmolekylär, Warfarin, antikoagulantia, internationellt normaliserat förhållande, acenokumarol, Dalteparin, Antitrombiner, venös tromboembolism, riskfaktorer, förmaksflimmer, polikliniker, forskningspersonal, livskvalitet, Pyridon, Pyrazoler, Pyridiner, Tiazoler, venös trombos, lungemboli, trombos, trombocytopeni, komorbiditet, hemostas, neoplasmer
< tillbaka till listor