toate celulele tisulare depind de metabolismul aerob pentru generarea energiei (sub formă de adenozină tri-fosfat, ATP) necesare supraviețuirii și funcției. Acest proces mitocondrial fundamental vital se caracterizează prin consumul de oxigen și producerea de dioxid de carbon, care poate varia de la aproximativ 200 mL/minut în stare de repaus la peste cinci ori această rată în timpul exercițiului.
soarta finală a acestui dioxid de carbon este eliminarea din organism în aerul expirat, iar o funcție importantă a sângelui este transportul dioxidului de carbon din celulele țesutului în plămâni.
înțelegerea acestui proces de transport depinde de aprecierea a ceea ce se înțelege prin presiunea parțială a unui gaz, precum și de unele legi fizice de bază care guvernează solubilitatea și mișcarea (difuzia) gazelor.
- CE ESTE PRESIUNEA PARȚIALĂ A UNUI GAZ?
- solubilitatea și difuzia gazelor
- transportul dioxidului de CARBON de la celulele tisulare la plămâni
- dioxidul de CARBON și PH-ul sanguin
- în laborator-definirea parametrilor CO2
- presiunea parțială a dioxidului de CARBON pCO2
- concentrația de bicarbonat (HCO3 -)
- concentrația totală de dioxid de CARBON în plasmă (ctCO2)
- metode chimice pentru măsurarea ctCO2
- discordanță între ctCO2 măsurat și bicarbonat calculat
- rezumat
CE ESTE PRESIUNEA PARȚIALĂ A UNUI GAZ?
cantitatea de gaz dintr-un sistem, inclusiv sistemele biologice, este definită de presiunea pe care o exercită, măsurată în mod tradițional ca înălțimea unei coloane de mercur (mmHg). Astfel, spunând că presiunea atmosferică este de 760 mmHg, înțelegem că gazele (oxigen, azot și dioxid de carbon) din aerul pe care îl respirăm au o presiune combinată suficientă pentru a susține o coloană standard de mercur de 760 mm înălțime.
această presiune totală este pur și simplu suma presiunilor parțiale ale fiecărui gaz constituent. Astfel, deoarece aerul cuprinde aproximativ 20% oxigen, 79% azot și 0.03% dioxid de carbon, presiunea parțială a oxigenului (pO2) în aerul inspirat este de aproximativ (20 x 760) / 100 = 152 mmHg și presiunea parțială a dioxidului de carbon (pCO2) este (0,03 x 760) / 100 = 0,2 mmHg.
unitatea de presiune systeme internationale (SI), utilizată în laboratoarele clinice din afara Americii de Nord, este kilopascalul (kPa). Factorul de conversie 0.133 poate fi utilizat pentru a converti mmHg în kPa.
solubilitatea și difuzia gazelor
Legea lui Henry afirmă că la echilibru cantitatea de gaz dizolvat într-un lichid este proporțională cu presiunea parțială a acelui gaz, atât timp cât temperatura este constantă:
gaz dizolvat = presiune parțială (p) x coeficient (s) de solubilitate
unde S este o constantă dependentă de temperatură pentru gazul respectiv. Coeficientul (coeficienții) de solubilitate pentru dioxidul de carbon la temperatura corpului este de 0,23 mmol/L/kPa (sau 0,03 mmol/mmHg) . Astfel, deoarece pCO2 arterial este de aproximativ 5.3 kPa (40 mmHg), cantitatea de CO2 dizolvată în sângele arterial (dCO2) este (5,3 x 0,23) sau 40 x 0,03) = 1,2 mmol/L.
mișcarea (difuzia) gazelor este determinată în mare parte de gradienții de concentrație. Gazul difuzează de la presiune parțială ridicată la presiune parțială scăzută .
transportul dioxidului de CARBON de la celulele tisulare la plămâni
călătoria dioxidului de carbon (figura 1a) începe în mitocondriile celulelor tisulare unde este produsă. Datorită gradientului de concentrație predominant, dioxidul de carbon difuzează din mitocondrii (unde pCO2 este cel mai mare) în citoplasmă, în afara celulei și în rețeaua capilară.
figura 1a: CO2 în țesuturi
Click Pentru mărire
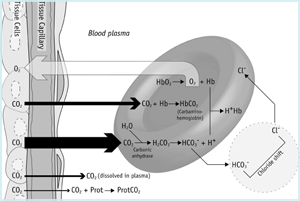
un pic din CO2 care ajunge în sânge din celulele tisulare rămâne dizolvat fizic în plasma sanguină (vezi mai sus) și o proporție și mai mică se leagă de grupările terminale NH2 (amino) ale proteinelor plasmatice, formând așa-numiții compuși carbamino. Cele mai multe cu toate acestea, difuzează în jos un gradient de concentrație în celule roșii.
o mică parte din aceasta rămâne dizolvată în citoplasma celulei roșii, iar unele sunt legate în mod liber de grupările terminale amino ale hemoglobinei reduse care formează carbamino-Hb. Cu toate acestea, cea mai mare parte a dioxidului de carbon care ajunge în celulele roșii este rapid hidratată în acid carbonic de către izoforma celulelor roșii a enzimei anhidrază carbonică. La pH fiziologic aproape toate (96%) din acest acid carbonic disociază la ioni de bicarbonat și hidrogen:
ecuația 1:
![]()
ionii de hidrogen sunt tamponați de hemoglobină redusă și majoritatea ionilor de bicarbonat trec de la celula roșie la plasmă în schimbul ionilor de clorură (această așa numită schimbare a clorurii menține neutralitatea electrochimică). Este clar din cele de mai sus că majoritatea dioxidului de carbon este transportat ca bicarbonat (predominant în plasma sanguină), dar există în total patru moduri de transport de CO2 :
- 90 % este transportat ca bicarbonat în plasmă (65 %) și celule roșii (25 %)
- 5 % este transportat fizic dizolvat în plasmă și citoplasma celulelor roșii
- 5% este transportat slab legat de hemoglobină în celulele roșii și
conținutul total de dioxid de carbon din sânge este suma acestor patru componente.
în microvasculatura plămânilor (figura 1b) gradientul de presiune parțială pe membrana alveolară determină că CO2 dizolvat trece din sânge în Alveole. Această pierdere de dioxid de carbon din sânge favorizează inversarea reacțiilor celulelor roșii descrise mai sus.
astfel bicarbonatul trece de la plasmă la celulele roșii, tamponând ionii de hidrogen eliberați din hemoglobină, deoarece este oxigenat. Inversarea reacției anhidrazei carbonice are ca rezultat producerea de CO2 care difuzează de la celulele roșii la plasmă și mai departe la Alveole.
sângele venos mixt care ajunge la plămâni are un conținut total de CO2 de aproximativ 23, 5 mmol/l (sau 52 mL/dL), în timp ce sângele arterial care părăsește plămânii are un conținut total de CO2 de 21, 5 mmol/l (48 mL/dL).
această diferență arterio-venoasă (2 mmol/l sau 4 mL/dL) reprezintă cantitatea de CO2 adăugată în sânge din celulele tisulare și pierdută din sânge pe măsură ce trece prin microvasculatura pulmonară, pentru a fi în cele din urmă excretată din organism în aer expirat.
figura 1b: CO2 în plămâni
Faceți clic pentru a mări
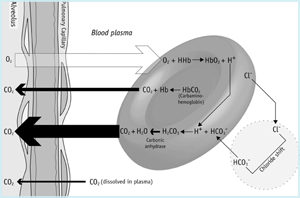
dioxidul de CARBON și PH-ul sanguin
potențialul acid al CO2, datorită reacției sale de hidratare la acidul carbonic (a se vedea ecuația 1 de mai sus), asigură că concentrația sa în sânge este un factor determinant major al pH-ului sanguin. Pe măsură ce concentrația de CO2 crește, la fel și concentrația ionului de hidrogen (H+). Reglarea CO2 din sânge, adică potrivirea ratei de eliminare a CO2 în aerul expirat cu rata de producție în mitocondriile celulelor tisulare, esențială pentru menținerea pH-ului normal al sângelui, este activitatea sistemului respirator.
rata de respirație (controlată de chemoreceptorii sensibili la pCO2 localizați în trunchiul cerebral și artera carotidă) este crescută dacă pCO2 crește și scade dacă pCO2 scade. Creșterea frecvenței respiratorii (respirații/min) duce la creșterea ratei de eliminare a CO2 și scăderea frecvenței respiratorii favorizează retenția CO2.
relația dintre pH și dioxidul de carbon este descrisă de o formă a ecuației Henderson-Hasselbach (ecuația 2). Acest lucru este derivat din aplicarea legii acțiunii în masă la reacțiile de hidratare și disociere descrise în ecuația 1 .
ecuație 2:
![]()
unde
| pK/1 | = | ‘constanta de disociere aparentă a acidului carbonic = 6.1 |
| = | concentrația bicarbonatului plasmatic (mmol / L) | |
| S | = | coeficientul de solubilitate pentru CO2 la 37 oC (0,23 dacă pCO2 este măsurat în kPa sau 0,03 dacă pCO2 este măsurat în mmHg) |
| pCO2 | = | presiunea parțială a pCO2 (kPa sau mmHg) |
după cum sa explicat anterior, numitorul din această ecuație (s x pCO2) este cantitatea de dioxid de carbon dizolvat (dCO2) mmol / L.
prin eliminarea tuturor constantelor, ecuația 2 poate fi simplificată la:
ecuația 3:
pH-ul / pCO2
astfel, pH-ul sângelui depinde de raportul dintre concentrația plasmatică de bicarbonat (componenta metabolică) și pCO2 (componenta respiratorie). Astfel, dacă pCO2 crește fără o creștere echivalentă a bicarbonatului, pH-ul scade. În schimb, dacă pCO2 scade fără o scădere echivalentă a bicarbonatului, pH-ul crește.
relația inversă este valabilă pentru concentrația de bicarbonat și anume creșterea HCO3– = creșterea pH-ului; scăderea bicarbonatului = scăderea pH-ului.
bicarbonatul este principalul tampon de sânge și concentrația sa la un moment dat reflectă echilibrul dintre cel produs din CO2 și cel consumat în tamponarea ionilor de hidrogen (H+) (vezi ecuația 1).
în laborator-definirea parametrilor CO2
parametrii CO2 generați de analizorul de gaze din sânge sunt:
- presiunea parțială a dioxidului de carbon (pCO2) (kPa/mmHg)
- concentrația plasmatică de bicarbonat (HCO3 -) (mmol/L)
- concentrația plasmatică totală dioxid de carbon (ctCO2) (mmol / L)
ultimul dintre acestea, ctCO2, poate fi măsurat și în plasmă sau ser prin metode chimice independente de analizorul de gaze din sânge.
presiunea parțială a dioxidului de CARBON pCO2
acest parametru este o măsură a presiunii exercitate de acea mică parte (5 %) a dioxidului de carbon total din sânge care rămâne în stare gazoasă, ‘dizolvată în’ faza apoasă a plasmei și a citoplasmei celulelor sanguine. Măsurarea se face folosind un electrod de pH specific CO2 încorporat în analizoarele de gaze din sânge.
în sănătate pCO2 de sânge arterial este menținut în intervalul 4,7-6,0 kPa (35-45 mmHg); pCO2 de sânge venos este puțin mai mare 5,6-6,8 kPa (41-51 mmHg).
concentrația de bicarbonat (HCO3 -)
aceasta este cantitatea de bicarbonat în unitatea de volum a plasmei. După cum sa menționat anterior, aceasta este forma în care majoritatea dioxidului de carbon (90 %) este transportat în sânge. Acest parametru nu poate fi măsurat, ci este generat prin calcul în timpul analizei gazelor din sânge. Calculul utilizat este o rearanjare a ecuației 2:
ecuație 4:
log = pH + log (S x pCO2) – pK/1
și depinde de a avea valori pentru pH și pCO2, ambele fiind măsurate în timpul analizei gazelor din sânge.
teoretic bicarbonatul plasmatic este diferența dintre CO2 total (ctCO2) și suma tuturor celorlalte forme de CO2 din plasmă, adică CO2 dizolvat (dCO2), CO2 legat de proteinele plasmatice (carbamino CO2) și acidul carbonic (H2CO3).
astfel:
bicarbonat de plasmă (mmol / L) =
ctCO2 – (dCO2 + carbamino-CO2 + H2CO3)
în practică, deoarece carbamino-CO2 și H2CO3 sunt nesemnificative cantitativ, se presupune că CO2 total este suma doar a bicarbonatului și a CO2 dizolvat . Astfel, bicarbonatul de plasmă este efectiv diferența dintre CO2 total plasmatic (ctCO2) și CO2 dizolvat în plasmă (dCO2).
în sănătate bicarbonatul plasmatic arterial (calculat în timpul analizei gazelor sanguine) se menține în intervalul de referință aproximativ: 22-28 mmol/L. bicarbonatul venos este puțin mai mare: 24-30 mmol/L.
în unele laboratoare se face distincția între bicarbonatul ‘real’ (parametrul descris mai sus) și bicarbonatul ‘standard’. Bicarbonatul Standard este un al doilea parametru calculat și este concentrația plasmatică de bicarbonat din sânge care a fost echilibrată cu gaz de tensiune normală pCO2 (40 mmHg, 5,3 kPa).
în sănătate, atunci concentrația reală de bicarbonat este aceeași cu concentrația standard de bicarbonat, deoarece în ambele cazuri pCO2 este normal. Prin normalizarea pCO2, componenta respiratorie a echilibrului acido-bazic, bicarbonatul standard este o măsură exclusiv a componentei metabolice și, prin urmare, este considerat util pentru elucidarea cauzei tulburărilor complexe ale echilibrului acido-bazic.
concentrația totală de dioxid de CARBON în plasmă (ctCO2)
aceasta este teoretic suma tuturor formelor de dioxid de carbon din plasmă. Nu se măsoară în timpul analizei gazelor din sânge, ci – ca bicarbonatul-calculat, presupunând ca mai sus că dioxidul de carbon total este suma bicarbonatului și a CO2 dizolvat:
deoarece plasma dCO2 mmol / L =(S x pCO2), ctCO2 se calculează astfel :
ctCO2 plasmatic (mmol/l) =
bicarbonat de plasmă (mmol/L) + (S x pCO2) (mmol / L)
CO2 dizolvat (s x pCO2) contribuie cu aproximativ 1.2 mmol/L la CO2 total din plasma sângelui arterial (vezi mai sus), astfel încât ctCO2 este cu aproximativ 1,2 mmol mai mare decât bicarbonatul plasmatic. Intervalul de referință ctCO2 este astfel de aproximativ 23-29 mmol / l pentru sângele arterial.
se va observa că la fel cum valoarea calculată a bicarbonatului generată în timpul analizei gazelor din sânge depinde de relația descrisă în ecuația 2, la fel și valoarea calculată pentru ctCO2 generată în timpul analizei gazelor din sânge.
deși ctCO2 și bicarbonatul oferă informații clinice echivalente, în practica clinică este invariabil bicarbonat mai degrabă decât ctCO2 care este utilizat împreună cu pH și pCO2 pentru a evalua starea acido-bazică. Valoarea clinică a ctCO2 calculată generată în timpul analizei gazelor din sânge este astfel limitată.
metode chimice pentru măsurarea ctCO2
spre deosebire de bicarbonat, care nu poate fi măsurat, ctCO2 poate și testul este de obicei o componentă a profilului ureei și electrolitului (U & E) al plasmei/serului venos. Deoarece U & E este comandat mult mai frecvent decât gazele arteriale din sânge, ctco2 măsurat poate fi primul indiciu al perturbării homeostaziei dioxidului de carbon (și, prin urmare, acido-bazic).
este o practică obișnuită ca unele laboratoare clinice să se refere la această componentă măsurată a profilului U& E ca ‘bicarbonat de plasmă’. Acest lucru este eronat, deoarece metodele chimice măsoară tot CO2 eliberat din plasmă (sau ser) prin adăugarea de acid puternic sau, alternativ, tot bicarbonatul produs ca urmare a adăugării unui alcalin puternic în plasmă .
include astfel nu numai bicarbonatul, ci și CO2 dizolvat și acidul carbonic. Dacă plasma sau serul utilizat în aceste teste au fost derivate din sângele arterial, atunci ctCO2 măsurat ar fi teoretic aproximativ la valoarea ctCO2 calculată generată în timpul analizei gazelor arteriale din sânge.
de fapt, profilele U & E sunt efectuate exclusiv pe plasmă sau ser recuperat din sângele venos, astfel încât există o diferență teoretică inevitabilă mică de 1-2 mmol/L (măsurată ctCO2 > calculată ctCO2) datorită diferenței arterio-venoase.
diferența teoretică dintre ctCO2 măsurat și bicarbonatul plasmatic calculat este puțin mai mare (ctCO2 măsurat > bicarbonat plasmatic calculat) deoarece în plus față de diferența arterio-venoasă de 1-2 mmol/l există o diferență suplimentară de 1, 5 mmol/l datorită includerii CO2 dizolvat și a acidului carbonic în ctCO2 măsurat.
cu toate acestea, această diferență presupune că nu se pierde dioxid de carbon dizolvat în atmosferă înainte de analiză. Este posibil să nu fie cazul, deoarece probele U&E nu sunt manipulate anaerob.
unii au susținut că termenul ‘bicarbonat seric/plasmatic’ pentru ctCO2 măsurat este justificat pe motiv că practica normală de laborator este asociată cu o pierdere inevitabilă de CO2 dizolvat din eșantionul U& E înainte de analiză, caz în care ctCO2 măsurat ar fi, teoretic cel puțin, aproximativ la bicarbonatul calculat.
discordanță între ctCO2 măsurat și bicarbonat calculat
fără a aduce atingere ușoarelor diferențe teoretice dintre valorile măsurate și cele calculate prezentate mai sus, există o acceptare generală a noțiunii că ctCO2 măsurat generat ca parte a unui profil U & E este pentru toate scopurile clinice practice aceeași cu concentrația plasmatică de bicarbonat calculată în timpul analizei gazelor sanguine.
acest lucru se reflectă în utilizarea termenului ‘bicarbonat de plasmă’ pentru a descrie ctCO2 măsurat.
cele mai bune dovezi până în prezent că rezultatele măsurate și calculate ale bicarbonatului pot fi în practică interschimbabile din punct de vedere clinic vin într-un raport foarte recent al Clinicii Mayo . Autorii acestui raport au recuperat 17.621 de înregistrări ale concentrației de bicarbonat măsurate și calculate pentru probele colectate simultan de la aceiași pacienți în perioada 2006/7. Concentrația de bicarbonat a acestei baze de date uriașe a variat de la 5 la 49 mmol/L.
diferența medie (SD) între valorile măsurate și calculate a fost de -0,36 (1,23 mmol/L), iar pentru 98.5% din rezultatele probelor împerecheate au fost la o distanță de 3 mmol/l una de cealaltă. Deși, așa cum sugerează raportul Mayo, există de obicei un acord acceptabil între cei doi parametri, nu este deloc rar ca rezultatele să fie complet discordante, ctCO2 măsurat diferind de bicarbonatul calculat cu până la 15 mmol/L .
numeroase studii din ultimii patruzeci de ani au căutat să stabilească frecvența, magnitudinea și cauza discrepanței dintre bicarbonatul calculat și ctCO2 măsurat.
o concentrare timpurie a acestei lucrări a pus sub semnul întrebării fiabilitatea calculului bicarbonatului, care depinde în mod crucial de Constanța pK/1 (vezi ecuația 4). De fapt, aceasta nu este o constantă termodinamică adevărată, ci o constantă de disociere’ aparentă ‘ determinată experimental din măsurarea pH – ului, pCO2 și CO2 dizolvat folosind următoarea relație derivată din ecuația Henderson-Hasselbach:
pK/1 = pH + log dCO2 – log
mai multe studii au evidențiat o variabilitate suficientă în pK/1, în special în rândul bolnavilor critici, pentru erori semnificative clinic în bicarbonatul calculat. De exemplu, într-un studiu, s-a constatat că pK/1 variază între 5,84 și 6,29.
autorii calculează că abaterile de la pK/1 6.1 de această magnitudine ar duce la erori în bicarbonatul calculat de ordinul 60 %. Un altul descrie cazul unui copil diabetic în cetoacidoză a cărui pK / 1 a variat între 5, 49 și 6, 02 pe o perioadă de șapte ore.
într-un studiu pe 79 de sugari îngrijiți într-o unitate de terapie intensivă pediatrică , 25% s-au dovedit a avea pK/1 în afara intervalului normal 6.055-6.195 definit de studiu, iar în trei cazuri pK/1 a fost > 6.3, cu o valoare uluitoare de 7.11. Aceste rapoarte și alte rapoarte de variabilitate semnificativă clinic în pK / 1 au fost contestate, iar fiabilitatea sau altfel a bicarbonatului calculat rămâne o problemă nerezolvată, controversată.
baza teoretică pentru opinia că bicarbonatul calculat nu este fiabil în boala critică a fost stabilită de Flear . O abordare la fel de teoretică însoțită de o multitudine de dovezi experimentale a fost desfășurată de Mass și colab.pentru a face cazul opus în apărarea bicarbonatului calculat.
autorii studiilor care nu au reușit să demonstreze o variabilitate semnificativă clinic în fc/1 sugerează că discordanța majoră dintre bicarbonatul calculat și ctCO2 măsurat, observată ocazional în practica clinică, este cel mai probabil rezultatul unei combinații de variabile preanalitice, diferență analitică și eroare analitică aleatorie .
măsurarea ctCO2 este deosebit de predispusă la variabilitatea pre-analitică, deoarece sângele pentru profilarea U&E este colectat universal și prelucrat aerob. Probele pot fi lăsate fără capac ore întregi înainte de analiză. Deoarece aerul ambiant conține mai puțin CO2 decât sângele, există tendința ca CO2 dizolvat să se piardă din probă. S-a estimat că aceasta reduce CO2 măsurat cu o rată de 6 mmol/oră.
prin contrast, bicarbonatul calculat nu este asociat cu același risc de variație preanalitică, deoarece analizele de sânge pentru gazele din sânge sunt prelevate în mod obișnuit anaerob și există o întârziere minimă (aproape invariabil
o altă cauză contributivă a discordanței dintre valorile măsurate și cele calculate ar putea fi diferența de probă, deoarece sângele arterial este utilizat pentru a calcula o valoare, iar probele de ser sau plasmă sunt utilizate pentru a măsura o valoare.
oricare ar fi cauza, studiile continuă să demonstreze o discordanță moderată, dar semnificativă clinic între cei doi parametri în rândul bolnavilor critici . Cu toate acestea, ca și cum ar confirma natura controversată a dezbaterii, cel mai recent studiu al pacienților cu boli critice oferă dovezi ale unui acord acceptabil între bicarbonatul calculat și ctCO2 măsurat .
în ciuda acestui ultim studiu, există un corp de opinie că, cel puțin pentru pacienții cu boli critice , ar putea fi prudent să se abandoneze bicarbonatul calculat în favoarea ctCO2 măsurat, deși trebuie subliniat faptul că acest punct de vedere este controversat și ar putea fi faptul că impactul clinic al diferențelor este limitat.
dovezile unui acord acceptabil furnizate de studiul Clinic Mayo foarte mare nu pot fi, din păcate, utilizate în dezbaterea specială care se concentrează asupra bolnavilor critici, deoarece populația de pacienți nu a fost definită.
dintre cei doi parametri, bicarbonatul calculat are avantajul distinct de comoditate față de ctCO2 măsurat, deoarece permite ca toți cei trei parametri (pH pCO2 și bicarbonat) utilizați în evaluarea acido-bazică să fie disponibili în același timp dintr-o singură probă.
nu există un consens în literatura de specialitate cu privire la multe dintre problemele discutate mai sus. Astfel, rămâne chiar neclar dacă există sau nu discordanță între CO2 măsurat și calculat, deși echilibrul dovezilor s-a schimbat recent în favoarea lipsei de discordanță de către marele studiu Clinic Mayo .
pentru cei care cred că echilibrul dovezilor sugerează că există discordanță, există alte două probleme nerezolvate.
acestea sunt: semnificația clinică a acelei discordanțe și cauza acelei discordanțe. Dezbaterea despre cauza discordanței s-a concentrat în principal pe faptul dacă pKl1 variază sau nu semnificativ între pacienți și măsura în care diferențele preanalitice, diferențele analitice și erorile aleatorii contribuie la discordanță.
în cele din urmă, cel puțin un comentator a pus sub semnul întrebării necesitatea clinică fie a bicarbonatului calculat, fie a ctCO2 măsurat, sugerând că pH-ul și pCO2 singure permit evaluarea completă a tulburărilor acido-bazice.
rezumat
dioxidul de Carbon este un produs al metabolismului celular aerob care este transportat în sânge la plămâni pentru excreție în aerul expirat. Un pic este transportat nemodificat dizolvat în sânge, dar cel mai mult este transportat ca bicarbonat.
reglarea cantității de dioxid de carbon din sânge sau, mai precis, reglarea raportului dintre bicarbonat și concentrația de dioxid de carbon dizolvat, este esențială pentru menținerea pH-ului sanguin (echilibrul acido-bazic normal).
investigarea clinică a perturbării acido-bazice include analiza gazelor arteriale din sânge, un test care generează trei parametri ai stării dioxidului de carbon. Dintre acestea, doar unul, pCO2, este de fapt măsurat; celelalte două – bicarbonatul plasmatic și concentrația totală de dioxid de carbon – sunt derivate prin calcule din pH-ul măsurat și pCO2.
validitatea acestor calcule a fost pusă la îndoială și există dovezi contradictorii că la unele grupuri de pacienți ar putea fi mai fiabil din punct de vedere clinic să se măsoare dioxidul de carbon total prin metode chimice, decât să se bazeze pe valori calculate.
aceasta din urmă rămâne o problemă extrem de controversată care poate fi rezolvată în cele din urmă doar prin studii suplimentare.