semnificație
există un interes tot mai mare pentru circrna datorită implicării lor în multe procese biologice și boli, pe lângă potențialul lor de biomarker. Acestea sunt detectate în principal prin prezența citirilor care cartografiază joncțiunea lor de backsplicing. Cu toate acestea, circrna-urile nu mai sunt singurele Transcrieri care conțin o astfel de joncțiune, deoarece studii recente au arătat că ADN-urile circulare sunt comune și pot fi transcrise, rezultând Transcrieri care ar imita un semnal circRNA. Prin urmare, acest nou tip de transcriere himerică poate schimba modul în care se face analiza circRNA și poate afecta unele dintre rezultatele deja raportate.
sunt ARN-urile circulare singurele Transcrieri himerice?
ARN Circular (circrna) au fost redescoperite cu câțiva ani în urmă ca forme ARN ne-canonice îmbinate prezente în diferite organisme, inclusiv în oameni (Salzman și colab., 2012; Jeck și colab., 2013). Sunt transcrieri închise covalent formate printr-un eveniment de îmbinare a ARN-ului, unde un donator de îmbinare al unui Exon din aval se alătură unui acceptor de îmbinare în amonte care duce la transcrieri închise covalent care se caracterizează prin prezența unei joncțiuni de îmbinare din spate care face ca circrn-urile să se distingă de omologii lor liniari (figura 1a) (Zhang și colab., 2016; Wilusz, 2018).
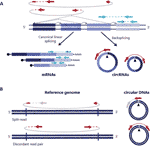
Figura 1 detectarea atât a ARN-ului circular, cât și a ADN-urilor se bazează pe citiri care acoperă joncțiunea. (A) îmbinarea din spate între exoni și îmbinarea canonică a exonilor sunt descrise cu linii non-continue și, respectiv, continue, dând naștere la circrna și ARNm. Citirile pereche-end care acoperă joncțiunile din spate sunt afișate în roșu, iar citirile pereche-end în concordanță cu o transcriere liniară sunt afișate în albastru. (B) Similar cu circrna, ADN-urile circulare (eccdna) sunt detectate pe baza variantelor de citire structurală în concordanță cu un eveniment de circularizare descris în roșu .
de la redescoperirea lor, comunitatea științifică și-a atras atenția asupra circrna și a investigat implicarea lor în mai multe procese celulare în sănătate și boli (Haque și Harries, 2017), rolul lor potențial de biomarkeri (Abu și Jamal, 2016) și funcțiile lor de reglementare (Floris și colab., 2016). Circrna-urile sunt acum cunoscute a fi abundente și stabile în citosol și nucleu (Salzman și colab., 2012; Jeck și colab., 2013; Li și colab., 2015) și au fost, de asemenea, găsite libere în biofluide (Bahn și colab., 2015; Memczak și colab., 2015; Chen și colab., 2018) și în veziculele extracelulare (Kyoung Mi și colab., 2017). Potențialul biomarker al circrna a fost intens studiat, de fapt, au fost publicate multe studii de caz-control care caută circrna exprimate diferențiat care ar putea fi biomarkeri ai diferitelor boli. Până în prezent, circrna-urile au fost implicate în mai multe boli, inclusiv cancerul (Kristensen și colab., 2017; Arnaiz și colab., 2018), tulburări neurologice (Akhter, 2018), boli cardiovasculare (Aufiero și colab., 2019) și boli legate de imunitate (Iparraguirre și colab., 2017; Liu și colab., 2019). În același timp, înțelegerea pe deplin a biogenezei, caracteristicilor, funcțiilor și implicațiilor lor în biologia umană rămân întrebări deschise pentru cercetătorii din domeniu.
deși funcția majorității circRNAs rămâne necunoscută, s-a demonstrat că unele circRNAs pot acționa ca bureți microARN, reglând nivelurile microARN și activitatea lor (Hansen și colab., 2013; Memczak și colab., 2013; Zheng și colab., 2016). Sunt implicați în reglarea expresiei genelor prin reglarea transcripției genelor lor parentale, concurând cu splicing liniar sau proteine spongioase (Ashwal-Fluss și colab., 2014; Li și colab., 2018). Interesant este că studiile de profilare a ribozomilor au arătat recent că circrna-urile pot fi traduse atât in vitro, cât și in vivo (Legnini și colab., 2017; Yang și colab., 2017).
caracteristica principală a circRNAs și responsabilă pentru majoritatea proprietăților lor speciale este circularitatea lor. Prin urmare, pe lângă detectarea joncțiunii lor caracteristice îmbinate în spate, testarea circularității acestor molecule, este unul dintre punctele cheie în fiecare studiu circRNA. Cu toate acestea, multe studii și-au bazat descoperirea circrna pe ARN total și, prin urmare, ar fi putut interpreta unele transcrieri chimerice liniare ca circrna, rezultând detectări fals pozitive ale circRNA. Pentru a ocoli această problemă, majoritatea studiilor au confirmat circularitatea transcrierilor găsite prin ARN-seq total folosind RNase r, Northern blot sau metode electroforetice (Jeck și Sharpless, 2014). Cu toate acestea, aceste validări de circularitate au dezvăluit uneori și transcrieri care par a fi liniare, mai degrabă decât circulare, confirmând că detectarea circrn-urilor pornind de la ARN total poate duce la unele fals pozitive. Aceste fals pozitive au fost atribuite artefactelor tehnice sau transcrierilor derivate din evenimente mai puțin frecvente, cum ar fi duplicările exonice sau evenimentele de transplant (Jeck și Sharpless, 2014; Szabo și Salzman, 2016). Acestea fiind spuse, opțiunea de a găsi transcrieri liniare adevărate, biologic active și funcționale, care conțin o secvență echivalentă cu o joncțiune de backsplicing (de acum înainte numită transcrieri liniare himerice), a fost oarecum trecută cu vederea, deoarece o sursă de astfel de ARN liniar nu a fost cunoscută pentru celulele sănătoase.
ADN Circular ca sursă de transcrieri liniare himerice
cea mai mare parte a genomului uman este organizată în cromozomi liniari, cu toate acestea, unele excepții au fost acceptate de mult timp, cum ar fi ADN-ul mitocondrial și aberațiile cromozomiale, cum ar fi cercurile ADN care transportă oncogene (de exemplu, minute duble) (Benner și colab., 1991; Nathanson și colab., 2014; Turner și colab., 2017) și cromozomi inelari (T., 2004). Nu a fost până de curând că diferite ADN-uri circulare, cum ar fi microDNAs (Shibata și colab., 2012) sau ADN-urile circulare extrachromozomale (eccDNAs) s-au dovedit a apărea, de asemenea, din părți mari ale diferitelor genomi eucariote, inclusiv umane și drojdii (m Electicller și colab., 2015; Kumar și colab., 2017; m Okticller și colab., 2018).
ADN-urile circulare se formează atunci când două capete ale unui ADN liniar sunt îmbinate împreună, rezultând o joncțiune similară cu joncțiunea din spate pe circRNAs numită în mod obișnuit joncțiune punct de întrerupere care este detectată pe baza variantelor de citire structurală în concordanță cu un eveniment de circularizare (Gresham și colab., 2010; m Okticller și colab., 2018; Prada-Luengo și colab., 2019) (figura 1B). De obicei, acestea variază de la o sută de baze la cercuri megabase și pot conține exoni și gene complete (Shibata și colab ., 2012; m Okticller și colab., 2015; Kumar și colab., 2017; Turner și colab., 2017; m Okticller și colab., 2018) și, în timp ce unele regiuni ale genomului se găsesc mai frecvent pe ADN-ul circular (Sinclair și Guarente, 1997;; m Okticller și colab., 2016; Turner și colab., 2017; m Okticller și colab., 2018), majoritatea ADN-ului circular par să apară la întâmplare (Shibata și colab., 2012; m Okticller și colab., 2015; Kumar și colab., 2017; m Okticller și colab., 2018).
interesant, într-o lucrare recentă m Elixtller și colab. a identificat mii de eccDNAs în leucocite și celule musculare în controale sănătoase. Cu ideea de a investiga dacă eccdna-urile ar putea fi transcrise, o bibliotecă de ARNm a fost, de asemenea, secvențiată din țesutul muscular și analizată pentru evenimentele de transcriere de-a lungul joncțiunii punctului de întrerupere a eccDNA detectată găsind mai multe potriviri (m Electicller și colab., 2018). Această constatare sugerează că ADN-ul circular din țesutul sănătos este transcris, dând naștere la transcrieri liniare și poliadenilate care vor purta o secvență echivalentă cu secvența de backsplicing a circRNAs (m Electicller și colab., 2018) (Figura 2).
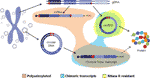
Figura 2 reprezentarea grafică a diferitelor transcrieri apărute fie din ADN genomic, fie din ADN circular. Exonii sunt colorați în violet, iar joncțiunile din spate sau joncțiunile himerice sunt afișate în roșu. Poliadenilat, joncțiune himerică conținând și RNase r transcrieri rezistente sunt evidențiate în portocaliu, albastru și galben, respectiv.
dovezile transcripționale ale ADN-urilor circulare, împreună cu abundența lor, ne conduc să sugerăm că ADN-urile circulare ar putea fi o sursă naturală a unei cantități substanțiale de ARN-uri liniare care transportă joncțiuni himerice. În multe cazuri, aceste joncțiuni himerice ar putea fi indistinguizabile de joncțiunile din spate ale circrna-urilor și, prin urmare, ar putea fi factori confuzi în studiile circRNA. În paragrafele următoare, vom explica datele care susțin această propunere.
detectarea arnc: Tot ceea ce strălucește nu este aur
așa cum a fost introdus anterior, circrna-urile se formează printr-un eveniment de îmbinare non-canonic numit backsplicing. Transcrierile rezultate din acest eveniment de backsplicing au o structură de buclă închisă covalent, fără polaritate de 5′-3′, nici o coadă poliadenilată și, mai important, se caracterizează prin prezența unui ordin Exon scrambled în raport cu transcrierea liniară (Zhang și colab., 2016; Wilusz, 2018). Acest ordin Exon scrambled devine evident în joncțiunea backspliced care conectează o secvență de 5′ în aval cu o secvență de 3′ în amonte. Astfel, toți algoritmii de detectare a circRNA exploatează prezența joncțiunilor îmbinate în spate ca o caracteristică de diagnostic pentru identificarea circRNA (figura 1A).
au fost adaptate diferite metode pentru detectarea acestor joncțiuni îmbinate în spate. Tablourile comerciale care conțin sonde care vizează aceste regiuni din spate au fost utilizate pe scară largă în studiile de screening pentru biomarker (Iparraguirre și colab., 2017; Liu și colab., 2017; Sui și colab., 2017; Li și colab., 2018). Validarea ulterioară se bazează adesea și pe amplificarea joncțiunilor backsplicing folosind primeri Divergenți (Panda și Gorospe, 2018). Multe alte lucrări au efectuat o analiză de secvențiere cu randament ridicat care depășește una dintre principalele limitări ale matricelor, permițând detectarea nu numai a circrn-urilor adnotate, ci și a evenimentelor de circularizare a ARN-ului de novo din regiunile genomice în care niciun circRNA nu a fost adnotat de studiile anterioare. Mai multe conducte bioinformatice au fost dezvoltate pentru detectarea circRNAs în seturile de date ARN-Seq, dar toate se bazează pe prezența citirilor care trec peste joncțiunile de îmbinare din spate și găsirea celei mai fiabile este încă o provocare pentru bioinformaticieni (Hansen și colab., 2016; Hansen, 2018; Prada-Luengo și colab., 2019).
două abordări principale pot fi urmate pentru detectarea circRNAs în datele ARN-Seq. În primul rând, multe studii ARN-seq circRNA se bazează pe probe tratate cu RNase R pentru a epuiza toate ARN-urile liniare înainte de secvențiere. Deși această abordare este special concepută pentru detectarea arncr, este de remarcat faptul că degradarea RNase R este variabilă, că există cazuri rare de ARNr liniare rezistente la RNase R și circRNAs sensibile la RNase r (Szabo și Salzman, 2016) și că acest tratament necesită un aport ridicat de ARN care ar putea fi limitativ pentru unele țesuturi. Alte studii circRNA aleg să secvențeze fie ARN total, ribozomal-epuizat (ribo -), fie non-poliadenilat (polyA -), unde pot fi găsite ARN-uri liniare și circulare (Salzman și colab., 2012; Memczak și colab., 2013; Broadbent și colab., 2015; Lu și colab., 2015; Memczak și colab., 2015). Această abordare evită utilizarea RNase R, care reduce cantitatea de ARN necesară pentru secvențiere și permite studierea expresiei altor tipuri de ARN din același set de date. S-a demonstrat că, cu o bună adâncime și calitate de secvențiere și o analiză atentă a datelor, circrn-urile adevărate pot fi detectate din secvențierea ARN totală (Wang și colab., 2017), cu toate acestea, în această a doua abordare, este necesară o confirmare ulterioară a circularității pentru circrna.
odată cu descoperirea ARN-urilor chimerice liniare transcrise din ADN-uri circulare, circrn-urile nu mai sunt singurele transcrieri cu joncțiuni himerice. Prin urmare, este extrem de important să rețineți că, în timp ce prima abordare va îmbogăți semnificativ proba de ARN în circRNAs, astfel încât majoritatea joncțiunilor himerice detectate să corespundă circRNAs adevărate, a doua ar putea supraestima numărul de transcrieri circRNA atribuind circRNAs semnalul provenit atât din circRNAs, cât și din transcrierile chimerice liniare transcrise din ADN-urile circulare. În consecință, luând în considerare coexistența circrn-urilor și a transcrierilor chimerice liniare, necesitatea testelor de circularitate și a testelor de funcționalitate câștigă importanță și trebuie acordată o atenție deosebită nu numai metodelor experimentale, ci și computaționale, pentru a evita confundarea transcrierilor himerice din ADN-urile circulare cu circrn-urile formate prin backsplicing.
discuție
câmpul circRNA este încă într-un stadiu incipient, cu toate acestea, circrna-urile s-au dovedit deja a fi molecule uimitoare, implicate în multe procese, cu un mare potențial de biomarker și care pot schimba și modul în care înțelegem procesele de transcriere și traducere. Din aceste motive, acestea câștigă atenție, iar câmpul circRNA este în prezent unul dintre cele mai active domenii de cercetare ARN. Cu toate acestea, există încă multe conflicte, controverse și întrebări deschise (Li, 2019) care trebuie discutate.
în acest raport și în lumina progreselor recente în domeniul ADN-ului circular, dorim să subliniem transcrierea din ADN-ul circular extrachromozomal ca una dintre principalele surse naturale de transcrieri liniare cu semnale îmbinate înapoi care ar putea interfera cu datele circRNA (m Okticller și colab., 2018). De acum înainte, în afară de artefactele tehnice, duplicările și evenimentele de transplant care ar putea duce la falsuri pozitive în detectarea circRNA, ar trebui să luăm în considerare și existența acestui nou tip de transcrieri himerice. Prin urmare, testele de circularizare și testele funcționale sunt mai importante ca niciodată.
în orice caz, aceste transcrieri liniare himerice nu ar trebui considerate doar ca un simplu factor de confuzie pentru studiile circRNA. În ciuda implicațiilor tehnice pentru caracterizarea arnc, existența acestor molecule de ARN liniar himeric asemănătoare arnc provenind de la eccdna adaugă un nou tip de moleculă la lista tot mai mare de ARN-uri și extinde viziunea noastră despre complexitatea transcriptomului și reglarea acestuia. Mai mult, aceste molecule liniare de ARN provenite din eccDNA ar putea prezenta, de asemenea, funcții similare cu circRNA, inclusiv funcțiile de reglare sau potențialul de a fi tradus. Produsele genetice din transcrierile eccDNA ar putea contribui potențial la fenotipul celulelor și țesuturilor somatice, așa cum este raportat în drojdie (Gresham și colab., 2010; Demeke și colab., 2015). Cu toate acestea, în acest domeniu în curs de formare, sunt necesare mai multe date și cercetări pentru a începe zgârierea suprafeței aisbergului.
contribuții autor
LI, IP-l, BR, și DO a scris lucrarea.
finanțare
acest studiu a fost finanțat de Institutul de Salud Carlos III prin proiectul „PI17/00189” (cofinanțat de Fondul European de dezvoltare regională/Fondul Social European) „investiția în viitorul tău”). IP-L și BR au fost susținute de Consiliul danez pentru cercetare independentă, 6108-00171B, iar LI a fost susținut de Departamentul de educație al Guvernului Basc .
Conflict de interese
autorii declară că cercetarea a fost realizată în absența oricăror relații comerciale sau financiare care ar putea fi interpretate ca un potențial conflict de interese.