nume Generic: Clindamycin fosfat
forma de dozare: vaginale cream
medical revizuite de Drugs.com. Ultima actualizare la 1 martie 2020.
- Prezentare generală
- efecte secundare
- dozare
- profesional
- interacțiuni
- mai mult
- numai pentru utilizare INTRAVAGINALĂNU pentru utilizare oftalmică, dermică sau orală
- Cleocin Vaginal Cream – Farmacologie Clinică
- mecanism de acțiune
- farmacocinetică
- microbiologie
- mecanism de acțiune
- rezistență
- activitatea antibacteriană
- indicații și utilizare pentru crema vaginală Cleocin
- contraindicații
- avertismente
- Precauții
- General
- informații pentru pacient
- interacțiuni medicamentoase
- carcinogeneză, mutageneză, afectarea fertilității
- sarcina
- mamele care alăptează
- utilizare pediatrică
- utilizare geriatrică
- reacții Adverse
- studii clinice
- supradozaj
- Cleocin Vaginal Cream dozare și Administrare
- cum se furnizează crema vaginală Cleocin
- studii clinice
- instrucțiuni de utilizare
- Panou principal de afișare-40 g etichetă tub
- panou de afișare PRINCIPAL-cutie de tub de 40 g
- mai multe despre Cleocin Vaginal (Clindamycin topic)
- resurse pentru consumatori
- resurse profesionale
- alte formulări
- ghiduri de tratament înrudite
numai pentru utilizare INTRAVAGINALĂNU pentru utilizare oftalmică, dermică sau orală
fosfatul de clindamicină este un ester solubil în apă al antibioticului semisintetic produs de o substituție 7(s)-clor a grupării 7(R)-hidroxil a antibioticului părinte Lincomicină. Denumirea chimică a fosfatului de clindamicină este metil 7-chloro-6,7,8-trideoxy-6-(1-methyl-trans-4-propyl-L-2-pyrrolidinecarboxamido)-1-thio-L-threo-α–D-galacto-octopiranozidă 2 – (fosfat dihidrogen). Are o greutate moleculară de 504,96, iar formula moleculară este C18H34ClN2O8PS. Formula structurală este reprezentată mai jos:
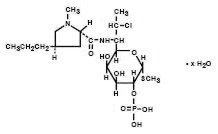
Cleocin Vaginal Cream 2%, este o cremă semi-solidă, albă, care conține 2% fosfat de clindamicină, USP, la o concentrație echivalentă cu 20 mg clindamicină pe gram. PH-ul cremei este cuprins între 3,0 și 6,0. Crema conține, de asemenea, alcool benzilic, alcool cetostearilic, esteri de acizi grași amestecați, ulei mineral, polisorbat 60, propilen glicol, apă purificată, monostearat de sorbitan și acid stearic.
fiecare Aplicator de 5 grame de cremă vaginală conține aproximativ 100 mg de fosfat de clindamicină.
Cleocin Vaginal Cream – Farmacologie Clinică
mecanism de acțiune
clindamicina este un medicament antibacterian (vezi microbiologie).
farmacocinetică
după o doză intravaginală o dată pe zi de 100 mg cremă vaginală cu fosfat de clindamicină 2%, administrată la 6 voluntari sănătoși timp de 7 zile, aproximativ 5% (interval 0,6% până la 11%) din doza administrată a fost absorbită sistemic. Concentrația serică maximă de clindamicină observată în prima zi a fost în medie de 18 ng/mL (interval 4 până la 47 ng/mL), iar în ziua 7 a fost în medie de 25 ng/mL (interval 6 până la 61 ng/mL). Aceste concentrații maxime au fost atinse la aproximativ 10 ore după administrare (interval 4-24 ore).
după o doză intravaginală o dată pe zi de 100 mg cremă vaginală cu fosfat de clindamicină 2%, administrată timp de 7 zile consecutive la 5 femei cu vaginoză bacteriană, absorbția a fost mai lentă și mai puțin variabilă decât cea observată la femeile sănătoase. Aproximativ 5% (între 2% și 8%) din doză a fost absorbită sistemic. Concentrația serică maximă de clindamicină observată în prima zi a fost în medie de 13 ng/mL (interval 6 până la 34 ng/mL), iar în ziua 7 a fost în medie de 16 ng/mL (interval 7 până la 26 ng/mL). Aceste concentrații maxime au fost atinse la aproximativ 14 ore după administrare (interval 4-24 ore).
a existat o acumulare sistemică mică sau deloc de clindamicină după administrarea vaginală repetată de clindamicină fosfat cremă vaginală 2%. Timpul de înjumătățire sistemic a fost de 1,5 până la 2,6 ore.
microbiologie
mecanism de acțiune
clindamicina inhibă sinteza proteinelor bacteriene prin legarea la ARN-ul 23S al subunității 50S a ribozomului. Clindamicina este predominant bacteriostatică. Deși fosfatul de clindamicină este inactiv in vitro, hidroliza rapidă in vivo îl transformă în clindamicină activă.
rezistență
rezistența la clindamicină este cel mai adesea cauzată de modificarea situsului țintă pe ribozom, de obicei prin modificarea chimică a bazelor ARN prin mutații punctuale în ARN sau ocazional în proteine. Rezistența încrucișată a fost demonstrată între lincosamide, macrolide și streptogramine B în unele organisme. Rezistența încrucișată a fost demonstrată între clindamicină și lincomicină.
activitatea antibacteriană
testarea Culturii și sensibilității bacteriilor nu se efectuează în mod obișnuit pentru stabilirea diagnosticului de vaginoză bacteriană (vezi indicații și utilizare); metodologia standard pentru testarea susceptibilității potențialilor agenți patogeni bacterieni, Gardnerella vaginalis, Mobiluncus spp., sau Mycoplasma hominis, nu a fost definit.
sunt disponibile următoarele date in vitro, dar semnificația lor clinică nu este cunoscută. Clindamicina este activă in vitro împotriva majorității izolatelor din următoarele organisme raportate a fi asociate cu vaginoza bacteriană:
- Bacteroides spp.
- Gardnerella vaginalis
- Mobiluncus spp.
- Mycoplasma hominis
- Peptostreptococcus spp.
indicații și utilizare pentru crema vaginală Cleocin
crema vaginală Cleocin 2%, este indicată în tratamentul vaginozei bacteriene (denumită anterior vaginită Haemophilus, vaginită Gardnerella, vaginită nespecifică, vaginită Corynebacterium sau vaginită anaerobă). Crema vaginală Cleocin 2%, poate fi utilizată pentru a trata femeile care nu sunt însărcinate și femeile însărcinate în al doilea și al treilea trimestru. (Vezi studii clinice.)
notă: În scopul acestei indicații, un diagnostic clinic de vaginoză bacteriană este de obicei definit de prezența unei secreții vaginale omogene care (a) are un pH mai mare de 4,5, (b) emite un miros de amină „pește” atunci când este amestecat cu o soluție KOH de 10% și (c) conține celule indiciu la examenul microscopic. Rezultatele colorației Gram în concordanță cu un diagnostic de vaginoză bacteriană includ (a) morfologia Lactobacilului semnificativ redusă sau absentă, (b) predominanța Morfotipului Gardnerella și (c) absența sau puține celule albe din sânge.
alți agenți patogeni frecvent asociați cu vulvovaginita, de exemplu, Trichomonas vaginalis, Chlamydia trachomatis, N. gonorrhoeae, Candida albicans și virusul Herpes simplex ar trebui excluși.
contraindicații
Cleocin Vaginal Cream 2%, este contraindicat la persoanele cu antecedente de hipersensibilitate la clindamicină, lincomicină sau la oricare dintre componentele acestei creme vaginale. Crema vaginală Cleocin 2% este, de asemenea, contraindicată la persoanele cu antecedente de enterită regională, colită ulcerativă sau antecedente de colită „asociată cu antibiotice”.
avertismente
colita pseudomembranoasă a fost raportată la aproape toți agenții antibacterieni, inclusiv clindamicina, și poate varia în severitate de la ușoară până la care poate pune viața în pericol. Clindamicina administrată oral și parenteral a fost asociată cu colită severă care se poate termina fatal. Diaree, diaree sângeroasă și colită (inclusiv colită pseudomembranoasă) au fost raportate cu utilizarea clindamicinei administrate oral și parenteral, precum și cu formulări topice (dermice și vaginale) de clindamicină. Prin urmare, este important să se ia în considerare acest diagnostic la pacienții care prezintă diaree după administrarea clindamicinei, chiar și atunci când este administrat pe cale vaginală, deoarece aproximativ 5% din doza de clindamicină este absorbită sistemic din vagin.
tratamentul cu agenți antibacterieni modifică flora normală a colonului și poate permite creșterea excesivă a clostridiei.Studiile indică faptul că o toxină produsă de Clostridium difficile este o cauză principală a colitei „asociate cu antibiotice”.
după stabilirea diagnosticului de colită pseudomembranoasă, trebuie inițiate măsuri terapeutice. Cazurile ușoare de colită pseudomembranoasă răspund de obicei la întreruperea tratamentului în monoterapie. În cazuri moderate până la severe, trebuie luată în considerare gestionarea cu lichide și electroliți, suplimentarea cu proteine și tratamentul cu un medicament antibacterian eficient clinic împotriva colitei Clostridium difficile.
debutul colitei pseudomembranoase simptomele pot apărea în timpul sau după tratamentul antimicrobian.
Precauții
General
Cleocin Vaginal Cream 2%, conține ingrediente care vor provoca arsuri și iritații ale ochiului. În caz de contact accidental cu ochiul, clătiți ochiul cu cantități mari de apă rece de la robinet.
utilizarea cremei vaginale Cleocin 2% poate duce la creșterea excesivă a organismelor nesusceptibile în vagin. În studiile clinice care au implicat 600 de femei care nu au fost însărcinate și care au primit tratament timp de 3 zile, Candida albicans a fost detectată, fie simptomatic, fie prin cultură, la 8, 8% dintre pacienți. La 9% dintre pacienți, a fost înregistrată vaginita. Studiile inclinice care au implicat 1325 de femei care nu au fost însărcinate și care au primit tratament timp de 7 zile, Candida albicans a fost detectată, fie simptomatic, fie prin cultură, la 10,5% dintre pacienți. Vaginita a fost înregistrată la 10,7% dintre pacienți. La 180 de femei însărcinate care au primit tratament timp de 7 zile, Candida albicans a fost detectată, fie simptomatic, fie prin cultură, la 13,3% dintre pacienți. La 7,2% dintre pacienți, a fost înregistrată vaginita. Candida albicans, după cum sa raportat aici, include Termenii: monilioza vaginală și monilioza (corpul în ansamblu). Vaginita include Termenii: tulburare vulvovaginală, vulvovaginită, secreție vaginală, vaginită trichomonală și vaginită.
informații pentru pacient
pacientul trebuie instruit să nu se angajeze în relații sexuale vaginale sau să utilizeze alte produse vaginale (cum ar fi tampoane sau dușuri) în timpul tratamentului cu acest produs.
pacientul trebuie, de asemenea, informat că această cremă conține ulei mineral care poate slăbi latex sau produse din cauciuc, cum ar fi prezervativele sau diafragmele contraceptive vaginale. Prin urmare, nu se recomandă utilizarea acestor produse în decurs de 72 de ore după tratamentul cu Cleocin Vaginal Cream 2%.
interacțiuni medicamentoase
s-a demonstrat că clindamicina sistemică are proprietăți de blocare neuromusculară care pot spori acțiunea altor agenți de blocare neuromusculară. Prin urmare, trebuie utilizat cu precauție la pacienții care primesc astfel de agenți.
carcinogeneză, mutageneză, afectarea fertilității
nu s-au efectuat studii pe termen lung la animale cu clindamicină pentru evaluarea potențialului carcinogen.
testele de genotoxicitate efectuate au inclus un test de micronucleu la șobolan și un test Ames. Ambele teste au fost negative. Studiile de fertilitate la șobolani tratați oral cu până la 300 mg/kg și zi (de 31 de ori expunerea la om pe baza mg/m2) nu au evidențiat efecte asupra fertilității sau capacității de împerechere.
sarcina
efecte teratogene
în studiile clinice cu femei gravide, administrarea sistemică de clindamicină în al doilea și al treilea trimestru nu a fost asociată cu o frecvență crescută a anomaliilor congenitale.
crema vaginală cu clindamicină trebuie utilizată în primul trimestru de sarcină numai dacă este clar necesară și beneficiile depășesc riscurile. Nu există studii adecvate și bine controlate la femeile gravide în timpul primului trimestru de sarcină.
Cleocin Vaginal Cream 2% a fost studiat la femeile gravide în timpul celui de-al doilea trimestru. La femeile tratate timp de șapte zile, travaliul anormal a fost raportat la 1,1% dintre pacienții care au primit cremă vaginală cu clindamicină 2%, comparativ cu 0,5% dintre pacienții care au primit placebo.
studiile de reproducere au fost efectuate la șobolani și șoareci utilizând doze orale și parenterale de clindamicină de până la 600 mg/kg și zi (de 62 și, respectiv, de 25 de ori expunerea maximă la om în funcție de suprafața corporală) și nu au evidențiat nici o dovadă de afectare a fătului datorată clindamicinei. Palatele despicate au fost observate la fetuși de la o tulpină de șoarece tratată intraperitoneal cu clindamicină la 200 mg/kg și zi (de aproximativ 10 ori doza recomandată pe baza conversiilor suprafeței corporale). Deoarece acest efect nu a fost observat la alte tulpini de șoarece sau la alte specii, efectul poate fi specific tulpinii.
mamele care alăptează
date publicate limitate bazate pe eșantionarea laptelui matern raportează că clindamicina apare în laptele matern uman în intervalul mai mic de 0,5 până la 3,8 mcg/mL la doze de 150 mg oral până la 600 mg intravenos. Nu se cunoaște dacă clindamicina este excretată în laptele matern uman după utilizarea fosfatului de clindamicină administrat vaginal.
clindamicina are potențialul de a provoca efecte adverse asupra florei gastrointestinale a sugarului alăptat. Dacă clindamicina este cerută de o mamă care alăptează, nu este un motiv pentru întreruperea alăptării, dar poate fi preferat un medicament alternativ. Monitorizați sugarul alăptat pentru posibile efecte adverse asupra florei gastro-intestinale, cum ar fi diaree, candidoză (aftere, erupții cutanate) sau rareori, sânge în scaun care indică o posibilă colită asociată cu antibiotice.
beneficiile pentru dezvoltare și sănătate ale alăptării trebuie luate în considerare împreună cu nevoia clinică a mamei de clindamicină și orice efecte adverse potențiale asupra copilului alăptat din clindamicină sau din starea maternă subiacentă.
utilizare pediatrică
siguranța și eficacitatea la pacienții pediatri nu au fost stabilite.
utilizare geriatrică
studiile clinice pentru Cleocin Vaginal Cream 2% nu au inclus un număr suficient de subiecți cu vârsta de 65 de ani și peste pentru a determina dacă răspund diferit față de subiecții mai tineri. Alte experiențe clinice raportate nu au identificat diferențe în răspunsurile dintre pacienții vârstnici și cei mai tineri.
reacții Adverse
studii clinice
femei care nu sunt însărcinate
în studiile clinice care au implicat femei care nu sunt însărcinate, 1, 8% din 600 de pacienți care au primit tratament cu Cleocin Vaginal Cream 2% timp de 3 zile și 2, 7% din 1325 de pacienți care au primit tratament timp de 7 zile au întrerupt tratamentul din cauza evenimentelor adverse legate de medicament. Evenimentele medicale considerate a fi legate, probabil legate, posibil legate sau de o relație necunoscută cu crema vaginală Clindamycin fosfat administrată vaginal 2% au fost raportate la 20,7% dintre pacienții care au primit tratament timp de 3 zile și la 21,3% dintre pacienții care au primit tratament timp de 7 zile. Evenimentele care au avut loc la 1% din pacienții care au primit Clindamycin phosphate vaginal cream 2% sunt prezentate în tabelul 1.
| eveniment | cremă vaginală Cleocin | |
|---|---|---|
| 3 zi n = 600 |
7 zi n=1325 |
|
| Urogenital | ||
| monilioza vaginală | 7.7 | 10.4 |
| vulvovaginită | 6.0 | 4.4 |
| tulburări vulvovaginale | 3.2 | 5.3 |
| vaginită Trichomonală | 0 | 1.3 |
| corpul ca întreg | ||
| Moniliasis (corp) | 1.3 | 0.2 |
alte evenimente care apar în < 1% din grupurile de cremă vaginală clindamicină 2% includ:
sistemul Urogenital: secreție vaginală, metroragie, infecții ale tractului urinar, endometrioză, tulburări menstruale, vaginită/infecție vaginală și dureri vaginale.
corpul ca întreg: dureri abdominale localizate, dureri abdominale generalizate, crampe abdominale, halitoză, cefalee, infecții bacteriene, umflături inflamatorii, reacții alergice și infecții fungice.
sistemul digestiv: greață, vărsături, constipație, dispepsie, flatulență, diaree și tulburări gastro-intestinale.
sistemul endocrin: hipertiroidism.
sistemul nervos Central: amețeli și vertij.
sistemul respirator: epistaxis.
piele: prurit (la locul neaplicării), monilioză, erupție cutanată, erupție maculopapulară, eritem și urticarie.
simțuri speciale: gust perversiune.
femei gravide
într-un studiu clinic care a implicat femei gravide în timpul celui de-al doilea trimestru, 1, 7% din 180 de pacienți care au primit tratament timp de 7 zile au întrerupt tratamentul din cauza evenimentelor adverse legate de medicament. Evenimentele medicale considerate a fi legate, probabil legate, posibil legate sau de o relație necunoscută cu crema vaginală clindamicină fosfat administrată vaginal 2% au fost raportate la 22,8% dintre pacientele gravide. Evenimentele care apar la 1% din pacienții cărora li s-a administrat fie Clindamycin phosphate vaginal cream 2%, fie placebo sunt prezentate în tabelul 2.
| eveniment | CLEOCIN cremă vaginală |
Placebo |
|---|---|---|
| 7 zi n = 180 |
7 zi n=184 |
|
| Urogenital | ||
| monilioza vaginală | 13.3 | 7.1 |
| tulburări vulvovaginale | 6.7 | 7.1 |
| muncă anormală | 1.1 | 0.5 |
| corpul ca întreg | ||
| infecții fungice | 1.7 | 0 |
| piele | ||
| prurit, la locul neaplicării | 1.1 | 0 |
alte evenimente care apar în <1% din grupul Clindamycin vaginal cream 2% includ:
sistemul Urogenital: disurie, metroragie, durere vaginală și vaginită trichomonală.
corpul în ansamblu: infecție respiratorie superioară.
piele: prurit (locul aplicării topice) și eritem.
experiența după punerea pe piață
deoarece aceste reacții sunt raportate voluntar de la o populație de dimensiuni incerte, nu este întotdeauna posibilă estimarea fiabilă a frecvenței acestora sau stabilirea unei relații de cauzalitate cu expunerea la medicament.
în perioada de după punerea pe piață, s-au raportat cazuri de colită pseudomembranoasă cu utilizarea cremei vaginale cu fosfat de clindamicină.
alte formulări de clindamicină
crema vaginală de clindamicină oferă niveluri serice maxime minime și expunere sistemică (ASC) a clindamicinei, comparativ cu dozarea orală de clindamicină de 100 mg. Deși aceste niveluri mai scăzute de expunere sunt mai puțin susceptibile de a produce reacțiile comune observate cu clindamicina orală, posibilitatea acestor reacții și a altor reacții nu poate fi exclusă în prezent. Nu sunt disponibile date din studii bine controlate care compară direct clindamicina administrată oral cu clindamicina administrată vaginal.
următoarele reacții adverse și teste de laborator modificate au fost raportate cu utilizarea orală sau parenterală a clindamicinei:
gastro-intestinale: dureri abdominale, esofagită, greață, vărsături, diaree și colită pseudomembranoasă. (Vezi avertismente.)
Hematopoietic: au fost raportate neutropenie tranzitorie (leucopenie), eozinofilie, agranulocitoză și trombocitopenie. În niciunul dintre aceste rapoarte nu s-a putut face nicio relație etiologică directă cu terapia concomitentă cu clindamicină.
Reacții De Hipersensibilitate: În timpul terapiei medicamentoase au fost observate erupții cutanate maculopapulare și urticarie. Erupțiile cutanate generalizate de tip morbiliform ușor până la moderat sunt cele mai frecvent raportate dintre toate reacțiile adverse. Cazuri Rare de eritem multiform, unele asemănătoare sindromului Stevens-Johnson, au fost asociate cu clindamicina. Au fost raportate câteva cazuri de reacții anafilactoide. Dacă apare o reacție de hipersensibilitate, medicamentul trebuie întrerupt.
ficat: icterul și anomaliile testelor funcției hepatice au fost observate în timpul terapiei cu clindamicină.
musculo-scheletice: Au fost raportate cazuri Rare de poliartrită.
Renal: deși nu a fost stabilită nicio relație directă a clindamicinei cu afectarea renală, în cazuri rare s-a observat disfuncție renală evidențiată de azotemie, oligurie și/sau proteinurie.
supradozaj
aplicat vaginal Clindamycin phosphate vaginal cream 2% ar putea fi absorbit în cantități suficiente pentru a produce efecte sistemice. (Vezi avertismente.)
Cleocin Vaginal Cream dozare și Administrare
doza recomandată este un aplicator de Clindamycin fosfat vaginal cream 2% (5 grame conținând aproximativ 100 mg Clindamycin fosfat) intravaginal, de preferință la culcare, timp de 3 sau 7 zile consecutive la pacienții care nu sunt gravide și timp de 7 zile consecutive la pacienții gravide. (Vezi studii clinice.)
cum se furnizează crema vaginală Cleocin
crema vaginală Cleocin 2% (crema vaginală cu fosfat de clindamicină) este furnizată după cum urmează:
tub de 40 g (cu 7 aplicatoare de unică folosință) NDC 0009-3448-01
a se păstra la temperatura camerei controlată de la 20 la 25 la 25 la 25 la 28 la 77 la 7) . A se proteja de îngheț.
studii clinice
în două studii clinice care au implicat 674 de femei care nu erau însărcinate și care prezentau vaginoză bacteriană, comparând crema vaginală Cleocin 2% timp de 3 sau 7 zile, ratele de vindecare clinică, determinate la 1 lună postterapie, au variat între 72% și 81% pentru tratamentul de 3 zile și 84% până la 86% pentru tratamentul de 7 zile.
| CLEOCIN 3 zile | CLEOCIN 7 zile | |||
|---|---|---|---|---|
| studiu american | 94/131 | 72% | 110/128 | 86% |
| Studiu European | 161/199 | 81% | 181/216 | 84% |
într-un studiu clinic care a implicat 249 de paciente gravide evaluabile în al doilea și al treilea trimestru tratate timp de 7 zile, rata de vindecare clinică, determinată la 1 lună postterapie, a fost de 60% (77/129) în brațul cu clindamicină și de 9% (11/120) pentru brațul vehiculului. Determinarea vindecării clinice s-a bazat pe absența unui miros de amină „pește” atunci când secreția vaginală a fost amestecată cu o soluție KOH de 10% și absența celulelor indiciu la examinarea microscopică.
numai Rx
este posibil ca eticheta acestui produs să fi fost actualizată. Pentru informații actuale complete de prescriere, vă rugăm să vizitați www.pfizer.com.

LAB-0043-12.0
revizuit 03/2020
instrucțiuni de utilizare
aplicatoare de plastic de unică folosință sunt prevăzute cu acest pachet. Acestea sunt concepute pentru a permite administrarea vaginală adecvată a cremei.
scoateți capacul tubului de cremă. Înșurubați un aplicator de plastic pe capătul filetat al tubului.
tub de rulare din partea de jos, strângeți ușor și forțați medicamentul în aplicator. Aplicatorul este umplut când pistonul atinge punctul de oprire predeterminat.
deșurubați aplicatorul din tub și înlocuiți capacul.
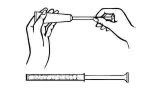
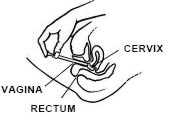
în timp ce vă aflați pe spate, apucați ferm butoiul aplicatorului și introduceți-l în vagin cât mai mult posibil, fără a provoca disconfort.
împingeți încet pistonul până se oprește.
scoateți cu grijă aplicatorul din vagin și aruncați aplicatorul.
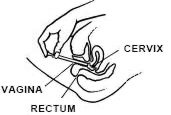
NU UITAȚI SĂ APLICAȚI UN APLICATOR ÎN FIECARE SEARĂ ÎNAINTE DE CULCARE SAU AȘA CUM V-A PRESCRIS MEDICUL DUMNEAVOASTRĂ.
instrucțiuni pentru pacient
acest ambalaj conține aplicatoare din plastic de unică folosință. Aplicatoarele sunt concepute pentru administrarea corectă a cremei în vagin.
scoateți capacul tubului de cremă și înșurubați aplicatorul de plastic pe tub.
strângeți ușor tubul de la capătul inferior și forțați medicamentul în aplicator. Aplicatorul va fi plin atunci când pistonul atinge lungimea maximă.
deșurubați aplicatorul din tub și înlocuiți capacul.
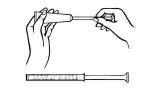
întindeți-vă pe spate și ținând ferm aplicatorul, introduceți-l în vagin cât mai mult posibil, fără a provoca disconfort.
împingeți încet pistonul până se oprește.
scoateți cu grijă aplicatorul din vagin și aruncați-l.
NU UITAȚI SĂ APLICAȚI UN APLICATOR COMPLET ÎN FIECARE SEARĂ LA CULCARE SAU CONFORM INDICAȚIILOR MEDICULUI DUMNEAVOASTRĂ.
laborator-1058-1.0
Panou principal de afișare-40 g etichetă tub
NDC 0009-3448-01
40 Gram
numai Rx
Cleocin
Clindamycin fosfat
crema vaginala, USP
pentru uz Intravaginal numai
2%*
panou de afișare PRINCIPAL-cutie de tub de 40 g
NDC 0009-3448-01
40 Gram cu 7 aplicatoare
numai Rx
Cleocin
fosfat de clindamicină
cremă vaginală, USP
numai pentru uz Intravaginal
2%*
Pfizer
distribuit de
Pharmacia & Upjohn Co
Divizia Pfizer Inc, NY, NY 10017
| CLEOCIN Clindamycin fosfat cremă |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Pharmacia și Upjohn Company LLC (618054084)
| înființare | |||
| nume | adresa | Id/Fei | operațiuni |
| Pharmacia și Upjohn Company LLC | 618054084 | analiză (0009-3448), fabricare API (0009-3448), etichetă (0009-3448), fabricare(0009-3448), ambalaj(0009-3448) | |
mai multe despre Cleocin Vaginal (Clindamycin topic)
- reacții adverse
- În timpul sarcinii sau alăptării
- informații privind dozajul
- interacțiuni medicamentoase
- prețuri & cupoane
- disponibilitate generică
- clasa de medicamente: antiinfecțioase vaginale
resurse pentru consumatori
- citire avansată
resurse profesionale
- informații de prescriere
- cremă vaginală clindamicină (FDA)
Alte mărci Clindamax, Clindagel, clindesse, Clindacin ETZ, … + 4 mai
alte formulări
- Cleocin
- … + 4 mai
ghiduri de tratament înrudite
- vaginită bacteriană
Disclaimer Medical