Innledning
Helicobacter pylori (h. pylori) Er En Gram-negativ mikroaerofil bakterie, hvis naturlige habitat er magen. Selv om den vanligvis har en bacillær form med flere flagella i den ene enden, vedtar den et coccoid utseende i ugunstige miljøforhold.1,2
H. pylori er en viktig etiologisk faktor i aktiv kronisk gastritt, magesår, mageslimhinneassosiert lymfoidvev (MALT) lymfom og magekreft. Selv om bakterien anslås å være tilstede i mageslimhinnen hos halvparten av verdens befolkning, utvikler disse sykdommene bare i ca 15-20% av koloniserte individer.2,3
de vanligste behandlingsregimene har resultert i en utryddelsesrate på rundt 85% i mange geografiske områder, 4-6, men effekten har blitt kompromittert, spesielt de siste årene, av den raske fremveksten av antibiotikaresistente stammer og dårlig behandlingsoverholdelse.5,7
det er viktig å vurdere at kur (samt forebygging av komplikasjoner) for aktiv kronisk gastritt og magesår og for noen lavverdige former for gastrisk MALT lymfom avhenger av suksessen Til h. pylori utryddelse. Videre vil sikre og opprettholde vellykket utrydding av denne mikroorganismen i alle dens biologiske former forhindre tilbakefall av infeksjonen og derfor sykdomsfall.
målet med denne gjennomgangen er å presentere en generell oversikt over coccoid form Av H. pylori, fremhever sin mikrobiologiske profil, antibiotikaresistens og virulens. Dens engasjement i magesykdom vil også bli analysert, og i hvilken grad det er forbundet med infeksjonsrekrudescens og sykdomsfall vil bli undersøkt.
Overlevelse og cellulær tilpasning Av H. pylorigenerelle hensyn
Alle levende organismer er utstyrt med mekanismer som gjør at de kan overleve i ugunstige miljøer. For noen innebærer deres respons (i tillegg til metabolske tilpasninger) endringer i cellemorfologi.8,9 flere mikroorganismer har evnen til å differensiere til en levedyktig, MEN ikke-kulturbar (VBNC) tilstand som svar på miljøforhold som er ugunstige for overlevelse og vekst. Denne strategien er mye brukt av mikroorganismer som Salmonella, Campylobacter og Escherichia.10,11
i vbnc tilstand, bakterier generelt redusere sin størrelse og endre form til å bli små sfæriske legemer. De reduserer respirasjonsfrekvensen og næringstransporten og endrer genuttrykk og molekylær syntese. I denne tilstanden kan de ikke oppdages ved hjelp av konvensjonelle kulturteknikker. Imidlertid kan endringer i miljøforhold føre til at disse mikroorganismer enten » gjenoppliver «(og rekonverterer til deres aktive tilstand) eller degenererer.10-13
Tilsvarende, H. pylori, når den opplever skadelige miljøforhold (i eller utenfor sitt naturlige habitat), endrer sin klassiske bacillære form og går inn I EN VBNC-tilstand som fører til morfologiske og metabolske endringer, samt endringer i vekstadferd.14,15
Levedyktig, Men ikke-kulturbar tilstand Av h. pylori
selv om noen forfattere først forsøkte å demonstrere at konverteringen fra bacillær til coccoid form var en passiv prosess som resulterte i celledød og derfor at coccoidformene var degenererte rester av døde bakterier, 16, 17 tre former For H. pylori anses for tiden å eksistere, nemlig (i rekkefølge av mest til minst virulente), levedyktig, kulturbar bacillær form, VBNC coccoid form og ikke-levedyktig degenerativ form.18-20
Morfologisk skjer konvertering fra bacillær til coccoid form gjennom mellomliggende V – og U-former13,14 (Fig. 1 og 2), hvor cellestrukturer som cytoplasma og cellemembran forblir intakte,15, 21 mens flagella har en tendens til å vikle rundt coccoidcellestrukturen, og dermed bli nær usynlig. Andre ultrastrukturelle modifikasjoner på coccoidformen resulterer i to undertyper. Type A har uregelmessige kanter med en grov overflate og anses å være en død celle, mens Type B har en jevnere overflate, er mindre og anses å være en levende celle.21,22
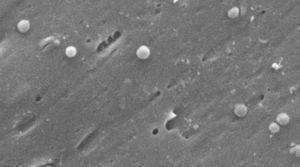
Bilder av coccoid form Av Helicobacter pylori. Skanning elektronmikroskop bilde gjengitt av Dr. Nuno F. Azevedo. LEPABE-Kjemisk Ingeniøravdeling Ved Fakultet For Ingeniørfag Ved Universitetet I Porto (Portugal).
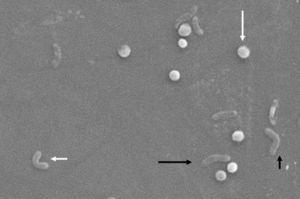
Morfologiske endringer I Helicobacter pylori. Spiral form (lang svart pil), V-form (kort svart pil), U-form (kort hvit pil) og coccoid form (lang hvit pil). Skanning elektronmikroskop bilde gjengitt av Dr. Nuno F. Azevedo. LEPABE-Kjemisk Ingeniøravdeling Ved Fakultet For Ingeniørfag Ved Universitetet I Porto (Portugal).
i scanning electron microscope (SEM) analyser av overflaten slimete gel laget av magekreft pasienter infisert Med h. pylori, Ogata et al.23 observert sameksistensen av både bacillære og coccoidformer. Andre forfattere har bekreftet tilstedeværelsen av kokoidformen i både magesekken og tolvfingertarmen,24-26, selv om det ser ut til at prosentandelen kokoidformer er høyere i tolvfingertarmen enn i magen, til det punktet hvor bare kokoidformen observeres i noen duodenale biopsier.26,27 dette faktum antyder enten At H. pylori er tvunget til å tilpasse seg biologiske forhold i tolvfingertarmen, eller at disse forholdene er ideelle For h. pylori å ta tilflukt der I vbnc-staten.
in vitro og in vivo eksperimenter har vist at i ugunstige forhold som aerobiosis, 28,29 alkalisk pH,29,30 høy temperatur,31 lange inkubasjonsperioder,29,32 langvarig inkubasjon i vann33 eller behandling med protonpumpehemmere32 eller antibiotika,34 coccoidfenotypen kan opprettholde et visst nivå av metabolsk aktivitet,da den uttrykker et bredt spekter av gener tilstede i bacillærformen, 35 opprettholder detekterbare nivåer av ureaseaktivitet,36 fortsetter å syntetisere proteiner,om enn i mindre mengder (mindre enn 1% av mengden proteiner syntetisert av bacillær form) 37 og produserer små mengder DNA, opprettholdt selv etter 3 måneders lagring i fysiologisk saltoppløsning ved 4°C. 29,38 alle disse dataene understreker det faktum at de biologiske endringene I h. pylori som svar på skadelige stimuli reflekterer sin kraftige evne, i løpet av sin levetid, for å bevare arten.
biofilmdannelse
som med andre bakterier, Er H. pylori evne til å fortsette som en smittsom enhet og motstå arsenalet av antimikrobielle midler som er rettet mot å utrydde det, på grunn av den genetiske variabiliteten som gjør Det mulig å utvikle bakteriell motstand. Overlevelsesstrategien forbedres ytterligere når bakterieceller danner det som kalles biofilmer.20 Biofilmer Er en slags mikrobiell «fellesskap» der bakteriene holder seg fast til biotiske eller abiotiske overflater ved hjelp av en egenprodusert matrise. Denne matrisen, bestående av ekstracellulære polymere stoffer,39, 40 skaper et miljø som er svært tolerant for antimikrobielle midler og sterkt resistent mot fagocytose. Ulike vertsforsvarsmekanismer er derfor unngått, noe som gjør utrydding vanskelig. Biofilmer anses å være virkelig komplekse, dynamiske systemer som letter horisontal genoverføring mellom bakterier. De gir dermed bakteriepopulasjoner med nye modifiserte genomer som bidrar betydelig til bakteriell motstand, belastningsvariabilitet og tilpasningsevne.41-43
i en studie av 21 biopsier fra pasienter der bakterien tidligere var utryddet, ble h. pylori isolert av kultur i 7 av biopsiene, mens genuttrykksteknikker oppdaget levedyktige H. pylori-celler i de fleste biopsiene. SEM viste i mellomtiden grupperte coccoid bakterier arrangert i en mikrobiell biofilm, noe som tyder på at coccoidformene kunne lette bakteriell utholdenhet og antibiotikaresistens.44
Følsomhet for antibiotika i coccoidformen
Mange studier har vist At h. pylori kan forandre Seg fra bacillær til coccoidform ved eksponering (in vitro) til forskjellige antimikrobielle midler. Ulike konsentrasjoner av amoksicillin, klaritromycin, metronidazol og erytromycin (for å nevne noen av de tilgjengelige antibiotika) kan indusere denne morfologiske transformasjonen.34,35,45 den største induksjonseffekten er observert med amoksicillin,27,34,46 kjent for å være svært effektiv in vitro mot h. pylori, men morfologiske observasjoner av kulturer viser at bacillære former reduseres i antall til fordel for coccoidformer.34,46 Faghri et al., 47 oppnådde bakteriedrepende effekter for coccoidformene, ved over 60% med metronidazol ved to ganger den minste hemmende konsentrasjonen (MIC), og ved 80-90% med klaritromycin ved MIC; amoksicillinbehandling med MIC og MIC× 2 hemmet imidlertid ikke levedyktige coccoidformer. Tilsvarende, Berry et al.34 observerte at mens amoksicillin ved MIC× 10 eliminerte bacillære former For h. pylori, induserte det også dannelsen av coccoidformer. Perkins et al.48 observert, i en studie av katter infisert naturlig Med H. pylori, at 6 uker etter utryddelsesbehandling var magesaft positivt for H. pylori i bare en katt, men polymerasekjedereaksjon (PCR) analyse identifiserte h. pylori genetisk materiale i alle kattene i studien. Selv Om H. pylori ble påvist i en enkelt katt, de histologiske lesjonene var konsistente med kronisk gastritt og ble preget av tilstedeværelse av lymfoide follikler.
med tanke på disse mikrobiologiske og grunnleggende forskningsdata, i en tidligere studie utført på pasienter infisert Med h. pylori—hvor følsomheten av de isolerte stammene til amoksicillin tidligere ble bestemt—fikk dobbeltterapi (protonpumpehemmere og amoksicillin) en kurrate for amoksicillinfølsomme stammer på bare 66%. Dette resultatet viser tilstedeværelsen av viktige ytterligere uavhengige bakterielle resistensfaktorer relatert til vellykket bruk av dette antibiotika.49 Dette er spesielt så hvis vi vurderer at det virker umulig at coccoidformer kan være følsomme for β-laktamantibiotika, fordi coccoidformer har forskjellige penicillinbindende proteinprofiler fra bacillære former.50 Det er derfor sannsynlig at ikke Alle h. pylori-organismer er helt eliminert etter utryddelsesbehandling; i stedet vil noen sannsynligvis bli omdannet til coccoidformer og dermed bli resistente mot antibakterielle stoffer. Dette vil forklare behandlingssvikt og tilbakefall.13,34,45
det er verdt å fremheve at noen svært nyere studier har vist at frie fettsyrer, som linolensyre og liposomal linolensyre, har en bakteriedrepende effekt på Begge H. pylori-former, uavhengig av deres resistens mot antibiotika.51,52 disse molekylene kan derfor ha en potensielt effektiv antimikrobiell effekt ved behandling av infeksjon Med h. pylori, spesielt i sin coccoidform.
Virulens og patogenitet av coccoidformen
virulensfaktorene For bacillærformen Av H. pylori og mekanismene som denne bakterien er involvert i utviklingen av gastrointestinale sykdommer, har blitt grundig studert.1,3,4 imidlertid er lite kjent om virulens og patogeniteten til coccoidformen. Nedenfor gjennomgår vi de mest relevante funnene om dette emnet.
som den bacillære formen uttrykker coccoidformen store virulensgener, som ureA, ureB, hpaA, vacA og cagA, cagE og BabA.35,53,54 dette uttrykket, som oppstår over en lengre periode, spiller sannsynligvis en viktig rolle i kroniske alvorlige magesykdommer.
Overholdelse Av H. pylori til gastroduodenal epitel er kjent for å være et viktig skritt i induksjonen av aktiv kronisk betennelse i slimhinnen. SEM studier har funnet at coccoid form av h. pylori kan presentere på plasmamembranoverflaten av gastriske epitelceller og, som bacillær form, har evnen til å invadere disse cellene.15,55 hvis celleinvasjon oppstår, er coccoidformene innelukket i tolags membranvesikler, og de gastriske epitelceller virker hovne og lytiske, som viser erosjon av slimhinnen.56 Gitt at coccoidformen er mindre utsatt for antibiotika, antas det at disse latente plasmamembranformene kan spre seg og infisere andre nærliggende epitelceller i fravær av en effektiv konsentrasjon av antibiotika.57
h. pylori-infeksjon er også kjent for å indusere en lokal immunrespons som ikke klarer å utrydde bakteriene, og dermed tillater magesykdommen å bli kronisk. Immunresponsen kan bestemmes ved antistoffdeteksjon ved hjelp av serologiske metoder utviklet ved hjelp Av bacillærformen Av h. pylori.58 faktisk kan tilstedeværelsen av disse spesifikke antistoffene brukes som en epidemiologisk indikator for infeksjon og for å bekrefte vellykket behandling. Det er imidlertid ingen serologiske metoder som oppdager coccoidformer. For å avgjøre om coccoid former hadde noen effekt på immunresponsen hos koloniserte individer, Figueroa et al.59 utviklet en spesifikk enzyme-linked immunosorbent assay (ELISA) teknikk for å evaluere og sammenligne immunresponsen mot coccoid og bacillary former mot et panel av sera fra symptomatiske og asymptomatiske infiserte individer. Coccoid former Av H. pylori ble vist å indusere en humoral immunrespons som ligner den som induseres av bacillære former hos infiserte individer. I en annen studie utført hos barn med epigastrisk smerte, ble den mulige rollen av coccoidformen i h. pylori-infeksjon undersøkt ved HJELP AV EN ELISA-teknikk og antigener fremstilt fra bacillære og coccoidcelleformer. Det ble funnet at 13,3% og 55,8% av cellene var seropositive for antigener av henholdsvis bacillærform og kokoidform, mens seropositivitetsverdier for astmatiske barn var henholdsvis 7,0% og 26,5%. Denne omtrent firedoble forskjellen i seropositivitet mellom coccoid-og bacillary-formantigenene hos symptomatiske og asymptomatiske pasienter kan tyde på en mulig infeksjonsrolle av coccoidformen Av h. pylori.60
Cellini et al.61 intragastrisk inokulerte konsentrerte suspensjoner Av h. pylori i coccoid form I EN BALB / c musemodell. H. pylori ble isolert 2 uker senere, histopatologiske endringer skjedde 1 måned senere og alle koloniserte mus viste en systemisk antistoffrespons på H. pylori. I andre eksperimenter MED BALB / c-mus utviklet dyr inokulert med coccoidformer signifikante patologiske forandringer i magen, inkludert erosive lesjoner og inflammatorisk celleinfiltrasjon av mageslimhinnen.36 Hun et al.,53 for å sammenligne virulens og smittsomhet, intragastrisk inokulerte BALB / c-mus Med H. pylori, en gruppe med bacillærformen og en annen gruppe med coccoidformen. I sem-undersøkelsen av prøver fra de 2 gruppene observert de adhesjon av både bacillære og coccoidformer til epitelceller i mageveggen og tilstedeværelsen av flagella i coccoidformene. Histologisk undersøkelse viste forskjellige grader av lesjoner i mageslimhinnen, fra mild inflammatorisk celleinfiltrasjon til erosjoner og sår. Mucosal lesjon var mildere i musene infisert av coccoidformen, mens et positivt resultat ikke ble oppnådd i kontrollgruppen som mottok sterilt vann.53 Rabelo-Gon@alves et al.62 viste at coccoid former Av H. pylori induserte en akutt inflammatorisk respons i musens mage fra de tidligste stadiene av infeksjonen. Ovennevnte resultater fremhever evnen til coccoidformer å kolonisere og infisere mageslimhinnen in vivo.
Flere studier har avslørt tilstedeværelsen av coccoidformen i vann.33,63 en slik studie—av vår gruppe—sammenlignet 2 grupper av avvente wistar-mus, en administrert brønnvann og kranvann i lengre tid og det andre administrerte sterile destillert vann, og fant at studiegruppens mus utviklet en kronisk inflammatorisk prosess med dannelse av lymfocytiske plakk og tilstedeværelsen av baciller i samsvar Med H. pylori.64
som tidligere nevnt, ville Det være logisk å anta At, i ugunstige forhold, H. pylori går inn i en» hvilende » tilstand, modifiserer sin klassiske bacillære form til coccoidformen uten å produsere degenerative endringer i genomet og beholde evnen til å gå tilbake til bacillærformen når miljø-eller naturlige habitatforhold forbedres.
Deltakelse av coccoid form i recrudescence
Gjentakelse Av h. pylori etter vellykket utrydding er sjelden i utviklede land sammenlignet med utviklingsland, med årlige tilbakefall på henholdsvis 2,67% og 13%.65,66
det er to typer tilbakefall Av h. pylori-infeksjon: recrudescence, når bakteriestammen som er ansvarlig for tilbakefall, er genetisk identisk med den som er isolert før utryddelse; og reinfeksjon, når tilbakefall skyldes en annen belastning.67 Differensierende rekrudescens fra reinfeksjon krever PCR eller genetisk polymorfismeanalyse for å identifisere bakteriestammer.67,68 siden disse metodene ikke brukes rutinemessig, er det ofte umulig å skille mellom rekrudescens og reinfeksjon i rutinemessig klinisk praksis.
H. tilbakefall av pylori er klinisk relevant, siden tilbakefall av magesår kan observeres hos en betydelig andel av infiserte pasienter, mens gjenopptreden av mikroorganismer kan forklare NOEN TILBAKEFALL av MALTLYMFOM etter behandling.69 Faktorer som drikkevann fra springen, tann-og tannkjøttsykdom, tilbakevendende tonsillitt, sykehusinnleggelse, dental og medisinsk utstyr og kontakt med familiemedlemmer antas å påvirke H. pylori tilbakefall.70-72 andre faktorer forbundet med tilbakefall av infeksjon er yngre alder, diabetes hos unge pasienter, lav årlig inntekt og langvarig hemming av magesyre etter utryddelse.73-76
Tilbakefall regnes som den mest sannsynlige årsaken til tilbakefall det første året etter utryddelse, mens reinfeksjon kan oppstå etter en lengre periode.68,77 Mange tilfeller av tilbakefall i utviklede land er i virkeligheten på grunn av tilbakefall. Re-infeksjon er vanligere i utviklingsland, siden folk tilsynelatende stadig blir utsatt For H. pylori.65,78
Ved hjelp av polyakrylamid gel protein elektroforese teknikker, Costas et al.79 fant at pasienter med tilbakefall 4 uker etter utryddelsesbehandling ikke var infisert med en annen stamme Av h. pylori; heller, stammen som hadde forårsaket den opprinnelige infeksjonen, hadde ikke blitt fullstendig utryddet av behandlingen, noe som førte til gjentakelse av infeksjonen. Derfor er det viktig å ta hensyn til effekten av terapeutisk regime: H. pylori tilbakefall er hyppig hos pasienter behandlet med lav effekt terapi, men er sjelden når høy effekt terapi brukes. Dette ble demonstrert av En studie på forekomsten Av H. pylori tilbakefall I Spania Av Gisbert et al.80 who fant at H. pylori tilbakefall 6 måneder etter utryddelse var 8,2% hos pasienter behandlet med lav effekt terapi, men bare 1,7% hos pasienter behandlet med høy effekt terapi.
I en studie utført I Korea fra 2007 til 2010, h. tilbakefall av pylori ble analysert etter 6 måneder med vellykkede første-og andrelinjebehandlinger, med årlig oppfølging-til slutten av studieperioden-basert på pustetester, magebiopsi og hurtige ureasetester.81 det ble funnet at de årlige tilbakefall innen og etter 2-års oppfølging var henholdsvis 9,3% og 2,0% etter førstelinjebehandling, og henholdsvis 4,5% og 2,9% etter andrelinjebehandling. Forfatterne konkluderte med at årlig H. tilbakefall av pylori hos pasienter som fikk utryddelsesbehandling viste et kraftig fall etter 2-års oppfølgingsperiode. Dette ble ansett som tilstrekkelig tid etter behandling for å bekrefte utryddelse, og også tilstrekkelig tid til å gjøre det mulig å skille mellom tilbakefall og rekrudescens Av h. pylori-stammer.81
Endelige betraktninger og konklusjoner
Gitt h. pylori for å gå inn I EN VBNC-tilstand når den blir utsatt for ugunstige forhold innenfor eller utenfor sitt habitat, er det rimelig å anta at antibiotikabehandlingsregimer som brukes til å utrydde bacillærformen Av H. pylori, kan indusere VBNC coccoidformer som er i stand til å overleve i lange perioder i gastroduodenalmiljøet. Herfra kan de ha direkte og indirekte patogen potensial som fører til gjentakelse av infeksjonen og som følge av behandlingsfeil, infeksjonsfall og tilbakefall av gastroduodenal sykdom. Vellykket utrydding kan derfor kreve ikke bare utrydding av bacillære former, men også av coccoidformer, eller sikre at coccoidformer ikke induseres.
Med tanke på at, siden rutinemessige metoder for tiden implementert i klinisk praksis for å bekrefte h. pylori utrydding ikke kan oppdage coccoid former, kan verter feilaktig diagnostisert som fri for infeksjon; videre kan disse metodene ikke være i stand til å gi fullstendig bevis på det kliniske potensialet til legemidlene som brukes til å utrydde H. pylori. For at utrydding skal anses som vellykket, anbefales derfor årlig oppfølging-ved hjelp av ikke-invasive teknikker eller, hvis tilgjengelig, molekylære metoder – for å avgjøre om bakterier er fullstendig eliminert, særlig i områder med høy prevalens og hos pasienter med risiko for tilbakefall.
til slutt er det nødvendig med videre studier av coccoid VBNC-formen Av H. pylori, dets patogene potensial, dets involvering i infeksjon og rekrudescens og dets rolle i å danne biofilmer i magen og andre steder i verten. Slike studier vil muliggjøre utvikling av både mer effektive diagnostiske protokoller som unngår å undervurdere kolonisering Av h. pylori og av nye terapeutiske strategier for å eliminere coccoidformer og «avvæpne» biofilmer.
Interessekonflikt
forfatterne erklærer at de ikke har noen interessekonflikt.