Innledning
Venøs tromboembolisme (VTE), inkludert dyp venetrombose (DVT), lungeemboli (PE), og splanchnic venetrombose, er en hyppig komplikasjon av kreft.1 utviklingen av kreftassosiert VTE er forbundet med redusert livskvalitet og legger en betydelig økonomisk byrde på både pasienten og helsevesenet.2 VTE er den nest ledende dødsårsaken hos kreftpasienter som får kjemoterapi, og har vist seg å være en uavhengig prediktor for dødelighet hos pasienter med kreft.3,4 behandling av kreftassosiert VTE-behandling kan være utfordrende fordi risikoen for tilbakevendende vte og antikoagulasjonsrelatert blødning er høy til tross for hensiktsmessig behandling.5 i tillegg øker legemiddelinteraksjoner og kreftrelaterte komorbiditeter, som nyre-og/eller leverdysfunksjon, redusert oralt inntak, kjemoterapiindusert kvalme og oppkast og trombocytopeni også behandlingskompleksiteten ved å begrense valget av antikoagulantmiddel.
Kliniske Studier Som Evaluerer Lavmolekylært Heparin for Behandling av Kreftassosiert VTE
langtidsbruk av lavmolekylært heparin (lmwh) for behandling AV VTE hos pasienter med aktiv kreft anbefales som førstelinjebehandling basert på resultatene fra flere åpne randomiserte kontrollerte studier (Rct).6,7 de to største studiene som hittil er publisert, CLOT (Sammenligning Av lavmolekylært heparin versus Oral antikoagulant Terapi for Forebygging Av Tilbakevendende Venøs Tromboembolisme hos Pasienter med Kreft) og CATCH (Sammenligning Av Akutt Behandling I Krefthemostase) studier, sammenlignet EN LMWH med vitamin K-antagonistbehandling hos pasienter med aktiv kreft og akutt symptomatisk proksimal DVT eller LE. Se Tabell 1 for baseline karakteristika og Tabell 2 for studieresultater.8,9 begge studiene brukte en åpen studiedesign, DET samme mål international normalized ratio (INR) i kontrollgruppen for vitamin K-antagonister, den samme aktive kreftdefinisjonen og den samme behandlingsvarigheten og hadde sammenlignbare pasientberettigelseskriterier.
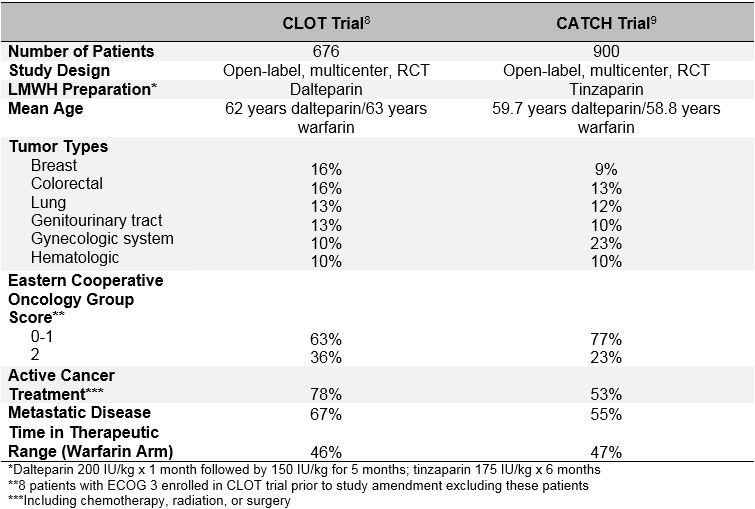
Tabell 1: Studiedesign Og Baseline Karakteristika For CATCH-Og CLOT-Studiene
Tabell 2: Resultater I KOAGULASJONS-Og FANGSTFORSØKENE

CLOT-studien, publisert i 2003, randomiserte 676 pasienter til å få dalteparin (200 IE / kg daglig i 1 måned etterfulgt av 150 IE/kg daglig i 5 måneder) eller vitamin K-antagonist (warfarin eller acenokumarol MED mål INR 2,5 i totalt 6 måneder med en innledende 5-7 dagers overlapping med dalteparin 200 IE / kg).8 Symptomatisk tilbakevendende DVT eller LE, inkludert DØD relatert TIL LE, ble observert hos 27 pasienter (7,0%) randomisert til dalteparin og hos 53 pasienter (15%) randomisert til vitamin K-antagonist (hazard ratio 0,48; 95% konfidensintervall, 0,30-0,77; p = 0,002). Ingen forskjell i forekomst av større blødninger (6 vs. 4%; p = 0,27), noen blødninger (15 vs. 19%; p = 0,09), eller død (39 vs. 41%; p = 0,53) ble observert mellom de 2 gruppene.
I CATCH-studien, publisert over 10 år senere i 2015, ble 900 pasienter randomisert til tinzaparin (175 IE/kg daglig uten dosereduksjon) eller warfarin (mål INR 2,0-3,0 med innledende tinzaparin 175 IE / kg overlapping i 5-10 dager) i totalt 6 måneder.9 det primære sammensatte endepunktet av tilbakevendende VTE inkludert tilfeldig proksimal DVT og LE forekom hos 31 pasienter (6,9%) i tinzaparin-armen og 45 pasienter (10%) i warfarin-armen (HR 0,65; 95% KI, 0,41-1,03; p = 0,07). Symptomatisk DVT forekom hos signifikant færre pasienter behandlet med tinzaparin (2,7 vs. 5,3%; HR 0,48; 95% KI, 0,24-0,96; p = 0,04). Selv om forekomsten av større blødninger var lik i begge armene, ble det observert en signifikant reduksjon i klinisk relevant, ikke-alvorlig blødning med tinzaparin (10,9 vs. 15,3%; HR 0,58; 95% KI, 0,40-0,84; p = 0,004). Dødeligheten var lik i begge gruppene, med omtrent en tredjedel av pasientene som døde i studieperioden (33,4 vs. 30,6%; p = 0,54). Selv om tinzaparin ikke signifikant reduserte det primære sammensatte endepunktet for residiverende VTE, støtter CATCH-studieresultatene bruk av langvarig LMWH som den foretrukne behandlingen for kreftassosiert VTE på grunn av lavere risiko for klinisk relevant alvorlig blødning og en signifikant reduksjon i residiverende DVT.
SVIKT i CATCH-studien til å oppfylle statistisk signifikans for det primære endepunktet kan skyldes lavere enn forventet tilbakevendende VTE-frekvens observert i warfarin-armen. En mulig forklaring på denne observasjonen kan være en forbedring i warfarinbehandling i CATCH-studien. Tilsvarende NIVÅER AV INR-kontroll i begge studiene argumenterer imidlertid mot dette (tid i terapeutisk område var 46% i BLODPROPP vs. 47% I FANGST; tid over terapeutisk område var 24% i BLODPROPP vs. 27% I FANGST). En mer sannsynlig forklaring er en skjevhet i utvalget av» mindre syke » pasienter for innmelding I CATCH-studien. SELV OM CATCH-og CLOT-studiene brukte lignende inklusjons-og eksklusjonskriterier, er det viktige forskjeller i baseline-karakteristika mellom de to pasientpopulasjonene, spesielt med hensyn til trombotiske og prognostiske risikofaktorer. En høyere andel av pasientene i CLOT-studien fikk aktiv kreftbehandling (72% CLOT vs. 53% CATCH), hadde TIDLIGERE VTE (11% CLOT vs. 6% CATCH), hadde tegn på metastatisk sykdom (67% CLOT vs. 55% FANGST), og hadde en dårligere ytelsesstatus (Eastern Cooperative Oncology Group score på 2 i 36% CLOT vs 23% FANGST). I tillegg var dødeligheten i løpet av 6-måneders behandlingsperioden også høyere i BLODPOPULASJONEN (39% BLODPROPP vs. 32% FANGST). DERMED hadde CATCH-pasientpopulasjonen sannsynligvis en lavere iboende risiko for tilbakevendende VTE sammenlignet med PASIENTER i CLOT-studien. Det er høyst sannsynlig at utprøverne ikke meldte pasienter inn I FANGST hvis DE følte AT LMWH ville være mer fordelaktig enn warfarin, noe som resulterte i selektiv registrering av pasienter som var mindre tilbøyelige til å utvikle tilbakevendende VTE.
Studier Som Evaluerer Direkte Orale Antikoagulantia ved Kreftassosiert VTE
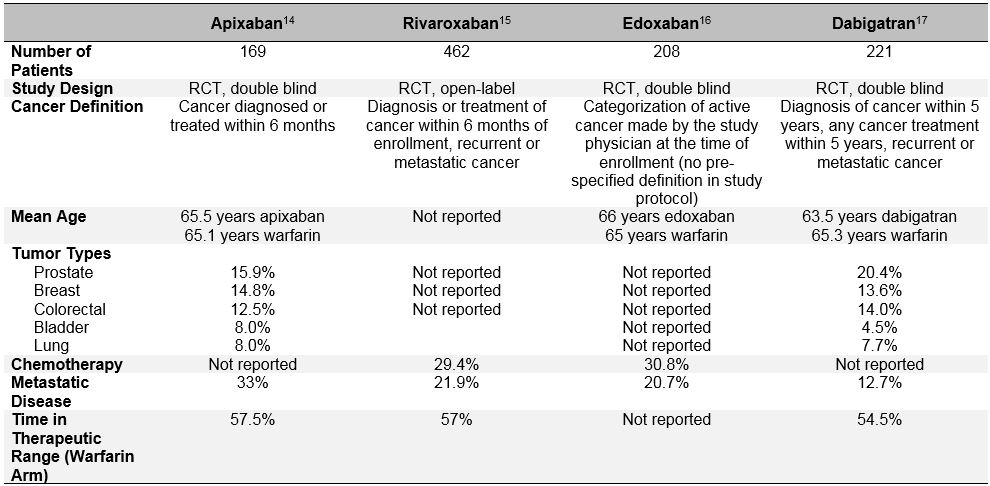
pasientseleksjonsbias er enda tydeligere i de siste randomiserte studiene som evaluerer effekt og sikkerhet av direkte orale antikoagulantia (DOACs) for behandling av akutt VTE.10 disse orale antikoagulantene har blitt grundig studert i løpet av det siste tiåret i atrieflimmer, VTE-behandling og vte-forebygging. I de kliniske fase III-studiene for akutt VTE-behandling ble det konsekvent vist at DOACs ikke er dårligere enn warfarin (samlet relativ risiko 0,90; 95% KI, 0,77-1.06) for å forebygge tilbakevendende VTE, og de har en tilsvarende eller redusert risiko for større blødninger (samlet RR 0,40; 95% KI, 0,45-0,83).11 blant de pasientene som ble klassifisert som «kreft» eller «aktiv kreft» i disse studiene, Synes DOACs også å utføre på samme måte som warfarin.12 men en mer grundig undersøkelse av disse post-hoc-dataene avslører viktig pasient-seleksjonsskjevhet og stiller spørsmål ved generaliserbarheten AV DOAC-studieresultatene til» virkelige » pasienter med kreft med VTE. I tillegg til de heterogene definisjonene av «aktiv kreft» som ble brukt i disse studiene som skilte SEG fra KOAGULASJONS-og FANGSTFORSØKENE, var viktige determinanter for tilbakevendende VTE og blødning også svært forskjellige hos DOAC-pasienter med kreft fra LMWH-kreftspesifikke studier (Tabell 3). Disse inkluderer tilstedeværelse av metastatisk sykdom og samtidig bruk av kreftbehandling. De store forskjellene i dødelighet i studieperioden hevder også at svært forskjellige grupper av pasienter med «kreft» ble inkludert I DOAC versus LMWH-studiene. Videre, i motsetning TIL LMWH, som er forbundet med en signifikant reduksjon i risiko for tilbakevendende VTE sammenlignet med vitamin K-antagonister (RR 0,52; 95% KI, 0,36-0.74), reduserte DOACs ikke signifikant denne risikoen i en meta-analyse av 1132 pasienter med kreft inkludert I EINSTEINS kliniske studieprogram, HOKUSAI-VTE (Edoksaban Versus Warfarin For Behandling Av Symptomatisk Venøs Tromboembolisme), GJENOPPRETTET (Effekt Og Sikkerhet Av Dabigatran Sammenlignet Med Warfarin For 6 Måneders Behandling Av Akutt Symptomatisk Venøs Tromboembolisme) og FORSTERKET (Apiksaban For Initial Behandling Av Lungeemboli og Dyp Venetrombose som Førstelinjebehandling) Rct (RR 0,66; 95% Ki, 0,39-1,11).10 Alle disse hensynene bør utvise forsiktighet ved ikke-valgt Bruk av DOACs hos pasienter med aktiv kreft og akutt, symptomatisk VTE.13
Tabell 3: Studiedesign og Baseline Karakteristika for Undergruppene Av Pasienter Med Kreft Fra Fase III DOAC-Studiene
Konklusjoner
alle større evidensbaserte konsensusretningslinjer anbefaler LMWH for initial og langsiktig behandling av kreftassosiert VTE.6,7,13 denne anbefalingen er basert på observasjonen at LMWH ikke bare er mer effektiv enn warfarin for forebygging av tilbakevendende VTE, men gir også ytterligere fordeler i forhold til orale midler, inkludert stabil antikoagulasjon hos pasienter med dårlig oralt inntak, mangel på legemiddelinteraksjoner og klinisk erfaring med behandling av antikoagulasjon rundt invasive prosedyrer og trombocytopeni. Selv Om DOACs for TIDEN ikke anbefales FOR VTE-behandling hos pasienter med kreft, Er Rcter som sammenligner rivaroksaban og edoksaban MED LMWH for tiden pågående og vil bidra til å avklare deres rolle i kreftassosiert VTE.6,13
- Khorana AA, Dalal M, Lin J, Connolly GC. Forekomst og prediktorer av venøs tromboembolisme (VTE) blant ambulerende høyrisiko kreftpasienter som gjennomgår kjemoterapi i Usa. Kreft 2013; 119: 648-55.
- Kourlaba G, Relakis J, Mylonas C, Et al. Den humanistiske og økonomiske byrden av venøs tromboembolisme hos kreftpasienter: en systematisk oversikt. Blodkoagul Fibrinolyse 2015; 26: 13-31.
- KUDERER NM, Ortel TL, Francis CW. Virkning av venøs tromboembolisme og antikoagulasjon på kreft og kreftoverlevelse. J Clin Oncol 2009;27:4902-11.
- Khorana AA, Francis CW, Culakova E, KUDERER NM, Lyman GH. Tromboembolisme er en ledende dødsårsak hos kreftpasienter som får poliklinisk kjemoterapi. J Thromb Haemost 2007; 5: 632-4.
- Prandoni P, Linsing AW, Piccioli A, Et al. Tilbakevendende venøs tromboembolisme og blødningskomplikasjoner under antikoagulasjonsbehandling hos pasienter med kreft og venøs trombose. Blod 2002;100:3484-8.
- Lyman GH, Bohlke K, Khorana AA, Et al. Venøs tromboembolisme profylakse og behandling hos pasienter med kreft: american society of clinical oncology klinisk praksis retningslinje oppdatering 2014. J Clin Oncol 2015; 33: 654-6.
- Streiff MB, Holmstrom B, Ashrani A, Et al. Kreftassosiert Venøs Tromboembolisk Sykdom, Versjon 1.2015. J Natl Compr Kan Netto 2015;13:1079-95.
- Lee AY, Levine MN, Baker RI, Et al. Lavmolekylært heparin versus kumarin for forebygging av tilbakevendende venøs tromboembolisme hos pasienter med kreft. N Engl J Med 2003;349:146-53.
- Lee AY, Kamphuisen PW, Meyer G, et al. Tinzaparin vs Warfarin Til Behandling Av Akutt Venøs Tromboembolisme Hos Pasienter Med Aktiv Kreft: En Randomisert Klinisk Studie. JAMA 2015; 314: 677-86.
- Transportør M, Cameron C, Delluc A, Castellucci L, Khorana AA, Lee AY. Effekt og sikkerhet av antikoagulant terapi for behandling av akutt kreftassosiert trombose: systematisk oversikt og meta-analyse. Thromb Res 2014; 134: 1214-9.
- van Es N, Coppens M, Schulman S, Middeldorp S, Bü Hr. direkte orale antikoagulantia sammenlignet med vitamin K-antagonister for akutt venøs tromboembolisme: bevis fra fase 3-studier. Blod 2014;124:1968-75.
- Vedovati MC, Germini F, Agnelli G, Becattini C. direkte orale antikoagulantia hos pasienter MED VTE og kreft: en systematisk oversikt og meta-analyse. Bryst 2015; 147: 475-83.
- Kearon C, Akl EA, Ornelas J, Et al. Antitrombotisk Terapi FOR VTE Sykdom: CHEST Guideline Og Ekspertpanel Rapport. Bryst 2016; 149: 315-52.
- Agnelli G, Bü Hr, Cohen A, Et al. Oral apiksaban til behandling av venøs tromboembolisme hos kreftpasienter: resultater FRA AMPLIFY-studien. J Thromb Haemost 2015; 13: 2187-91.
- Prins MH, Lensing AW, Brighton TA, Et al. Oral rivaroksaban versus enoksaparin med vitamin K-antagonist til behandling av symptomatisk venøs tromboembolisme hos pasienter med kreft( EINSTEIN-DVT og EINSTEIN-PE): en samlet undergruppeanalyse av to randomiserte kontrollerte studier. Lansetthematol 2014; 1: e37-46.
- raskob GE, fra Es N, Segers A, et al. Edoksaban for venøs tromboembolisme hos pasienter med kreft: resultater fra en non-inferiority subgroup analyse Av hokusai-VTE randomisert, dobbeltblind, dobbelt-dummy studie. Lansetthematol 2016; 3: e379-87.
- Schulman S, Goldhaber SZ, Kearon C, et al. Behandling med dabigatran eller warfarin hos pasienter med venøs tromboembolisme og kreft. Thromb Haemost 2015;114:150-7.
Kliniske Emner: Anticoagulation Management, Arrhythmias and Clinical EP, Cardio-Oncology, Pulmonary Hypertension and Venous Thromboembolism, Anticoagulation Management and Atrial Fibrillation, Anticoagulation Management and Venothromboembolism, Atrial Fibrillation/Supraventricular Arrhythmias
Keywords: Kardiotoksiner, Kardiotoksisitet, Heparin, Lavmolekylær, Warfarin, Antikoagulantia, Internasjonal Normalisert Ratio, Acenokumarol, Dalteparin, Antitrombin, Venøs Tromboembolisme, Risikofaktorer, Atrieflimmer, Polikliniske Pasienter, Forskningspersonell, Livskvalitet, Pyridoner, Pyrazoler, Pyridiner, Tiazoler, Venøs Trombose, Lungeemboli, Trombose, Trombocytopeni, Komorbiditet, Hemostase, Neoplasmer
< Tilbake til Oppføringer
>