Holger J Schü, Julian PT Higgins, Gunn E Vist, Paul Glasziou, Elie A Akl, Nicole Skoetz, Gordon H Guyatt; på vegne Av Cochrane GRADEing Methods Group (tidligere Applicability and Recommendations Methods Group) Og Cochrane Statistical Methods Group
- viktige punkter:
- 14.1′ Sammendrag av funn ‘tabeller
- 14.1.1 Introduksjon til’ Sammendrag av funn ‘tabeller
- 14.1.2 Valg av utfall for ‘sammendrag av funn’ – tabeller
- 14.1.3 Generell mal for’ sammendrag av funn ‘tabeller
- 14.1.4 Produsere ‘Sammendrag av funn’ tabeller
- 14.1.5 Statistiske betraktninger i’ Sammendrag av funn ‘tabeller
- 14.1.5.1 Dikotomiske utfall
- 14.1.5.2 Time-to-event utfall
- 14.1.6 Detaljert innhold i en ‘sammendrag av funn’ – tabell
- 14.1.6.1 Tabelltittel og overskrift
- 14.1.6.2 Utfall
- 14.1.6.3 Beste estimat av risiko med komparatorintervensjon
- 14.1.6.4 Risiko med intervensjon
- 14.1.6.5 Risikodifferanse
- 14.1.6.6 Relativ effekt (95% KI)
- 14.1.6.7 antall deltakere (studier)
- 14.1.6.8 Sikkerhet av dokumentasjonen (GRADE)
- 14.1.6.9 Kommentarer
- 14.1.6.10 Forklaringer
- 14.2 Vurdering av sikkerheten eller kvaliteten på et bevislegeme
- 14.2.1 GRADE-tilnærmingen
viktige punkter:
- En ‘Sammendrag av funn’ – tabell for en gitt sammenligning av tiltak gir nøkkelinformasjon om størrelsene på relative og absolutte effekter av de undersøkte tiltakene, mengden tilgjengelig dokumentasjon og sikkerheten (eller kvaliteten) av tilgjengelig dokumentasjon.
- ‘Sammendrag av funn’ tabeller inneholder en rad for hvert viktig utfall (opptil maksimalt syv). Godkjente formater Av ‘Sammendrag av funn’ tabeller og interaktive ‘Sammendrag av funn’ tabeller kan produseres VED HJELP AV GRADE programvare GRADEpro GDT.
- Cochrane har vedtatt GRADE-tilnærmingen (Grading of Recommendations Assessment, Development And Evaluation) for å vurdere sikkerhet (eller kvalitet) av et dokument.
- GRADE-tilnærmingen spesifiserer fire nivåer av sikkerhet for et dokument for et gitt utfall: høy, moderat, lav og svært lav.
- GRADEVURDERINGER av sikkerhet fastsettes gjennom vurdering av fem domener: risiko for skjevhet, inkonsekvens, indirekthet, unøyaktighet og publiseringsskjevhet. For bevis fra ikke-randomiserte studier og sjelden randomiserte studier, kan vurderinger deretter oppgraderes gjennom vurdering av ytterligere tre domener.
Sitere dette kapittelet Som: Schü HJ, Higgins JPT, Vist GE, Glasziou P, Akl EA, Skoetz N, Guyatt GH. Kapittel 14: Fullføre ‘Sammendrag av funn’ tabeller og gradering sikkerheten av bevis. I: Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, Page MJ, Welch VA (redaktører). Cochrane Handbook for Systematic Reviews of Interventions versjon 6.2 (oppdatert februar 2021). Cochrane, 2021. Tilgjengelig fra www.trening.cochrane.org/handbook.
14.1′ Sammendrag av funn ‘tabeller
14.1.1 Introduksjon til’ Sammendrag av funn ‘tabeller
‘ Sammendrag av funn ‘ tabeller presenterer hovedfunnene i en gjennomgang i et gjennomsiktig, strukturert og enkelt tabellformat. Spesielt gir de nøkkelinformasjon om sikkerhet eller kvalitet av bevis (dvs. tillit eller sikkerhet i området for et effektestimat eller en forening), omfanget av effekten av de undersøkte tiltakene og summen av tilgjengelige data om hovedresultatene. Cochrane-Oversikter bør inkludere ‘Sammendrag av funn’ – tabeller under planlegging og publisering, og bør ha minst en nøkkel ‘Sammendrag av funn’ – tabell som representerer de viktigste sammenligningene. Noen oversikter kan inneholde mer enn En ‘sammendrag av funn’ – tabell, for eksempel hvis oversiktene omhandler mer enn en større sammenligning, eller inneholder vesentlig forskjellige populasjoner som krever separate tabeller (for eksempel fordi effektene er forskjellige eller det er viktig å vise resultatene separat). I Cochrane Database Of Systematic Reviews (Cdsr) vises den viktigste Oppsummeringstabellen for en oversikt i begynnelsen, før Bakgrunnsdelen. Andre ‘Sammendrag av funn’ – tabeller vises mellom Resultatene og Diskusjonsseksjonene.
14.1.2 Valg av utfall for ‘sammendrag av funn’ – tabeller
Planlegging av ‘sammendrag av funn’ – tabellen starter tidlig i den systematiske oversikten, med valg av utfall som skal inkluderes i: (i) oversikten; og (ii) ‘Sammendrag av funn’ – tabellen. Dette er et viktig skritt, og en som gjennomgang forfattere må ta nøye.
For å sikre produksjon av optimalt nyttig informasjon, Begynner Cochrane-Oversiktene med å utvikle et oversiktsspørsmål og ved å liste opp alle hovedresultatene som er viktige for pasienter og andre beslutningstakere (Se Kapittel 2 Og Kapittel 3). GRADE-tilnærmingen for å vurdere sikkerheten i dokumentasjonen (Se Avsnitt 14.2) definerer og operasjonaliserer en vurderingsprosess som bidrar til å skille utfall i de som er kritiske, viktige eller ikke viktige for beslutningstaking. Konsultasjon og tilbakemelding på gjennomgangsprotokollen, inkludert fra forbrukere og andre beslutningstakere, kan forbedre denne prosessen.
Kritiske utfall vil sannsynligvis inkludere klart viktige endepunkter; typiske eksempler er dødelighet og større morbiditet (som slag og hjerteinfarkt). Imidlertid kan de også representere hyppige mindre og sjeldne store bivirkninger, symptomer, livskvalitet, byrder forbundet med behandling og ressursproblemer (kostnader). Byrder representerer virkningen av helsevesenets arbeidsbelastning på pasientfunksjon og velvære, og inkluderer kravene til å overholde et inngrep som pasienter eller omsorgspersoner (f.eks. familie) kan mislike, for eksempel å måtte gjennomgå hyppigere tester eller restriksjonene på livsstil som visse tiltak krever (Spencer-Bonilla et al 2017).
ofte, når du formulerer spørsmål som inkluderer alle pasient-viktige utfall for beslutningstaking, vil oversiktsforfattere konfrontere rapporter om studier som ikke har inkludert alle disse utfallene. Dette gjelder spesielt for uønskede utfall. For eksempel kan randomiserte studier bidra med bevis på tilsiktede effekter, og på hyppige, relativt små bivirkninger, men ikke rapportere om sjeldne uønskede utfall som selvmordsforsøk. Kapittel 19 diskuterer strategier for å håndtere bivirkninger. For å få data for alle viktige utfall kan det være nødvendig å undersøke resultatene av ikke-randomiserte studier (Se Kapittel 24). Cochrane har i samarbeid med andre utviklet veiledning for oversiktsforfattere for å støtte sin beslutning om når man skal se etter og inkludere ikke-randomiserte studier (Sch@nemann et al 2013).
hvis en gjennomgang bare inneholder randomiserte studier, kan disse forsøkene ikke adressere alle viktige utfall, og det kan derfor ikke være mulig å adressere disse utfallene innenfor begrensningene i vurderingen. Gjennomgangsforfattere bør erkjenne disse begrensningene og gjøre dem gjennomsiktige for leserne. Forfatterne oppfordres til å inkludere ikke-randomiserte studier for å undersøke sjeldne eller langsiktige bivirkninger som kanskje ikke tilstrekkelig studeres i randomiserte studier. Dette øker muligheten for at skadeutfall kan komme fra studier der deltakerne skiller seg fra de i studier som brukes i analysen av nytte. Oversiktsforfattere må da vurdere hvor mye slike forskjeller sannsynligvis vil påvirke funnene, og dette vil påvirke bevissikkerheten på grunn av bekymringer om indirekthet relatert til befolkningen (Se Avsnitt 14.2.2).
Ikke-randomiserte studier kan gi viktig informasjon, ikke bare når randomiserte studier ikke rapporterer om et utfall eller randomiserte studier lider av indirekthet, men også når bevisene fra randomiserte studier er vurdert som svært lave og ikke-randomiserte studier gir bevis på høyere sikkerhet. Videre drøfting av disse spørsmålene vises også I Kapittel 24.
14.1.3 Generell mal for’ sammendrag av funn ‘tabeller
Flere alternative standardversjoner av’ sammendrag av funn ‘ tabeller er utviklet For å sikre konsistens og brukervennlighet på tvers av vurderinger, inkludering av den viktigste informasjonen som trengs av beslutningstakere, og optimal presentasjon (se eksempler På Figur 14.1.a og 14.1.b). Disse formatene støttes av forskning som fokuserte på bedre forståelse av informasjonen de har til hensikt å formidle(Carrasco-Labra et al 2016, Langendam et al 2016, Santesso et al 2016). DE er tilgjengelige GJENNOM GRADE offisielle programvarepakke utviklet for å støtte GRADE tilnærming: GRADEpro GDT (www.gradepro.org).
Standard Cochrane ‘sammendrag av funn’ – tabeller inneholder følgende elementer ved hjelp av et av de aksepterte formatene. Ytterligere veiledning om hver av disse er gitt I Avsnitt 14.1.6.
- en kort beskrivelse av populasjonen og innstillingen adressert av tilgjengelig bevis (som kan være litt annerledes enn eller smalere enn de som er definert av vurderingsspørsmålet).
- En kort beskrivelse av sammenligningen adressert i ‘Sammendrag av funn’ – tabellen, inkludert både eksperimentelle og sammenligningsintervensjoner.
- en liste over de mest kritiske og/eller viktige helseutfallene, både ønskelige og uønskede, begrenset til syv eller færre utfall.
- et mål på den typiske byrden av hvert utfall (f. eks. illustrerende risiko, eller illustrerende gjennomsnitt, på komparatorintervensjon).
- den absolutte og relative størrelsen på effekten målt for hver (hvis begge er passende).
- antall deltakere og studier som bidrar til analysen av hvert utfall.
- EN KARAKTERVURDERING av samlet sikkerhet i dokumentasjonen for hvert utfall(som kan variere etter utfall).
- Plass til kommentarer.
- Forklaringer (tidligere kjent som fotnoter).
Ideelt sett støttes ‘Sammendrag av funn’ – tabeller av mer detaljerte tabeller (kjent som ‘bevisprofiler’) som gjennomgangen kan knyttes til, noe som gir mer detaljerte forklaringer. Evidensprofiler inkluderer de samme viktige helseutfallene, og gir større detalj enn ‘Sammendrag av funn’ tabeller av både de individuelle hensynene som går inn i gradering av sikkerhet og resultatene av studiene(Guyatt et al 2011a). De sikrer at en strukturert tilnærming brukes til å vurdere sikkerheten til bevis. Selv om de er sjelden publisert I Cochrane Vurderinger, bevis profiler er ofte brukt, for eksempel, av retningslinje utviklere i å vurdere sikkerheten av bevis for å støtte retningslinje anbefalinger. Gjennomgangsforfattere vil finne det lettere å utvikle ‘Sammendrag av funn’ – tabellen ved å fullføre vurderingen av visshet om bevis i bevisprofilen først i GRADEpro GDT. De kan deretter automatisk konvertere dette til et Av Formatene’ Sammendrag av funn ‘I GRADEpro GDT, inkludert et interaktivt’ Sammendrag av funn ‘ for publisering.
Som et mål på omfanget av effekt for dikotomiske utfall, bør Tabellen ‘sammendrag av funn’ gi et relativt mål for effekt (f.eks. risikoratio, oddsratio, fare) og mål for absolutt risiko. For andre typer data kan et absolutt mål alene (for eksempel en forskjell i midler for kontinuerlige data) være tilstrekkelig. Det er viktig at omfanget av effekten presenteres på en meningsfull måte, noe som kan kreve en viss transformasjon av resultatet av en meta-analyse (se Også Kapittel 15, Avsnitt 15.4 og Avsnitt 15.5). Anmeldelser med mer enn en hoved sammenligning bør inneholde en egen ‘Sammendrag av funn’ tabell for hver sammenligning.
Figur 14.1.a gir et eksempel på En’ Sammendrag av funn ‘ tabell. Figur 15.1.b gir et alternativt format som kan legge til rette for brukernes forståelse og tolkning av gjennomgangens funn. Evidens som evaluerer ulike formater tyder på at’ Sammendrag av funn ‘ – tabellen bør inneholde en risikoforskjell som et mål på den absolutte effekten, og forfattere bør helst bruke et format som inkluderer en risikoforskjell .
en detaljert beskrivelse av innholdet i En ‘Sammendrag av funn’ – tabell vises I Avsnitt 14.1.6.
Figur 14.1.et eksempel på En’ Sammendrag av funn ‘ tabell
Sammendrag av funn (for interaktiv versjon klikk her)
|
Kompresjonstrømper sammenlignet med ingen kompresjonstrømper for folk som tar lange flyreiser |
||||||
|
Pasienter eller populasjon: alle som tar en lang flytur (varer mer enn 6 timer) Innstillinger: internasjonal flyreise Intervensjon: kompresjonsstrømpera Sammenligning: uten strømper |
||||||
|
Resultater |
illustrative komparative risikoer* (95% KI) |
Relativ effekt (95% KI) |
antall deltakere (studier) |
Visshet om bevis (GRAD) |
||
|
Antatt risiko |
Tilsvarende risiko |
|||||
|
uten strømper |
med strømper |
|||||
|
Symptomatisk dyp venetrombose (DVT)) |
Se kommentar |
Se kommentar |
ikke estimerbar |
(9 studier) |
Se kommentar |
0 deltakerne utviklet symptomatisk DVT i disse studiene |
|
Symptomfri DVT |
lav risiko befolkningb |
RR 0.10 (0.04 til 0.26) |
(9 studier) |
⊕⊕⊕⊕ Høy |
||
|
10 per 1000 |
1 per 1000 (0 til 3) |
|||||
|
høyrisikopopulasjonb |
||||||
|
20 per 1000 |
2 per 1000 (1 til 8) |
|||||
|
Overfladisk venetrombose |
13 per 1000 |
6 per 1000 (2 til 15) |
RR 0.45 (0.18 til 1.13) |
(8 studier) |
⊕⊕⊕◯ Moderatec |
|
|
Ødem Verdier etter flygning målt på en skala fra 0, ingen ødem, til 10, maksimalt ødem |
gjennomsnittlig ødemscore varierte på tvers av kontrollgrupper fra 6 til 9 |
gjennomsnittlig ødemscore i intervensjonsgruppene var i gjennomsnitt 4,7 lavere (95% KI -4,9 til -4.5) |
(6 studier) |
⊕⊕◯◯ Lowd |
||
|
Lungeembolus |
Se kommentar |
Se kommentar |
ikke estimerbar |
(9 studier) |
Se kommentar |
0 deltakere utviklet lungeembolus i disse studiene |
|
Døden |
Se kommentar |
Se kommentar |
Ikke estimable |
(9 studier) |
Se kommentar |
0 deltakerne døde i disse studiene |
|
Bivirkninger |
Se kommentar |
Se kommentar |
ikke estimerbar |
(4 studier) |
Se kommentar |
toleransen av strømpene ble beskrevet som veldig bra uten klager på bivirkninger i 4 studierf |
|
*grunnlaget for den antatte risikoen er gitt i fotnote. Tilsvarende risiko (og 95% konfidensintervall) er basert på antatt risiko i intervensjonsgruppen og den relative effekten av intervensjonen (og 95% KI). KI: konfidensintervall; RR: risikoforhold; GRAD: Grad Arbeidsgruppe grader av bevis (se forklaringer). |
||||||
a alle strømper i de ni studiene som ble inkludert i denne anmeldelsen var under-knestrømper. I fire studier var kompresjonsstyrken 20 mmHg til 30 mmHg ved ankelen. Det var 10 mmHg til 20 mmHg i de andre fire studiene. Strømper kommer i forskjellige størrelser. Hvis en strømpe er for stramt rundt kneet, kan det forhindre essensiell venøs retur som forårsaker at blodet samler seg rundt kneet. Kompresjonstrømper skal monteres riktig. En strømpe som er for stram kan kutte inn i huden på en lang flytur og potensielt forårsake sårdannelse og økt risiko FOR DVT. Noen strømper kan være litt tykkere enn vanlig benbelegg og kan være potensielt restriktive med tett fotslitasje. Det er en god ide å ha på seg strømper rundt huset før du reiser for å sikre en god, behagelig passform. Deltakerne satte sine strømper på to til tre timer før flyet i de fleste studiene. Tilgjengeligheten og kostnaden for strømper kan variere.
B to studier rekrutterte høyrisikodeltagere definert som de med tidligere EPISODER AV DVT, koagulasjonsforstyrrelser, alvorlig fedme, begrenset mobilitet på grunn av bein-eller leddproblemer, neoplastisk sykdom i løpet av de to foregående årene, store åreknuter eller, i en av studiene, deltakere høyere enn 190 cm og tyngre enn 90 kg. Forekomsten for de syv studiene som ekskluderte høyrisikodeltakere var 1.45% og insidensen for de to studiene som rekrutterte høyrisikodeltakere (med minst en risikofaktor) var 2,43%. Vi har brukt henholdsvis 10 og 30 per 1000 for å uttrykke ulike risikostater.
c konfidensintervallet krysser ingen forskjell og utelukker ikke en liten økning.
d måling av ødem ble ikke validert (indirekthet av utfallet) eller blindet for intervensjonen (risiko for skjevheter).
e hvis det er svært få eller ingen hendelser og antall deltakere er store, kan vurdering om bevissikkerhet (spesielt vurderinger om unøyaktighet) være basert på den absolutte effekten. Her kan sikkerhetsvurderingen betraktes som ‘ høy ‘ hvis utfallet ble riktig vurdert og hendelsen faktisk ikke skjedde i 2821 studerte deltakere.
f ingen av de andre studiene rapporterte bivirkninger, bortsett fra fire tilfeller av overfladisk venetrombose i åreknuter i kneregionen som ble komprimert av øvre kant av strømpen i en studie.
Figur 14.1.B Eksempel på alternativ ‘Sammendrag av funn’ tabell
|
Sammendrag av funn (for interaktiv versjon klikk her): |
||||||
|
Probiotika sammenlignet med ingen probiotika som et supplement til antibiotika hos barn |
||||||
|
Pasient eller populasjon: barn som får antibiotika Innstillinger: innleggelse og poliklinisk Intervensjon: probiotika Sammenligning: ingen probiotika |
||||||
|
Utfall Ingen av deltakerne (studier) |
Relative effekter |
Forventede absolutte effekter* (95% KI) |
Sikkerhet av dokumentasjonen |
|||
|
uten probiotika |
med probiotika |
Forskjell |
||||
|
Forekomst av diare: Probiotisk dose 5 milliarder CFU / dag Oppfølging: 10 dager til 3 måneder Barn < 5 år |
Barn < 5 år |
⊕⊕⊕⊝ moderateb På grunn av risiko for skjevheter |
Sannsynligvis reduserer forekomsten av diare. |
|||
|
1474 (7 studier) |
RR 0,41 (0,29 til 0.55) |
22.3%a |
8.9% (6.5 til 12.2) |
13.4% færre barn (10,1 til 15.8 færre) |
||
|
Barn > 5 år |
Barn > 5 år |
⊕⊕⊝⊝ lowb, c På grunn av risiko for skjevheter og unøyaktigheter |
kan redusere forekomsten av diare. |
|||
|
624 (4 studier) |
RR 0,81 (0,53 til 1.21) |
11.2%a |
9% (5.9 til 13.6) |
2.2% færre barn (5,3 færre til 2.4 mer) |
||
|
Bivirkningerd Oppfølging: 10 til 44 dager 1575 (11 studier) |
1.8%a |
2.3% (0.8 til 3.8) |
0.5% flere bivirkninger (1 færre til 2 flere) |
⊕⊕⊝⊝ lowf, g på grunn av risiko for skjevhet og inkonsekvens |
det kan være liten eller ingen forskjell i bivirkninger. |
|
|
Varighet av diare Oppfølging: 10 dager til 3 måneder 897 (5 studier) |
gjennomsnittlig varighet av diare uten probiotika var 4 dager. |
0.6 færre dager (1,18 til 0,02 færre dager) |
⊕⊕⊝⊝ lowh, i På grunn av unøyaktighet og inkonsekvens |
kan redusere varigheten av diare. |
||
|
Avføring per dag Oppfølging: 10 dager til 3 måneder 425 (4 studier) |
gjennomsnittlig avføring per dag uten probiotika var 2,5 avføring per dag. |
0.3 færre avføring per dag (0,6 til 0 færre) |
⊕⊕⊝⊝ lowj, k på grunn av unøyaktighet og inkonsekvens |
det kan være liten eller ingen forskjell i avføring per dag. |
||
|
*grunnlaget for risikoen i kontrollgruppen (f. eks. median kontrollgrupperisiko på tvers av studier) er gitt i fotnoter. Risikoen i intervensjonsgruppen (og 95% konfidensintervall) er basert på antatt risiko i sammenligningsgruppen og den relative effekten av intervensjonen (og 95% KI). KI: konfidensintervall; RR: risikoforhold. |
||||||
|
FORKLARINGER En Kontrollgrupperisikoestimat kommer fra samlede estimater av kontrollgrupper. Relativ effekt basert på tilgjengelig kasusanalyse B Høy risiko for skjevhet på grunn av stort tap for oppfølging. C Unøyaktighet på grunn av få hendelser og konfidensintervaller inkluderer merkbar nytte eller skade. D Bivirkninger: utslett, kvalme, flatulens, oppkast, økt slim, brystsmerter, forstoppelse, smaksforstyrrelser og lav appetitt. E-Risiko ble beregnet ut fra samlede risikoforskjeller. F Høy risiko for skjevheter. Bare 11 av 16 studier rapporterte om bivirkninger, noe som tyder på en selektiv rapporteringsskjevhet. G Alvorlig inkonsekvens. Tallrike probiotiske midler og doser ble evaluert blant et relativt lite antall forsøk, noe som begrenser vår evne til å trekke konklusjoner om sikkerheten til de mange probiotiske midler og doser som ble administrert. H Alvorlig uforklarlig inkonsekvens (stor heterogenitet I2 = 79%, p-verdi, punktestimater og konfidensintervall varierer betydelig). Jeg Alvorlig unøyaktighet. Øvre grense på 0,02 færre dager med diare anses ikke som viktig for pasienten. J Alvorlig uforklarlig inkonsekvens (stor heterogenitet I2 = 78%, p-verdi, punktestimater og konfidensintervall varierer betydelig). K Alvorlig unøyaktighet. 95% konfidensintervall inkluderer ingen effekt og nedre grense på 0,60 avføring per dag er av tvilsom betydning for pasienten. |
||||||
14.1.4 Produsere ‘Sammendrag av funn’ tabeller
GRADE Arbeidsgruppens programvare, GRADEpro GDT (www.gradepro.org), inkludert GRADE interaktive håndbok, er tilgjengelig for å hjelpe gjennomgang forfattere i utarbeidelsen av ‘Sammendrag av funn’ tabeller. GRADEpro kan bruke data om komparatorgrupperisiko og effektestimat (angitt av oversiktsforfatterne eller importert fra filer generert I RevMan) for å produsere de relative effektene og absolutte risikoene forbundet med eksperimentelle inngrep. I tillegg leder den brukeren gjennom PROSESSEN MED EN VURDERINGSVURDERING, og produserer en tabell som kan brukes som en frittstående tabell i en gjennomgang (inkludert ved direkte import til programvare Som RevMan eller integrasjon med RevMan Web), eller en interaktiv ‘Sammendrag av funn’ – tabell (se hjelperessurser I GRADEpro).
14.1.5 Statistiske betraktninger i’ Sammendrag av funn ‘tabeller
14.1.5.1 Dikotomiske utfall
‘ Sammendrag av funn ‘ tabeller bør inneholde både absolutte og relative effektmål for dikotomiske utfall. Risikoforhold, oddsforhold og risikoforskjeller er forskjellige måter å sammenligne to grupper med dikotom utfallsdata (Se Kapittel 6, Avsnitt 6.4.1). Videre er det to forskjellige risikoforhold, avhengig av hvilken hendelse (f. eks.’ ja ‘eller’ nei’) som er fokus for analysen (Se Kapittel 6, Avsnitt 6.4.1.5). I nærvær av en ikke-null intervensjonseffekt vil enhver variasjon på tvers av studier i komparatorgruppen (dvs . variasjon i risikoen for at hendelsen skjer uten interesseintervensjon, for eksempel i forskjellige populasjoner) gjør det umulig for mer enn ett av disse tiltakene å være virkelig det samme i hver studie.
det har lenge vært antatt i epidemiologi at relative tiltak av effekt er mer konsistente enn absolutte tiltak av effekt fra ett scenario til et annet. Det er empiriske bevis for å støtte denne antagelsen(Engels et al 2000, Deeks and Altman 2001, Furukawa et al 2002). Av denne grunn bør metaanalyser generelt bruke enten et risikoratio eller et oddsratio som et mål på effekt (Se Kapittel 10, Avsnitt 10.4.3). Tilsvarende vil et enkelt estimat av relativ effekt sannsynligvis være et mer hensiktsmessig sammendrag enn et enkelt estimat av absolutt effekt. Hvis en relativ effekt faktisk er konsistent på tvers av studier, vil ulike komparatorgrupperisiko ha forskjellige implikasjoner for absolutt nytte. For eksempel, hvis risikoforholdet er konsekvent 0.75, da ville eksperimentell intervensjon redusere en komparatorgrupperisiko på 80% til 60% i intervensjonsgruppen (en absolutt risikoreduksjon på 20 prosentpoeng), men ville også redusere en komparatorgrupperisiko på 20% til 15% i intervensjonsgruppen (en absolutt risikoreduksjon på 5 prosentpoeng).
‘Sammendrag av funn’ tabeller er bygget rundt antagelsen om en konsekvent relativ effekt. Det er derfor viktig å vurdere konsekvensene av denne effekten for ulike komparatorgrupperisiko (disse kan utledes eller estimeres fra En rekke kilder, se Pkt. 14.1.6.3), som kan kreve en vurdering av sikkerheten til bevis for prognostisk bevis (Spencer et al 2012, Iorio et al 2015). For enhver komparatorgruppe risiko er det mulig å estimere en tilsvarende intervensjonsgruppe risiko (dvs. den absolutte risikoen med intervensjonen) fra meta-analytisk risiko ratio eller odds ratio. Merk at tallene i Kolonnen ‘Tilsvarende risiko’ er spesifikke for ‘risikoene’ i den tilstøtende kolonnen.
for meta-analytic risk ratio (RR) og antatt komparatorrisiko (ACR) er tilsvarende intervensjonsrisiko oppnådd som:
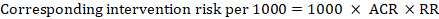 .
.
som Et eksempel, I Figur 14.1.a, det meta-analytiske risikoforholdet for symptomfri dyp venetrombose (DVT) ER RR = 0,10 (95% KI 0,04 til 0,26). Forutsatt en komparatorrisiko FOR ACR = 10 per 1000 = 0,01, oppnår vi:
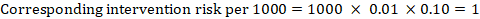 .
.
FOR metaanalytisk oddsratio (OR) OG antatt komparatorrisiko, ACR, oppnås den tilsvarende intervensjonsrisikoen som:
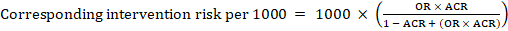 .
.
øvre og nedre konfidensgrense for tilsvarende intervensjonsrisiko oppnås ved å erstatte RR eller OR med henholdsvis øvre og nedre konfidensgrense (f. eks. erstatte 0.10 med 0,04, deretter med 0,26, i eksemplet). Slike konfidensintervaller inneholder ikke usikkerhet i de antatte komparatorrisikoene.
ved håndtering av risikoforhold er det kritisk at den samme definisjonen av’ hendelse ‘ brukes som ble brukt for metaanalysen. For eksempel, hvis meta-analysen fokuserte på ‘ død ‘(i motsetning til overlevelse) som hendelse, må tilsvarende risiko i Tabellen ‘Sammendrag av funn’ også referere til ‘død’.
i (sjeldne) omstendigheter der det er klart grunnlag for å anta en konsistent risikoforskjell i metaanalysen, er det i prinsippet mulig å presentere dette for relevante ‘antatte risikoer’ og deres tilsvarende risikoer, og å presentere de tilsvarende (forskjellige) relative effektene for hver antatt risiko.
risikoforskjellen uttrykker forskjellen MELLOM ACR og tilhørende intervensjonsrisiko(eller forskjellen mellom eksperimentell og komparatorintervensjon).
for meta-analytic risk ratio (RR) og antatt komparatorrisiko (ACR) er den tilsvarende risikoforskjellen oppnådd som (merk at risiko også kan uttrykkes ved hjelp av prosent eller prosentpoeng):
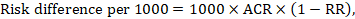
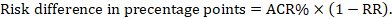
som Et eksempel, I Figur 14.1.b den meta-analytiske risikoforholdet er 0,41 (95% KI 0,29 til 0,55) for diare hos barn under 5 år. Forutsatt en komparatorgrupperisiko på 22,3% oppnår vi:
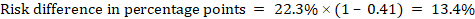 .
.
for metaanalytisk oddsratio (OR) og antatt komparatorrisiko (ACR) oppnås den absolutte risikodifferansen som (prosentpoeng):
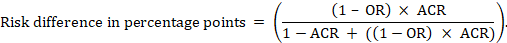
Øvre og nedre konfidensgrenser for den absolutte risikodifferansen oppnås ved å kjøre beregningen over på nytt mens du erstatter rr eller OR med henholdsvis øvre og nedre konfidensgrenser (f.eks. erstatte 0,41 med 0,28, deretter med 0,55, i eksemplet). Slike konfidensintervaller inneholder ikke usikkerhet i de antatte komparatorrisikoene.
14.1.5.2 Time-to-event utfall
Time-to-event utfall måler om og når en bestemt hendelse (f. eks død) oppstår (van Dalen et al 2007). Virkningen av eksperimentell intervensjon i forhold til sammenligningsgruppen på utfall fra tid til hendelse måles vanligvis ved hjelp AV et hazard ratio (HR) (Se Kapittel 6, Avsnitt 6.8.1).
et hazard ratio uttrykker et relativt effektestimat. Det kan brukes på ulike måter for å oppnå absolutt risiko og andre tolkbare mengder for en bestemt populasjon. Her beskriver vi hvordan du re-express hazard ratio i form av: (i) absolutt risiko for hendelsesfri overlevelse innen en bestemt tidsperiode; (ii) absolutt risiko for en hendelse innen en bestemt tidsperiode; og (iii) median tid til hendelsen. Alle metoder er bygget på en antagelse om konsistente relative effekter (dvs.at hazard ratio ikke varierer over tid).
(i) Absolutt risiko for hendelsesfri overlevelse innen en bestemt tidsperiode Hendelsesfri overlevelse (f.eks. total overlevelse) rapporteres vanligvis i individuelle studier. For å oppnå absolutte effekter for utfall fra tid til hendelse målt som hendelsesfri overlevelse, kan sammendraget HR brukes sammen med en antatt andel pasienter som er hendelsesfrie i komparatorgruppen (Tierney et al 2007). Denne andelen pasienter vil være spesifikk for en observasjonsperiode. Det er imidlertid ikke strengt nødvendig å spesifisere denne tidsperioden. For eksempel kan en andel på 50% av pasientene uten hendelser gjelde for pasienter med høy hendelsesrate observert over 1 år, eller for pasienter med lav hendelsesrate observert over 2 år.

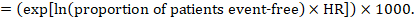
som et eksempel, anta at meta-analytisk hazard ratio er 0,42 (95% KI 0,25 til 0,72). Forutsatt en komparatorgruppe risiko for hendelsesfri overlevelse (f. eks. for totaloverlevelse mennesker er i live) ved 2 år MED ACR = 900 per 1000 = 0,9 får vi:

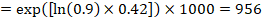
slik at 956 per 1000 mennesker vil være i live med eksperimentell intervensjon på 2 år. Avledningen av risikoen bør forklares i en kommentar eller fotnote.
(ii) Absolutt risiko for en hendelse innen en bestemt tidsperiode for å oppnå denne absolutte effekten, igjen kan sammendraget HR brukes (Tierney et al 2007):

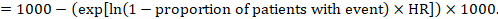
i eksemplet antar vi at vi antar en komparatorgruppe risiko for hendelser (f.eks. for dødelighet, mennesker er døde) ved 2 år MED ACR = 100 per 1000 = 0,1. Vi får:

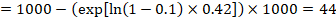
slik at 44 per 1000 mennesker vil være døde med eksperimentell intervensjon på 2 år.
(iii) median tid Til hendelsen I stedet for absolutte tall kan tiden til hendelsen i intervensjons-og sammenligningsgruppene uttrykkes som median overlevelsestid i måneder eller år. For å oppnå median overlevelsestid kan samlet HR brukes på en antatt median overlevelsestid i komparatorgruppen (Tierney et al 2007):
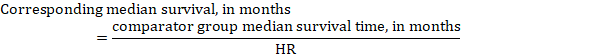
i eksemplet, forutsatt en komparatorgruppe median overlevelsestid på 80 måneder, oppnår vi:
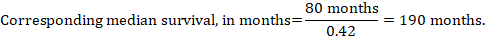
for alle disse tre alternativene for å re-uttrykke resultater av time-to-event analyser, oppnås øvre og nedre konfidensgrenser for den tilsvarende intervensjonsrisikoen ved å erstatte HR med henholdsvis øvre og nedre konfidensgrenser (f.eks. erstatte 0,42 med 0,25, deretter med 0,72, i eksemplet). Igjen, når det gjelder dikotomiske utfall, inneholder slike konfidensintervaller ikke usikkerhet i de antatte komparatorgrupperisikoene. Dette er spesielt bekymringsfullt for langtidsoverlevelse med lav eller moderat dødelighet og et tilsvarende høyt antall sensurerte pasienter(dvs. et lavt antall risikopasienter og en høy sensureringsrate).
14.1.6 Detaljert innhold i en ‘sammendrag av funn’ – tabell
14.1.6.1 Tabelltittel og overskrift
tittelen på hver ‘sammendrag av funn’ – tabell skal angi helsespørsmålet, innrammet i forhold til populasjonen og gjøre det klart nøyaktig hvilken sammenligning av tiltak som er gjort. I Figur 14.1.a, befolkningen er folk som tar lange flyfly, intervensjonen er kompresjonstrømper, og kontrollen er ingen kompresjonstrømper.
de første radene i Hver ‘Sammendrag av funn’ – tabell skal gi følgende ‘ overskriftsinformasjon:
Pasienter Eller populasjon dette klargjør ytterligere populasjonen (og muligens subpopulasjonene) av interesse og ideelt sett omfanget av risikoen for det mest avgjørende negative utfallet som en intervensjon er rettet mot. For eksempel, folk på en lang hale fly kan være på ulike risikoer FOR DVT; de som bruker selektive serotoninreopptakshemmere (Ssri) kan ha forskjellig risiko for bivirkninger; mens de med atrieflimmer kan være lav (< 1%), moderat (1% til 4%) eller høy (> 4%) årlig risiko for slag.
Innstilling Dette bør angi eventuelle spesifikke egenskaper ved innstillingene i helsespørsmålet som kan begrense bruken av sammendraget av funn til andre innstillinger (for eksempel primærhelsetjenesten I Europa og Nord-Amerika).
Intervensjon den eksperimentelle intervensjonen.
Sammenligning komparatorintervensjonen(inkludert ingen spesifikk intervensjon).
14.1.6.2 Utfall
radene i en ‘sammendrag av funn’ – tabell bør inneholde alle ønskelige og uønskede helseutfall (oppført i rekkefølge av betydning)som er avgjørende for beslutningstaking, opp til maksimalt syv utfall. Hvis det er flere utfall i gjennomgangen, må gjennomgangsforfattere utelate de mindre viktige utfallene fra tabellen, og beslutningen om å velge hvilke utfall som er kritiske eller viktige for gjennomgangen, bør gjøres under protokollutvikling (Se Kapittel 3). Gjennomgangsforfattere bør gi tidsrammer for måling av resultatene (f.eks. 90 dager eller 12 måneder) og typen instrumentskår (f. eks. fra 0 til 100).
Vær oppmerksom på at forfatterne av gjennomgangen bør inkludere de forhåndsdefinerte kritiske og viktige utfallene i tabellen om data er tilgjengelige eller ikke. De bør imidlertid være oppmerksomme på muligheten for at betydningen av et utfall (f. eks. en alvorlig negativ effekt) først kan bli kjent etter at protokollen ble skrevet eller analysen ble utført, og bør treffe hensiktsmessige tiltak for å inkludere disse i sammendraget av funn-tabellen.
tabellen ‘sammendrag av funn’ kan inkludere effekter i undergrupper av populasjonen for ulike komparatorrisikoer og effektstørrelser separat. For Eksempel I Figur 14.1.b-effekter presenteres for barn yngre og eldre enn 5 år separat. Gjennomgangsforfattere kan også velge å produsere separate ‘Sammendrag av funn’ tabeller for forskjellige populasjoner.
Oversiktsforfattere bør inkludere alvorlige bivirkninger, men det kan være mulig å kombinere mindre bivirkninger som et enkelt utfall, og beskrive dette i en forklarende fotnote (merk at det ikke er hensiktsmessig å legge til hendelser sammen med mindre de er uavhengige, det vil si at en deltaker som har opplevd en bivirkning har en upåvirket sjanse til å oppleve den andre bivirkningen).
Utfall målt på flere tidspunkter representerer et bestemt problem. Generelt, for å holde bordet enkelt, bør gjennomgangsforfattere presentere flere tidspunkter bare for utfall som er kritiske for beslutningstaking, hvor enten resultatet eller beslutningen sannsynligvis vil variere over tid. Resten skal presenteres på et felles tidspunkt der det er mulig.
Oversiktsforfattere kan presentere kontinuerlige utfallsmål i ‘sammendrag av funn’ – tabellen og bør forsøke å gjøre disse tolkbare for målgruppen. Dette krever at enhetene er klare og lett tolkbare, for eksempel dager med smerte eller hyppighet av hodepine, og navnet og skalaen til eventuelle måleverktøy som brukes, skal oppgis (for Eksempel En Visuell Analog Skala, fra 0 til 100). Imidlertid er mange måleinstrumenter ikke lett tolkbare av ikke-spesialiserte klinikere eller pasienter, for eksempel poeng på En Beck Depresjon Inventar eller livskvalitet score. For disse kan en mer tolkbar presentasjon innebære å konvertere en kontinuerlig til et dikotomt utfall, for eksempel >50% forbedring (Se Kapittel 15, Avsnitt 15.5).
14.1.6.3 Beste estimat av risiko med komparatorintervensjon
Oversiktsforfattere bør gi opptil tre typiske risikoer for deltakere som mottar komparatorintervensjonen. For dikotomiske utfall anbefaler vi at disse presenteres i form av antall personer som opplever hendelsen per 100 eller 1000 personer (naturlig frekvens) avhengig av frekvensen av utfallet. For kontinuerlige utfall vil dette bli oppgitt som en gjennomsnitts-eller medianverdi av det målte utfallet.
Estimert eller antatt komparator intervensjonsrisiko kan være basert på vurderinger av typiske risikoer i ulike pasientgrupper avledet fra selve gjennomgangen, individuelle representative studier i gjennomgangen, eller risiko avledet fra en systematisk gjennomgang av prognosestudier eller andre beviskilder som igjen kan kreve en vurdering av sikkerheten for prognostisk bevis (Spencer et al 2012, iorio et al 2015). Ideelt sett vil risikoen gjenspeile grupper som klinikere enkelt kan identifisere på grunnlag av deres presentasjonsfunksjoner.
en forklarende fotnote bør angi kilden eller begrunnelsen for hver komparatorgrupperisiko, inkludert tidsperioden den tilsvarer der det er hensiktsmessig. I Figur 14.1.a, klinikere kan enkelt skille personer med risikofaktorer for dyp venøs trombose fra de uten. Hvis det er kjent at det er liten variasjon i baseline-risiko, kan oversiktsforfattere bruke median komparatorgrupperisiko på tvers av studier. Hvis typiske risikoer ikke er kjent, er et alternativ å velge risikoen fra de inkluderte studiene, som gir den nest høyeste for en høy og den nest laveste for en lavrisikopopulasjon.
14.1.6.4 Risiko med intervensjon
for dikotomiske utfall bør oversiktsforfattere gi en tilsvarende absolutt risiko for hver komparatorgrupperisiko, sammen med et konfidensintervall. Denne absolutte risikoen med (eksperimentell) intervensjon vil vanligvis være avledet fra metaanalyseresultatet presentert i kolonnen relativ effekt (Se Avsnitt 14.1.6.6). Formler er gitt I Avsnitt 14.1.5. Oversiktsforfattere bør presentere den absolutte effekten i samme format som risikoen med komparatorintervensjon (Se Avsnitt 14.1.6.3), for eksempel som antall personer som opplever hendelsen per 1000 personer.
for kontinuerlige resultater bør en forskjell i middel eller standardisert forskjell i middel presenteres med konfidensintervallet. Disse vil typisk bli hentet direkte fra en meta-analyse. Forklarende tekst bør brukes til å klargjøre betydningen, som I Figur 14.1.a og 14.1.b.
14.1.6.5 Risikodifferanse
for dikotomiske utfall kan risikodifferansen gis ved hjelp av et Av Tabellformatene ‘sammendrag av funn’ som et tilleggsalternativ (Se Figur 14.1.b). Denne risikoforskjellen uttrykker forskjellen mellom eksperimentell og komparator intervensjon og vil vanligvis være avledet fra meta-analyse resultatet presentert i den relative effekt kolonne (Se Avsnitt 14.1.6.6). Formler er gitt I Avsnitt 14.1.5. Oversiktsforfattere bør presentere risikodifferansen i samme format som antatt og tilsvarende risiko med komparatorintervensjon (Se Pkt. 14.1.6.3); for eksempel som antall personer som opplever hendelsen per 1000 personer eller som prosentpoeng dersom antatt og tilsvarende risiko uttrykkes i prosent.
hvis Tabellen ‘sammendrag av funn’ inneholder dette alternativet, kan gjennomsnittlig forskjell presenteres her og kolonnen ’tilsvarende risiko’ stå tom (Se Figur 14.1 .b).
14.1.6.6 Relativ effekt (95% KI)
den relative effekten vil typisk være et risikoratio eller oddsratio (eller av og til et hazard ratio) med tilhørende 95% konfidensintervall, hentet fra en meta-analyse utført på grunnlag av samme effektmål. Risikoforhold og oddsforhold er like når komparatorintervensjonsrisikoen er lav og effektene er små, men kan variere betydelig når komparatorgrupperisikoen øker. Meta-analysen kan innebære en antagelse om enten faste eller tilfeldige effekter, avhengig av hva oversiktsforfatterne anser som passende, og innebærer at den relative effekten enten er et estimat av effekten av tiltaket, eller et estimat av gjennomsnittlig effekt av tiltaket på tvers av studier.
14.1.6.7 antall deltakere (studier)
denne kolonnen skal inneholde antall deltakere vurdert i de inkluderte studiene for hvert utfall og tilsvarende antall studier som bidro til disse deltakerne.
14.1.6.8 Sikkerhet av dokumentasjonen (GRADE)
Forfatterne av Oversiktene bør kommentere sikkerheten av dokumentasjonen (også kjent som kvaliteten av dokumentasjonen eller tillit til effektestimatene). Gjennomgangsforfattere bør bruke det spesifikke bevisgraderingssystemet utviklet av GRADE Working Group (ATKINS Et al 2004, Guyatt et al 2008, Guyatt et al 2011a), som er beskrevet i detalj I Avsnitt 14.2. GRADE-tilnærmingen kategoriserer sikkerheten i et bevismateriale som ‘høy’, ‘moderat’, ‘lav’ eller ‘svært lav’ etter utfall. Dette er et resultat av dommen, men dommen prosessen opererer innenfor en gjennomsiktig struktur. For eksempel vil sikkerheten være ‘ høy ‘ hvis sammendraget var av flere randomiserte studier med lav risiko for skjevhet, men vurderingen av sikkerhet blir lavere hvis det er bekymringer om risiko for skjevhet, inkonsekvens, indirekthet, unøyaktighet eller publikasjonsskjevhet. Andre vurderinger enn ‘ høy ‘sikkerhet bør gjøres oversiktlige ved hjelp av forklarende fotnoter eller ‘Kommentarer’ – kolonnen i ‘sammendrag av funn’ – tabellen (Se Avsnitt 14.1.6.10).
14.1.6.9 Kommentarer
Målet Med Kommentarfeltet er å bidra til å tolke informasjonen eller dataene som er identifisert i raden. For eksempel kan dette være på gyldigheten av utfallsmålet eller tilstedeværelsen av variabler som er knyttet til effektens størrelse. Viktige advarsler om resultatene skal flagges her. Ikke alle rader trenger kommentarer, og det er best å legge igjen et tomt hvis det ikke er noe som garanterer en kommentar.
14.1.6.10 Forklaringer
Detaljerte forklaringer bør inkluderes som fotnoter for å underbygge bedømmelsene i ‘sammendrag av funn’ – tabellen, for eksempel DEN SAMLEDE KARAKTERVURDERINGEN. Forklaringene skal beskrive begrunnelsen for viktige aspekter av innholdet. Tabell 14.1.en viser veiledning for nyttige forklaringer. Forklaringer bør være konsise, informative, relevante, enkle å forstå og nøyaktige. Hvis forklaringer ikke kan beskrives tilstrekkelig i fotnoter, bør oversiktsforfattere gi ytterligere detaljer om problemene i Resultatene og Diskusjonsseksjonene i anmeldelsen.
Tabell 14.1.En Veiledning for å gi nyttige forklaringer i’ Sammendrag av funn ‘ (SoF) tabeller. Tilpasset Fra Santesso et al (2016)
Generell veiledning
- Legg inn informasjon for lesere direkte i tabellen hvis det er mulig(f. eks. informasjon om varigheten av oppfølgingen eller vekten som brukes).
- generelt skal du ikke sitere referanser i forklaringsdelen, med mindre det for eksempel er spesifikke grunner til å gi informasjon om kilder til grunnlinjerisiko (se punkt 3).
- Gi kilden til informasjon om baseline risiko som brukes til å beregne absolutte effekter.
- når tabellen er fullført, går du gjennom alle forklaringer for å avgjøre om noen kan refereres flere ganger hvis de omformuleres eller kombineres.
- Oppgi grunner for å oppgradere og nedgradere dokumentasjonen (se domenespesifikk veiledning nedenfor) og bruk GRADEpro gdt-programvare for å følge vurderingsveiledningen.
- beviset for et bestemt utfall kan være fast bestemt på å ha alvorlige eller svært alvorlige problemer for det berørte domenet (eller kritisk alvorlig for risiko for skjevhet når ROBINS-I brukes). Det kan derfor være nyttig å angi antall nivåer for nedgradering (f.eks. nedgradert med ett nivå for risiko for skjevhet), men unngå gjentakelse av hva som er i tabellen (og inntrykk av formalistisk eller algoritmisk rapportering). I bevisprofiler er denne informasjonen allerede i tabellens celler.
- selv om forklaringer om sikkerheten i bevisene først og fremst kreves når de endrer sikkerheten, bør du vurdere å legge til en forklaring når sikkerheten i bevisene ikke er endret, men når denne avgjørelsen kan bli stilt spørsmål ved av andre. Dette vil bidra til å forstå årsakene til uenighet.
- Kontroller at tabellen ikke brukes som en beskrivelse av metodene for gjennomgangen(for eksempel ikke beskriv årsakene til den statistiske analysen).
- Skriv inn resultater for utfall som ikke kunne kombineres statistisk i en meta-analyse (dvs. narrative utfall) direkte inn I SoF-tabellen i resultatkolonnene. En forklaring er kanskje ikke nødvendig for å kommunisere disse resultatene. Hvis det anses å være gunstig for den tiltenkte målgruppen, legg til komplementære estimater av intervensjonseffekter (f. eks. antall som trengs for å behandle for nytte og skade, risikodifferanse uttrykt som prosentandel, kontinuerlig utfall uttrykt i minimale viktige differanseenheter) i Kommentarkolonnen.
- Bruk informasjonen som presenteres i forklaringene om VURDERINGSPROSESSEN til å informere andre sentrale deler av gjennomgangen, inkludert sammendragsversjoner og diskusjonen.
Domenespesifikk veiledning for å skrive nyttige forklaringer
risiko for skjevhet
- Beskrive antall studier, eller mengden informasjon de gir i meta-analysen, som hadde høy risiko for skjevhet og for hvilket kriterium.
- Bruker begreper som flertall, minoritet, alle, noen eller ingen; eller antall studier Som X/X studier.
- for randomiserte studier nevner du de spesifikke kriteriene, inkludert tildelingssekvensskjuling, selektiv utfallsrapportering, etc. For ikke-randomiserte studier, beskriv kriteriet i verktøyet som brukes (for eksempel VED HJELP AV ROBINS-i-verktøyet).
- Indikerer om effekten av risiko for skjevheter ble undersøkt i en sensitivitetsanalyse. Når det er hensiktsmessig, nevne bidraget fra studiene med høy risiko for skjevhet til estimatene.
- Informasjon om studiedesign kan være inkludert i forklaringene, spesielt I SoF når ulike studiedesign er inkludert.
Inkonsekvens
- Angir tiltaket som brukes til å bedømme inkonsekvens, for eksempel statistisk test eller mål (I2, Chi2, Tau), eller overlapping av konfidensintervaller eller likhet med punktestimater.
- hvis inkonsekvens er basert På I2, beskriv det som betydelig, betydelig, moderat eller ikke viktig.
- hvis aktuelt, nevn om heterogenitet ble undersøkt I undergruppeanalyser av PICO (pasienter, intervensjon, sammenligning, utfall), og om det er andre mulige årsaker til heterogeniteten.
- i tilfelle av en enkelt studie for et utfall, si at det er ‘ingen’ heller enn ‘ikke aktuelt’.
Upresision
- Angir hvor utvalgsstørrelsen eller antall hendelser ikke oppfyller den optimale informasjonsstørrelsen som beregnet, eller tommelfingerreglene (f. eks. 400 hendelser). Unngå henvisning til antall studier som grunn til unøyaktighet.
- Indikerer om konfidensintervallene inkluderer mulighet for liten eller ingen effekt OG viktig nytte eller skade. Hvis kjent, gi den numeriske verdien av terskelen til viktig fordel.
- Unngå å rapportere resultatet som statistisk eller ikke-statistisk signifikant.
Oppgradering
- Nevn grunnen til oppgradering: på grunn av stor effekt; en dose-respons gradient; eller plausibel gjenværende motstridende confounding øker sikkerheten av bevis.
- for store effekter rapporterer du om den relative effekten er > 2 eller > 5. For doseresponsgradienter, angi graden av intervensjon og effekt på utfallet. For domenet ‘plausibel residual motstridende confounding’, beskrive effekten av confounding faktor på estimatet.
14.2 Vurdering av sikkerheten eller kvaliteten på et bevislegeme
14.2.1 GRADE-tilnærmingen
Grader Av Anbefalings -, Vurderings -, Utviklings-og Evalueringsarbeidsgruppe (GRADE Working Group) har utviklet et system for gradering av sikkerheten til bevis (Sch@nemann et al 2003, Atkins et al 2004, Schü et al 2006, Guyatt et al 2008, Guyatt et al 2011a). Over 100 organisasjoner, Inkludert Verdens Helseorganisasjon (WHO), American College Of Physicians, American Society Of Hematology (ASH), Det Kanadiske Byrået For Narkotika og Teknologi I Helse (CADTH) og National Institutes Of Health And Clinical Excellence (NICE) i STORBRITANNIA har vedtatt GRADE-systemet (www.gradeworkinggroup.org).
Cochrane har også formelt tatt i bruk denne tilnærmingen, og Alle Cochrane-Oversikter bør bruke GRADE for å vurdere sikkerheten i dokumentasjonen for viktige utfall (se MECIR Boks 14.2.en).
MECIR Boks 14.2.Relevante forventninger til gjennomføring av intervensjonsgjennomganger
|
C74 Vurdering av sikkerheten i bevismaterialet (Obligatorisk)) |
|
|
Bruk de fem VURDERINGSHENSYNENE (risiko for skjevhet, konsekvensvirkninger, unøyaktighet, indirekthet og publikasjonsskjevhet) til å vurdere sikkerheten i bevismaterialet for hvert utfall, og til å trekke konklusjoner om sikkerheten i bevismaterialet i oversiktsteksten. |
GRADE ER den mest brukte tilnærmingen for å oppsummere tillit til effekter av tiltak etter utfall på tvers av studier. Det er å foretrekke å bruke Online GRADEpro-verktøyet, og å bruke det som beskrevet i hjelpesystemet til programvaren. Dette bør bidra til å sikre at forfatterlagene får tilgang til samme informasjon for å informere sine vurderinger. Ideelt sett bør to personer som arbeider selvstendig, vurdere sikkerheten til bevismaterialet og nå en konsensus om eventuelle nedgraderingsbeslutninger. De fem VURDERINGSHENSYNENE bør tas opp uavhengig av om gjennomgangen inneholder En ‘sammendrag av funn’ – tabell. Det er nyttig å trekke på denne informasjonen i Diskusjonen, I Forfatterens konklusjoner og å formidle sikkerheten i bevisene I Abstrakt og Vanlig språk sammendrag. |
|
C75 Begrunne vurderinger av bevislegemets sikkerhet (Obligatorisk)) |
|
|
Begrunne og dokumentere alle vurderinger av sikkerheten til bevismaterialet(f. eks. nedgradering eller oppgradering VED BRUK AV GRADE). |
vedtakelsen av en strukturert tilnærming sikrer åpenhet i å formulere en tolkning av bevisene, og resultatet er mer informativ for brukeren. |
FOR systematiske oversikter definerer GRADE-tilnærmingen sikkerheten til et bevismateriale som i hvilken grad man kan være sikker på at et estimat av effekt eller tilknytning er nær mengden av spesiell interesse. Vurdering av sikkerhet i et dokument innebærer vurdering av risiko for skjevhet innenfor og på tvers av studier (begrensninger i studiedesign og utførelse eller metodisk kvalitet), inkonsekvens (eller heterogenitet), indirekthet av bevis, unøyaktighet av effektestimater og risiko for publikasjonsskjevhet (Se Avsnitt 14.2.2), samt domener som kan øke vår tillit til effektestimatet (som beskrevet I Avsnitt 14.2.3). GRADE-systemet innebærer en vurdering av sikkerheten til et dokument for hvert enkelt utfall. Vurderinger om domenene som bestemmer bevissikkerheten, bør beskrives i resultat-eller diskusjonsseksjonen og som en del av Oppsummeringstabellen.
KARAKTERTILNÆRMINGEN angir fire sikkerhetsnivåer (Figur 14.2.en). For intervensjoner, inkludert diagnostiske og andre tester som vurderes som intervensjoner (Sch@nemann et al 2008b, Schü Et al 2008a, Balshem et al 2011, Schü et al 2012), er utgangspunktet for vurdering av bevissikkerhet kategorisert i to typer:
- randomiserte forsøk; og
- ikke-randomiserte studier av tiltak (NRSI), inkludert observasjonsstudier (inkludert, men ikke begrenset til, kohortstudier og kasus-kontrollstudier, tverrsnittsstudier, kasuserier og kasusrapporter, selv om ikke alle disse designene vanligvis er inkludert i Cochrane-Oversikter).
det er mange tilfeller der oversiktsforfattere stoler på informasjon FRA NRSI, spesielt for å vurdere potensielle skader (Se Kapittel 24). I tillegg kan oversiktsforfattere hente relevante data fra både randomiserte studier og NRSI, med hver type bevis som supplerer den andre (Sch@nemann et al 2013).
I GRADE begynner en mengde bevis fra randomiserte studier med høy grad av sikkerhet, mens EN mengde bevis fra NRSI begynner med lav grad av sikkerhet. Den lavere karakteren MED NRSI er resultatet av den potensielle bias indusert av mangel på randomisering(dvs. confounding og selection bias).
men ved bruk av DET nye Verktøyet Risk Of Bias I IKKE-randomiserte Studier av Tiltak (ROBINS-I) (Sterne et al 2016), et vurderingsverktøy som dekker risikoen for skjevhet på grunn av manglende randomisering, kan alle studier starte som høy sikkerhet for dokumentasjonen (Schü et al 2018). Tilnærmingen til å starte alle studiedesign (INKLUDERT NRSI) som høy sikkerhet er ikke i konflikt med den første KARAKTEREN tilnærming til å starte vurdering AV NRSI som lav sikkerhet bevis. Dette skyldes at en mengde bevis fra NRSI generelt bør nedgraderes av to nivåer på grunn av den iboende risikoen for skjevhet forbundet med mangel på randomisering, nemlig confounding og seleksjonsbias. Ikke nedgradering AV NRSI fra høy til lav sikkerhet trenger gjennomsiktig og detaljert begrunnelse for hva som reduserer bekymringer om confounding og selection bias (Sch@nemann et al 2018). Svært få eksempler på hvor ikke vurdering ned med to nivåer er hensiktsmessig for tiden eksisterer.
den høyeste sikkerhetsklassifiseringen er et bevismateriale når DET ikke er noen bekymringer i NOEN AV KARAKTERFAKTORENE oppført I Figur 14.2.Forfatterne nedgraderer ofte bevis til moderat, lav eller til og med svært lav sikkerhetsbevis, avhengig av tilstedeværelsen av de fem faktorene I Figur 14.2.a. vanligvis vil sikkerhetsvurdering falle med ett nivå for hver faktor, opp til maksimalt tre nivåer for alle faktorer. Hvis det er svært alvorlige problemer for ett domene (f. eks. ved vurdering av risiko for skjevheter, var alle studier utilslørt, avblindet og mistet over 50% av pasientene til oppfølging), bevis kan falle med to nivåer på grunn av denne faktoren alene. Det er ikke mulig å rangere lavere enn’ svært lav sikkerhet ‘ bevis.
Gjennomgangsforfattere vil generelt gradere bevis fra lyd ikke-randomiserte studier som lav sikkerhet, selv OM ROBINS-I brukes. Hvis slike studier imidlertid gir store effekter og det ikke er noen åpenbar skjevhet som forklarer disse effektene, kan oversiktsforfattere vurdere dokumentasjonen som moderat eller – hvis effekten er stor nok – til og med så høy sikkerhet (Figur 14.2.en). Det svært lave sikkerhetsnivået passer for, men er ikke begrenset til, studier med kritiske problemer og usystematiske kliniske observasjoner(f. eks. kasuserier eller kasusrapporter).