Comme vous le savez, une planification préopératoire minutieuse est essentielle pour réussir une chirurgie de la cataracte. Qu’il s’agisse de nous renseigner sur l’utilisation d’anticoagulants, d’évaluer la capacité d’un patient à se coucher à plat ou d’identifier des modifications anatomiques telles que des zonules faibles ou une chambre antérieure peu profonde, notre succès repose en grande partie sur la recherche de sources de complications potentielles avant la chirurgie et sur l’ajustement de notre approche au besoin.
Une difficulté majeure est la présence d’une pathologie cornéenne qui provoque une opacification et empêche une vision claire à travers la cornée jusqu’au cristallin, augmentant la probabilité de calculs d’IOL inexacts. Les causes courantes de ce type de pathologie cornéenne comprennent une cicatrice centrale, une maladie grave de la surface cornéenne, une carence en cellules souches limbales et un dysfonctionnement des cellules endothéliales. Dans cet article, nous aborderons chacune de ces sources de cornées « nuageuses » et vous fournirons des conseils pour vous aider à relever les défis qu’elles présentent en toute confiance.
Optimisation de la surface oculaire
Avant d’effectuer des calculs de LIO pour un patient présentant une cornée trouble, vous devez traiter une maladie de la surface oculaire de manière adéquate. Cette étape permet d’assurer des lectures biométriques et topographiques précises, qui peuvent changer de manière significative avant et après le traitement. De plus, le traitement de la maladie de la surface oculaire améliore non seulement la visualisation pendant la chirurgie, mais diminue également les risques que la maladie récalcitrante peut poser après la chirurgie. Plus important encore, le contrôle de l’OSD conduira à un meilleur résultat de réfraction globale et à une plus grande satisfaction des patients.
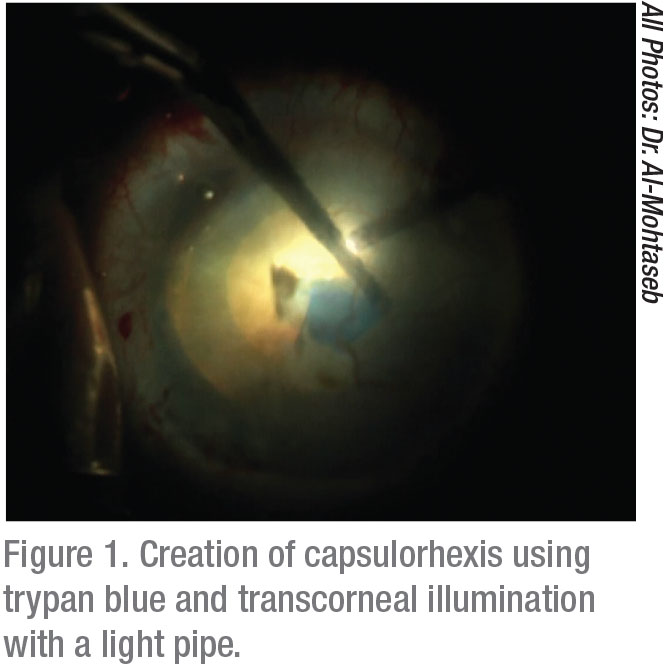
La kératométrie est essentielle pour cartographier une bonne approche de ces patients. Regarder les anneaux de placido aide à diagnostiquer des cas subtils de maladie de la membrane basale épithéliale, par exemple. Si nécessaire, effectuer un débridement épithélial ou une kératectomie photothérapeutique au laser excimère au moins trois mois avant d’obtenir les calculs finaux de la LIO pour ces patients.1 Le fait de ne pas identifier la présence d’EBMD entraînera une sélection inexacte de la LIO et des patients insatisfaits avec de mauvais résultats visuels.
Des affections moins fréquentes mais plus graves pouvant entraîner une mauvaise visualisation comprennent le syndrome de Stevens-Johnson 2 et la maladie du greffon contre l’hôte. Les mesures préventives et stabilisantes préopératoires sont les clés pour obtenir des résultats visuels satisfaisants dans ces cas. Dans le SJS et le greffon contre l’hôte, l’inflammation entraîne des changements, prédisposant les patients à une sécheresse sévère, à un compromis conjonctival, à une production de larmes déficiente et à une maladie de la marge des paupières. Parce que la manipulation chirurgicale peut exacerber le processus de la maladie, vous devez contrôler agressivement toute maladie de surface ou inflammation existante.
Traitements à considérer
Envisager un large arsenal lors de la préparation de la surface oculaire pour la chirurgie. Vous pouvez essayer l’utilisation fréquente de larmes artificielles sans conservateur, de corticostéroïdes topiques, de cyclosporine topique à 0,05% (Restasis, Allergan) ou de lifitegrast à 0,5% (Xiidra, Shire) et / ou de larmes sériques.
Ces traitements peuvent cependant ne pas suffire, et l’utilisation d’une greffe de membrane amniotique, de lentilles de contact à bandage, d’une tarsorgraphie ou de la lentille PROSE (remplacement prothétique de l’écosystème de la surface oculaire) (BostonSight) peut être utile dans les cas graves, avant et après la chirurgie.
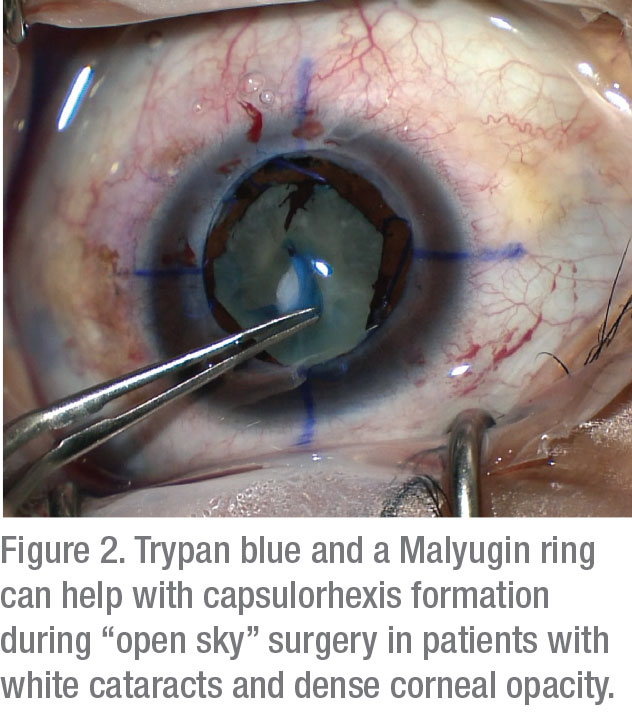
Les patients ayant des antécédents d’infection oculaire par l’herpès simplex ou le zona doivent être soigneusement informés des risques accrus de réactivation de la maladie.3
En général, les patients ne doivent pas présenter de signes d’infection active pendant au moins trois mois avant la chirurgie.4 Il n’existe pas de lignes directrices claires pour la prophylaxie antivirale. Cependant, pour les patients qui ne reçoivent pas déjà de traitement, envisagez de commencer à les administrer à titre prophylactique (selon le type d’infection antérieure) pendant au moins une semaine avant la chirurgie. Continuez ce traitement jusqu’à six mois après la chirurgie, jusqu’à l’arrêt des stéroïdes topiques.
En plus d’utiliser ces stratégies, vous devrez peut-être tenter une transplantation de cellules souches limbales pour optimiser la surface et la vue à travers la cornée avant la chirurgie en cas de déficit en cellules souches limbales et de conjonctivalisation cornéenne sévère.
Planification préopératoire
Une fois que le contrôle des pathologies préexistantes est optimisé au maximum, la visualisation à travers une cornée trouble devrait s’améliorer et peut être maximisée avec des stratégies chirurgicales spécifiques.
Comme pour toutes les chirurgies de la cataracte, une sélection correcte des lentilles est la clé pour obtenir un bon résultat. Cependant, les opacités cornéennes qui persistent même après l’optimisation de la surface peuvent empêcher des lectures biométriques précises, bien que cela soit vrai dans une moindre mesure avec les systèmes de biométrie optique plus récents. Si vous craignez que les résultats de biométrie ne soient pas exacts, vous pouvez utiliser des lectures K moyennes (~ 45) ou une kératométrie de l’œil comme alternative raisonnable.
Vous devriez fortement envisager d’utiliser une LIO en trois parties; de telles lentilles offrent plusieurs options en cas de compromis capsulaire antérieur ou postérieur, y compris la mise en place de la LIO dans le sulcus, avec ou sans capture optique et fixation sclérale.
Chirurgicalement Parlant
En salle d’opération, deux tactiques ont été montrées pour améliorer la visualisation: la coloration capsulaire et les ajustements d’éclairage. Une étude a rapporté que l’utilisation de 0,06% de bleu de trypan améliore considérablement le BCVA chez les patients présentant des opacités cornéennes.5 Bien que l’instillation de cette tache puisse rendre la capsule cassante, le bénéfice d’une meilleure visualisation l’emporte largement sur les risques insignifiants de cet effet secondaire.
Les réglages d’éclairage qui peuvent améliorer la visualisation incluent l’utilisation de réglages faibles à moyens pour réduire la rétrodiffusion. En cas d’opacification cornéenne importante, l’illumination oblique transcornienne est idéale.6 L’utilisation de cette nouvelle stratégie peut grandement améliorer la vue de la chambre antérieure. Depuis qu’elle a été décrite pour la première fois,7 il a été démontré que cette méthode augmente le succès dans un large éventail de chirurgies du segment antérieur. La technique nécessite l’utilisation d’une source de lumière de faible calibre, généralement le tuyau de lumière utilisé à partir d’une machine de vitrectomie. L’éclairage du lustre est placé dans la paracentèse; lorsqu’il est utilisé lors de la coloration capsulaire, il vous permet de créer confortablement un capsulorhexis et d’effectuer une phacoémulsification.
Pour diminuer le risque de déchirure capsulaire antérieure ou de radialisation lors de la construction du rhexis dans l’œil de votre patient, envisagez des étapes pouvant réduire la pression postérieure:
• une vitrectomie antérieure.8
De plus, démarrez le rhexis avec une visualisation optimale loin de l’opacité pour assurer une initiation et un contrôle idéaux avant de vous diriger vers des zones moins visibles.
Défis endothéliaux
En cas de dysfonctionnement endothélial, le plus souvent observé dans la dystrophie de Fuchs concomitante à une cataracte visuellement significative, nous recommandons d’effectuer des procédures combinées impliquant une phacoémulsification et une kératoplastie endothéliale décapante de Descemet (DSEK)9 ou une kératoplastie endothéliale membranaire de Descemet (DMEK).10
Les approches combinées sont plus rentables, accélèrent la récupération visuelle et évitent la nécessité de chirurgies multiples. Une grande étude n’a trouvé aucune différence dans les taux de complication, la perte de cellules endothéliales, le succès de la greffe ou l’amélioration visuelle associée à l’une ou l’autre de ces approches, par rapport à la chirurgie séquentielle (DMEK suivie d’une chirurgie de la cataracte).11 Une chirurgie séquentielle peut également être envisagée chez les patients présentant un astigmatisme important, tant que la cornée est stable avant les mesures de LIO et l’implantation de LIO torique.
Cependant, si vous avez un patient qui a certainement besoin d’une greffe de cornée, mais que vous envisagez de bénéficier ou non d’une procédure de cataracte en même temps, gardez à l’esprit que les procédures de greffe endothéliale seules peuvent augmenter le risque de formation de cataracte, en particulier chez les patients de plus de 50 ans qui ont des chambres antérieures peu profondes.12
Par conséquent, une procédure de greffe seule doit être envisagée plus fortement chez les patients présentant un risque plus faible de formation de cataracte (patients plus jeunes et patients présentant un SCa profond). Chez les patients plus âgés ou ceux avec un SCa peu profond, une procédure combinée pourrait être un meilleur choix car la formation plus précoce de la cataracte est plus à risque chez ces personnes.
Conseils de chirurgie combinée
Si vous combinez la chirurgie DSEK / DMEK et la chirurgie de la cataracte chez ces patients, utilisez des viscoélastiques cohésifs pour minimiser les interférences avec le greffon, en gardant à l’esprit que les dispersifs sont plus difficiles à éliminer complètement. Évitez les dommages optiques de la LIO au greffon en construisant un capsulorhexis légèrement plus petit et en utilisant des myotiques intracaméraux, minimisant le déplacement antérieur de la LIO. Enfin, notez que des décalages hypermétropes ont été notés après DSEK et DMEK.13 Une cible de réfraction plus myope (-0,5 D à – 1D pour le DMEK et -0,75 D à -1,5 D pour le DSEK) peut faciliter l’emmétropie, si désiré.
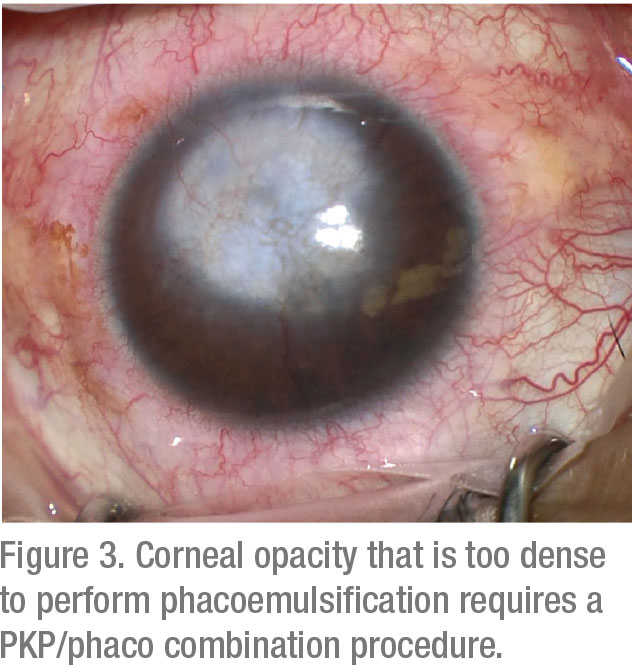
Pour les patients atteints de cicatrices cornéennes sévères et d’opacification, la combinaison d’une kératoplastie pénétrante et d’une extraction de la cataracte offre les avantages attendus de prévenir la nécessité d’une deuxième intervention chirurgicale et de réduire le risque de perte de cellules endothéliales.
Cependant, comprenez que les résultats de réfraction postopératoires sont imprévisibles et peuvent être significativement décevants après avoir utilisé cette approche. Une étude a démontré seulement un taux d’emmétropie de 62% dans les 2 jours. La combinaison PKP et phacoémulsification de 14
peut être envisagée chez les patients prêts à porter des lentilles de contact, désirant une récupération visuelle rapide et souhaitant éviter de multiples chirurgies. Sinon, une chirurgie séquentielle après l’atteinte de la stabilité réfractive (nécessitant généralement au moins un an) est préférée.
Si l’opacification stromale est plus antérieure, gardez à l’esprit qu’il a été démontré que la kératoplastie lamellaire antérieure profonde produisait des résultats de réfraction plus prévisibles et une récupération visuelle plus rapide si elle était associée à une chirurgie de la cataracte, par rapport à une PKP combinée.15 Pour les patients présentant des cicatrices cornéennes centrales sévères — en particulier dans le SJS et le greffon par rapport à l’hôte — envisager une extraction de la cataracte extracapsulaire. Si vous poursuivez une phacoémulsification, des paramètres d’aspiration faibles sont recommandés. La suture des plaies chez ces patients est également importante.
Pas de solution miracle
Comme vous pouvez le constater, la chirurgie de la cataracte par une cornée « trouble » présente de nombreux défis qui nécessitent une planification préopératoire minutieuse et des stratégies peropératoires pour obtenir un résultat visuel satisfaisant.
Bien qu’aucune approche unique ne puisse garantir le succès, en utilisant les conseils de cet article, en particulier dans les combinaisons appropriées, vous pouvez minimiser de nombreux résultats évitables et décevants. AVIS
Dr. Al-Mohtaseb est professeur agrégé d’ophtalmologie et directeur du programme de résidence associé, Chirurgie réfractive de la cornée, de la Cataracte &, au Baylor College of Medicine de Houston.
Le Dr Naguib est résident en ophtalmologie de 2e année au Baylor College of Medicine.
Ni le Dr Al-Mohtaseb ni le Dr Naguid ne font état d’un intérêt financier pertinent pour les produits mentionnés.
1. Jeng BH, Dupps WJ, Meisler DM, Schoenfield L. Débridement Épithélial pour le Traitement des Anomalies de la Membrane Basale Épithéliale Coïncidant Avec des Troubles Endothéliaux. Cornea 2008; 27:10:1207-1211.
2. Narang P, Mohamed A, Mittal V, Sangwan VS. Chirurgie de la cataracte dans le syndrome chronique de Stevens-Johnson: Aspects et résultats. Br J Ophthalmol 2016; 100: 11: 1542-1546.
3. Il Y, de Melo Franco R, Kron-Gray MM, et al. Résultats de la chirurgie de la cataracte dans les yeux avec un herpès zoster ophtalmique antérieur. J Réfraction de la cataracte Surg 2015; 41: 4: 771-777.
4. Sykakis E, Karim R, Parmar DN. Prise en charge des patients atteints d’une maladie oculaire à virus de l’herpès simplex ayant subi une chirurgie de la cataracte au Royaume-Uni. J Cataracte Réfract Surg 2013;39:8:1254-1259
5. Panda A, Krishna SN, Dada T. Résultat de la phacoémulsification des yeux avec cataracte et opacité cornéenne obscurcissant partiellement la zone pupillaire. Népal J Ophthalmol 2012; 4:2:217-223.
6. Yokokura S, Hariya T, Uematsu M, et al. Efficacité de l’éclairage du lustre pour l’opération combinée de la cataracte et la kératoplastie pénétrante. Cornée 2015; 34:3:275-278.
7. Oshima Y, Shima C, Maeda N, Tano Y. Oscillation de torsion assistée par rétroillumination de lustre pour la chirurgie de la cataracte chez les patients présentant une opacité cornéenne sévère. J Réfraction de la cataracte Surg 2007; 33: 12:2018-2022.
8. Shimomura Y, Hosotani H, Kiritoshi A, Watanabe H, Tano Y. Vitrectomie du noyau précédant la procédure de triple cornée chez les patients à haut risque d’augmentation de la pression de la chambre postérieure. Jpn J Ophthalmol 41:4:251-254
10. Prix FW, Prix MO. Cataracte combinée / DSEK / DMEK: attentes changeantes. Asie-Pacifique J Ophthalmol (Phila). 2017;6:4:388-392.
11. Chaurasia S, Price FW Jr, Gunderson L, et al. Kératoplastie endothéliale membranaire de Descemet: Résultats cliniques de procédures simples ou triples (combinées à une chirurgie de la cataracte). Ophtalmologie. 2014;121:454-458.
12. Prix MO, Prix DA, Fairchild KM, et al. Taux et facteurs de risque de formation et d’extraction de la cataracte après une kératoplastie endothéliale par décapage de Descemet. Br J Ophthalmol. 2010;94:1468-1471
13. Schoenberg ED, Prix FW, Miller J, McKee Y, Prix MO. Résultats réfractifs des procédures triples de kératoplastie endothéliale membranaire de Descemet (combinées à une chirurgie de la cataracte). J Chirurgie réfractaire de la Cataracte.2015; 41:6:1182-1189.
14. Crawford GJ, chemin Stulting, Waring GO, Van Meter WS, Wilson LA. La procédure triple. Analyse des résultats, de la réfraction et du calcul de la puissance de la lentille intraoculaire. Ophtalmologie 1986; 93:6:817-824.
15. Den S, Shimmura S, Shimazaki J. Chirurgie de la cataracte après kératoplastie lamellaire antérieure profonde et kératoplastie pénétrante dans les yeux assortis à l’âge et à la maladie. J Réfraction de la cataracte Surg 2018; 44: 4: 496-503.