alle vævsceller afhænger af aerob metabolisme til generering af den energi (i form af adenosintriphosphat, ATP), der kræves for overlevelse og funktion. Denne fundamentalt vitale mitokondrie-proces er kendetegnet ved forbrug af ilt og produktion af kulsyre, som kan variere fra omkring 200 mL/minut i hviletilstand til over fem gange denne hastighed under træning.
den ultimative skæbne for denne kulsyre er eliminering fra kroppen i udløbet luft, og en vigtig funktion af blod er transporten af kulsyre fra vævsceller til lunger.
en forståelse af denne transportproces afhænger af en forståelse af, hvad der menes med partialtryk af en gas samt nogle grundlæggende fysiske love, der styrer opløseligheden og bevægelsen (diffusion) af gasser.
- HVAD ER PARTIALTRYK AF EN GAS?
- opløselighed og DIFFUSION af gasser
- TRANSPORT af kulsyre fra vævsceller til lunge
- kulsyre og blod PH
- i laboratoriet-DEFINITION af CO2-parametre
- partialtryk af kulsyre pCO2
- BICARBONATKONCENTRATION (HCO3 -)
- Total KULSTOFKONCENTRATION i PLASMA (ctCO2)
- kemiske metoder til måling af ctCO2
- uoverensstemmelse mellem målt ctCO2 og beregnet bicarbonat
- resume
HVAD ER PARTIALTRYK AF EN GAS?
mængden af gas i et system, herunder biologiske systemer, defineres af det tryk, det udøver, traditionelt målt som højden af en kolonne af kviksølv (mmHg). Ved at sige, at atmosfæretrykket er 760 mmHg, mener vi således, at gasserne (ilt, nitrogen og kulsyre) i den luft, vi indånder, har et kombineret tryk, der er tilstrækkeligt til at understøtte en standardkolonne af kviksølv 760 mm høj.
dette samlede tryk er simpelthen summen af partialtrykket for hver bestanddel gas. Da luften således omfatter ca. 20% ilt, 79% nitrogen og 0.03% kulsyre, partialtrykket af ilt (pO2) i inspireret luft er ca. (20 gange 760) / 100 = 152 mmHg og partialtrykket af kulsyre (pCO2) er (0,03 gange 760) / 100 = 0,2 mmHg.
systeme internationale (SI) trykenhed, der anvendes i kliniske laboratorier uden for Nordamerika, er kilopascal (kPa). Konverteringsfaktoren 0.133 kan bruges til at konvertere mmHg til kPa.
opløselighed og DIFFUSION af gasser
Henrys lov siger, at ved ligevægt er mængden af gas opløst i en væske proportional med partialtrykket af denne gas, så længe temperaturen er konstant:
opløst gas = partialtryk (p) * opløselighedskoefficient (r)
hvor S er en temperaturafhængig konstant for den pågældende gas. Opløselighedskoefficienten (er) for kulsyre ved kropstemperatur er 0,23 mmol/L/kPa (eller 0,03 mmol/mmHg) . Således da arteriel pCO2 er cirka 5.3 kPa (40 mmHg), mængden af CO2 opløst i arterielt blod (dCO2) er (5,3 * 0,23) eller 40 * 0,03) = 1,2 mmol/L.
bevægelsen (diffusion) af gasser bestemmes i vid udstrækning af koncentrationsgradienter. Gas diffunderer fra højt partialtryk til lavt partialtryk .
TRANSPORT af kulsyre fra vævsceller til lunge
kulsyre-rejsen (figur 1a) begynder i mitokondrionen af vævsceller, hvor den produceres. På grund af den fremherskende koncentrationsgradient diffunderer kulsyre fra mitokondrier (hvor pCO2 er højest) over cytoplasmaet, ud af cellen og ind i kapillærnetværket.
figur 1A: CO2 i væv
Klik for at forstørre
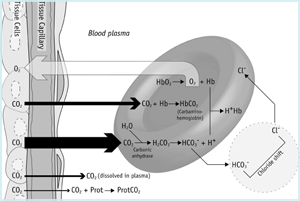
lidt af den CO2, der ankommer i blod fra vævsceller, forbliver fysisk opløst i blodplasma (se ovenfor), og en endnu mindre andel binder til NH2 (amino) terminale grupper af plasmaproteiner, der danner såkaldte carbaminoforbindelser. De fleste diffunderer dog en koncentrationsgradient ned i røde celler.
lidt af dette forbliver opløst i cytoplasmaet i den røde celle, og nogle er løst bundet til amino terminale grupper af reduceret hæmoglobin, der danner carbamino-Hb. Men det meste af kulsyre, der ankommer i røde blodlegemer, hydreres hurtigt til kulsyre ved hjælp af den røde celleisoform af kulsyreanhydrasen. Ved fysiologisk pH dissocieres næsten alle (96 %) af denne kulsyre til bicarbonat og hydrogenioner:
ligning 1:
![]()
hydrogenionerne bufres af reduceret hæmoglobin, og de fleste bicarbonationer passerer fra den røde celle til plasma i bytte for chloridioner (dette såkaldte ‘chloridskift’ opretholder elektrokemisk neutralitet). Det fremgår klart af ovenstående, at størstedelen af kulsyre transporteres som bicarbonat (overvejende i blodplasma), men der er i alt fire former for CO2-transport :
- 90 % transporteres som bicarbonat i plasma (65 %) og røde blodlegemer (25 %)
- 5 % transporteres fysisk opløst i plasma og røde blodlegemer cytoplasma
- 5% transporteres løst bundet til hæmoglobin i røde blodlegemer og
det samlede kulstofindhold i blodet er summen af disse fire komponenter.
inden for lungernes mikrovaskulatur (figur 1b) bestemmer partialtrykgradienten over den alveolære membran, at opløst CO2 passerer fra blod til alveoler. Dette tab af kulsyre fra blod favoriserer reversering af de røde blodlegemer, der er beskrevet ovenfor.
således passerer bicarbonat fra plasma til røde blodlegemer, der bufferer hydrogenioner frigivet fra hæmoglobin, da det er iltet. Reversering af carbonanhydrase-reaktionen resulterer i produktion af CO2, der diffunderer fra røde celler til plasma og fremefter til alveoler.
blandet venøst blod, der ankommer til lungerne, har et samlet CO2-indhold på cirka 23, 5 mmol/L (eller 52 mL/dL), mens arterielt blod, der forlader lungerne, har et samlet CO2-indhold på 21, 5 mmol/L (48 mL/dL).
denne arterio-venøse Forskel (2 mmol/L eller 4 mL/dL) repræsenterer mængden af CO2 tilsat til blod fra vævsceller og tabt fra blod, når det passerer gennem lungemikrovaskulaturen, der til sidst udskilles fra kroppen i udløbet luft.
figur 1B: CO2 i lungerne
Klik for at forstørre
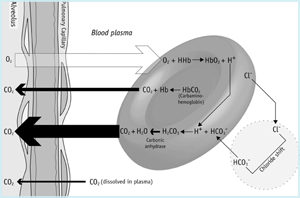
kulsyre og blod PH
CO2 ‘ s sure potentiale på grund af dets hydratiseringsreaktion over for kulsyre (se ligning 1 ovenfor) sikrer, at dets koncentration i blod er en vigtig determinant for blodets pH. Når CO2-koncentrationen stiger, gør også hydrogenion (H+) koncentration. Regulering af blod CO2, der matcher hastigheden af CO2-eliminering i udløbet luft til produktionshastigheden i mitokondrionen af vævsceller, der er afgørende for at opretholde normal blod-pH, er åndedrætssystemets forretning.
respirationsfrekvens (kontrolleret af pCO2-følsomme kemoreceptorer placeret i hjernestammen og halspulsåren) øges, hvis pCO2 stiger og falder, hvis pCO2 falder. Øget respirationsfrekvens (åndedræt/min) resulterer i øget CO2-elimination og nedsat respirationsfrekvens fremmer CO2-retention.
forholdet mellem pH og kulsyre er beskrevet ved en form for Henderson-Hasselbach ligningen (ligning 2). Dette er afledt af anvendelse af loven om masseaktion på hydratiserings-og dissociationsreaktionerne beskrevet i ligning 1 .
ligning 2:
![]()
hvor
| pK/1 | = | ’tilsyneladende’ dissociationskonstant af kulsyre = 6.1 |
| = | koncentration af plasmabicarbonat (mmol / L) | |
| S | = | opløselighedskoefficient for CO2 ved 37 oC (0,23, hvis pCO2 måles i kPa eller 0,03, hvis pCO2 måles i mmHg) |
| pCO2 | = | partialtryk af pCO2 (kPa eller mmHg) |
som tidligere forklaret er nævneren i denne ligning (s pCO2) mængden af opløst kulsyre (dCO2) mmol / L.
ved at fjerne alle konstanter kan ligning 2 forenkles til:
ligning 3:
pH-liter / pCO2
således er blodets pH afhængig af forholdet mellem plasmabicarbonatkoncentration (den metaboliske komponent) og pCO2 (den respiratoriske komponent). Således hvis pCO2 stiger uden en tilsvarende stigning i bicarbonat, falder pH. Omvendt, hvis pCO2 falder uden et tilsvarende fald i bicarbonat, stiger pH.
det omvendte forhold gælder for bicarbonatkoncentration, nemlig øget HCO3– = øget pH; nedsat bicarbonat = nedsat pH.
bicarbonat er princippet blodbuffer, og dens koncentration på et bestemt tidspunkt afspejler balancen mellem den, der produceres af CO2, og den, der forbruges i buffering af hydrogenioner (H+) (SE ligning 1).
i laboratoriet-DEFINITION af CO2-parametre
CO2-parametrene genereret af blodgasanalysatoren er:
- partialtryk af kulsyre (pCO2) (kPa/mmHg)
- plasmabicarbonatkoncentration (HCO3 -) (mmol/L)
- plasmakoncentration kulsyre (ctCO2) (mmol / L)
den sidste af disse, ctCO2, kan også måles i plasma eller serum ved kemiske metoder uafhængigt af blodgasanalysatoren.
partialtryk af kulsyre pCO2
denne parameter er et mål for det tryk, der udøves af den lille del (5 %) af total kulsyre i blod, der forbliver i gasformig tilstand, ‘opløst i’ den vandige fase af plasma og blodcellecytoplasma. Målingen foretages ved hjælp af en CO2-specifik pH-elektrode inkorporeret i blodgasanalysatorer.
i sundhed opretholdes pCO2 af arterielt blod inden for området 4,7-6,0 kPa (35-45 mmHg); pCO2 af venøst blod er lidt højere 5,6-6,8 kPa (41-51 mmHg).
BICARBONATKONCENTRATION (HCO3 -)
dette er mængden af bicarbonat i enhedsvolumen af plasma. Som tidligere nævnt er dette den form, hvor de fleste kulsyre (90 %) transporteres i blod. Denne parameter kan ikke måles, men genereres ved beregning under blodgasanalyse. Den anvendte beregning er en omlægning af ligning 2:
ligning 4:
log = pH + log (s pCO2) – pK/1
og afhænger af at have værdier for pH og pCO2, som begge måles under blodgasanalyse.
teoretisk er plasmabicarbonat forskellen mellem total CO2 (ctCO2) og summen af alle andre former for CO2 i plasma, dvs.opløst CO2 (dCO2), CO2 bundet til plasmaproteiner (carbamino CO2) og kulsyre (H2CO3).
således:
Plasmabicarbonat (mmol / L) =
ctCO2- (dCO2 + carbamino-CO2 + H2CO3)
i praksis, fordi carbamino-CO2 og H2CO3 er kvantitativt ubetydelige, antages det, at total CO2 er summen af bare bicarbonat og opløst CO2 . Således er plasmabicarbonat effektivt forskellen mellem plasma total CO2 (ctCO2) og plasma opløst CO2 (dCO2).
i sundhed arterielt plasma bicarbonat (som beregnet under blodgasanalyse) opretholdes inden for det omtrentlige referenceområde: 22-28 mmol/L. venøs bicarbonat er lidt højere: 24-30 mmol/L.
i nogle laboratorier skelnes der mellem ‘faktisk’ bicarbonat (parameteren beskrevet ovenfor) og ‘standard’ bicarbonat. Standard bicarbonat er en anden beregnet parameter og er plasmabicarbonatkoncentrationen af blod, der er blevet ækvilibreret med gas med normal pCO2 (40 mmHg, 5,3 kPa) spænding .
i sundhed er den faktiske bicarbonatkoncentration den samme som standard bicarbonatkoncentration, fordi pCO2 i begge tilfælde er normal. Ved normalisering af pCO2, den respiratoriske komponent i syre-base balance, standard bicarbonat er et mål udelukkende af den metaboliske komponent og betragtes derfor som nyttigt til at belyse årsagen til komplekse forstyrrelser i syre-base balance.
Total KULSTOFKONCENTRATION i PLASMA (ctCO2)
dette er teoretisk summen af alle former for kulstof i plasma. Det måles ikke under blodgasanalyse, men beregnes – ligesom bicarbonat-under forudsætning af, at den samlede kulsyre er summen af bicarbonat og opløst CO2:
da plasma dCO2 mmol / L = (s pCO2) beregnes ctCO2 således :
plasma ctCO2 (mmol / L) =
plasmabicarbonat (mmol / L) + (s pCO2) (mmol / L)
opløst CO2 (s pCO2) bidrager med ca.1.2 mmol / L til den totale CO2 i plasmaet af arterielt blod (se ovenfor), så ctCO2 er omkring 1,2 mmol højere end plasmabicarbonat. Ctco2-referenceområdet er således cirka 23-29 mmol/L for arterielt blod.
det vil bemærkes, at ligesom den beregnede bicarbonatværdi, der genereres under blodgasanalyse, afhænger af forholdet beskrevet i ligning 2, Det gør også den beregnede værdi for ctCO2 genereret under blodgasanalyse.
selvom ctCO2 og bicarbonat giver tilsvarende klinisk information, er det i klinisk praksis altid bicarbonat snarere end ctCO2, der bruges sammen med pH og pCO2 til at evaluere syre-base status. Den kliniske værdi af beregnet ctCO2 genereret under blodgasanalyse er således begrænset.
kemiske metoder til måling af ctCO2
i modsætning til bicarbonat, som ikke kan måles, kan ctCO2 og analysen almindeligvis være en komponent i urinstof-og elektrolytprofilen (U &E) for venøst plasma/serum. Da U & e bestilles meget hyppigere end arterielle blodgasser, kan målt ctCO2 være den første indikation af forstyrrelse i kulsyre (og derfor syre-base) homeostase.
det er almindelig praksis for nogle kliniske laboratorier at henvise til denne målte komponent i U& e-profilen som ‘plasmabicarbonat’. Dette er fejlagtigt, fordi kemiske metoder måler al CO2 frigivet fra plasma (eller serum) ved tilsætning af stærk syre eller alternativt alt bicarbonat produceret som et resultat af tilsætning af en stærk alkali til plasma .
det omfatter således ikke kun bicarbonat, men også opløst CO2 og kulsyre. Hvis plasma eller serum anvendt i disse analyser blev afledt af arterielt blod, ville målt ctCO2 teoretisk tilnærme sig den beregnede ctCO2-værdi genereret under arteriel blodgasanalyse.
faktisk u&E-profiler udføres udelukkende på plasma eller serum genvundet fra venøst blod, så der er en uundgåelig lille teoretisk forskel på 1-2 mmol/L (målt ctCO2 > beregnet ctCO2) på grund af arterio-venøs forskel.
den teoretiske forskel mellem målt ctCO2 og beregnet plasmabicarbonat er lidt højere (målt ctCO2 > beregnet plasmabicarbonat), fordi der ud over den arterio-venøse forskel på 1-2 mmol/L er en yderligere 1,5 mmol/L forskel på grund af inkluderingen af opløst CO2 og kulsyre i målt ctCO2.
denne forskel forudsætter dog, at ingen opløst kulsyre går tabt i atmosfæren før analysen. Dette er muligvis ikke tilfældet, fordi u&e-prøver ikke håndteres anaerobt.
nogle har hævdet, at udtrykket ‘serum/plasma bicarbonat’ for målt ctCO2 er berettiget med den begrundelse, at normal laboratoriepraksis er forbundet med et uundgåeligt tab af opløst CO2 fra U& e-prøven før analyse, i hvilket tilfælde målt ctCO2 i det mindste teoretisk ville tilnærme sig beregnet bicarbonat.
uoverensstemmelse mellem målt ctCO2 og beregnet bicarbonat
uanset de små teoretiske forskelle mellem målte og beregnede værdier skitseret ovenfor er der generel accept af forestillingen om, at den målte ctCO2 genereret som en del af en U & e-profil er til alle praktiske kliniske formål den samme som plasmabicarbonatkoncentration beregnet under blodgasanalyse.
dette afspejles i brugen af udtrykket ‘plasmabicarbonat’ til beskrivelse af målt ctCO2.
det bedste bevis til dato, at målte og beregnede bicarbonatresultater i praksis kan være klinisk udskiftelige, kommer i en meget nylig rapport fra Mayo Clinic . Forfatterne af denne rapport gendannede 17.621 optegnelser over målt og beregnet bicarbonatkoncentration for prøver indsamlet samtidigt fra de samme patienter i løbet af 2006/7. Bicarbonatkoncentration i denne enorme database varierede fra 5 til 49 mmol/L.
den gennemsnitlige forskel (SD) mellem målte og beregnede værdier var -0,36 (1,23 mmol/L) og for 98.5% af resultaterne af parrede prøver var inden for 3 mmol / L af hinanden. Selvom der, som Mayo-rapporten antyder, normalt er acceptabel enighed mellem de to parametre, er det på ingen måde sjældent, at resultaterne er helt uoverensstemmende, med målt ctCO2, der adskiller sig fra beregnet bicarbonat med så meget som 15 mmol/L .
talrige undersøgelser i løbet af de sidste fyrre år har forsøgt at fastslå hyppigheden, størrelsen og årsagen til uoverensstemmelse mellem beregnet bicarbonat og målt ctCO2.
et tidligt fokus på dette arbejde satte spørgsmålstegn ved pålideligheden af bicarbonatberegningen, som afgørende afhænger af konstansen af pK/1 (se ligning 4). Faktisk er dette ikke en sand termodynamisk konstant, men en ’tilsyneladende’ dissociationskonstant bestemt eksperimentelt fra måling af pH, pCO2 og opløst CO2 ved hjælp af følgende forhold afledt af Henderson-Hasselbach-ligningen:
pK/1 = pH + log dCO2 – log
flere undersøgelser afslørede tilstrækkelig variation i pK/1, især blandt de kritisk syge, til klinisk signifikant fejl i beregnet bicarbonat. For eksempel i en undersøgelse blev pK/1 fundet at variere fra 5,84 til 6,29.
forfatterne beregner, at afvigelser fra pK/1 6.1 af denne størrelsesorden ville resultere i fejl i beregnet bicarbonat af ordren på 60 %. En anden beskriver tilfældet med et diabetisk barn i ketoacidose, hvis pK/1 varierede fra 5,49 til 6,02 over en syv-timers periode.
i en undersøgelse af 79 spædbørn , der blev plejet på en pædiatrisk intensivafdeling, viste det sig, at 25% havde pK/1 uden for det ‘normale’ interval 6.055-6.195 defineret af undersøgelsen, og i tre tilfælde var pK/1 > 6.3 med en ‘forbløffende’ værdi på 7.11. Disse og andre rapporter om klinisk signifikant variation i pK/1 er blevet bestridt, og pålideligheden eller på anden måde af beregnet bicarbonat forbliver et uløst, omstridt spørgsmål.
det teoretiske grundlag for synspunktet om, at beregnet bicarbonat er upålideligt ved kritisk sygdom, er beskrevet af Flear . En lige så teoretisk tilgang ledsaget af et væld af eksperimentelle beviser er blevet anvendt af Mass et al.for at gøre den modsatte sag til forsvar for beregnet bicarbonat.
forfattere af undersøgelser, der ikke har påvist klinisk signifikant variation i pK/1, antyder, at den største uoverensstemmelse mellem beregnet bicarbonat og målt ctCO2, lejlighedsvis set i klinisk praksis, sandsynligvis er resultatet af en kombination af præanalytiske variabler, analytisk forskel og tilfældig analytisk fejl .
måling af ctCO2 er særlig tilbøjelig til præanalytisk variabilitet, fordi blod til U & e profilering er universelt indsamlet og behandlet aerobt. Prøver kan efterlades uden lukning i timer før analyse. Da den omgivende luft indeholder mindre CO2 end blod, er der en tendens til, at opløst CO2 går tabt fra prøven. Dette er blevet estimeret til at reducere målt CO2 med en hastighed på 6 mmol/time.
derimod er beregnet bicarbonat ikke forbundet med den samme risiko for præanalytisk variation, fordi blod til blodgasanalyser rutinemæssigt udtages anaerobt, og der er minimal forsinkelse (næsten altid
en anden medvirkende årsag til uoverensstemmelse mellem målte og beregnede værdier kan være prøveforskel, da arterielt blod bruges til at beregne en værdi, og serum-eller plasmaprøver bruges til at måle en værdi.
uanset årsagen viser undersøgelser fortsat moderat, men klinisk signifikant uoverensstemmelse mellem de to parametre blandt de kritisk syge . Som for at bekræfte den omstridte karakter af debatten giver den seneste undersøgelse af kritisk syge patienter imidlertid bevis for acceptabel aftale mellem beregnet bicarbonat og målt ctCO2 .
uanset denne sidste undersøgelse er der en opfattelse af, at det i det mindste for kritisk syge patienter kan være klogt at opgive beregnet bicarbonat til fordel for målt ctCO2, skønt det skal understreges , at denne opfattelse er omstridt, og det kan være, at den kliniske virkning af forskelle er begrænset.
beviset for acceptabel aftale leveret af den meget store Mayo Clinic-undersøgelse kan desværre ikke bruges i den særlige debat, der centrerer sig om kritisk syge, fordi patientpopulationen ikke blev defineret.
af de to parametre har beregnet bicarbonat den klare fordel af bekvemmelighed i forhold til målt ctCO2, fordi det gør det muligt for alle tre parametre (pH pCO2 og bicarbonat), der anvendes til vurdering af syre-base, at være tilgængelige på samme tid fra en enkelt prøve.
der er ingen konsensus i litteraturen om mange af de spørgsmål, der er diskuteret ovenfor. Således forbliver det endda uklart, om der er eller ikke er uoverensstemmelse mellem målt og beregnet CO2, skønt bevisbalancen for nylig er skiftet til fordel for ingen uoverensstemmelse fra den store Mayo Clinic-undersøgelse .
for dem, der mener, at balancen af beviser tyder på, at der er uoverensstemmelse, er der yderligere to uløste problemer.
disse er: den kliniske betydning af denne uoverensstemmelse og årsagen til denne uoverensstemmelse. Debatten om årsagen til uoverensstemmelse har primært fokuseret på, hvorvidt pKl1 varierer markant mellem patienter og i hvilket omfang præanalytiske forskelle, analytiske forskelle og tilfældig fejl bidrager til uoverensstemmelse.
endelig har mindst en kommentator stillet spørgsmålstegn ved det kliniske behov for enten beregnet bicarbonat eller målt ctCO2, hvilket antyder, at pH og pCO2 alene tillader fuld vurdering af syre-base forstyrrelser.
resume
kulsyre er et produkt af aerob cellemetabolisme, der transporteres i blod til lungerne for udskillelse i udgået luft. Lidt transporteres uændret opløst i blod, men de fleste transporteres som bicarbonat.
regulering af mængden af kulsyre i blod, eller mere præcist regulering af forholdet mellem bicarbonat og opløst kulsyre koncentration, er afgørende for opretholdelse af blodets pH (normal syre-base balance).
klinisk undersøgelse af syre-base-forstyrrelse inkluderer arteriel blodgasanalyse, en test, der genererer tre parametre for kulstofstatus. Af disse er kun en, pCO2, faktisk målt; de to andre-plasmabicarbonat og total kulstofkoncentration – stammer fra beregninger ud fra målt pH og pCO2.
gyldigheden af disse beregninger er blevet sat spørgsmålstegn ved, og der er modstridende beviser for, at det i nogle patientgrupper kan være mere klinisk pålideligt at måle total kulilte ved kemiske metoder end at stole på beregnede værdier.
dette sidste er stadig et meget omstridt spørgsmål, der kun kan løses endelig ved yderligere undersøgelse.