pladecellecarcinom i hoved og nakke (SCCHN) er den sjette mest almindelige neoplasma globalt med ~600.000 tilfælde diagnosticeret årligt. De sidste 20 år har givet et væld af kliniske forsøgsdata, og dette har ændret standarderne for pleje til behandling af SCCHN. Historisk set har dårlig lokal sygdomsbekæmpelse og samlet overlevelse givet drivkraft til en lang række kliniske forsøg, der evaluerer multimodalitetsterapi hos patienter med SCCHN. Den indviklede anatomi og de kritiske funktionelle og sociale roller i hoved-og nakkeområdet har uden tvivl også motiveret en betydelig indsats for at identificere alternativer til onkologisk resektion af ondartede tumorer i denne region. I denne gennemgang opsummerer vi den historiske udvikling af kombineret kemoradiationsterapi til behandling af SCCHN, giver en opdatering af nyere litteratur på dette område og diskuterer nutidige kliniske spørgsmål, som fremtidige undersøgelser kan løse.
samtidig Kemoradiation—fra eksperimentel til foretrukken behandling
klinisk undersøgelse af rollen som kombineret kemoradiationsbehandling for SCCHN-datoer til mindst slutningen af 1960 ‘ erne med tidlige undersøgelser, der undersøgte sekventiel og samtidig anvendelse af enkeltmidler inklusive fluorouracil (5FU), bleomycin, cisplatin, metotreksat og mitomycin.1 sådanne forsøg viste dårlig respons på enkeltmiddelkemoterapi alene, mens de pegede på cisplatin som det mest effektive enkeltmiddel med en 25-30% responsrate.2-4 efterfølgende undersøgelser undersøgte rollen som multi-agent kemoterapi og viste markant forbedring i sygdomsrespons på 70% med kombineret cisplatin og bleomycin5 og >90% responsrater med cisplatin og kontinuerlig infusion 5FU.6,7 det er vigtigt, at disse tidlige undersøgelser pegede på en potentiel overlevelsesfordel ved tilsætning af kemoterapi til traditionelle endelige behandlinger af stråling og/eller kirurgi for SCCHN og førte til yderligere undersøgelse i større randomiserede fase III-forsøg.
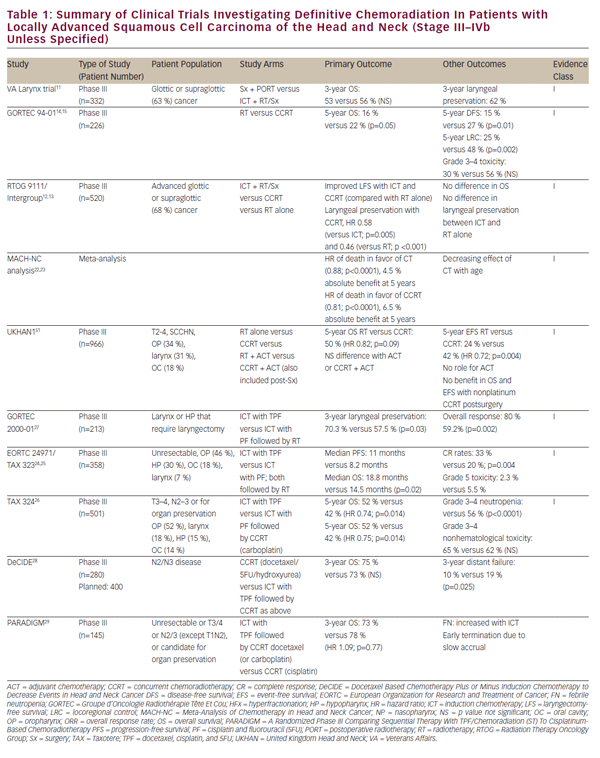
med forfining af kemoterapeutiske regimer, overvejelse henvendte sig til potentialet for endelige og organbesparende kemoradiationsmetoder hos patienter med lokalt avanceret SCCHN. Dette arbejde blev oprindeligt avanceret af en række enkeltinstitutionsstudier, der demonstrerede levedygtigheden af endelig kemoradiation som et alternativ til kirurgi for glottiske og supraglottiske laryngeale tumorer.8-10 den historisk vigtige veterananliggender Laryngeal kræftundersøgelse viste i sidste ende, at induktionskemoterapi (IKT) efterfulgt af stråling kunne opnå organbevarelse hos SCCHN-patienter uden kompromis med den samlede overlevelse.11 Dette forsøg etablerede en begrundelse for landmark Radiation Therapy Oncology Group (RTOG) 9111-undersøgelsen, der behandlede den passende sekventering af kemoterapi og stråling hos patienter med lokalt avanceret supraglottisk eller glottisk strubehovedkræft. Patienter blev randomiseret til: IKT efterfulgt af stråling; samtidig kemoradiation (CCRT); eller stråling alene.12,13 resultaterne af RTOG 9111 viste overlegenhed af CCRT med hensyn til lokoregional sygdomsbekæmpelse og strubehovedbevarelse, mens der ikke blev observeret nogen forskel i den samlede overlevelse blandt de tre arme. Derefter blev Groupe d ‘ Oncologie Radioth Pristrapie t priste et Cou (GORTEC) 94-01 forsøg randomiserede patienter med lokalt avancerede oropharyngeale primære tumorer til stråling eller CCRT med carboplatin/5FU og demonstrerede forbedret lokal sygdomsbekæmpelse såvel som samlet overlevelse.14,15 lignende forbedringer i overlevelse og lokoregional kontrol er rapporteret for nasopharyngeale patienter behandlet med CCRT.16-21 en rapport fra Metaanalysen af kemoterapi i hoved-og halskræft (MACHNC) har foreslået en samlet overlevelsesfordel på 6,5% efter 5 år med CCRT, men ikke med IKT eller adjuverende kemoterapi.22,23 effekten af kemoterapi på overlevelse i denne metaanalyse blev observeret at falde med alderen for dem over 50 år uden påviselig fordel vist i de 71 år eller ældre. Kollektivt, selvom disse undersøgelser adskiller sig i inklusions-og eksklusionskriterier, kliniske endepunkter og behandlingsmetoder (se tabel 1), bekræfter de en fordel ved CCRT versus strålebehandling alene som en endelig behandling for lokalt avanceret SCCHN.
Induktionskemoterapi Forud For (Kemo) Stråling-En Levedygtig Strategi?
selvom en head-to-head sammenligning med CCRT indikerede underlegenhed af IKT med hensyn til lokal sygdomsbekæmpelse i det kliniske forsøg RTOG 9111,12 Der er stadig interesse for denne terapeutiske tilgang. Data fra RTOG 9111 indikerer ækvivalens af disse tilgange med hensyn til toksiciteter af høj kvalitet, hvilket gør det vanskeligt at retfærdiggøre valget af IKT på grund af patienttolerance. Ikke desto mindre har opfølgningsundersøgelser til RTOG 9111 forsøgt at udvikle sig på IKT-platformen for at gøre dette til en mere levedygtig behandlingsmulighed. EORTC 24971 / ta 323 trial24, 25 viste forbedret samlet overlevelse med tilføjelse af TPF (TPF) til cisplatin og 5FU (PF) IKT-regimen anvendt i rtog 9111-studiet hos patienter med inoperabel SCCHN. 324-forsøget evaluerede ligeledes TPF versus PF i indstillingen af CCRT og substituerede ugentlig carboplatin med cisplatin i disse regimer. Denne undersøgelse viste forbedret lokoregional og fjern sygdomskontrol samt forbedret samlet overlevelse med TPF sammenlignet med PF.26 En yderligere opfølgningsundersøgelse (GORTEC 2000-01) i lokalt avanceret laryngeal og hypopharyngeal cancer bekræftede forbedret sygdomsrespons og strubehovedbevarelse med induktion TPF sammenlignet med PF, men viste ingen effekt på overlevelse.27 selv om disse undersøgelser er forskellige med hensyn til inklusions-og eksklusionskriterier, kliniske endepunkter og behandlingsmetoder (se tabel 1), understøtter de samlet TPF ‘ s overlegenhed i forhold til PF-baseret IKT. Ikke desto mindre mangler direkte sammenligning af IKT med cisplatinbaseret CCRT-standard.
MACH-NC-metaanalysen, som tidligere nævnt, antydede mindreværd af IKT sammenlignet med CCRT med hensyn til samlet overlevelse og lokoregional sygdomskontrol.22 Det er imidlertid bemærkelsesværdigt, at fordelene ved IKT var mere udtalt end fordelene ved CCRT med hensyn til fjernmetastaser.22 dette kan afspejle en særskilt rolle af kemoterapi i disse behandlingsmetoder. Samtidig kemoterapi kan spille en dominerende radiosensibiliserende rolle, hvilket resulterer i en dominerende effekt på lokal sygdomsbekæmpelse, mens multi-agent IKT kan tilvejebringe en effektiv systemisk behandling af mikrometastatisk sygdom. Denne hypotesegenererende observation antyder en potentielt komplementær karakter af disse behandlinger og har skabt interesse for deres kombination. Indtil videre har bestræbelserne på at undersøge kombinationen af IKT og CCRT resulteret i dårlige periodiserings-og ufattelige fund (DeCIDE and PARADIGM studies).28,29 en igangværende randomiseret fase III-undersøgelse sammenligner IKT med PF eller TPF efterfulgt af cisplatin-baseret CCRT versus CCRT alene som førstelinjebehandling for lokalt avanceret SCCHN (NCT00261703). Resultater fra ovennævnte undersøgelser af CCRT og IKT er også opsummeret i tabel 1.
adjuverende Kemoradiation
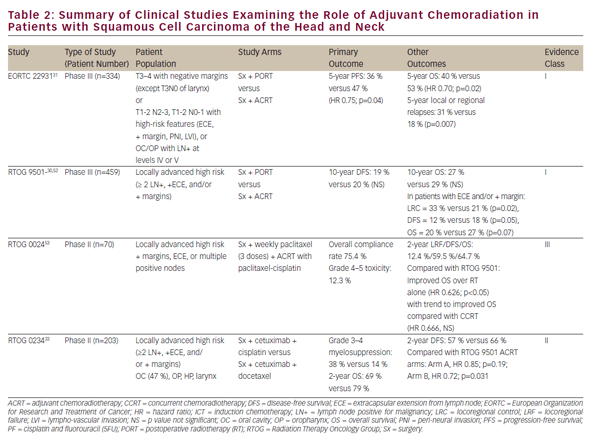
de førnævnte kliniske forsøg har etableret CCRT som en levedygtig endelig behandling til organbevarelse i lokalt avanceret SCCHN. Ikke desto mindre forbliver endelig onkologisk resektion en vigtig behandlingsmulighed for lokaliseret sygdom og en vital del af multimodalitetsterapi for avancerede tumorer i mundhulen, strubehovedet og hypofysen. Kemoradiationens rolle i adjuvansindstillingen efter onkologisk resektion er stort set defineret af to fase III randomiserede forsøg— EORTC 22931 og RTOG 950130,31 (se tabel 2). Disse undersøgelser undersøgte brugen af postoperativ stråling versus adjuverende kemoradiation med cisplatin givet hver 3.uge i tre cyklusser hos postoperative SCCHN-patienter. Begge studier viste forbedring i lokoregional sygdomskontrol og progressionsfri overlevelse, mens EORTC-studiet også viste en forbedring i den samlede overlevelse. En post-hoc-analyse af disse to undersøgelser antydede, at fordelen ved adjuvans CCRT var størst hos dem med positive kirurgiske marginer og/ eller ekstrakapsulær forlængelse (ECE) fra resekterede lymfeknuder.32 adjuvans CCRT ‘ s rolle hos patienter med tætte kirurgiske marginer er mindre klar og blev understøttet af EORTC 22931, som omfattede patienter med kirurgiske marginer på 5 mm. På den anden side inkluderede rtog 9501 patienter baseret på positive, men ikke tætte marginer. Post-hoc-analyse har ikke antydet nogen åbenbar fordel ved CCRT for patienter, der opfylder adgangskriterier for kun en af disse undersøgelser.32 på samme måde er adjuvans CCRT ikke blevet tilstrækkeligt undersøgt hos ældre patienter, da de over 70 år blev ekskluderet fra EORTC 22931 og kun udgør et lille mindretal (5%) af patienterne i RTOG 9501.30,31
Pursuant to EORTC 22931 and RTOG 9501, adjuvant CCRT has now become standard-of-care treatment in high-risk postoperative SCCHN patients. The phase II RTOG 0234 study has explored alternative adjuvant chemoradiation treatment regimens, randomizing patients with multiple involved lymph nodes, ECE, or positive margins to the epidermal growth factor receptor (EGFR) antibody, cetuximab, plus docetaxel or cetuximab plus cisplatin. This study demonstrated an apparent survival benefit from concurrent adjuvant cetuximab and docetaxel.33 resultaterne af denne spændende fase II-undersøgelse kræver validering i en fase III-undersøgelse inden inkorporering i klinisk praksis.
radioterapi fraktionering indvirkning på Kemoradiation
i et forsøg på at øge effektiviteten har tidligere kliniske studier undersøgt alternative fraktioneringsordninger til administration af strålebehandling med eller uden samtidig kemoterapi hos SCCHN-patienter. Rtog 9003-og Danish Head and Neck Cancer Group (DAHANCA) – forsøgene viste forbedring i lokoregional sygdomsbekæmpelse med accelererede eller hyperfraktionerede strålebehandlingsregimer, når stråling anvendes alene.34,35 en efterfølgende metaanalyse har endda antydet en beskeden overlevelsesfordel ved hyper-fraktionering af stråling, når den anvendes som en eneste behandlingsmodalitet.36 i indstillingen af samtidig kemoterapi har rtog 0129 og gortec 99-02-undersøgelserne imidlertid ikke vist nogen forbedring i klinisk resultat med anvendelse af accelereret versus konventionel strålebehandling.37,38 Hyper-fraktioneret CCRT, sammenlignet med hyper-fraktioneret stråling alene, resulterede i forbedret lokoregional sygdomskontrol i en enkelt institution undersøgelse fra Duke University og en fase III undersøgelse fra Jugoslavien, hvor sidstnævnte også viser forbedret samlet overlevelse og fjern metastasefri overlevelse.39,40 disse undersøgelser indikerer, at fordelen ved CCRT vedvarer med hyper-fraktioneret strålebehandling. En direkte sammenligning af konventionelt fraktioneret CCRT og hyper-fraktioneret CCRT er endnu ikke foretaget. Det er dog bemærkelsesværdigt, at mach-NC-metaanalysen ikke påviste nogen forskel i resultatet blandt patienter behandlet med CCRT ved hjælp af konventionelle eller ændrede fraktioneringsteknikker.22
toksicitet—omkostningerne ved Kemoradiation
i overensstemmelse med mange enkeltinstitutionsstudier, der gik forud for det, viste RTOG 9111, at fordelene ved kemoterapi, hvad enten det administreres sekventielt eller samtidig med stråling, kommer på bekostning af yderligere toksicitet.12 tilsvarende viste både EORTC 2291 og RTOG 9501 kliniske forsøg i adjuvansindstillingen en omtrentlig fordobling af grad 3-toksiciteter med kemoradiation sammenlignet med stråling alene.30,31 en sådan tendens vedvarer selv i indstillingen af hyper-fraktioneret strålebehandling.39 skønt den forventede hastighed for enhver specifik toksicitet som bestemt ud fra historiske undersøgelser sandsynligvis overvurderes i den nuværende æra med stærkt konforme strålebehandlingsteknikker, såsom intensitetsmoduleret strålebehandling (IMRT). To små, randomiserede forsøg har rapporteret signifikant reduktion i forekomsten og sværhedsgraden af kserostomianvendelse af IMRT sammenlignet med konventionel tredimensionel konform strålebehandling til kræft i hoved og hals (Parotidsparende intensitetsmoduleret versus konventionel strålebehandling i hoved-og halskræft og Tata Memorial Hospital forsøg).41,42 seneste forsøg, der undersøger CCRT, tillader IMRT-baseret behandlingslevering som en standard tilgang til styring af SCCHN. Det er stadig at se, hvilken indvirkning IMRT vil have på toksicitetshastigheder, når de kombineres med kemoterapi i disse større randomiserede undersøgelser.
forbedrede strålebehandlingsteknikker kombineret med stigende betydning og tilgængelighed af understøttende pleje og hjælpetjenester såsom talesluge patologi og tandpleje begrænser forekomsten af alvorlige ikke-hæmatologiske toksiciteter endnu mere. Imidlertid forventes toksiciteten fra CCRT stadig at være højere end strålebehandling alene. Denne persistente toksicitet afspejler de kliniske ‘omkostninger’ ved at kombinere kemoterapi og stråling. I denne indstilling er det fortsat altafgørende, at læger omfattende vurderer patienter for at bestemme, at de potentielle fordele ved CCRT berettiger denne omkostning. Anvendelse af enkeltmodalitet radioterapibaserede behandlinger hos patienter med markante komorbiditeter/lav baseline-præstationsstatus eller med lav risiko, tidligt stadium sygdom kan være rimelig tilgang til at maksimere terapeutisk forhold. Denne risiko-fordel-Analyse bliver endnu vigtigere med fremkomsten af molekylære målrettede stoffer, der tilbyder en levedygtig alternativ mulighed for samtidig terapi.
den nye rolle af molekylært målrettede stoffer
toksiciteten af kemoradiationsbehandling samt et ønske om yderligere at forbedre kliniske resultater har skabt en voksende interesse for molekylærmålrettede agenters rolle til behandling af SCCHN. EGFR er overudtrykt eller muteret i 80-90% af SCCHN-tumorer, og dette er forbundet med nedsat respons på strålebehandling og dårligere kliniske resultater.43-45 i 2006, Bonner et al. patienter med lokalt avanceret SCCHN behandlet med enten stråling alene eller stråling samtidig med EGFR-antistoffet. Denne undersøgelse viste, at samtidig cetuksimab og stråling øgede lokoregional sygdomskontrol og samlet overlevelse uden at forværre almindelige toksiciteter af stråling.46 denne undersøgelse definerede en rolle for samtidig cetuksimab og stråling hos patienter, der ikke er kandidater til cisplatin.
efterfølgende undersøgelser har forsøgt at sammenligne CCRT med samtidig cetuksimab med cisplatin. Retrospektive og tidlige fasestudier har været forskellige i denne vurdering, og en randomiseret fase III-sammenligning er i gang i RTOG 1016. Rtog 0522-forsøget vurderede især den potentielle ekstra fordel ved CETUKSIMAB til et cisplatinbaseret regime af CCRT47. Denne undersøgelse viste, at når den blev tilføjet til standard platinbaseret CCRT, forbedrede cetukmab ikke yderligere progressionsfri eller samlet overlevelse. I den postoperative indstilling vil RTOG 0920 evaluere adjuverende strålebehandling med eller uden cetuksim i lokalt avanceret resekteret SCCHN, mens fase II/III RTOG 1216-forsøget vil vurdere adjuvans CCRT med samtidig cisplatin versus docetaksel versus docetaksel og cetuksim for højrisiko SCCHN.
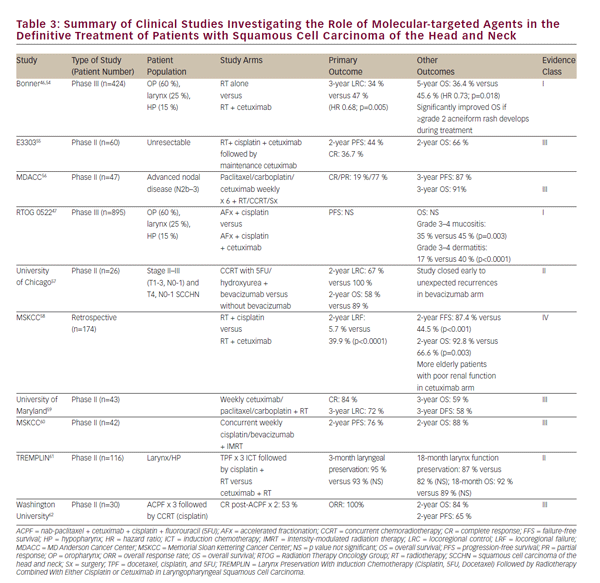
talrige tidlige fase kliniske forsøg med yderligere molekylære målrettede stoffer sammen med stråling til behandling af SCCHN er blevet udført eller er i gang. Et udvalg af disse er opsummeret i i>tabel 3. Intet andet molekylært målrettet middel er kommet frem til et punkt, hvor det påvirker den nuværende praksis uden for en klinisk forsøgsindstilling. Mens udsigten til molekylært målrettede stoffer er lovende, samtidig højdosis cisplatin kemoterapi forbliver den foretrukne, niveau 1 anbefaling af nuværende National Comprehensive Care (NCCN) retningslinjer for CCRT.
Kemoradiationsterapi i hoved—og halskræft-et udviklende paradigme
de sidste 20 år har set en fremkomst af kemoradiation som en standard for pleje i den endelige behandling af SCCHN. Hos passende udvalgte patienter opvejer den påviselige overlevelsesfordel ved denne behandling risikoen for yderligere toksiciteter. Der er dog stadig vigtige spørgsmål vedrørende optimal anvendelse af kemoradiation. En række kliniske forsøg har yderligere undersøgt den potentielle kliniske nytte af IKT hos lokalt avancerede SCCHN-patienter, og mens disse undersøgelser har vist forbedring af IKT-regimer på bekostning af toksicitet, Ingen har endeligt vist meningsfuld klinisk forbedring sammenlignet med cisplatin-baseret CCRT.
fremtidige undersøgelser vil uden tvivl fortsætte med at undersøge alternative kemoterapiregimer og doseringsplaner samt radioterapi fraktionering, dosering og leveringsmetoder i et forsøg på at fremme eksisterende teknikker. Desuden vil fremtidige undersøgelser med fortsat udvikling af nye molekylærmålrettede kemoterapeutika næsten helt sikkert definere en spirende rolle for disse midler i behandlingen af SCCHN. Særligt spændende kan være brugen af disse midler i en induktionsindstilling før CCRT, hvor de kan målrette mod mikrometastatisk sygdom og mindske fjernt sygdomsfald uden at pålægge toksicitetsrelaterede begrænsninger på CCRT-færdiggørelseshastigheder. Mens brugen af CCRT udvikler sig, fortsat undersøgelse af den passende rolle som operation i SCCHN er også berettiget. Fremskridt inden for både robotkirurgi og kemoradiationsbehandlingsmetoder giver ligevægt til en sådan undersøgelse. Nuværende retningslinjer for praksis anbefaler adjuverende kemoradiation til postoperative patienter med positive margener eller ECE, mens adjuverende stråling alene eller overvejelse af kemoradiation anbefales til postoperative patienter med en pT3 eller pT4 primær, PN2 eller pN3 nodal sygdom, niveau IV eller V lymfeknudeinddragelse eller med peri-neural eller lymfovaskulær invasion. Yderligere undersøgelser, der identificerer præoperative radiografiske og kliniske forudsigere for højrisikostatus blandt patienter med tidligt stadium SCCHN vil vise sig værdifulde til at styre behandlingen af sådanne patienter, der kan blive skånet for et kirurgisk indgreb med en up-front endelig kemoradiationsbehandlingsmetode.
den nylige anerkendelse af human papillomavirus (HPV) infektion som årsag og gunstig prognostisk faktor i SCCHN, der stammer fra oropharynks48 og potentielt andre steder, transformerer opfattelsen af SCCHN som en sygdomsenhed. I en retrospektiv analyse af RTOG 0129 var 3-års samlet overlevelse for patienter med tumorer, der var positive for HPV,82,4% versus 57% for HPV-negativ sygdom (p49, 50 i lyset af dette vil fremtidige undersøgelser nødvendigvis blive stratificeret efter HPV-status eller skræddersyet til en delmængde af HPV-positive eller-negative patienter, hvilket fik en voksende skisma i behandlingsmetoder. Allerede rejst er udsigten til at undersøge mindre toksiske behandlingsmetoder for HPV-positive tumorer og mere aggressive endelige behandlinger for HPV-negative tumorer for at tage højde for skarpe forskelle i deres respektive svar på nuværende behandlingsmetoder. RTOG 1016 er en sådan undersøgelse, der specifikt vurderer HPV-positive patienter til behandling afintensivering ved brug af samtidig cetuksimab med stråling versus standard cisplatin-baseret CCRT. Interaktionen mellem specifikke behandlingsregimer og særlige molekylære målrettede stoffer med tumor HPV-status vil uden tvivl vise sig frugtbar grund til fremtidig forskning. Det skal stadig ses, hvilken indflydelse den spirende HPV-epidemi og de nuværende vaccinationsprogrammer vil have på kliniske resultater og behandlingsmetoder hos patienter med SCCHN.