introduktion
venøs tromboemboli (VTE), inklusive dyb venetrombose (DVT), lungeemboli (PE) og splanchnisk venetrombose, er en hyppig komplikation af kræft.1 udviklingen af kræftassocieret VTE er forbundet med nedsat livskvalitet og lægger en betydelig økonomisk byrde på både patienten og sundhedssystemet.2 VTE er den næstledende dødsårsag hos kræftpatienter, der får kemoterapi, og har vist sig at være en uafhængig forudsigelse for dødelighed i populationen af patienter med kræft.3,4 håndteringen af kræftassocieret VTE-behandling kan være udfordrende, fordi risikoen for tilbagevendende VTE og antikoagulantrelateret blødning er høj på trods af passende behandling.5 derudover øger lægemiddelinteraktioner og kræftrelaterede comorbiditeter, såsom nyre-og/eller leverdysfunktion, nedsat oral indtagelse, kemoterapiinduceret kvalme og opkast og trombocytopeni også behandlingskompleksiteten ved at begrænse valget af antikoagulerende middel.
kliniske forsøg, der evaluerer Heparin med lav molekylvægt til behandling af Kræftassocieret VTE
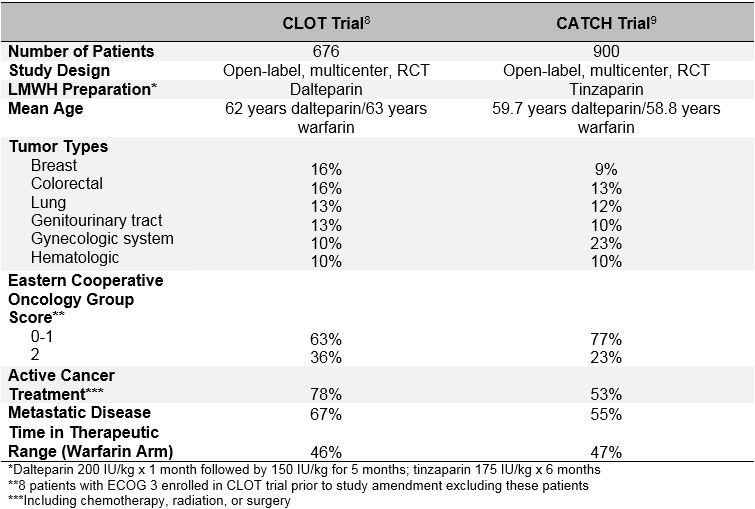
langvarig brug af heparin med lav molekylvægt til behandling af VTE hos patienter med aktiv cancer anbefales som førstelinjebehandling baseret på resultaterne af flere åbne randomiserede kontrollerede forsøg (RCT ‘ er).6,7 de to hidtil største undersøgelser, CLOT (sammenligning af heparin med lav molekylvægt versus Oral antikoagulant terapi til forebyggelse af tilbagevendende venøs tromboemboli hos patienter med kræft) og CATCH (sammenligning af akutte behandlinger i Kræfthæmostaseforsøg), sammenlignede en LMVH med vitamin K-antagonistbehandling hos patienter med aktiv cancer og akut symptomatisk proksimal DVT eller PE. Se tabel 1 For baseline-karakteristika og tabel 2 for undersøgelsesresultater.8,9 begge forsøg anvendte et åbent studiedesign, det samme mål international normaliseret ratio (INR) i vitamin K-antagonistkontrolarmen, den samme aktive kræftdefinition og den samme behandlingsvarighed og havde sammenlignelige patientberettigelseskriterier.
tabel 1: forsøgsdesign og Baselinekarakteristika for fangst-og KOAGULATIONSFORSØG
tabel 2: Resultater i koagulations-og FANGSTFORSØGENE

CLOT-forsøget, der blev offentliggjort i 2003, randomiserede 676 patienter til at modtage dalteparin (200 IE/kg dagligt i 1 måned efterfulgt af 150 IE/kg dagligt i 5 måneder) eller vitamin K-antagonist (varfarin eller acenocoumarol med target INR 2, 5 i alt 6 måneder med en indledende 5-7 dages overlapning med dalteparin 200 IE/kg).8 symptomatisk tilbagevendende DVT eller PE, inklusive død relateret til PE, blev observeret hos 27 patienter (7,0%) randomiseret til dalteparin og hos 53 patienter (15%) randomiseret til vitamin K-antagonist (fareforhold 0,48; 95% konfidensinterval, 0,30-0,77; p = 0,002). Der blev ikke observeret nogen forskel i antallet af større blødninger (6 vs. 4%; p = 0,27), enhver blødning (15 vs. 19%; p = 0,09) eller død (39 vs. 41%; p = 0,53) mellem de 2 grupper.
I CATCH-forsøget, der blev offentliggjort over 10 år senere i 2015, blev 900 patienter randomiseret til tinsaparin (175 IE/kg dagligt uden dosisreduktion) eller varfarin (target INR 2,0-3,0 med initial 175 IE/kg overlapning i 5-10 dage) i alt 6 måneder.9 det primære sammensatte endepunkt for recidiverende VTE inklusive incidental proksimal DVT og PE forekom hos 31 patienter (6,9%) i arm og 45 patienter (10%) i arm (HR 0,65; 95% CI, 0,41-1,03; p = 0,07). Symptomatisk DVT forekom hos signifikant færre patienter behandlet med tinsaparin (2,7 vs. 5,3%; HR 0,48; 95% CI, 0,24-0,96; p = 0,04). Selvom de største blødningshastigheder var ens i begge arme, blev der observeret en signifikant reduktion i klinisk relevant, ikke-større blødning med tinsaparin (10,9 vs. 15,3%; HR 0,58; 95% CI, 0,40-0,84; p = 0,004). Mortaliteten var den samme i begge grupper, hvor ca.en tredjedel af patienterne døde i undersøgelsesperioden (33,4 vs. 30,6%; p = 0,54). Det primære sammensatte endepunkt for recidiverende VTE er ikke signifikant reduceret, men resultaterne af CATCH-undersøgelsen understøtter brugen af langvarig LMVH som den foretrukne behandling for cancerassocieret VTE på grund af en lavere risiko for klinisk relevant større blødning og en signifikant reduktion i recidiverende DVT.
FANGSTFORSØGETS manglende opfyldelse af statistisk signifikans for det primære endepunkt kan skyldes den lavere end forventede tilbagevendende VTE-rate, der er observeret i varfarin-armen. En mulig forklaring på denne observation kunne være en forbedring af varfarinforvaltningen i FANGSTFORSØGET. Imidlertid argumenterer lignende niveauer af INR-kontrol i begge undersøgelser imod dette (Tid i terapeutisk interval var 46% i koagel vs. 47% i fangst; tid over det terapeutiske interval var 24% i koagel vs. 27% i fangst). En mere sandsynlig forklaring er en bias i udvælgelsen af “mindre syge” patienter til tilmelding til FANGSTFORSØGET. Selvom CATCH-og CLOT-undersøgelserne anvendte lignende inklusions-og eksklusionskriterier, findes der vigtige forskelle i baseline-karakteristika mellem de to patientpopulationer, især med hensyn til trombotiske og prognostiske risikofaktorer. En højere andel af patienterne i CLOT-studiet fik aktiv kræftbehandling (72% CLOT vs. 53% CATCH), havde tidligere VTE (11% CLOT vs. 6% CATCH), havde tegn på metastatisk sygdom (67% CLOT vs. 55% fangst) og havde en dårligere præstationsstatus (Eastern Cooperative Oncology Group score på 2 i 36% CLOT vs. 23% fangst). Derudover var dødeligheden i 6-måneders behandlingsperioden også højere i KOAGULATIONSPOPULATIONEN (39% blodprop vs. 32% fangst). Således havde FANGSTPATIENTPOPULATIONEN sandsynligvis en lavere iboende risiko for tilbagevendende VTE sammenlignet med patienter med CLOT-undersøgelse. Det er meget sandsynligt, at efterforskere ikke tilmeldte patienter til fangst, hvis de følte, at LMVH ville være mere gavnligt end varfarin, hvilket resulterede i selektiv tilmelding af patienter, der var mindre tilbøjelige til at udvikle tilbagevendende VTE.
forsøg, der evaluerer direkte orale antikoagulantia i Kræftassocieret VTE
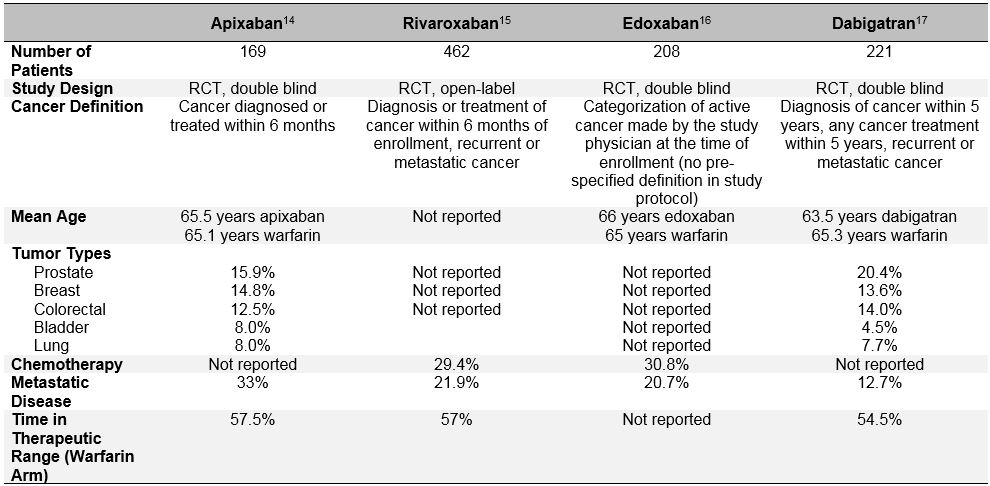
patientudvælgelsesforstyrrelse er endnu mere tydelig i de nylige randomiserede forsøg, der evaluerer effekten og sikkerheden af direkte orale antikoagulantia (Doac ‘ er) til behandling af akut VTE.10 disse orale antikoagulantia er blevet grundigt undersøgt i løbet af det sidste årti i atrieflimren, VTE-behandling og VTE-forebyggelse. I de skelsættende fase III kliniske forsøg med akut VTE-behandling blev det konsekvent påvist, at Doac ‘ er ikke er ringere end varfarin (samlet relativ risiko 0,90; 95% CI, 0,77-1.06) til forebyggelse af tilbagevendende VTE, og de har en lignende eller reduceret risiko for større blødninger (samlet RR 0,40; 95% CI, 0,45-0,83).11 blandt de patienter, der blev klassificeret som “kræft” eller “aktiv kræft” i disse undersøgelser, synes DOACs også at udføre på samme måde som varfarin.12 Men en mere dybdegående undersøgelse af disse post-hoc-data afslører vigtig bias for patientvalg og sætter spørgsmålstegn ved generaliserbarheden af DOAC-forsøgsresultaterne til “virkelige” patienter med kræft med VTE. Ud over de heterogene definitioner af “aktiv kræft”, der blev brugt i disse forsøg, der adskiller sig fra koagulations-og FANGSTFORSØGENE, var vigtige determinanter for tilbagevendende VTE og blødning også meget forskellige hos DOAC-patienter med kræft fra de kræftspecifikke forsøg (tabel 3). Disse inkluderer tilstedeværelse af metastatisk sygdom og samtidig brug af kræftbehandling. De store forskelle i dødelighed i undersøgelsesperioden hævder også, at meget forskellige grupper af patienter med “kræft” var inkluderet i doac versus lmvh forsøg. Desuden, i modsætning til LMVH, som er forbundet med en signifikant reduktion i risikoen for tilbagevendende VTE sammenlignet med vitamin K-antagonister (RR 0,52; 95% CI, 0,36-0.74) reducerede DOACs ikke signifikant denne risiko i en metaanalyse af 1.132 patienter med kræft, der var inkluderet i Einsteins kliniske forsøgsprogram, HOKUSAI-VTE (Edoksaban Versus Varfarin til behandling af symptomatisk venøs tromboembolisme), RECOVER (Dabigatrans virkning og sikkerhed sammenlignet med Varfarin til 6 måneders behandling af akut symptomatisk venøs tromboemboli) og AMPLIFY (APIKSABAN til den indledende behandling af lungeemboli og dyb venetrombose som førstelinjebehandling) RCT ‘ er (RR 0,66; 95% CI, 0, 39-1, 11).10 alle disse overvejelser bør være forsigtige med ikke-valgt anvendelse af Doac ‘ er til patienter med aktiv cancer og akut, symptomatisk VTE.13
tabel 3: studiedesign og Baseline-karakteristika for undergrupperne af patienter med kræft fra fase III DOAC-forsøg
konklusioner
alle større evidensbaserede konsensusretningslinjer anbefaler LMV til den indledende og langsigtede behandling af kræftassocieret VTE.6,7,13 denne anbefaling er baseret på den observation, at LMV ikke kun er mere effektiv end varfarin til forebyggelse af tilbagevendende VTE, men også giver yderligere fordele i forhold til orale midler, herunder stabil antikoagulation hos patienter med dårlig oral indtagelse, mangel på lægemiddelinteraktioner og klinisk erfaring med håndtering af antikoagulation omkring invasive procedurer og trombocytopeni. Selvom Doac ‘er i øjeblikket ikke anbefales til VTE-behandling hos patienter med kræft, er RCT’ er i øjeblikket i gang og vil bidrage til at afklare deres rolle i kræftassocieret VTE.6,13
- Khorana AA, Dalal M, Lin J, Connolly GC. Forekomst og forudsigere af venøs tromboemboli (VTE) blandt ambulante højrisikokræftpatienter, der gennemgår kemoterapi i USA. Kræft 2013; 119:648-55.
- Kourlaba G, Relakis J, Mylonas C, et al. Den humanistiske og økonomiske byrde ved venøs tromboemboli hos kræftpatienter: en systematisk gennemgang. Blodkoagulfibrinolyse 2015; 26:13-31.
- Kuderer NM, Ortel TL, Francis. Virkning af venøs tromboembolisme og antikoagulation på kræft og kræftoverlevelse. J Clin Oncol 2009; 27: 4902-11.
- Khorana AA, Francis CULAKOVA E, KUDERER NM, Lyman GH. Tromboembolisme er en førende dødsårsag hos kræftpatienter, der får ambulant kemoterapi. J Thromb Haemost 2007; 5: 632-4.
- Prandoni P, Lensing av, Piccioli A, et al. Tilbagevendende venøs tromboembolisme og blødningskomplikationer under antikoagulantbehandling hos patienter med kræft og venøs trombose. Blod 2002; 100:3484-8.
- Lyman GH, Bohlke K, Khorana AA, et al. Venøs tromboemboli profylakse og behandling hos patienter med kræft: american society of clinical oncology klinisk praksis retningslinje opdatering 2014. J Clin Oncol 2015; 33: 654-6.
- Streiff MB, Holmstrom B, Ashrani A, et al. Kræftassocieret Venøs Tromboembolisk Sygdom, Version 1.2015. J Natl Compr Canc Netto 2015; 13: 1079-95.
- Lee AY, Levine MN, Baker RI, et al. Heparin med lav molekylvægt versus et coumarin til forebyggelse af tilbagevendende venøs tromboemboli hos patienter med kræft. N Engl J Med 2003; 349: 146-53.
- Lee AY, Kamphuisen PV, Meyer G, et al. Behandling af akut venøs tromboemboli hos patienter med aktiv Cancer: et randomiseret klinisk forsøg. JAMA 2015; 314: 677-86.
- Carrier M, Cameron C, Delluc A, Castellucci L, Khorana AA, Lee AY. Effektivitet og sikkerhed af antikoagulant terapi til behandling af akut cancer-associeret trombose: systematisk gennemgang og meta-analyse. Thromb Res 2014; 134:1214-9.
- van Es N, Coppens M, Schulman s, Middeldorp S, B Larrller HR. direkte orale antikoagulantia sammenlignet med vitamin K-antagonister til akut venøs tromboemboli: bevis fra fase 3-forsøg. Blod 2014; 124:1968-75.
- Vedovati mc, Germini F, Agnelli G, Becattini C. direkte orale antikoagulantia hos patienter med VTE og kræft: en systematisk gennemgang og metaanalyse. Bryst 2015; 147:475-83.
- Kearon C, Akl EA, Ornelas J, et al. Antitrombotisk terapi mod VTE-sygdom: Bryst retningslinje og ekspert Panel rapport. Bryst 2016; 149:315-52.
- Agnelli G, B Lartller HR, Cohen A, et al. Til behandling af venøs tromboemboli hos cancerpatienter: resultater fra AMPLIFY-forsøget. J Thromb Hæmost 2015; 13: 2187-91.
- Prins MH, Brighton TA, et al. Til behandling af symptomatisk venøs tromboemboli hos patienter med cancer (EINSTEIN-DVT og EINSTEIN-PE): en samlet undergruppeanalyse af to randomiserede kontrollerede forsøg. Lancet Haematol 2014; 1: e37-46.
- Raskob GE, van Es N, Segers A, et al. Resultater fra en non-inferioritetsundergruppeanalyse af Hokusai-VTE randomiseret, dobbeltblind, dobbelt-dummy undersøgelse. Lancet Haematol 2016; 3: e379-87.
- Schulman S, Goldhaber s, Kearon C, et al. Behandling med dabigatran eller varfarin hos patienter med venøs tromboemboli og kræft. Thromb Haemost 2015; 114: 150-7.
kliniske emner: Anticoagulation Management, Arrhythmias and Clinical EP, Cardio-Oncology, Pulmonary Hypertension and Venous Thromboembolism, Anticoagulation Management and Atrial Fibrillation, Anticoagulation Management and Venothromboembolism, Atrial Fibrillation/Supraventricular Arrhythmias
Keywords: Antikoagulanter, international normaliseret Ratio, Acenocoumarol, Dalteparin, Antithrombiner, venøs tromboembolisme, risikofaktorer, atrieflimren, ambulante patienter, forskningspersonale, livskvalitet, Pyridoner, Pyrasoler, pyridiner, Thiasoler, venøs trombose, lungeemboli, trombose, trombocytopeni, comorbiditet, hæmostase, neoplasmer
< tilbage til lister