Holger J Schrisnemann, Julian PT Higgins, Gunn E Vist, Paul A Akl, Elie a Akl, Nicole Skoetts, Gordon h Guyatt; på vegne af Cochrane GRADEing Methods Group (tidligere Applicability and Recommendations Methods Group) og Cochrane Statistical Methods Group
- nøglepunkter:
- 14.1 ‘oversigt over fund’ tabeller
- 14.1.1 Introduktion til ‘Oversigt over fund’ tabeller
- 14.1.2 valg af resultater for ‘Oversigt over fund’ tabeller
- 14.1.3 generel skabelon til’ oversigt over fund ‘ – tabeller
- 14.1.4 udarbejdelse af tabeller
- 14.1.5 statistiske overvejelser i ‘resume af fund’ tabeller
- 14.1.5.1 dikotomiske resultater
- 14.1.5.2 resultater fra tid til begivenhed
- 14.1.6 detaljeret indhold af en ‘oversigt over fund’ tabel
- 14.1.6.1 Tabeltitel og overskrift
- 14.1.6.2 resultater
- 14.1.6.3 bedste skøn over risiko med komparatorintervention
- 14.1.6.4 risiko med intervention
- 14.1.6.5 risikoforskel
- 14.1.6.6 relativ effekt (95% CI)
- 14.1.6.7 antal deltagere (undersøgelser)
- 14.1.6.8 bevisets sikkerhed (karakter)
- 14.1.6.9 Kommentarer
- 14.1.6.10 forklaringer
- 14.2 vurdering af sikkerheden eller kvaliteten af et bevismateriale
- 14.2.1 GRADE-tilgangen
nøglepunkter:
- en oversigt over resultater for en given sammenligning af interventioner indeholder nøgleoplysninger om størrelsen af de relative og absolutte virkninger af de undersøgte interventioner, mængden af tilgængelig evidens og sikkerheden (eller kvaliteten) af tilgængelig evidens.
- ‘oversigt over resultater’ tabeller indeholder en række for hvert vigtigt resultat (op til maksimalt syv). Accepterede formater af’ Oversigt over fund ‘ tabeller og interaktive ‘oversigt over fund’ tabeller kan fremstilles ved hjælp af GRADE ‘ s program GRADEpro GDT.
- Cochrane har vedtaget KARAKTERMETODEN (klassificering af anbefalinger vurdering, udvikling og evaluering) til vurdering af sikkerhed (eller kvalitet) af et bevismateriale.
- KARAKTERMETODEN specificerer fire niveauer af sikkerhed for et bevismateriale for et givet resultat: højt, moderat, lavt og meget lavt.
- karaktervurderinger af sikkerhed bestemmes ved overvejelse af fem domæner: risiko for bias, inkonsekvens, indirektehed, upræcision og publikationsforstyrrelse. For bevis fra ikke-randomiserede undersøgelser og sjældent randomiserede undersøgelser kan vurderinger derefter opgraderes gennem overvejelse af yderligere tre domæner.
Citer dette kapitel som: Schristnemann HJ, Higgins JPT, Vist GE, Glassiou P, AKL EA, skoets N, Guyatt GH. Kapitel 14: udfyldelse af tabeller over resultater og klassificering af bevissikkerheden. I: Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, side MJ, va (redaktører). Cochrane-håndbog til systematiske gennemgange af interventioner version 6.2 (opdateret Februar 2021). Cochrane, 2021. Tilgængelig fra DK.uddannelse.cochrane.org/handbook.
14.1 ‘oversigt over fund’ tabeller
14.1.1 Introduktion til ‘Oversigt over fund’ tabeller
‘oversigt over fund’ tabeller præsenterer de vigtigste fund i en gennemgang i et gennemsigtigt, struktureret og simpelt tabelformat. De giver navnlig vigtige oplysninger om evidensens sikkerhed eller kvalitet (dvs.tilliden eller sikkerheden i intervallet for et effektestimat eller en sammenhæng), størrelsen af effekten af de undersøgte interventioner og summen af tilgængelige data om de vigtigste resultater. Cochrane-anmeldelser bør inkorporere’ oversigt over fund ‘- tabeller under planlægning og offentliggørelse og bør have mindst en vigtig’ oversigt over fund ‘ – tabel, der repræsenterer de vigtigste sammenligninger. Nogle anmeldelser kan omfatte mere end en’ oversigt over fund ‘ – tabel, for eksempel hvis gennemgangen vedrører mere end en større sammenligning, eller inkluderer væsentligt forskellige populationer, der kræver separate tabeller (f.eks. fordi virkningerne er forskellige, eller det er vigtigt at vise resultater separat). I Cochrane Database of Systematic gennemgange (CDSR), den vigtigste ‘oversigt over resultater’ tabel over en gennemgang vises i begyndelsen, før afsnittet Baggrund. Andre’ oversigt over resultater ‘ tabeller vises mellem resultaterne og Diskussionsafsnittene.
14.1.2 valg af resultater for ‘Oversigt over fund’ tabeller
planlægning af tabellen ‘oversigt over fund’ starter tidligt i den systematiske gennemgang med udvælgelsen af de resultater, der skal medtages i: (i) gennemgangen og (ii) tabellen ‘oversigt over fund’. Dette er et afgørende skridt, og en, der gennemgår forfattere nødt til at tage fat omhyggeligt.
for at sikre produktion af optimalt nyttige oplysninger begynder Cochrane-anmeldelser med at udvikle et gennemgangsspørgsmål og ved at liste alle de vigtigste resultater, der er vigtige for patienter og andre beslutningstagere (se Kapitel 2 og kapitel 3). 14.2) definerer og operationaliserer en vurderingsproces, der hjælper med at adskille resultater i dem, der er kritiske, vigtige eller ikke vigtige for beslutningstagningen. Høring og feedback om revisionsprotokollen, herunder fra forbrugere og andre beslutningstagere, kan forbedre denne proces.
kritiske resultater vil sandsynligvis omfatte klart vigtige endepunkter; typiske eksempler inkluderer dødelighed og større sygelighed (såsom slagtilfælde og myokardieinfarkt). De kan dog også repræsentere hyppige mindre og sjældne større bivirkninger, symptomer, livskvalitet, byrder forbundet med behandling og ressourceproblemer (omkostninger). Byrder repræsenterer indvirkningen af sundhedsbyrden på patientens funktion og trivsel og inkluderer kravene til at overholde en intervention, som patienter eller plejere (f.eks. familie) kan ikke lide, såsom at skulle gennemgå hyppigere test eller de begrænsninger i livsstil, som visse interventioner kræver (Spencer-Bonilla et al 2017).
ofte, når man formulerer spørgsmål, der inkluderer alle patientvigtige resultater til beslutningstagning, vil gennemgangsforfattere konfrontere rapporter om undersøgelser, der ikke har inkluderet alle disse resultater. Dette gælder især for negative resultater. For eksempel kan randomiserede forsøg bidrage med bevis for tilsigtede virkninger og på hyppige, relativt mindre bivirkninger, men ikke rapportere om sjældne bivirkninger såsom selvmordsforsøg. Kapitel 19 diskuterer strategier til håndtering af bivirkninger. For at få data for alle vigtige resultater kan det være nødvendigt at undersøge resultaterne af ikke-randomiserede undersøgelser (se Kapitel 24). Cochrane har i samarbejde med andre udviklet vejledning til gennemgangsforfattere til støtte for deres beslutning om, hvornår de skal kigge efter og inkludere ikke-randomiserede undersøgelser (Sch Hell et al 2013).
hvis en gennemgang kun inkluderer randomiserede forsøg, adresserer disse forsøg muligvis ikke alle vigtige resultater, og det er muligvis ikke muligt at tackle disse resultater inden for begrænsningerne i gennemgangen. Anmeldelsesforfattere bør anerkende disse begrænsninger og gøre dem gennemsigtige for læserne. Anmeldelsesforfattere opfordres til at inkludere ikke-randomiserede undersøgelser for at undersøge sjældne eller langsigtede bivirkninger, der muligvis ikke undersøges tilstrækkeligt i randomiserede forsøg. Dette rejser muligheden for, at skaderesultater kan komme fra undersøgelser, hvor deltagerne adskiller sig fra dem i undersøgelser, der anvendes til analyse af fordel. Anmeldelsesforfattere skal derefter overveje, hvor meget sådanne forskelle sandsynligvis vil påvirke resultaterne, og dette vil påvirke evidenssikkerheden på grund af bekymringer om indirektehed relateret til befolkningen (se Afsnit 14.2.2).
ikke-randomiserede undersøgelser kan give vigtig information, ikke kun når randomiserede forsøg ikke rapporterer om et resultat, eller randomiserede forsøg lider af indirektehed, men også når beviserne fra randomiserede forsøg vurderes som meget lave, og ikke-randomiserede undersøgelser giver bevis for højere sikkerhed. Yderligere diskussion af disse spørgsmål fremgår også af kapitel 24.
14.1.3 generel skabelon til’ oversigt over fund ‘ – tabeller
der er udviklet flere alternative standardversioner af ‘Oversigt over fund’ – tabeller for at sikre konsistens og brugervenlighed på tværs af anmeldelser, inkludering af de vigtigste oplysninger, som beslutningstagere har brug for, og optimal præsentation (se eksempler på figur 14.1.a og 14.1.b). Disse formater understøttes af forskning, der fokuserer på forbedret forståelse af de oplysninger, de har til hensigt at formidle (Carrasco-Labra et al 2016, Langendam et al 2016, Santesso et al 2016). De er tilgængelige via GRADE officielle programpakke udviklet til at understøtte GRADE tilgang: GRADEpro GDT (www.gradepro.org).
standard Cochrane ‘oversigt over fund’ tabeller indeholder følgende elementer ved hjælp af et af de accepterede formater. Yderligere vejledning om hver af disse findes i afsnit 14.1.6.
- en kort beskrivelse af befolkningen og indstillingen adresseret af de tilgængelige beviser (som kan være lidt anderledes end eller snævrere end dem, der er defineret i gennemgangsspørgsmålet).
- en kort beskrivelse af sammenligningen behandlet i tabellen ‘oversigt over fund’, herunder både eksperimentelle og sammenligningsinterventioner.
- en liste over de mest kritiske og/eller vigtige sundhedsresultater, både ønskelige og uønskede, begrænset til syv eller færre resultater.
- et mål for den typiske byrde for hvert resultat (f.eks. illustrativ risiko eller illustrativt gennemsnit ved komparatorintervention).
- den absolutte og relative effektstørrelse målt for hver (hvis begge er passende).
- antallet af deltagere og undersøgelser, der bidrager til analysen af hvert resultat.
- en KARAKTERVURDERING af den samlede sikkerhed for bevismaterialet for hvert resultat (som kan variere efter resultat).
- plads til kommentarer.
- forklaringer (tidligere kendt som fodnoter).
ideelt set understøttes ‘oversigt over fund’ – tabeller af mere detaljerede tabeller (kendt som ‘evidensprofiler’), som gennemgangen kan knyttes til, som giver mere detaljerede forklaringer. Evidensprofiler inkluderer de samme vigtige sundhedsresultater og giver større detaljer end ‘oversigt over fund’ tabeller over begge de individuelle overvejelser, der indgår i klassificeringen af sikkerhed og resultaterne af undersøgelserne (Guyatt et al 2011a). De sikrer, at der anvendes en struktureret tilgang til vurdering af bevissikkerheden. Selvom de sjældent offentliggøres i Cochrane-anmeldelser, evidensprofiler bruges ofte, for eksempel, af retningslinjeudviklere til at overveje bevissikkerheden til støtte for retningslinjeanbefalinger. Anmeldelsesforfattere vil finde det lettere at udvikle tabellen ‘oversigt over fund’ ved at udfylde vurderingen af bevissikkerheden i bevisprofilen først i GRADEpro GDT. De kan derefter automatisk konvertere dette til et af formaterne’ oversigt over fund ‘i GRADEpro GDT, herunder en interaktiv’ oversigt over fund ‘ til offentliggørelse.
som et mål for effektens størrelse for dikotomiske resultater skal tabellen ‘oversigt over fund’ give et relativt mål for effekt (f.eks. risikoforhold, oddsforhold, fare) og målinger af absolut risiko. For andre typer data kan en absolut foranstaltning alene (såsom en forskel i midler til kontinuerlige data) være tilstrækkelig. Det er vigtigt, at effektstørrelsen præsenteres på en meningsfuld måde, hvilket kan kræve en vis transformation af resultatet af en metaanalyse (se også Kapitel 15, afsnit 15.4 og afsnit 15.5). Anmeldelser med mere end en hovedsammenligning bør indeholde en separat ‘oversigt over fund’ – tabel for hver sammenligning.
figur 14.1.A giver et eksempel på en ‘oversigt over fund’ tabel. Figur 15.1.B giver et alternativt format, der yderligere kan lette brugernes forståelse og fortolkning af undersøgelsens resultater. Dokumentation, der evaluerer forskellige formater, antyder, at tabellen’ oversigt over fund ‘ bør indeholde en risikoforskel som et mål for den absolutte effekt, og forfattere bør helst bruge et format, der inkluderer en risikoforskel .
en detaljeret beskrivelse af indholdet i en oversigt over resultater fremgår af afsnit 14.1.6.
figur 14.1.et eksempel på en’ oversigt over fund ‘ tabel
oversigt over fund (for interaktiv version Klik her)
|
kompressionsstrømper sammenlignet med ingen kompressionsstrømper til folk, der tager lange flyvninger |
||||||
|
patienter eller befolkning: enhver, der tager en lang flyvning (varer mere end 6 timer) indstillinger: international flyrejser Intervention: kompression stockingsa sammenligning: uden strømper |
||||||
|
resultater |
Illustrative sammenlignende risici* (95% CI) |
relativ effekt (95% CI) |
antal deltagere (undersøgelser) |
bevisets sikkerhed (karakter) |
||
|
antaget risiko |
tilsvarende risiko |
|||||
|
uden strømper |
med strømper |
|||||
|
symptomatisk dyb venetrombose (DVT) |
se kommentar |
se kommentar |
ikke estimerbar |
(9 undersøgelser) |
se kommentar |
0 deltagerne udviklede symptomatisk DVT i disse undersøgelser |
|
symptomløs DVT |
lav risiko befolkningb |
RR 0.10 (0.04 til 0.26) |
(9 undersøgelser) |
⊕⊕⊕⊕ høj |
||
|
10 per 1000 |
1 per 1000 (0 til 3) |
|||||
|
høj risiko befolkningb |
||||||
|
20 per 1000 |
2 per 1000 (1 til 8) |
|||||
|
overfladisk venetrombose |
13 per 1000 |
6 per 1000 (2 til 15) |
RR 0.45 (0.18 til 1.13) |
(8 undersøgelser) |
⊕⊕⊕◯ Moderatec |
|
|
ødem værdier efter flyvning målt på en skala fra 0, intet ødem, til 10, maksimalt ødem |
den gennemsnitlige ødemscore varierede på tværs af kontrolgrupper fra 6 til 9 |
den gennemsnitlige ødemscore i interventionsgrupperne var i gennemsnit 4, 7 lavere (95% CI -4, 9 til -4.5) |
(6 undersøgelser) |
⊕⊕◯◯ Lavd |
||
|
lungeemboli |
se kommentar |
se kommentar |
ikke estimerbar |
(9 undersøgelser) |
se kommentar |
0 deltagerne udviklede lungeembolus i disse studier |
|
død |
se kommentar |
se kommentar |
ikke estimerbar |
(9 undersøgelser) |
se kommentar |
0 deltagerne døde i disse undersøgelser |
|
bivirkninger |
se kommentar |
se kommentar |
ikke estimerbar |
(4 undersøgelser) |
se kommentar |
tolerabiliteten af strømperne blev beskrevet som meget god uden klager over bivirkninger i 4 undersøgelserf |
|
*grundlaget for den antagne risiko findes i fodnote. Den tilsvarende risiko (og dens 95% konfidensinterval) er baseret på den formodede risiko i interventionsgruppen og den relative effekt af interventionen (og dens 95% CI). CI: konfidensinterval; RR: risikoforhold; lønklasse: lønklasse arbejdsgruppe evidensgrader (se forklaringer). |
||||||
a ALLE strømperne i de ni undersøgelser, der var inkluderet i denne anmeldelse, var kompressionstrømper under knæet. I fire undersøgelser var kompressionsstyrken 20 mmHg til 30 mmHg ved anklen. Det var 10 mmHg til 20 mmHg i de andre fire undersøgelser. Strømper kommer i forskellige størrelser. Hvis en strømpe er for stram omkring knæet, kan det forhindre væsentlig venøs tilbagevenden, der får blodet til at samle sig omkring knæet. Kompressionsstrømper skal monteres korrekt. En strømpe, der er for stram, kan skære ind i huden på en lang flyvning og potentielt forårsage sårdannelse og øget risiko for DVT. Nogle strømper kan være lidt tykkere end normalt benbeklædning og kan være potentielt restriktive med stramt fodslitage. Det er en god ide at bære strømper rundt i huset inden rejsen for at sikre en god, behagelig pasform. Deltagerne sætter deres strømper på to til tre timer før flyvningen i de fleste af undersøgelserne. Tilgængeligheden og omkostningerne ved strømper kan variere.
b to undersøgelser rekrutterede højrisikodeltagere defineret som dem med tidligere episoder af DVT, koagulationsforstyrrelser, svær fedme, begrænset mobilitet på grund af knogler eller ledproblemer, neoplastisk sygdom inden for de foregående to år, store åreknuder eller i en af undersøgelserne deltagere højere end 190 cm og tungere end 90 kg. Incidensen for de syv undersøgelser, der udelukkede højrisikodeltagere, var 1.45% og incidensen for de to undersøgelser, der rekrutterede højrisikodeltagere (med mindst en risikofaktor) var 2,43%. Vi har brugt henholdsvis 10 og 30 pr.1000 til at udtrykke forskellige risikolag.
c konfidensintervallet krydser ingen forskel og udelukker ikke en lille stigning.
d måling af ødem blev ikke valideret (resultatets indirektehed) eller blindet for interventionen (risiko for bias).
e hvis der er meget få eller ingen begivenheder, og antallet af deltagere er stort, kan dommen om bevissikkerheden (især domme om upræcision) være baseret på den absolutte effekt. Her kan sikkerhedsvurderingen betragtes som ‘høj’, hvis resultatet blev vurderet korrekt, og begivenheden faktisk ikke fandt sted hos 2821 undersøgte deltagere.
f ingen af de andre undersøgelser rapporterede bivirkninger bortset fra fire tilfælde af overfladisk venetrombose i åreknuder i knæområdet, der blev komprimeret af den øverste kant af strømpen i en undersøgelse.
figur 14.1.B eksempel på alternativ ‘oversigt over resultater’ tabel
|
oversigt over resultater (for interaktiv version Klik her): |
||||||
|
probiotika sammenlignet med ingen probiotika som et supplement til antibiotika hos børn |
||||||
|
Patient eller befolkning: børn fik antibiotika indstillinger: indlagte og ambulante Intervention: probiotika sammenligning: ingen probiotika |
||||||
|
resultater antal deltagere (undersøgelser) |
Relative virkninger |
forventede absolutte virkninger* (95% CI) |
bevisets sikkerhed |
|||
|
uden probiotika |
med probiotika |
forskel |
||||
|
forekomst af diarre: probiotisk dosis 5 milliarder CFU / dag opfølgning: 10 dage til 3 måneder børn < 5 år |
børn < 5 år |
⊕⊕⊕⊝ moderateb på grund af risiko for bias |
sandsynligvis nedsætter forekomsten af diarre. |
|||
|
1474 (7 undersøgelser) |
RR 0, 41 (0,29 Til 0.55) |
22.3%a |
8.9% (6.5 til 12.2) |
13.4% færre childrena (10,1 til 15.8 færre) |
||
|
børn > 5 år |
børn > 5 år |
⊕⊕⊝⊝ lavb, c på grund af risiko for bias og upræcision |
kan nedsætte forekomsten af diarre. |
|||
|
624 (4 undersøgelser) |
RR 0, 81 (0,53 Til 1.21) |
11.2%a |
9% (5.9 til 13.6) |
2.2% færre childrena (5,3 færre til 2.4 mere) |
||
|
Bivirkningerd opfølgning: 10 til 44 dage 1575 (11 studier) |
1.8%a |
2.3% (0.8 til 3.8) |
0.5% flere bivirkninger (1 færre til 2 flere) |
⊕⊕⊝⊝ lavf, g på grund af risiko for bias og inkonsekvens |
der kan være ringe eller ingen forskel i bivirkninger. |
|
|
varighed af diarre opfølgning: 10 dage til 3 måneder 897 (5 studier) |
den gennemsnitlige varighed af diarre uden probiotika var 4 dage. |
0.6 færre dage (1, 18 til 0, 02 færre dage) |
⊕⊕⊝⊝ jeg på grund af upræcision og inkonsekvens |
kan nedsætte varigheden af diarre. |
||
|
afføring pr. dag opfølgning: 10 dage til 3 måneder 425 (4 studier) |
dag uden probiotika var 2,5 afføring om dagen. |
0.3 færre afføring om dagen (0,6 til 0 færre) |
⊕⊕⊝⊝ lav, k på grund af upræcision og inkonsekvens |
der kan være ringe eller ingen forskel i afføring om dagen. |
||
|
*grundlaget for risikoen i kontrolgruppen (f.eks. median kontrolgruppens risiko på tværs af undersøgelser) findes i fodnoter. Risikoen i interventionsgruppen (og dens 95% konfidensinterval) er baseret på den formodede risiko i sammenligningsgruppen og den relative effekt af interventionen (og dens 95% CI). CI: konfidensinterval; RR: risikoforhold. |
||||||
|
forklaringer en Kontrolgruppes risikoestimater kommer fra samlede skøn over kontrolgrupper. Relativ effekt baseret på tilgængelig caseanalyse b høj risiko for bias på grund af stort tab til opfølgning. C upræcision på grund af få begivenheder og konfidensintervaller inkluderer mærkbar fordel eller skade. D bivirkninger: udslæt, kvalme, flatulens, opkastning, øget slim, brystsmerter, forstoppelse, smagsforstyrrelser og lav appetit. e risici blev beregnet ud fra poolede risikoforskelle. f høj risiko for bias. Kun 11 ud af 16 forsøg rapporterede om bivirkninger, hvilket tyder på en selektiv rapporteringsforstyrrelse. g alvorlig inkonsekvens. Talrige probiotiske midler og doser blev evalueret blandt et relativt lille antal forsøg, hvilket begrænsede vores evne til at drage konklusioner om sikkerheden ved de mange indgivne probiotika og doser. h alvorlig uforklarlig inkonsekvens (stor heterogenitet I2 = 79%, p-værdi , punktsestimater og konfidensintervaller varierer betydeligt). jeg alvorlig upræcision. Den øvre grænse på 0,02 færre dage med diarre anses ikke for patientvigtig. J alvorlig uforklarlig inkonsekvens (stor heterogenitet I2 = 78%, p-værdi , punktsestimater og konfidensintervaller varierer betydeligt). K alvorlig upræcision. 95% konfidensintervallet inkluderer ingen effekt, og nedre grænse på 0,60 afføring pr. |
||||||
14.1.4 udarbejdelse af tabeller
GRADE-arbejdsgruppens program, GRADEpro GDT (www.gradepro.org), herunder GRADE interaktive håndbog, er til rådighed til at hjælpe gennemgang forfattere i udarbejdelsen af ‘Oversigt over resultater’ tabeller. GRADEpro kan bruge data om sammenligningsgruppens risiko og effektestimatet (indtastet af anmeldelsesforfatterne eller importeret fra filer genereret i RevMan) til at producere de relative effekter og absolutte risici forbundet med eksperimentelle interventioner. Derudover fører det brugeren gennem processen med en KARAKTERVURDERING og producerer en tabel, der kan bruges som en enkeltstående tabel i en gennemgang (inklusive ved direkte import til programmer som f.eks RevMan eller integration med RevMan) eller en interaktiv ‘oversigt over fund’ tabel (se hjælpressourcer i GRADEpro).
14.1.5 statistiske overvejelser i ‘resume af fund’ tabeller
14.1.5.1 dikotomiske resultater
‘resume af fund’ tabeller skal omfatte både absolutte og relative målinger af effekt for dikotomiske resultater. Risikoforhold, oddsforhold og risikoforskelle er forskellige måder at sammenligne to grupper med dikotom resultatdata (se Kapitel 6, afsnit 6.4.1). Desuden er der to forskellige risikoforhold, afhængigt af hvilken hændelse (f.eks. ‘ja’ eller ‘nej’), der er fokus for analysen (se Kapitel 6, afsnit 6.4.1.5). I nærvær af en ikke-nul interventionseffekt risikerer enhver variation på tværs af undersøgelser i komparatorgruppen (dvs. variation i risikoen for, at begivenheden finder sted uden indblanding af interesse, for eksempel i forskellige populationer) gør det umuligt for mere end en af disse foranstaltninger at være virkelig den samme i hver undersøgelse.
det har længe været antaget i epidemiologi, at relative effektmål er mere konsistente end absolutte effektmål fra et scenarie til et andet. Der er empiriske beviser til støtte for denne antagelse (Engels et al 2000, Deeks and Altman 2001, Furuka et al 2002). Af denne grund bør metaanalyser generelt bruge enten et risikoforhold eller et odds-forhold som et mål for effekt (se Kapitel 10, afsnit 10.4.3). Tilsvarende er et enkelt skøn over relativ effekt sandsynligvis et mere passende sammendrag end et enkelt skøn over absolut effekt. Hvis en relativ effekt faktisk er konsistent på tværs af undersøgelser, vil forskellige sammenligningsgrupperisici have forskellige implikationer for absolut fordel. For eksempel, hvis risikoforholdet er konsekvent 0.75, så ville den eksperimentelle intervention reducere en komparatorgrupperisiko på 80% til 60% i interventionsgruppen (en absolut risikoreduktion på 20 procentpoint), men ville også reducere en komparatorgrupperisiko på 20% til 15% i interventionsgruppen (en absolut risikoreduktion på 5 procentpoint).
‘oversigt over fund’ tabeller er bygget op omkring antagelsen om en konsistent relativ effekt. Det er derfor vigtigt at overveje konsekvenserne af denne effekt for forskellige sammenligningsgrupperisici (disse kan udledes eller estimeres ud fra en række kilder, Se afsnit 14.1.6.3), som kan kræve en vurdering af bevissikkerheden for prognostiske beviser (Spencer et al 2012, Iorio et al 2015). For enhver sammenligningsgrupperisiko er det muligt at estimere en tilsvarende interventionsgrupperisiko (dvs.den absolutte risiko med interventionen) ud fra det meta-analytiske risikoforhold eller odds-forhold. Bemærk, at tallene i kolonnen ’tilsvarende risiko’ er specifikke for ‘risiciene’ i den tilstødende kolonne.
for meta-analytisk risikoforhold (RR) og antaget komparatorrisiko (ACR) opnås den tilsvarende interventionsrisiko som:
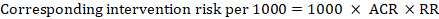 .
.
som et eksempel i figur 14.1.A, det meta-analytiske risikoforhold for symptomløs dyb venetrombose (DVT) er RR = 0,10 (95% CI 0,04 til 0,26). Hvis vi antager en komparatorrisiko på ACR = 10 pr. 1000 = 0,01, opnår vi:
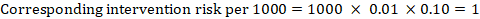 .
.
for den meta-analytiske odds ratio (OR) og antagede sammenligningsrisiko, ACR, opnås den tilsvarende interventionsrisiko som:
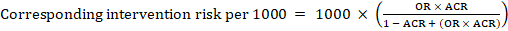 .
.
øvre og nedre konfidensgrænser for den tilsvarende interventionsrisiko opnås ved at erstatte henholdsvis RR eller eller med deres øvre og nedre konfidensgrænser (f.eks. erstatte 0.10 med 0,04, derefter med 0,26, i eksemplet). Sådanne konfidensintervaller omfatter ikke usikkerhed i de formodede sammenligningsrisici.
når man beskæftiger sig med risikoforhold, er det kritisk, at den samme definition af ‘begivenhed’ bruges som anvendt til metaanalysen. For eksempel, hvis metaanalysen fokuserede på ‘død’ (i modsætning til overlevelse) som begivenheden, skal tilsvarende risici i tabellen ‘oversigt over fund’ også henvise til ‘død’.
under (sjældne) omstændigheder, hvor der er klar begrundelse for at antage en konsekvent risikoforskel i metaanalysen, er det i princippet muligt at præsentere dette for relevante ‘antagne risici’ og deres tilsvarende risici og at præsentere de tilsvarende (forskellige) relative virkninger for hver antaget risiko.
risikoforskellen udtrykker forskellen mellem ACR og den tilsvarende interventionsrisiko (eller forskellen mellem den eksperimentelle og komparatorinterventionen).
for meta-analytisk risikoforhold (RR) og antaget komparatorrisiko (ACR) opnås den tilsvarende risikoforskel som (bemærk, at risici Også kan udtrykkes ved hjælp af procent eller procentpoint):
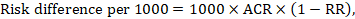
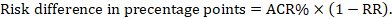
som et eksempel i figur 14.1.B det meta-analytiske risikoforhold er 0,41 (95% CI 0,29 til 0,55) for diarre hos børn under 5 år. Hvis vi antager en sammenligningsgrupperisiko på 22,3%, opnår vi:
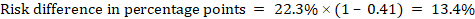 .
.
for meta-analytisk odds ratio (OR) Og antaget sammenligningsrisiko (ACR) opnås den absolutte risikoforskel som (procentpoint):
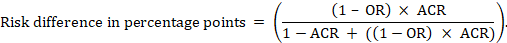
øvre og nedre konfidensgrænser for den absolutte risikoforskel opnås ved at køre ovenstående beregning igen, mens henholdsvis RR eller eller erstattes af deres øvre og nedre konfidensgrænser (f.eks. erstatte 0,41 med 0,28 og derefter med 0,55 i eksemplet). Sådanne konfidensintervaller omfatter ikke usikkerhed i de formodede sammenligningsrisici.
14.1.5.2 resultater fra tid til begivenhed
resultater fra tid til begivenhed måler, om og hvornår en bestemt begivenhed (f.eks. død) forekommer (van Dalen et al 2007). Virkningen af den eksperimentelle intervention i forhold til sammenligningsgruppen på resultater fra tid til begivenhed måles normalt ved hjælp af et fareforhold (HR) (se Kapitel 6, afsnit 6.8.1).
et fareforhold udtrykker et relativt effektestimat. Det kan anvendes på forskellige måder til at opnå absolutte risici og andre fortolkelige mængder for en bestemt population. Her beskriver vi, hvordan man udtrykker fareforhold i form af: (i) absolut risiko for hændelsesfri overlevelse inden for en bestemt tidsperiode; (ii) absolut risiko for en begivenhed inden for en bestemt tidsperiode; og (iii) mediantid til begivenheden. Alle metoder er bygget på en antagelse om ensartede relative effekter (dvs.at fareforholdet ikke varierer over tid).
(i) absolut risiko for hændelsesfri overlevelse inden for en bestemt tidsperiode hændelsesfri overlevelse (f.eks. samlet overlevelse) rapporteres almindeligvis af individuelle studier. For at opnå absolutte effekter for time-to-event-resultater målt som hændelsesfri overlevelse kan den sammenfattende HR bruges sammen med en antaget andel af patienter, der er hændelsesfrie i komparatorgruppen (Tierney et al 2007). Denne andel af patienterne vil være specifik for en periode med observation. Det er dog ikke strengt nødvendigt at specificere denne tidsperiode. For eksempel kan en andel på 50% af hændelsesfrie patienter gælde for patienter med en høj hændelsesfrekvens observeret over 1 år eller for patienter med en lav hændelsesfrekvens observeret over 2 år.

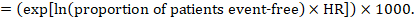
Antag for eksempel, at det meta-analytiske fareforhold er 0,42 (95% CI 0,25 til 0,72). Forudsat en komparator gruppe risiko for hændelsesfri overlevelse (f. eks. for samlet overlevelse mennesker er i live) ved 2 års ACR = 900 per 1000 = 0.9 vi opnår:

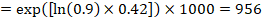
så at 956 per 1000 mennesker vil være i live med den eksperimentelle intervention på 2 år. Afledningen af risikoen skal forklares i en kommentar eller fodnote.
(ii) absolut risiko for en begivenhed inden for en bestemt periode for at opnå denne absolutte effekt, igen kan resumeet HR bruges (Tierney et al 2007):

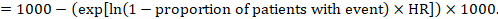
Antag i eksemplet, at vi antager en komparatorgrupperisiko for begivenheder (f.eks. for dødelighed, mennesker er døde) ved 2 års ACR = 100 pr. 1000 = 0,1. Vi får:

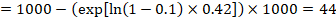
så at 44 per 1000 mennesker vil være døde med den eksperimentelle intervention på 2 år.
(iii) Mediantid til begivenheden i stedet for absolutte tal kan tiden til begivenheden i interventions-og sammenligningsgrupperne udtrykkes som median overlevelsestid i måneder eller år. For at opnå median overlevelsestid kan den samlede HR anvendes på en antaget median overlevelsestid i komparatorgruppen (Tierney et al 2007):
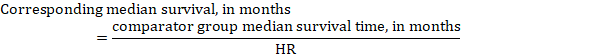
i eksemplet, under forudsætning af en komparatorgruppe median overlevelsestid på 80 måneder, vi opnår:
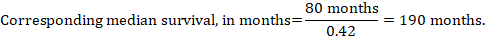
for alle tre af disse muligheder for at udtrykke resultaterne af Time-to-event-analyser igen opnås øvre og nedre konfidensgrænser for den tilsvarende interventionsrisiko ved at erstatte HR med henholdsvis dens øvre og nedre konfidensgrænser (f.eks. erstatte 0,42 med 0,25 og derefter med 0,72 i eksemplet). Igen, som for dikotom resultater, omfatter sådanne konfidensintervaller ikke usikkerhed i de antagede sammenligningsgrupperisici. Dette er særlig bekymrende for langvarig overlevelse med en lav eller moderat dødelighed og et tilsvarende stort antal censurerede patienter (dvs.et lavt antal patienter under risiko og en høj censureringsrate).
14.1.6 detaljeret indhold af en ‘oversigt over fund’ tabel
14.1.6.1 Tabeltitel og overskrift
titlen på hver ‘oversigt over fund’ tabel skal specificere sundhedsspørgsmålet, indrammet med hensyn til befolkningen og gøre det klart nøjagtigt, hvilken sammenligning af interventioner der foretages. I Figur 14.1.a, befolkningen er mennesker, der tager lange flyflyvninger, interventionen er kompressionsstrømper, og kontrollen er ingen kompressionsstrømper.
de første rækker i hver ‘oversigt over fund’ – tabel skal give følgende ‘overskrift’ – information:
patienter eller population dette præciserer yderligere populationen (og muligvis underpopulationerne) af interesse og ideelt set størrelsen af risikoen for det mest afgørende negative resultat, som en intervention er rettet mod. For eksempel, mennesker på en langdistanceflyvning kan have forskellige risici for DVT; de, der bruger selektive serotoningenoptagelsesinhibitorer (SSRI ‘ er), kan have en anden risiko for bivirkninger; mens de med atrieflimren kan have lav (< 1%), moderat (1% til 4%) eller høj (> 4%) årlig risiko for slagtilfælde.
Indstilling af dette skal angive eventuelle specifikke karakteristika ved indstillingerne for sundhedsspørgsmålet, der kan begrænse anvendeligheden af resumeet af fund til andre indstillinger (f.eks. primærpleje i Europa og Nordamerika).
Intervention den eksperimentelle intervention.
sammenligning sammenligningsinterventionen (inklusive ingen specifik intervention).
14.1.6.2 resultater
rækkerne i en ‘oversigt over fund’ – tabel skal indeholde alle ønskelige og uønskede sundhedsresultater (anført i rækkefølge efter betydning), der er essentielle for beslutningstagning, op til maksimalt syv resultater. Hvis der er flere resultater i gennemgangen, skal anmeldelsesforfattere udelade de mindre vigtige resultater fra tabellen, og beslutningen om at vælge, hvilke resultater der er kritiske eller vigtige for gennemgangen, skal foretages under protokoludvikling (se Kapitel 3). Anmeldelsesforfattere bør angive tidsrammer for måling af resultaterne (f.eks. 90 dage eller 12 måneder) og typen af instrumentresultater (f. eks. fra 0 til 100).
Bemærk, at anmeldelsesforfattere skal medtage de forud specificerede kritiske og vigtige resultater i tabellen, om data er tilgængelige eller ej. De bør dog være opmærksomme på muligheden for, at betydningen af et resultat (f.eks. en alvorlig negativ virkning) først bliver kendt, efter at protokollen er skrevet, eller analysen er udført, og bør træffe passende foranstaltninger for at medtage disse i tabellen over resultater.
tabellen ‘oversigt over fund’ kan omfatte effekter i undergrupper af populationen for forskellige sammenligningsrisici og effektstørrelser separat. For eksempel i figur 14.1.B-effekter præsenteres for børn yngre og ældre end 5 år separat. Anmeldelsesforfattere kan også vælge at udarbejde separate’ resume af fund ‘ – tabeller for forskellige populationer.
Anmeldelsesforfattere bør inkludere alvorlige bivirkninger, men det kan være muligt at kombinere mindre bivirkninger som et enkelt resultat og beskrive dette i en forklarende fodnote (bemærk, at det ikke er hensigtsmæssigt at tilføje begivenheder sammen, medmindre de er uafhængige, dvs.en deltager, der har oplevet en bivirkning, har en upåvirket chance for at opleve den anden bivirkning).
resultater målt på flere tidspunkter repræsenterer et særligt problem. Generelt, for at holde tabellen enkel, anmeldelsesforfattere bør kun præsentere flere tidspunkter for resultater, der er kritiske for beslutningstagning, hvor enten resultatet eller den trufne beslutning sandsynligvis vil variere over tid. Resten skal præsenteres på et fælles tidspunkt, hvor det er muligt.
Anmeldelsesforfattere kan præsentere løbende resultatmål i tabellen ‘oversigt over fund’ og bør bestræbe sig på at gøre disse fortolkelige for målgruppen. Dette kræver, at enhederne er klare og let fortolkelige, for eksempel smertedage eller hyppighed af hovedpine, og navnet og skalaen på de anvendte måleværktøjer skal angives (f.eks. en visuel analog skala, der spænder fra 0 til 100). Imidlertid, mange måleinstrumenter kan ikke let fortolkes af ikke-specialiserede klinikere eller patienter, for eksempel, peger på en Beck Depression opgørelse eller livskvalitet score. For disse kan en mere fortolkelig præsentation involvere konvertering af en kontinuerlig til et dikotomt resultat, såsom >50% forbedring (se Kapitel 15, Afsnit 15.5).
14.1.6.3 bedste skøn over risiko med komparatorintervention
Anmeldelsesforfattere bør give op til tre typiske risici for deltagere, der modtager komparatorinterventionen. For dikotomiske resultater anbefaler vi, at disse præsenteres i form af antallet af personer, der oplever begivenheden pr.100 eller 1000 personer (naturlig frekvens) afhængigt af hyppigheden af resultatet. For kontinuerlige resultater angives dette som en middel-eller medianværdi af det målte resultat.
estimerede eller antagede sammenligningsinterventionsrisici kunne baseres på vurderinger af typiske risici i forskellige patientgrupper afledt af selve gennemgangen, individuelle repræsentative undersøgelser i gennemgangen eller risici afledt af en systematisk gennemgang af prognosestudier eller andre evidenskilder, som igen kan kræve en vurdering af sikkerheden for det prognostiske bevis (Spencer et al 2012, Iorio et al 2015). Ideelt set ville risici afspejle grupper, som klinikere let kan identificere på baggrund af deres præsentationsfunktioner.
en forklarende fodnote bør angive kilden eller begrundelsen for hver sammenligningsgrupperisiko, herunder den tidsperiode, som den svarer til, hvor det er relevant. I Figur 14.1.en, klinikere kan let differentiere personer med risikofaktorer for dyb venøs trombose fra dem uden. Hvis der vides at være ringe variation i baseline-risiko, kan gennemgangsforfattere bruge den mediane sammenligningsgrupperisiko på tværs af studier. Hvis typiske risici ikke er kendt, er en mulighed at vælge risikoen fra de inkluderede undersøgelser, hvilket giver den næsthøjeste for en høj og den næstlaveste for en lavrisikopopulation.
14.1.6.4 risiko med intervention
for dikotome resultater skal gennemgangsforfattere give en tilsvarende absolut risiko for hver sammenligningsgrupperisiko sammen med et konfidensinterval. Denne absolutte risiko med den (eksperimentelle) intervention vil normalt være afledt af metaanalyseresultatet præsenteret i kolonnen relativ effekt (Se afsnit 14.1.6.6). Formler findes i afsnit 14.1.5. Anmeldelsesforfattere bør præsentere den absolutte effekt i samme format som risiciene ved sammenligningsintervention (se Afsnit 14.1.6.3), for eksempel som antallet af personer, der oplever begivenheden pr.1000 personer.
for kontinuerlige resultater skal en forskel i middel eller standardiseret forskel i middel præsenteres med dets konfidensinterval. Disse vil typisk blive opnået direkte fra en meta-analyse. Forklarende tekst skal bruges til at afklare betydningen, som i figur 14.1.a og 14.1.b.
14.1.6.5 risikoforskel
for dikotomiske resultater kan risikoforskellen tilvejebringes ved hjælp af et af tabelformaterne ‘oversigt over fund’ som en ekstra mulighed (se figur 14.1.b). Denne risikoforskel udtrykker forskellen mellem den eksperimentelle og komparatorintervention og vil normalt være afledt af metaanalyseresultatet præsenteret i kolonnen relativ effekt (Se afsnit 14.1.6.6). Formler findes i afsnit 14.1.5. Anmeldelsesforfattere skal præsentere risikoforskellen i samme format som antagne og tilsvarende risici med komparatorintervention (se Afsnit 14.1.6.3); for eksempel som antallet af personer, der oplever begivenheden pr.1000 personer eller som procentpoint, hvis de antagne og tilsvarende risici udtrykkes i procent.
for kontinuerlige resultater, hvis tabellen ‘oversigt over fund’ indeholder denne mulighed, kan den gennemsnitlige forskel præsenteres her, og kolonnen ’tilsvarende risiko’ er tom (se figur 14.1.b).
14.1.6.6 relativ effekt (95% CI)
den relative effekt vil typisk være et risikoforhold eller odds ratio (eller lejlighedsvis et risikoforhold) med dets ledsagende 95% konfidensinterval opnået ved en metaanalyse udført på basis af det samme effektmål. Risikoforhold og odds-forhold er ens, når komparatorinterventionsrisikoen er lav, og virkningerne er små, men kan variere betydeligt, når komparatorgruppens risici stiger. Metaanalysen kan involvere en antagelse om enten faste eller tilfældige effekter, afhængigt af hvad gennemgangsforfatterne finder passende, og antyder, at den relative effekt enten er et skøn over effekten af interventionen, eller et skøn over den gennemsnitlige effekt af interventionen på tværs af undersøgelser, henholdsvis.
14.1.6.7 antal deltagere (undersøgelser)
denne kolonne skal indeholde antallet af deltagere vurderet i de inkluderede studier for hvert resultat og det tilsvarende antal undersøgelser, der bidrog med disse deltagere.
14.1.6.8 bevisets sikkerhed (karakter)
Anmeldelsesforfattere bør kommentere bevisets sikkerhed (også kendt som kvaliteten af bevismaterialet eller tilliden til effektestimaterne). Anmeldelsesforfattere bør bruge det specifikke evidensklassificeringssystem udviklet af GRADE-arbejdsgruppen (Atkins et al 2004, Guyatt et al 2008, Guyatt et al 2011a), som er beskrevet detaljeret i afsnit 14.2. Karakteren tilgang kategoriserer sikkerheden i et bevismateriale som ‘høj’, ‘moderat’, ‘lav’ eller ‘meget lav’ efter resultat. Dette er et resultat af dom, men domsprocessen fungerer inden for en gennemsigtig struktur. Som et eksempel ville sikkerheden være’ høj’, hvis sammendraget var af flere randomiserede forsøg med lav risiko for bias, men vurderingen af sikkerhed bliver lavere, hvis der er bekymring for risiko for bias, inkonsekvens, indirektehed, upræcision eller publikationsforstyrrelse. Andre vurderinger end ‘ høj ‘sikkerhed bør gøres gennemsigtige ved hjælp af forklarende fodnoter eller kolonnen’ kommentarer ‘i tabellen’ sammenfatning af resultater ‘ (Se afsnit 14.1.6.10).
14.1.6.9 Kommentarer
formålet med feltet ‘kommentarer’ er at hjælpe med at fortolke de oplysninger eller data, der er identificeret i rækken. For eksempel kan dette være på gyldigheden af resultatmålingen eller tilstedeværelsen af variabler, der er forbundet med effektens størrelse. Vigtige advarsler om resultaterne skal markeres her. Ikke alle rækker har brug for kommentarer, og det er bedst at efterlade et tomt, hvis der ikke er noget, der berettiger en kommentar.
14.1.6.10 forklaringer
detaljerede forklaringer bør medtages som fodnoter til støtte for bedømmelserne i tabellen over resultater, såsom den samlede KARAKTERVURDERING. Forklaringerne skal beskrive begrundelsen for vigtige aspekter af indholdet. Tabel 14.1.en lister vejledning til nyttige forklaringer. Forklaringer skal være koncise, informative, relevante, lette at forstå og nøjagtige. Hvis forklaringer ikke kan beskrives tilstrækkeligt i fodnoter, skal anmeldelsesforfattere give yderligere detaljer om emnerne i resultaterne og Diskussionsafsnittene i gennemgangen.
tabel 14.1.en vejledning til at give nyttige forklaringer i SOF-tabeller. Tilpasset fra Santesso et al (2016)
generel vejledning
- Indtast oplysningerne til læsere direkte i tabellen, hvis det er muligt (f.eks. oplysninger om varigheden af opfølgningen eller den anvendte skala).
- Angiv generelt ikke referencer i forklaringsafsnittet, medmindre der f.eks. er særlige grunde til at give oplysninger om kilder til basisrisici (se punkt 3).
- Angiv kilden til information om de basislinjerisici, der bruges til at beregne absolutte effekter.
- når tabellen er færdig, skal du gennemgå alle forklaringer for at afgøre, om nogle kan henvises til flere gange, hvis de omformuleres eller kombineres.
- Angiv grunde til opgradering og nedgradering af beviserne (se domænespecifik vejledning nedenfor), og brug GRADEpro GDT-programmet til at overholde KVALITETSVEJLEDNINGEN.
- bevismaterialet for et bestemt resultat kan bestemmes at have alvorlige eller meget alvorlige problemer for det berørte domæne (eller kritisk alvorligt for risiko for bias, når ROBINS-i Bruges). Det kan således være nyttigt at angive antallet af niveauer for nedgradering (f.eks. nedgraderet med et niveau for risiko for bias), men undgå gentagelse af, hvad der er i tabellen (og indtrykket af formel eller algoritmisk rapportering). I bevisprofiler findes disse oplysninger allerede i cellerne i tabellen.
- selvom forklaringer om sikkerheden i bevismaterialet primært er nødvendige, når de ændrer sikkerheden, kan du overveje at tilføje en forklaring, når sikkerheden i bevismaterialet ikke er ændret, men når denne beslutning kan stilles spørgsmålstegn ved af andre. Dette vil hjælpe med at forstå årsagerne til uenighed.
- sørg for, at tabellen ikke bruges som en beskrivelse af metoderne til gennemgangen (beskriv f.eks. ikke årsagerne til den statistiske analyse).
- indtast resultater for resultater, der ikke kunne kombineres statistisk i en metaanalyse (dvs. narrative resultater) direkte ind i SoF-tabellen i resultatkolonnerne. En forklaring er muligvis ikke nødvendig for at kommunikere disse resultater. Hvis det anses for gavnligt for det tilsigtede publikum, skal der tilføjes supplerende skøn over interventionseffekter (f.eks. antal, der er nødvendige for at behandle for gavn og skade, risikoforskel udtrykt i procent, kontinuerligt resultat udtrykt i minimale vigtige forskelenheder) i kommentarfeltet.
- brug oplysningerne i forklaringerne om KARAKTERPROCESSEN til at informere andre vigtige dele af gennemgangen, herunder oversigtsversioner og diskussionen.
Domænespecifik vejledning til at skrive nyttige forklaringer
risiko for bias
- beskriv antallet af undersøgelser eller mængden af information, de giver i metaanalysen, der var i høj risiko for bias og for hvilket kriterium.
- brug udtryk som flertal, mindretal, alle, nogle eller ingen; eller antallet af undersøgelser som f.eks.
- for randomiserede forsøg skal du nævne de specifikke kriterier, herunder skjult tildelingssekvens, selektiv resultatrapportering osv. For ikke-randomiserede undersøgelser skal du beskrive kriteriet i det anvendte værktøj (f.eks.
- Angiv, om effekten af risikoen for bias blev undersøgt i en følsomhedsanalyse. Når det er relevant, nævnes bidraget fra undersøgelserne med høj risiko for bias til estimaterne.
- oplysninger om undersøgelsesdesign kan indgå i forklaringerne, især i SoF, når forskellige undersøgelsesdesign er inkluderet.
inkonsekvens
- angiv det mål, der bruges til at bedømme inkonsekvens, såsom den statistiske test eller måling (I2, Chi2, Tau) eller overlapningen af konfidensintervaller eller lighed mellem punktestimater.
- hvis inkonsekvens er baseret på I2, skal du beskrive den som betydelig, væsentlig, moderat eller ikke vigtig.
- hvis relevant, angiv, om heterogenitet blev undersøgt i UNDERGRUPPEANALYSER af PICO (patienter, intervention, sammenligning, resultat), og hvis der er andre potentielle årsager til heterogeniteten.
- i tilfælde af en enkelt undersøgelse for et resultat skal du sige, at der er ‘ingen’ snarere end ‘ikke relevant’.
upræcision
- Angiv, hvor stikprøvestørrelsen eller antallet af begivenheder ikke opfylder den optimale informationsstørrelse som beregnet, eller ‘tommelfingerregler’ (f.eks. 400 begivenheder). Undgå at henvise til antallet af undersøgelser som en grund til upræcision.
- Angiv, om konfidensintervallerne inkluderer muligheden for en lille eller ingen effekt og vigtig fordel eller skade. Hvis det er kendt, angiv den numeriske værdi af tærsklen for vigtig fordel.
- undgå at rapportere resultatet som statistisk eller ikke-statistisk signifikant.
opgradering
- nævn årsagen til opgradering: på grund af stor effekt; en dosis-responsgradient; eller plausibel resterende modstående forvirring øger bevissikkerheden.
- for store effekter skal du rapportere, om den relative effekt er >2 eller > 5. For dosisresponsgradienter skal der gives interventionsniveau og effekt på udfaldet. For domænet ‘plausibel resterende modsatte confounding’, beskrive effekten af den confounding faktor på estimatet.
14.2 vurdering af sikkerheden eller kvaliteten af et bevismateriale
14.2.1 GRADE-tilgangen
grades of Recommendation, Assessment, Development and Evaluation arbejdsgruppe (Grade-arbejdsgruppe) har udviklet et system til klassificering af evidenssikkerheden (Sch Kursnemann et al 2003, Atkins et al 2004, Sch Kursnemann et al 2006, Guyatt et al 2008, Guyatt et al 2011a). Over 100 organisationer, herunder Verdenssundhedsorganisationen (hvem), American College of Physicians, American Society of Hematology( ASH), Canadian Agency for Drugs and Technology in Health (CADTH) og National Institutes of Health and Clinical topkvalitet (NICE) i Storbritannien har vedtaget KARAKTERSYSTEMET (www.gradeworkinggroup.org).
Cochrane har også formelt vedtaget denne tilgang, og alle Cochrane-anmeldelser skal bruge GRADE til at evaluere sikkerheden ved bevis for vigtige resultater (se Mecir-boks 14.2.en).
Mecir rubrik 14.2.relevante forventninger til gennemførelse af interventionsundersøgelser
|
C74: vurdering af bevisets sikkerhed (obligatorisk) |
|
|
Brug de fem karakterovervejelser (risiko for bias, effektkonsistens, upræcision, indirektehed og publikationsforstyrrelse) til at vurdere sikkerheden i bevismaterialet for hvert resultat og til at drage konklusioner om bevissikkerheden i teksten til gennemgangen. |
grad er den mest anvendte tilgang til opsummering af tillid til effekter af interventioner efter resultat på tværs af undersøgelser. Det er bedst at bruge værktøjet online GRADEpro, og at bruge det som beskrevet i programmets hjælpesystem. Dette skal bidrage til at sikre, at forfatterhold får adgang til de samme oplysninger for at informere deres domme. Ideelt set bør to personer, der arbejder uafhængigt, vurdere sikkerheden i bevismaterialet og nå til enighed om eventuelle nedgraderingsbeslutninger. Der bør tages hensyn til de fem lønklasser, uanset om gennemgangen indeholder en oversigt over resultaterne. Det er nyttigt at trække på disse oplysninger i diskussionen, i forfatterens konklusioner og at formidle sikkerheden i beviserne i det abstrakte og almindelige sprogoversigt. |
|
C75: begrundelse for vurdering af bevissikkerheden (obligatorisk) |
|
|
begrunde og dokumentere alle vurderinger af bevisets sikkerhed (f.eks. nedgradering eller opgradering ved hjælp af kvalitet). |
vedtagelsen af en struktureret tilgang sikrer gennemsigtighed i formuleringen af en fortolkning af beviset, og resultatet er mere informativt for brugeren. |
til systematiske gennemgange definerer KARAKTERTILGANGEN sikkerheden ved et bevismateriale som det omfang, i hvilket man kan være sikker på, at et skøn over effekt eller tilknytning er tæt på mængden af specifik interesse. Vurdering af sikkerheden ved et bevismateriale indebærer overvejelse af risiko for bias inden for og på tværs af studiet (begrænsninger i undersøgelsesdesign og udførelse eller metodologisk kvalitet), inkonsekvens (eller heterogenitet), bevisets indirektehed, upræcision af effektestimaterne og risiko for publikationsforstyrrelse (se Afsnit 14.2.2) samt domæner, der kan øge vores tillid til effektestimatet (som beskrevet i afsnit 14.2.3). KARAKTERSYSTEMET indebærer en vurdering af sikkerheden ved et bevismateriale for hvert enkelt resultat. Vurderinger om de domæner, der bestemmer bevissikkerheden, skal beskrives i afsnittet Resultater eller diskussion og som en del af tabellen ‘oversigt over fund’.
KARAKTERMETODEN angiver fire niveauer af sikkerhed (figur 14.2.en). Til interventioner, herunder diagnostiske og andre tests, der evalueres som interventioner (Sch Schrismann et al 2008b, Schrimmemann et al 2008a, Balshem et al 2011, Schrimmemann et al 2012), udgangspunktet for vurdering af bevissikkerheden er kategoriseret i to typer:
- randomiserede forsøg; og
- ikke-randomiserede undersøgelser af interventioner (NRSI), herunder observationsstudier (inklusive men ikke begrænset til kohortestudier og case-control-undersøgelser, tværsnitsstudier, sagsserier og sagsrapporter, selvom ikke alle disse designs normalt er inkluderet i Cochrane-anmeldelser).
der er mange tilfælde, hvor anmeldelsesforfattere er afhængige af oplysninger fra NRSI, især for at evaluere potentielle skader (se Kapitel 24). Derudover kan gennemgangsforfattere få relevante data fra både randomiserede forsøg og NRSI, hvor hver type bevis supplerer den anden (Sch Kristnemann et al 2013).
i lønklasse begynder et bevismateriale fra randomiserede forsøg med en højsikkerhedsvurdering, mens et bevismateriale fra NRSI begynder med en lavsikkerhedsvurdering. Den lavere rating med NRSI er resultatet af den potentielle bias induceret af manglen på randomisering (dvs.confounding og selection bias).
men når man bruger den nye risiko for Bias i ikke-randomiserede undersøgelser af interventioner (ROBINS-i) værktøj (Sterne et al 2016), et vurderingsværktøj, der dækker risikoen for bias på grund af manglende randomisering, kan alle undersøgelser starte som høj sikkerhed for beviserne (Sch Kristnemann et al 2018). Tilgangen til at starte alle undersøgelsesdesign (inklusive NRSI) som høj sikkerhed er ikke i konflikt med den indledende karakter tilgang til at starte vurderingen af NRSI som bevis for lav sikkerhed. Dette skyldes, at et bevismateriale fra NRSI generelt bør nedgraderes med to niveauer på grund af den iboende risiko for bias forbundet med manglen på randomisering, nemlig confounding og selection bias. Ikke nedgradering af NRSI fra høj til lav sikkerhed har brug for gennemsigtig og detaljeret begrundelse for, hvad der mildner bekymringer om forvirring og selektionsforstyrrelse (Sch Schristnemann et al 2018). Meget få eksempler på, hvor ikke rating ned med to niveauer er passende, findes i øjeblikket.
den højeste sikkerhedsvurdering er et bevismateriale, når der ikke er nogen bekymringer i nogen af de KARAKTERFAKTORER, der er anført i figur 14.2.a. Anmeldelsesforfattere nedgraderer ofte beviser til moderate, lave eller endda meget lave sikkerhedsbeviser afhængigt af tilstedeværelsen af de fem faktorer i figur 14.2.normalt vil sikkerhedsvurderingen falde med et niveau for hver faktor, op til maksimalt tre niveauer for alle faktorer. Hvis der er meget alvorlige problemer for et domæne (f. eks. ved vurdering af risiko for bias var alle undersøgelser ikke afsløret, ublindet og tabt over 50% af deres patienter til opfølgning), bevis kan falde med to niveauer på grund af denne faktor alene. Det er ikke muligt at bedømme lavere end ‘meget lav sikkerhed’ beviser.
Anmeldelsesforfattere vil generelt klassificere bevis fra lyd ikke-randomiserede undersøgelser som lav sikkerhed, selvom ROBINS-i Bruges. Hvis sådanne undersøgelser imidlertid giver store effekter, og der ikke er nogen åbenbar bias, der forklarer disse effekter, kan anmeldelsesforfattere bedømme beviset som moderat eller – hvis effekten er stor nok – endda som høj sikkerhed (figur 14.2.en). Det meget lave sikkerhedsniveau er passende til, men er ikke begrænset til, undersøgelser med kritiske problemer og usystematiske kliniske observationer (f.eks.