obecný název: clindamycin fosfát
dávková forma: vaginální krém
lékařsky hodnoceno Drugs.com. Naposledy aktualizováno 1. Března 2020.
- přehled
- nežádoucí účinky
- dávkování
- Profesionální
- interakce
- více
- pro intravaginální použití pouze pro oční, dermální nebo perorální použití
- Cleocin vaginální krém-Klinická farmakologie
- mechanismus účinku
- farmakokinetika
- mikrobiologie
- mechanismus účinku
- rezistence
- antibakteriální aktivita
- indikace a použití pro Cleocin vaginální krém
- kontraindikace
- varování
- bezpečnostní opatření
- Obecné
- informace pro pacienta
- lékové interakce
- karcinogeneze, mutageneze, zhoršení Fertility
- těhotenství
- kojící matky
- pediatrické použití
- geriatrické použití
- nežádoucí účinky
- klinické studie
- předávkování
- Cleocin vaginální krém dávkování a podání
- jak se dodává Cleocin vaginální krém
- klinické studie
- návod k použití
- hlavní zobrazovací PANEL – 40 g štítek zkumavky
- hlavní zobrazovací PANEL – 40 g krabička na zkumavky
- více o Cleocin vaginální (clindamycin topický)
- spotřebitelské zdroje
- profesionální zdroje
- jiné formulace
- související průvodce léčbou
pro intravaginální použití pouze pro oční, dermální nebo perorální použití
klindamycin fosfát je ve vodě rozpustný ester polosyntetického antibiotika produkovaného substitucí 7(S)-chlorem 7(S). R)-hydroxylová skupina mateřského antibiotika linkomycinu. Chemický název pro klindamycin fosfát je methyl 7-chloro-6,7,8-trideoxy-6-(1-methyl-trans-4-propyl-L-2-pyrrolidinecarboxamido)-1-thio-L-threo-α–D-galacto-oktopyranosid 2 – (dihydrogenfosforečnan). Má molekulovou hmotnost 504,96 a molekulární vzorec je C18H34ClN2O8PS. Strukturní vzorec je uveden níže:
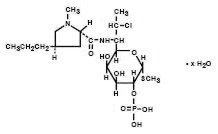
Cleocin vaginální krém 2% je polotuhý bílý krém, který obsahuje 2% klindamycin fosfátu, USP, v koncentraci odpovídající 20 mg klindamycinu na gram. PH krému je mezi 3,0 a 6,0. Krém také obsahuje benzylalkohol, cetostearylalkohol, smíšené estery mastných kyselin, minerální olej, polysorbát 60, propylenglykol, čištěnou vodu, sorbitanmonostearát a kyselinu stearovou.
jeden aplikátor obsahující 5 gramů vaginálního krému obsahuje přibližně 100 mg klindamycin fosfátu.
Cleocin vaginální krém-Klinická farmakologie
mechanismus účinku
klindamycin je antibakteriální léčivo (viz mikrobiologie).
farmakokinetika
po intravaginální dávce 100 mg klindamycin fosfátu vaginální krém 2% podávané 6 zdravým dobrovolnicím po dobu 7 dnů bylo přibližně 5% (rozmezí 0, 6% až 11%) podané dávky absorbováno systémově. Maximální koncentrace klindamycinu v séru pozorovaná první den byla v průměru 18 ng / mL (rozmezí 4 až 47 ng/mL) a 7. den byla v průměru 25 ng/mL (rozmezí 6 až 61 ng / mL). Těchto vrcholových koncentrací bylo dosaženo přibližně 10 hodin po podání dávky (rozmezí 4-24 hodin).
po intravaginální dávce 100 mg vaginálního krému klindamycin fosfátu 2% podávané po dobu 7 po sobě jdoucích dnů 5 ženám s bakteriální vaginózou byla absorpce pomalejší a méně variabilní než u zdravých žen. Přibližně 5% (rozmezí 2% až 8%) dávky bylo absorbováno systémově. Maximální koncentrace klindamycinu v séru pozorovaná první den byla v průměru 13 ng / mL (rozmezí 6 až 34 ng/mL) a 7. den byla v průměru 16 ng/mL (rozmezí 7 až 26 ng / mL). Těchto vrcholových koncentrací bylo dosaženo přibližně 14 hodin po podání dávky (rozmezí 4-24 hodin).
po opakovaném vaginálním podání klindamycin fosfátu vaginálního krému 2% došlo k malé nebo žádné systémové akumulaci klindamycinu. Systémový poločas byl 1,5 až 2,6 hodiny.
mikrobiologie
mechanismus účinku
klindamycin inhibuje syntézu bakteriálních proteinů vazbou na 23S RNA 50S podjednotky ribozomu. Klindamycin je převážně bakteriostatický. Ačkoli je klindamycin fosfát in vitro neaktivní, rychlá hydrolýza in vivo jej převádí na aktivní klindamycin.
rezistence
rezistence na klindamycin je nejčastěji způsobena modifikací cílového místa na ribozomu, obvykle chemickou modifikací RNA bází bodovými mutacemi v RNA nebo příležitostně v proteinech. U některých organismů byla prokázána zkřížená rezistence mezi linkosamidy, makrolidy a streptograminy B. Byla prokázána zkřížená rezistence mezi klindamycinem a linkomycinem.
antibakteriální aktivita
testování kultury a citlivosti bakterií se běžně neprovádí ke stanovení diagnózy bakteriální vaginózy (viz indikace a použití); standardní metodika pro testování citlivosti potenciálních bakteriálních patogenů, Gardnerella vaginalis, Mobiluncus spp., nebo Mycoplasma hominis, nebyl definován.
jsou k dispozici následující údaje in vitro, ale jejich klinický význam není znám. Klindamycin je účinný in vitro proti většině izolátů následujících organismů, o nichž se uvádí, že jsou spojeny s bakteriální vaginózou:
- Bacteroides spp.
- Gardnerella vaginalis
- Mobiluncus spp.
- Mycoplasma hominis
- Peptostreptococcus spp.
indikace a použití pro Cleocin vaginální krém
Cleocin vaginální krém 2% je indikován k léčbě bakteriální vaginózy (dříve označované jako Haemophilus vaginitis, Gardnerella vaginitis, nespecifická vaginitida, Corynebacterium vaginitis nebo anaerobní vaginóza). Cleocin vaginální krém 2%, lze použít k léčbě netehotných žen a těhotných žen během druhého a třetího trimestru. (Viz klinické studie.)
poznámka: Pro účely této indikace je klinická diagnóza bakteriální vaginózy obvykle definována přítomností homogenního vaginálního výboje, který (a) má pH vyšší než 4, 5, (b) vydává „rybí“ aminový zápach, když je smíchán s 10% roztokem KOH, A (c) obsahuje vodící buňky při mikroskopickém vyšetření. Gramovy výsledky skvrn v souladu s diagnózou bakteriální vaginózy zahrnují (a) výrazně sníženou nebo nepřítomnou morfologii Lactobacillus, (b) převahu Morfotypu Gardnerella a (c) chybějící nebo málo bílých krvinek.
jiné patogeny běžně spojené s vulvovaginitidou, např. Trichomonas vaginalis, Chlamydia trachomatis, N. gonorrhoeae, Candida albicans a Herpes simplex virus by měly být vyloučeny.
kontraindikace
Cleocin vaginální krém 2% je kontraindikován u jedinců s anamnézou přecitlivělosti na klindamycin, linkomycin nebo kteroukoli složku tohoto vaginálního krému. Cleocin vaginální krém 2%, je také kontraindikován u jedinců s anamnézou regionální enteritidy, ulcerózní kolitidy nebo s anamnézou kolitidy spojené s antibiotiky.
varování
pseudomembranózní kolitida byla hlášena u téměř všech antibakteriálních látek, včetně klindamycinu, a může se pohybovat v závažnosti od mírné až po život ohrožující. Perorálně a parenterálně podávaný klindamycin byl spojen s těžkou kolitidou, která může skončit fatálně. Průjem, krvavý průjem a kolitida (včetně pseudomembranózní kolitidy) byly hlášeny při použití perorálně a parenterálně podávaného klindamycinu, jakož i při topických (dermálních a vaginálních) formulacích klindamycinu. Proto je důležité zvážit tuto diagnózu u pacientů, kteří mají průjem po podání klindamycinu, i když jsou podáváni vaginální cestou, protože přibližně 5% dávky klindamycinu je systémově absorbováno z pochvy.
léčba antibakteriálními látkami mění normální flóru tlustého střeva a může umožnit přerůstání klostridií.Studie ukazují, že toxin produkovaný Clostridium difficile je primární příčinou kolitidy spojené s antibiotiky.
po stanovení diagnózy pseudomembranózní kolitidy by měla být zahájena terapeutická opatření. Mírné případy pseudomembranózní kolitidy obvykle reagují na přerušení léčby samotné. Ve středně těžkých až těžkých případech je třeba zvážit léčbu tekutinami a elektrolyty, suplementaci bílkovin a léčbu antibakteriálním léčivem klinicky účinným proti kolitidě Clostridium difficile.
nástup příznaků pseudomembranózní kolitidy se může objevit během nebo po antimikrobiální léčbě.
bezpečnostní opatření
Obecné
Cleocin vaginální krém 2%, obsahuje složky, které způsobí pálení a podráždění oka. V případě náhodného kontaktu s okem vypláchněte oko velkým množstvím studené vody z vodovodu.
použití vaginálního krému Cleocin 2% může vést k přerůstání nesusceptovatelných organismů v pochvě. V klinických studiích zahrnujících 600 netehotných žen, které byly léčeny po dobu 3 dnů, byl Candida albicans detekován symptomaticky nebo kulturou u 8,8% pacientů. U 9% pacientů byla zaznamenána vaginitida. Inklinické studie zahrnující 1325 netehotných žen, které byly léčeny po dobu 7 dnů, Candida albicans byla detekována, buď symptomaticky, nebo kulturou, u 10, 5% pacientů. Vaginitida byla zaznamenána u 10,7% pacientů. U 180 těhotných žen, které dostávaly léčbu po dobu 7 dnů, byla Candida albicans detekována buď symptomaticky, nebo kulturou, u 13,3% pacientů. U 7,2% pacientů byla zaznamenána vaginitida. Candida albicans, jak je zde uvedeno, zahrnuje termíny: vaginální moniliáza a moniliáza (tělo jako celek). Vaginitida zahrnuje termíny: vulvovaginální porucha, vulvovaginitida, vaginální výtok, trichomonální vaginitida a vaginitida.
informace pro pacienta
pacient by měl být poučen, aby se během léčby tímto přípravkem neúčastnil vaginálního styku ani nepoužíval jiné vaginální přípravky (jako jsou tampony nebo sprchy).
pacient by měl být také upozorněn, že tento krém obsahuje minerální olej, který může oslabit latexové nebo gumové výrobky, jako jsou kondomy nebo vaginální antikoncepční membrány. Proto se použití těchto přípravků do 72 hodin po léčbě vaginálním krémem Cleocin 2% nedoporučuje.
lékové interakce
bylo prokázáno, že systémový klindamycin má neuromuskulární blokující vlastnosti, které mohou zvýšit účinek jiných neuromuskulárních blokátorů. Proto by měl být používán s opatrností u pacientů užívajících takové látky.
karcinogeneze, mutageneze, zhoršení Fertility
dlouhodobé studie na zvířatech nebyly provedeny s klindamycinem k vyhodnocení kancerogenního potenciálu.
provedené testy Genotoxicity zahrnovaly mikronukleární test na potkanech a amesův test. Oba testy byly negativní. Studie Fertility u potkanů léčených perorálně dávkou až 300 mg / kg / den (31násobek expozice u člověka na základě mg / m2) neodhalily žádné účinky na fertilitu nebo schopnost Páření.
těhotenství
teratogenní účinky
v klinických studiích s těhotnými ženami nebylo systémové podávání klindamycinu během druhého a třetího trimestru spojeno se zvýšenou frekvencí vrozených abnormalit.
Clindamycin vaginální krém by měl být používán během prvního trimestru těhotenství pouze tehdy, je-li to nezbytně nutné a přínosy převažují nad riziky. Neexistují adekvátní a dobře kontrolované studie u těhotných žen během prvního trimestru těhotenství.
Cleocin vaginální krém 2% byl studován u těhotných žen během druhého trimestru. U žen léčených po dobu sedmi dnů byla abnormální práce hlášena u 1, 1% pacientů, kteří dostávali klindamycinový vaginální krém 2% ve srovnání s 0, 5% pacientů, kteří dostávali placebo.
reprodukční studie byly provedeny na potkanech a myších s použitím perorálních a parenterálních dávek klindamycinu až do 600 mg/kg/den (62 a 25násobek maximální expozice u člověka na základě plochy povrchu těla) a neodhalily žádné známky poškození plodu v důsledku klindamycinu. Rozštěp patra byl pozorován u plodů z jednoho myšího kmene léčeného intraperitoneálně klindamycinem v dávce 200 mg/kg/den (asi 10násobek doporučené dávky založené na přepočtu plochy povrchu těla). Protože tento účinek nebyl pozorován u jiných myších kmenů nebo u jiných druhů, může být účinek specifický pro kmen.
kojící matky
omezené publikované údaje založené na zprávách o odběru mateřského mléka, že klindamycin se objevuje v lidském mateřském mléce v rozmezí méně než 0, 5 až 3, 8 mcg/mL při dávkách 150 mg perorálně až 600 mg intravenózně. Není známo, zda se klindamycin vylučuje do mateřského mléka po použití vaginálně podávaného klindamycin fosfátu.
klindamycin může mít nepříznivé účinky na gastrointestinální flóru kojeného dítěte. Pokud je klindamycin vyžadován kojící matkou, není důvodem k přerušení kojení, ale může být upřednostňováno alternativní léčivo. Sledujte kojené dítě na možné nežádoucí účinky na gastrointestinální flóru, jako je průjem, kandidóza (drozd, vyrážka plenky) nebo vzácně krev ve stolici, což naznačuje možnou kolitidu spojenou s antibiotiky.
vývojový a zdravotní přínos kojení by měl být zvážen spolu s klinickou potřebou klindamycinu matky a případnými nežádoucími účinky klindamycinu nebo základního mateřského stavu na kojené dítě.
pediatrické použití
bezpečnost a účinnost u dětských pacientů nebyla stanovena.
geriatrické použití
klinické studie pro Cleocin Vaginal Cream 2% nezahrnovaly dostatečný počet subjektů ve věku 65 a více let, aby bylo možné určit, zda reagují odlišně od mladších subjektů. Jiné hlášené klinické zkušenosti nezjistily rozdíly v odpovědích mezi staršími a mladšími pacienty.
nežádoucí účinky
klinické studie
netehotné ženy
v klinických studiích zahrnujících netehotné ženy přerušilo léčbu 1, 8% z 600 pacientů, kteří byli léčeni vaginálním krémem Cleocin 2% po dobu 3 dnů a 2, 7% z 1325 pacientů, kteří byli léčeni po dobu 7 dnů, kvůli nežádoucím účinkům souvisejícím s léčivem. 2% vaginálního krému klindamycin fosfátu bylo hlášeno u 20,7% pacientů léčených po dobu 3 dnů a 21,3% pacientů léčených po dobu 7 dnů. Příhody vyskytující se u ≥1% pacientů užívajících klindamycin fosfát vaginální krém 2% jsou uvedeny v tabulce 1.
| událost | Cleocin vaginální krém | |
|---|---|---|
| 3 den n = 600 |
7 dní n=1325 |
|
| urogenitální | ||
| vaginální moniliáza | 7.7 | 10.4 |
| vulvovaginitida | 6.0 | 4.4 |
| vulvovaginální porucha | 3.2 | 5.3 |
| trichomonální vaginitida | 0 | 1.3 |
| tělo jako celek | ||
| moniliáza (tělo) | 1.3 | 0.2 |
další příhody vyskytující se u <1% skupin klindamycinového vaginálního krému 2% zahrnují:
urogenitální systém: vaginální výtok, metrorágie, infekce močových cest, endometrióza, menstruační porucha, vaginitida/vaginální infekce a vaginální bolest.
tělo jako celek: lokalizovaná bolest břicha, generalizovaná bolest břicha, křeče v břiše, zápach z úst, bolest hlavy, bakteriální infekce, zánětlivý otok, alergická reakce a plísňová infekce.
trávicí systém: nevolnost, zvracení, zácpa, dyspepsie, plynatost, průjem a gastrointestinální porucha.
endokrinní systém: hypertyreóza.
centrální nervový systém: závratě a závratě.
respirační systém: epistaxe.
kůže: pruritus (místo aplikace), moniliáza, vyrážka, makulopapulární vyrážka, erytém a kopřivka.
zvláštní smysly: chuťová zvrácenost.
těhotné ženy
v klinické studii zahrnující těhotné ženy během druhého trimestru ukončilo 1, 7% ze 180 pacientů, kteří byli léčeni po dobu 7 dnů, léčbu kvůli nežádoucím účinkům souvisejícím s léčivem. U 22,8% těhotných pacientek byly hlášeny zdravotní příhody, které byly považovány za související, pravděpodobně související, možná související nebo s neznámým vztahem k vaginálně podávanému vaginálnímu krému klindamycin fosfátu 2%. Příhody vyskytující se u ≥1% pacientů užívajících klindamycin fosfát vaginální krém 2% nebo placebo jsou uvedeny v tabulce 2.
| příhoda | CLEOCIN vaginální krém |
Placebo |
|---|---|---|
| 7 den n = 180 |
7 dní n=184 |
|
| urogenitální | ||
| vaginální moniliáza | 13.3 | 7.1 |
| vulvovaginální porucha | 6.7 | 7.1 |
| abnormální práce | 1.1 | 0.5 |
| tělo jako celek | ||
| plísňová infekce | 1.7 | 0 |
| kůže | ||
| Pruritus, místo aplikace | 1.1 | 0 |
další příhody vyskytující se u <1% skupiny klindamycinových vaginálních krémů 2% zahrnují:
urogenitální systém: dysurie, metroragie, vaginální bolest a trichomonální vaginitida.
tělo jako celek: infekce horních cest dýchacích.
kůže: pruritus (místo lokální aplikace) a erytém.
postmarketingové zkušenosti
vzhledem k tomu, že tyto reakce jsou hlášeny dobrovolně z populace s nejistou velikostí, není vždy možné spolehlivě odhadnout jejich frekvenci nebo stanovit příčinnou souvislost s expozicí léku.
v postmarketingovém období byly hlášeny případy pseudomembranózní kolitidy s použitím vaginálního krému clindamycin fosfátu.
jiné formulace klindamycinu
Klindamycinový vaginální krém poskytuje minimální maximální sérové hladiny a systémovou expozici (AUC) klindamycinu ve srovnání s perorálním dávkováním klindamycinu 100 mg. Ačkoli tyto nižší úrovně expozice jsou méně pravděpodobné, že vyvolávají běžné reakce pozorované při perorálním klindamycinu, v současné době nelze vyloučit možnost těchto a dalších reakcí. Údaje z dobře kontrolovaných studií přímo porovnávajících klindamycin podávaný perorálně s klindamycinem podávaným vaginálně nejsou k dispozici.
při perorálním nebo parenterálním podání klindamycinu byly hlášeny následující nežádoucí účinky a změněné laboratorní testy:
gastrointestinální: bolest břicha, ezofagitida, nauzea, zvracení, průjem a pseudomembranózní kolitida. (Viz varování.)
hematopoetická: byla hlášena přechodná neutropenie (leukopenie), eozinofilie, agranulocytóza a trombocytopenie. Žádný přímý etiologický vztah k souběžné léčbě klindamycinem nemohl být v žádném z těchto zpráv.
Hypersenzitivní Reakce: Během farmakoterapie byla pozorována makulopapulární vyrážka a kopřivka. Generalizované mírné až středně závažné morbilliformní kožní vyrážky jsou nejčastěji hlášené ze všech nežádoucích účinků. Vzácné případy erythema multiforme, některé připomínající Stevens-Johnsonův syndrom, byly spojeny s klindamycinem. Bylo hlášeno několik případů anafylaktoidních reakcí. Pokud dojde k reakci přecitlivělosti, léčivo by mělo být přerušeno.
játra: během léčby klindamycinem byla pozorována žloutenka a abnormality v jaterních funkčních testech.
muskuloskeletální: Byly hlášeny vzácné případy polyartritidy.
renální: ačkoli nebyl prokázán žádný přímý vztah klindamycinu k poškození ledvin, renální dysfunkce, o čemž svědčí azotemie, oligurie a/nebo proteinurie, byla ve vzácných případech pozorována.
předávkování
vaginálně aplikovaný klindamycin fosfát vaginální krém 2% by mohl být absorbován v dostatečném množství k vyvolání systémových účinků. (Viz varování.
Cleocin vaginální krém dávkování a podání
doporučená dávka je jedna aplikátor klindamycin fosfátu vaginální krém 2%, (5 gramů obsahující přibližně 100 mg klindamycin fosfátu) intravaginálně, nejlépe před spaním, po dobu 3 nebo 7 po sobě jdoucích dnů u netehotných pacientek a po dobu 7 po sobě jdoucích dnů u těhotných pacientek. (Viz klinické studie.
jak se dodává Cleocin vaginální krém
Cleocin vaginální krém 2%, (klindamycin fosfát vaginální krém) se dodává následovně:
40 g zkumavka (se 7 jednorázovými aplikátory) NDC 0009-3448-01
Skladujte při kontrolované pokojové teplotě 20° až 25° C (68° až 77° F). Chraňte před mrazem.
klinické studie
ve dvou klinických studiích zahrnujících 674 hodnotitelných netehotných žen s bakteriální vaginózou srovnávajících Cleocin vaginální krém 2% po dobu 3 nebo 7 dnů se míra klinické léčby stanovená 1 měsíc po léčbě pohybovala od 72% do 81% pro 3denní léčbu a 84% až 86% pro 7denní léčbu.
| CLEOCIN 3 den | CLEOCIN 7 den | |||
|---|---|---|---|---|
| americká studie | 94/131 | 72% | 110/128 | 86% |
| evropská studie | 161/199 | 81% | 181/216 | 84% |
v klinické studii zahrnující 249 hodnotitelných těhotných pacientek ve druhém a třetím trimestru léčených po dobu 7 dnů byla míra klinické vyléčení stanovená 1 měsíc po léčbě 60% (77/129) v rameni s klindamycinem a 9% (11/120) v rameni s klindamycinem. rameno vozidla. Stanovení klinického vyléčení bylo založeno na nepřítomnosti“ rybího “ aminového zápachu, když byl vaginální výtok smíchán s 10% roztokem KOH a nepřítomností stopových buněk při mikroskopickém vyšetření.
pouze Rx
štítek tohoto produktu mohl být aktualizován. Aktuální úplné informace o předepisování, prosím navštivte www.pfizer.com.

LAB-0043-12.0
revidované 03/2020
jednorázové plastové aplikátory jsou dodávány s tímto obalem. Jsou navrženy tak, aby umožňovaly správné vaginální podání krému.
odstraňte víčko ze smetanové zkumavky. Našroubujte plastový aplikátor na závitový konec trubky.
válcovací trubice ze spodu jemně stlačte a zatlačte lék do aplikátoru. Aplikátor se naplní, když píst dosáhne svého předem stanoveného bodu zastavení.
odšroubujte aplikátor z trubice a nasaďte kryt.
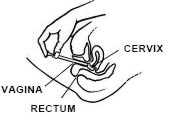
zatímco ležíte na zádech, pevně uchopte hlaveň aplikátoru a vložte do vagíny co nejvíce, aniž byste způsobili nepohodlí.
pomalu zatlačte píst, dokud se nezastaví.
opatrně vytáhněte aplikátor z pochvy a zlikvidujte aplikátor.
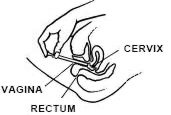
NEZAPOMEŇTE APLIKOVAT JEDEN APLIKÁTOR KAŽDOU NOC PŘED SPANÍM NEBO PODLE POKYNŮ LÉKAŘE.
pokyny pro pacienta
toto balení obsahuje jednorázové plastové aplikátory. Aplikátory jsou určeny pro správné podání krému do pochvy.
sejměte víčko ze smetanové zkumavky a našroubujte plastový aplikátor na zkumavku.
jemně stlačte zkumavku ze spodního konce a zatlačte lék do aplikátoru. Aplikátor bude plný, jakmile píst dosáhne své maximální délky.
odšroubujte aplikátor z trubice a nasaďte kryt.
Lehněte si na záda a Držte aplikátor pevně, vložte jej do vagíny co nejvíce, aniž byste způsobovali nepohodlí.
pomalu zatlačte píst, dokud se nezastaví.
opatrně vyjměte aplikátor z pochvy a zlikvidujte jej.
NEZAPOMEŇTE APLIKOVAT PLNÝ APLIKÁTOR KAŽDOU NOC PŘED SPANÍM NEBO PODLE POKYNŮ LÉKAŘE.
LAB-1058-1.0
hlavní zobrazovací PANEL – 40 g štítek zkumavky
NDC 0009-3448-01
40 Gram
pouze Rx
Cleocin®
clindamycin fosfát
vaginální krém, USP
pouze pro intravaginální použití
2%*
hlavní zobrazovací PANEL – 40 g krabička na zkumavky
NDC 0009-3448-01
40 gramů se 7 aplikátory
pouze Rx
Cleocin®
clindamycin fosfát
vaginální krém, USP
pouze pro intravaginální použití
2%*
Pfizer
distribuováno
Pharmacia & Upjohn Co
divize Pfizer Inc, NY, NY 10017
| CLEOCIN klindamycin fosfátový krém |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Pharmacia a Upjohn Company LLC (618054084)
| zřízení | |||
| jméno | adresa | ID / FEI | operace |
| Pharmacia a Upjohn Company LLC | 618054084 | analýza (0009-3448), API výroba (0009-3448), štítek (0009-3448), výroba (0009-3448), balení(0009-3448) | |
více o Cleocin vaginální (clindamycin topický)
- nežádoucí účinky
- Během těhotenství nebo kojení
- informace o dávkování
- lékové interakce
- ceny & kupóny
- generická dostupnost
- třída léků: vaginální antiinfektiva
spotřebitelské zdroje
- pokročilé čtení
profesionální zdroje
- informace o předepisování
- clindamycin vaginální krém (FDA)
ostatní značky Clindamax, Clindagel, Clindesse, Clindacin Etz, … + 4 další
jiné formulace
- Cleocin
- … + 4 více
související průvodce léčbou
- bakteriální vaginitida
lékařské zřeknutí se odpovědnosti